流体流动分析的制作方法
本发明涉及用于使用超声波来分析流体导管中的流体流动的方法和设备。具体地,尽管不是唯一的,本发明适用于用于分析人或动物循环系统中的流体流动的此类方法和设备。
背景技术:
在每次心跳期间,当心脏收缩时,心脏会增加立即连接到其的动脉中的血液的压力和速度。这种干扰随着波向下传播到动脉系统。这种现象的日常实例是可以在手腕上感觉到脉搏。波行进的速度(speed或velocity)取决于动脉的僵硬度,并且波的反射在血管几何形状或壁特性变化的任何点处发生。因此,波的速度和初始波的强度和其反射含有关于心脏的性能和血管的状态的信息。因此,测量这些特性以提供用于诊断心血管疾病和处于患有所述心血管疾病的风险中的那些患者的有用的装置是有用的。
因此,动脉中的脉搏波可以用于评估(a)心脏的性能,因为心脏会产生波;(b)确定波的速度的动脉僵硬度;以及(c)反射波的动脉或外周血管横截面或机械特性的变化。波动现象可以容易地根据侵入式的基于导液管的测量进行评估并且越来越多地用于对冠状动脉狭窄进行功能评估。波动现象在心血管医学的其它领域中的使用受到进行准确的非侵入式测量的困难的阻碍。
wo2017/163030描述了一种用于确定流动通过导管的流体的波速量度的方法和设备,所述方法和设备使用超声测量通过跟踪对体积元件进行采样的连续帧中的在流体流动内的对象并且获得所述对象的位移向量来确定作为时间的函数的流体速度。然后,与测量到导管直径的变化结合的流体速度的变化用于确定波速或波强度。在wo2017/163030中所描述的技术中,对流体导管(如动脉)中的流体流动的分析可以非侵入式地实施并且提供一种用于评估波动现象的基于超声的系统,所述基于超声的系统是非侵入式的并且适合于对例如心力衰竭、动脉硬化、血管张力改变和内皮功能障碍进行临床研究。
技术实现要素:
本发明的目标是提供wo2017/163030中所描述的技术的替代性技术。本文所描述的那些替代性技术可以提供确定波速和/或波强度的提高的效率和提高的准确度,并且因此可以允许使用更简单的检测系统。
根据一方面,本发明提供了一种确定流动通过流体导管的流体的波速量度的方法,所述方法包括:
使用超声测量来确定在所述导管的纵向位置处的作为时间的函数的导管直径或导管横截面面积;
使用超声测量来确定在所述导管的所述纵向位置处的体积元件中的作为时间的函数的流体速度量度,用于确定所述流体速度量度的所述超声测量是通过使对所述体积元件进行采样的连续帧中的在流体流动内的散射对象去相关来实现的;
根据(i)作为时间的函数的在所述纵向位置处的流体速度的变化和(ii)作为时间的函数的所述导管直径或导管横截面面积的变化的函数确定所述波速量度。
所述流体速度量度可以包括所述连续帧中的所述散射对象的去相关系数。所述波速可以是根据以下任一项确定的:
(i)作为时间的函数的在所述纵向位置处的所述流体速度量度的变化与作为时间的函数的所述导管直径的对数函数的变化之比,或
(ii)在所述纵向位置处的所述流体速度量度在一定时间间隔内的变化与所述导管直径的对数函数在同一时间间隔内的对应变化之比。
所述波速可以是根据在所述纵向位置处的所述流体速度量度在一定时间间隔内的变化和所述导管直径在同一时间间隔内的对应变化确定的。所述流体速度可以是使用散斑去相关测速法确定的。用于确定流体速度量度的所述超声测量可以包括一系列m模式或b模式图像或m模式或b模式rf数据。确定所述流体速度量度可以包括测量在所述m模式或b模式图像或所述m模式或b模式rf数据的连续帧中的所述散射对象的去相关系数。用于确定导管直径和去相关系数的所述超声测量可以均是从共同超声换能器头导出的。所述共同换能器头可以被定向成使得束轴线与所述流体流动导管的流体流动轴线正交、与所述流体流动轴线斜交或与所述流动导管同轴。用于确定导管直径或导管横截面面积和所述流体速度量度的所述超声测量可以均是从共同超声激发和响应信号导出的。
所述波速c'可以是根据方程c'=0.5(du'/dlnd)确定的,其中du'是作为时间的函数的所述去相关系数u'的变化,并且dlnd是作为时间的函数的d的自然对数的变化,并且c'是真实波速的缩放量度。
所述流体导管可以包括人或动物循环系统的一部分。所述方法可以进一步包含在心动周期期间多次重复所述超声测量并且确定波速,并且使波速的测量与所述心动周期内的时间相关。被跟踪对象可以包括红细胞、白细胞、血小板或造影剂实体。所述方法可以进一步包含根据所述波速确定在所述体积元件处的流体导管壁弹性或扩张性的量度。
所述波速c'可以是根据方程c'=adu'/da或c'=du'/dlna确定的,其中a是横截面面积,da是作为时间的函数的横截面面积的变化,du'是作为时间的函数的所述去相关系数u'的变化,并且dlna是作为时间的函数的a的自然对数的变化,并且c'是真实波速的缩放量度。
根据另一方面,本发明提供了一种确定流动通过流体导管的流体的波速量度的方法,所述方法包括:
使用超声测量来确定在所述导管的纵向位置处的作为时间的函数的导管直径;
使用超声测量来确定在所述导管的所述纵向位置处的体积元件中的作为时间的函数的流体速度量度,用于确定所述流体速度量度的所述超声测量是通过使对所述体积元件进行采样的连续帧中的在流体流动内的散射对象去相关来实现的;
基于所述流体速度量度和导管直径测量确定通过所述导管的流动速率的变化;
基于所述导管直径测量确定所述导管的横截面面积的变化;以及
根据作为时间的函数的在所述纵向位置处的流动速率的变化与作为时间的函数的导管横截面面积的变化之比确定所述波速量度。
所述流体速度量度可以包括所述连续帧中的所述散射对象的去相关系数。用于确定流体速度量度的所述超声测量可以包括一系列m模式或b模式图像或m模式或b模式rf数据。确定所述流体速度量度可以包括测量在所述m模式或b模式图像或所述m模式或b模式rf数据的连续帧中的所述散射对象的去相关系数。
用于确定导管直径和去相关系数的所述超声测量可以均是从共同超声换能器头导出的。所述共同换能器头可以被定向成使得束轴线与所述流体流动导管的流体流动轴线正交、与所述流体流动轴线斜交或与所述流动导管同轴。用于确定导管直径和所述流体速度量度的所述超声测量可以均是从共同超声激发和响应信号导出的。
所述波速c可以是根据方程c=dq/da确定的,其中dq是所述流体流动速率的变化并且da是所述导管的所述横截面面积的变化。
所述流体导管可以包括人或动物循环系统的一部分。所述方法可以进一步包含在心动周期期间多次重复所述超声测量并且确定波速,并且使波速的测量与所述心动周期内的时间相关。被跟踪对象可以包括红细胞、白细胞、血小板或造影剂实体。所述方法可以进一步包含根据所述波速确定在所述体积元件处的流体导管壁弹性或扩张性的量度。
根据另一方面,本发明提供了一种确定流体导管中的波强度量度的方法,所述方法包括:
使用超声测量来确定在所述导管的纵向位置处的作为时间的函数的导管直径;
使用超声测量来确定在所述导管的所述纵向位置处的体积元件中的作为时间的函数的流体速度量度,用于确定所述流体速度量度的所述超声测量是通过使对所述体积元件进行采样的连续帧中的在流体流动内的散射对象去相关来实现的;
确定作为所确定的导管直径的变化和所述流体速度量度的对应变化的函数的波强度量度。
所述流体速度量度可以包括所述连续帧中的所述散射对象的去相关系数。用于确定流体速度量度的所述超声测量可以包括一系列m模式或b模式图像或m模式或b模式rf数据。确定所述流体速度量度可以包括测量在所述m模式或b模式图像或所述m模式或b模式rf数据的连续帧中的所述散射对象的去相关系数。用于确定导管直径和去相关系数的所述超声测量可以均是从共同超声换能器头导出的。所述共同换能器头可以被定向成使得束轴线与所述流体流动导管的流体流动轴线正交、与所述流体流动轴线斜交或与所述流体流动轴线同轴。用于确定导管直径和所述流体速度量度的所述超声测量可以均是从共同超声激发和响应信号导出的。所述方法可以进一步包含确定所述流体导管中的波速,并且所述波强度量度可以被确定为所确定的导管直径、所确定的流体速度量度和所确定的波速的函数。
波强度量度可以是根据以下方程确定的:
其中ndi'+是如根据非侵入式测量确定的前向波强度,ndi'-是如根据非侵入式测量确定的后向波强度;d是所述导管直径;dd是所述导管直径的变化;c'是根据所述去相关系数确定的波速;du'是所述去相关系数的变化。所述波强度量度可以是根据方程ndi=dddu确定的,其中ndi是根据非侵入式测量确定的波强度;dd是所述导管直径的变化;并且du是所述流体速度量度的变化。所述方法可以进一步包含通过对一段时间内的波强度求积分来确定波能量。所述波速可以被确定为作为时间的函数的在所述纵向位置处的所述流体速度量度的变化与作为时间的函数的所述导管直径的对数函数的变化之比的函数。波速量度c'可以是根据方程c'=0.5(du'/dlnd)确定的,其中du'是作为时间的函数的所述去相关系数u'的变化,并且dlnd是作为时间的函数的d的自然对数的变化。所述流体导管可以包括人或动物循环系统的一部分。所述方法可以进一步包含在心动周期期间多次重复所述超声测量并且确定波强度,并且使波强度的测量与所述心动周期内的时间相关。被跟踪对象可以包括红细胞、白细胞、血小板或造影剂实体。所述方法可以进一步包含根据所述波强度确定在所采样的体积元件上游和或下游的流体导管横截面特性的量度。所述方法可以进一步包含根据所述波强度确定心输出量分布。
根据另一方面,本发明提供了一种用于确定流体导管中的波速量度的设备,所述设备包括分析模块,所述分析模块被配置成执行如上文所定义的确定流体导管中的波速的步骤。根据另一方面,本发明提供了一种用于确定流体导管中的波强度量度的设备,所述设备包括分析模块,所述分析模块被配置成执行如上文所定义的确定流体导管中的波强度的步骤。
附图说明
现在将通过举例并且参考附图来描述本发明的实施例,在附图中:
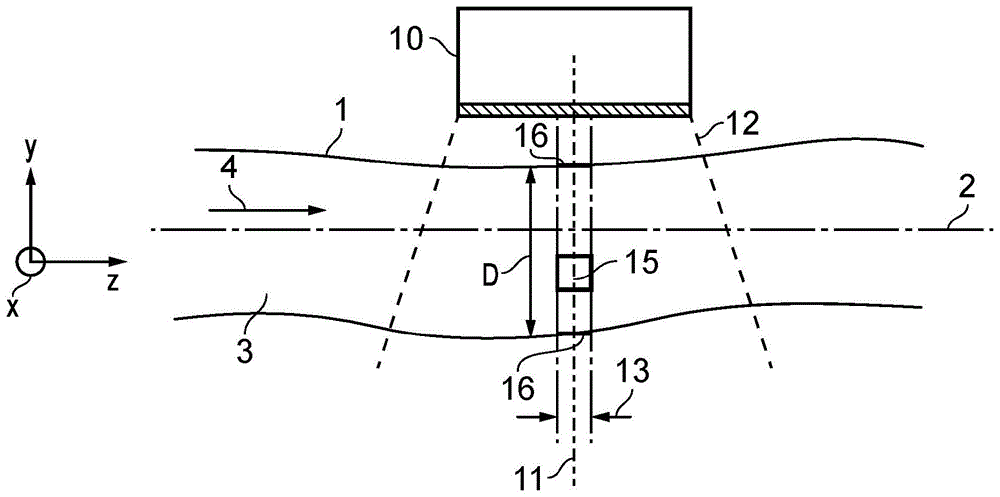
图1是流体导管和超声换能器的横截面示意图,其用于解释流体流动分析技术;
图2是超声流体流动分析系统的示意性功能框图;
图3和图3a示出了作为连续的超声帧的散射体(散斑)移动的函数的超声散斑相关系数的示意性分布,其展示了相关系数的相当大范围内的总体线性关系;
图4示出了针对通过流体导管的流体的不同流动速率的作为通过流体导管的横截面的深度的函数的超声散斑相关系数的示意性分布,从而提供了流体速度曲线的量度;
图5示出了与多普勒方法相比使用散斑去相关技术进行的血流速度测量;
图6示出了超声图像测速法与使用散斑去相关技术进行的血流速度测量之间的相关性。
具体实施方式
动脉脉搏波和其与临床上重要的心血管特性的关系
a)波基础
脉搏波起源于心脏,并且从动脉系统的近端(上游)朝向周围向前行进。反射更加外围地在血管特性改变的位点处起源;经过反射的波向后行进,并且然后可以在反射位点之间向前和向后重新反射,直到其消散为止。将更多的血液推动到动脉中会产生压缩波,而抽吸会产生减压波。如果压缩波在测量位点的近端起源,则压缩波将增加压力并且加速流动,而减压波将降低压力并且减慢流动。本公开中所描述的方法可以总体上涉及测量通过在流体导管(如循环系统)中流动的流体行进的此类压缩/减压波的速度和/或强度和/或反射。通常,波可以被认为包括随着时间沿流体导管传播的流体压力、流体速度和流体导管直径中的干扰。在本文所例示的优选的布置中,流体为血液并且流体导管包括血管和循环系统的组件。
b)波和心脏性能
左心室在非冠状全身动脉中产生前向行进的波。因为心室的收缩导致血液的压力和流动增加,所以压缩波在收缩开始时出现。收缩晚期出现的前向膨胀波被认为是由动量产生的,所述动量随着心室收缩变慢并且然后放松而将血液向前输送,从而导致压力和流动降低。这些波在临床上重要的条件下会改变。例如,在患有收缩性心力衰竭(包含扩张型心肌病[1,2])的患者中,左心室产生较小的压缩波,而肥厚型心肌病则引起舒张功能障碍并且导致较不强大的膨胀波[2]。
c)局部动脉顺应性
动脉中的波行进的速度c常规地被称为脉搏波速度(pwv)。根据以下bramwellhill方程,所述速度c与壁的扩张性和血液的密度有关:
c2=1/(密度×扩张性)。
因此,pwv是动脉僵硬度的量度:动脉越僵硬,则波速越快。周围动脉的pwv高于中心动脉,并且动脉随年龄而硬化[3]。因为pwv是强大的、独立的心血管风险因素[4],并且因为动脉在其病变时会变硬[5],所以pwv是在临床上是重要的。
根据以下moens-korteweg方程,血管的弹性可以根据波速(或pwv)获得:
c2=(einch)/(2rrho)
einc是递增弹性模量,h是血管壁厚度,r是血管半径,并且rho(ρ)是血液密度。
有弹性的动脉具有低弹性模量和高扩张性,因此对于同一个血管(即,对于相同的h和r),它们相反地相关:
扩张性=(2r)/(heinc)。
d)波反射
脉搏波在横截面面积或波速有变化的血管位点处反射。面积的变化在支化或逐渐变窄的位点处发生,并且波速的变化在壁结构改变的位置发生。波反射在临床上是重要的;例如,ascot试验示出反射增加是高血压患者中的心血管事件的强大独立预测因子[6]。尽管肱动脉血压相似[7],但是波反射可以对服用不同抗高血压药物的患者中的左心室质量的差异作出解释,并且所述波反射可以维持患有心力衰竭的患者中的收缩血压[1]。
动脉脉搏波特性的测量
已经通过传导时间方法对pwv进行了评估。在侵入式传导时间技术中,将具有相隔距离已知的两个压力传感器的导液管插入动脉中,并且将两个位点处的压力波到达之间的时间延迟与两者的分离结合使用以找到波速。使用这种原理对pwv进行非侵入式评估也是可能的。检测可以基于通过压平眼压测量法测量到的压力、使用多普勒超声测量到的速度或通过光电容积描记法测量到的体积。还可以使用mri[9,10]进行测量,但是这对于常规使用而言可能过于昂贵。与侵入式技术相比,位点相隔更远:通常,对颈动脉与股动脉之间的传导时间进行评估。
基于导液管的方法被认为对于供人们常规使用而言过于侵入式。不幸的是,非侵入式方法也具有局限性。第一,难以获得从心脏到测量位点中的每个测量位点的路径长度的准确值,特别是在在患有肥胖症或血管曲折的患者中。第二,所述方法给出对多个血管取平均的pwv,而不是局部值。这是重要的问题,因为不同的动脉以不同速率随年龄而硬化[3]并且与疾病具有不同的关系[10,11];局部测量本应该具有更大的临床价值(尽管由于所述局部测量使用较不广泛,所以仅存在少数验证其预测价值的尝试)。第三,股波形可能难以被准确地记录或可能在患有一系列的医学病状的患者中被修改。第四,并且也是最重要的,所有这些方法对波的速度而不是所述波的强度或反射进行评估。
已经尝试通过开发用于获得单个位点处的pwv的方法来克服这些问题。这消除了与跨大动脉距离对pwv进行平均相关联的问题并且避免了对估计那些距离的需要。另外,如下文所解释的,确定单个位点处的pwv所需的测量通常也使得能够分析波强度和反射。然后,理论上,此类技术可能具有很大价值。
在这些单个位点方法中,波特性是通过连续地且同时地测量血压(p)和血流速度(u)来确定的。如果p和u在前向波占主导的心动周期的阶段期间进行测量,则pwv可从介于连续测量之间的p(dp)的变化与u(du)的变化之比导出[12]。由parker和同事在过去20年内开发的波强度分析(wia)方法彻底改变了波的进一步表征[13];在[14]处给出了在线教程。所述wia方法的数学推导是复杂的,但是针对实际应用而导出的方程是简单的。心动周期中的任何时间处的波强度di是根据dp和du的乘积获得的。另外,知道pwv(参见上文)允许波被分解为前向分量和后向分量。
可以使用基于导液管的动脉探针对p和u进行侵入式测量。这种方法已经在许多wia研究中使用,例如在wia研究中,wia用于确定冠状动脉狭窄的严重程度[15]。然而,所述技术的侵入式性质高度受限。因此,已经尝试开发非侵入式替代方案。
在动脉覆盖坚硬结构并且相对靠近于身体表面的位置中,可以通过压平眼压测量法测量p并且通过多普勒超声测量u[1]。实用性受到可以以此方式进入的血管的数量以及对校准眼压计数据的需求的限制。(动脉之间的峰值收缩压由于波反射的模式不同而有所不同;因此,应当通过肱动脉的血压测量法对压力进行评估以获得绝对平均压力和舒张压—这些压力在整个动脉系统中是恒定的并且可以因此用于校准来自感兴趣的血管的眼压测量的测量值。可替代地,可以通过已经通过同一血管的血压测量法校准的眼压测量法对压力进行评估)。最重要的是,不可能同时将两个探针应用于同一位点;这意味着p数据流和u数据流必须单独地获取,被整体平均并且然后通过ecg进行时间对准,从而引入有效位误差。
使用多普勒超声和m模式超声的组合来分别测量u和动脉直径d的另一种非侵入式方法[2]已经实施。为了获得常规wia所需的p,假定动脉的直径与其内部的压力之间存在线性关系。多普勒和m模式的使用可能是有问题的,因为这些模式需要不同的束角度,从而使得难以对同一动脉区段进行成像。此外,对压力-直径关系的校准是复杂的,如刚才针对眼压测量法所描述的。(实际上,这种校准涉及过多以至于很少进行,并且颈动脉直径被简单的肱动脉血压测量法不正确地校准)。最后,由于动脉具有非线性应力-应变曲线,因此p和d成正比的假设从根本上是不正确的。beulen等人[16]已经提出了用于通过根据d对p进行非线性估计来克服这最后一个问题的方法,但是这些方法涉及一长串的假设并且尚未在生理条件下进行测试。在[55]中给出了将多普勒超声与b模式或m模式超声结合的另一种技术。
本文所描述的技术克服了现有系统的局限性,因为所述技术避免了对p进行(侵入式)测量或根据直径d的测量(不准确)对其进行估计的需要。
wia的可替代形式直接基于u和d,而非u和p[17]。pwv可以根据u的变化与d的自然对数的同时变化之比(优选地,在前向波占主导的周期中的某个点处)获得:
c=0.5(du/dlnd)。
波强度由下式给出:
其中ndi+是如从非侵入式测量导出的前向波强度,ndi-是如从非侵入式测量导出的后向波强度;d是导管直径;dd是导管直径的变化;c是波速;du是流体速度的变化。
已经在硅模型系统[18](包含人主动脉和其主要分支的几何学上和机械学上准确的模型[19])中并且用由威尔金森博士和同事(剑桥)使用mri在人主动脉中获取的数据[20]对这种分析技术进行了验证。
可以使用超声来获得这种新的分析技术所需的d和u数据,从而避免使用昂贵的mri。可以使用常规的超声b模式方法来确定d。为了避免在多普勒和m模式测量中固有的不同束角度要求的问题(上文所讨论的),在wo2017/163030中所描述的技术中,不使用多普勒超声来确定u。相反,使用称为超声图像测速法(uiv)的粒子图像测速法的形式。在这种方法中,获取一系列b模式图像或从所述一系列b模式图像导出的射频(rf)数据并且对序列图像执行区域互相关以确定超声散射体的局部位移。超声散射体可以是可以通过连续的图像帧对其进行跟踪的任何合适的对象,如红细胞、白细胞、血小板或微泡造影剂。根据这些位移和获取帧速率,可以找到完整的2d速度场。将通过这种方法获得的轴向速度与wia方程相结合意味着可以根据在同一位置处同时获得的数据流非侵入式地获得波速度、波强度和波反射,而无需将d可靠地转换为p。在本文现在所描述的替代方法中,执行粒子或散斑去相关技术,而不使用粒子图像测速法技术来使用区域互相关技术确定超声散射体的局部位移。
参考图1,流体导管1具有纵向轴线2,所述纵向轴线可以被称为z轴线并且以大致沿z轴线的主要流动方向4通过其运输流体3。在实例中,流体导管1可以是人或动物循环系统中的血管。超声换能器10被定位成沿可以横向于流体导管纵向轴线2的束轴线11引导超声激发能量并且可以如图1的实例中所示出的与流体导管纵向轴线2正交(即,束轴线11如所示出的在y轴线上,x轴线在图平面内)。优选地,换能器包括可以横向延伸以提供如图1中所示出的宽激发束12的换能器元件阵列,其中束的横向范围是沿着导管z轴线的。可替代地,换能器10可被取向成提供束跨流体导管1的宽度的横向范围,例如束宽度尺寸与流体导管的x轴线或y轴线对准。
超声换能器10生成包括被配置成沿z轴线对导管1的纵向位置或范围13进行采样并且沿x轴线对横向范围进行采样的激发信号的激发束12。沿z轴线的纵向范围13可以有效地被认为是束宽度。换能器10接收从其中生成一系列的图像帧的响应信号。每个图像帧的至少一部分表示体积元件15。体积元件15表示导管沿z轴线的有限区段,并且可以表示导管在x空间和y空间(与主要流动轴线正交)的一部分或可以表示通过导管的完整切片(即,在x和y之一或两者中的完整导管宽度)。在基础配置中,对是通过导管直径的完整切片和所陈述的导管沿z轴线的有限区段的体积元件进行散斑去相关(可以对应于束宽度),并且不考虑跨导管直径的流体速度的变化。
每个图像帧提供流动中的超声散射对象的空间图或与之有关的数据集,并且连续图像帧的相关性使得能够确定穿过体积元件15的所选对象的速度。例如,对象可以是通过人或动物循环系统中的动脉的血流中的红细胞、白细胞或血小板。例如,对象可以是血流内的微泡造影剂。更具体地说,对象可以是能够在超声图像中与接收到的超声回波信号区分的任何对象(如单个粒子或粒子团)。在一般方面,所有这些对象可以被描述为给出散斑或散斑图案。在wo2017/163030中所描述的技术中,体积元件15的第一图像中的可识别对象在体积元件的连续(例如,第二)图像中被识别以使用自相关方法来查看对象已经行进的距离,例如在所述方法中,使来自体积元件的数据沿z轴线纵向加窗,并且将沿z轴线的连续重叠窗口(z1、z2、z3等)与第一窗口(z0)进行比较以找到最大相关的z位置。自相关方法可以应用于对象组。在本文所描述的不同技术中,代替自相关方法,使用优选地以横向于流体流动方向的其束轴线定向的超声束对流体流动方向上的速度分量进行基于去相关的流体速度测量或流体速度分布测量。
在现有技术(如daewoopark等人,“基于超声相关的流动速度映射的定量和边缘速度梯度测量(quantificationofultrasoundcorrelation-basedflowvelocitymappingandedgevelocitygradientmeasurement)”,《超声医学杂志(jultrasoundmed)》,2013;32:1815-1830)中,已经描述了散斑去相关速度测量来研究血管壁处的血流速度梯度以评估血管壁剪切应力。发明人已经发现,此类技术可以有利地适于在本技术中用于确定波速和波强度,并且与先前描述的自相关技术相比提供许多潜在的优点。
在散斑去相关中,当引起超声信号中的散斑或散斑图案的粒子(如上所定义)行进通过超声成像体积元件15时,接收到的回波信号以一定速率随时间去相关,所述速率是粒子流动速度的函数。获取以短时间间隔分开的两个图像或数据集,并且计算出第一图像或数据集中的散射体的模式与第二图像或数据集中的散射体的图案之间的相关性。如果流体是静止的,则两个图像或数据集之间的相关性将高,例如在1.0处或附近。如果流体移动缓慢,则粒子(即,散射体)中的一些粒子(但并不多)将会移动到经过成像的体积15之外(被不同的粒子代替),并且相关性将不完美但仍然相当良好,例如介于0与1.0之间的中间。如果流体速度高,则在第一图像或数据集中所看到的大多数粒子将不再出现在第二图像或数据集中。因此,散射体的图案将非常不同并且相关性将低。本发明上下文中所使用的表达“图像”或“数据集”是指表示对应于粒子/散射体的散斑图案的空间位置/空间分布的任何数据集。如图3中示意性地示出的,发现去相关的程度与粒子速度近似成线性并且因此在相关系数值的有效范围31内与流体速度近似成线性,从而在某个点处达到最小值32。因此,去相关系数(1-(相关系数))证明可以提供流体速度的良好量度或替代物,条件是系统被限定于在线性范围31内进行操作。在其它研究中,已经发现这种相关系数近似于(半)高斯分布(如图3a中所见),其中相关系数仍证明可以提供流体速度的良好量度或替代物,条件是系统被限定于在高斯分布的更加线性的部分(例如,介于大约0.9与0.2之间)内进行操作。在图3a中,水平轴线表示与时间成正比并且因此与粒子速度成正比的帧号。
可以测量针对一个或多个体积元件15的去相关流动速度以获得如图1中所示出的特定横向(x和/或y)位置处的速度测量值、或跨x和/或y的流动速度分布或跨流体导管1中的所有x和/或y位置的平均流动速度。体积元件的z位置被选择成对应于在其处对导管直径或导管面积进行测量的z位置。为了获得最大流动速度测量值,可能期望使用定位在流体导管1的中央纵向轴线2附近的体积元件15。在本领域中已经观察到,在大约0.5mm的粒子移动之后,相关系数急剧且线性地从1.0减小到0.3(park等人)。在流动的所有层中已经观察到,作为粒子移动的函数的相关系数线性减小(即,在整个x和y中下降到0.3相关水平)。绘制作为散射体的深度的函数的相关系数(如图4所例示的)使得能够准确确定流体导管1中的每个横截面位置处的流动速度(如图4中所见,几种不同的流动速率(迹线40a、40b、40c、40d))。
绘制相关系数还使得能够通过参考作为超声反射深度的函数的相关系数的拐点41、42来准确确定导管直径d。可以例如基于速度分布的二阶梯度来使用适合的边缘检测算法。这可以与如本文所描述的用于确定导管直径的其它技术结合使用。
在本上下文中使用的散斑去相关方法可以提供优势,因为所述方法可以使用较小的空间窗口(即,在体积元件15的x、y和/或z维度中)并且可以在连续帧内执行相关,而粒子成像测速法技术在空间内执行相关,因此需要在z方向上延伸的较大的有效体积元件15(图1)。具体地说,粒子成像测速法技术通常需要在第一时间和第二时间处捕获体积元件的图像、沿流动或z维度将第二时间图像的体积划分为多个窗口、计算每个窗口与原始体积的自相关值并且找到最佳匹配。与上文所描述的散斑去相关技术相比,这具有相当大的计算负担。去相关技术可以通过沿线观察散射体的图案来实施(例如,在z上较小的体积元件15=例如,仅束宽度),而uiv需要提供大的粒子空间图的体积元件15。因此,散斑去相关技术可以潜在地在成本较低、帧速率较慢的机器上执行,例如因为每次只可以击发阵列的一部分。这可以大大提高临床实用性。
散斑去相关流动速度测量技术也可以更容易地被实施成生成跨血管横截面的流体速度分布。散斑去相关技术在测量流动所需的每秒扫描次数方面,的要求也可以较低,并且因此对所需的设备的成本和可用性的要求较低。潜在地,所述方法可以被简化成对跨流体导管的单条线进行成像。散斑去相关方法在通过去相关系数提供流体速度的直接量度或替代物中的计算强度也可以较低。与wo2017/163030的自相关技术相比,这可以潜在地根据较少的相关运算来获得,所述自相关技术可能需要对多个z位置处的体积元件15内的多个窗口进行比较以找到对应于由粒子行进的距离的最大相关值。相比之下,散斑去相关技术可能仅需要对两个帧进行比较以获得单个去相关量度。
在下文所描述的波速和波强度分析的上下文中,可以更容易地用去相关系数而不是相关系数来起作用。去相关系数可以被定义为:
去相关系数=1–相关系数。
因此对于下降到0.3的相关系数(即,高达大约1-0.3=0.7的去相关系数),去相关系数=常数×流体速度。
因此,返回参考上文所讨论的波强度方程,用去相关系数u'取代速度u,使得u'/u=常数。
在上文所给出的波速c的方程中:
用u'取代u,然后c变为例如c',其与真实c相差相同的常数因子(并且如果c'对临床意义的值变为已知,或者如果常数因子是已知的,则其可能仍然是有用的)。因此,可以将c'用作真实波速c的量度或替代物。
对于波强度,首先考虑如非侵入式地测量到的在任何时刻处的总强度(即,前向波和后向波之和)ndi,其为:
ndi=dddu。
同样,可以用u'代替u并且发现强度也已经通过相同的常数因子而变化。
最后,在上文已经给出的方程中考虑前向和后向波强度:
首先查看最后一个圆括号中的项,c乘以常数变为c'并且u乘以同一常数变为u'。因为一个是分母并且一个是同一个项中的分子,所以这些变化抵消。在最后的圆括号之前,u中没有项,并且“双分母”中(即,分子中)有c。c变为c',即,其乘以与之前相同的常数。因此,前向和后向波强度通过与总强度相同的因子而改变。因此,使用去相关系数u'作为流体速度量度可以得到波强度i'量度或前向和后向波强度ndi'±量度,其也是真实波强度i或ndi±的缩放版本。
这给出了波强度分析的内部一致的方法,其中所有值仅按常数因子缩放。这给出了在其中可以直接根据去相关系数(并且因此根据相关系数)加上直径测量值来获得有用的强度的系统,从而降低计算复杂性和所需资源。可替代地,散斑去相关系数可以与适合的校准数据一起使用以确定真实流体速度u而不是u',并且因此直接确定真实波速c和/或波强度i或ndi±。
尽管导管直径可以根据速度分布来确定但是所述导管直径也可以直接根据相同的超声数据来确定或超声换能器10也可以被配置成将单独的超声激发信号传输到导管1并且接收指示导管壁的位置16的对应的超声响应信号。可以使用连续测量来确定导管1在体积元件15的纵向位置/范围13处的直径d的变化,哪些测量在时间上与对应的对象速度测量相关。获得速度测量的换能器10和获得导管壁位置16的换能器可以包括相同的换能器头。在一种布置中,可以使用奇异值分解来将图像分裂成血液分量和根据其容易地获得壁位置的壁分量。
如先前所讨论的,在导管1中流动的流体经受压力波,如由心脏泵送动作、动脉弹性和动脉拓扑引起的那些压力波。此类压力波的波速度可以根据表达式c=0.5(du/dlnd)来确定,其中du是作为时间的函数的流体速度的变化,并且dlnd是作为时间的函数的d的自然对数的变化。表达“作为时间的函数”旨在涵盖通过以已知时间间隔(如单位时间间隔(例如,超声成像帧速率))或可变时间间隔或在所测量到的两种不同特性可以与共同时间点或时间间隔相关的时间处对相关特性进行连续测量以及对所述特性的第一时间导数进行瞬时测量所确定的任何变化。在优选的布置中,d和u是根据超声换能器10的帧速率周期性地确定的。在另一种布置中,du/dt和dlnd/dt可以用于确定波速(speed)或速度(velocity)。
体积元件15内的流体速度的变化可以例如使用散斑去相关技术通过在两个或更多个连续的时间处测量流体速度来确定。d的对数函数的变化可以通过在相同的两个或更多个连续的时间处根据超声响应信号测量直径来确定。
然后,波速度c可以通过直接计算这两个变化之比来确定。可替代地,可针对某一采样周期确定流体速度的变化率du/dt,并且可针对对应的但并不一定相同的采样周期确定导管直径对数函数的变化率dlnd/dt。采样周期优选地是共同延伸的、重叠的或连续的,但是在任何情况下在时间上都足够接近使得测量到的流体速度的变化与测量到的导管直径的变化在时间上相关。
流体速度可以表示为体积元件15的平均流体速度。如先前所陈述的,体积元件可以包括导管直径的完整横截面并且平均流体速度可以因此为跨导管直径的平均速度。
用于导出流体速度和导管直径两者的超声响应信号可以包括m模式或b模式数据。m模式或b模式数据可以包括可以从其导出m模式或b模式图像的rf数据,并且流体速度和导管直径可以直接根据rf数据来确定。b模式图像数据可以包括b模式图像。可以获取用于导出流体速度和导管直径两者的超声响应信号作为对共同超声激发信号的响应。用于导出流体速度和导管直径两者的超声响应信号可以包括b模式数据。导管直径可以用与b模式图像所需的换能器元件相比较少的换能器元件(甚至可以降低到更频繁使用的(例如,m模式)单个换能器元件)来获得,。这可以与用于获得速度的完整b模式成像交错。使用m模式可以给出作为时间的函数的直径的更加准确的量度。
对于在人或动物循环系统中进行的测量,流体速度和导管直径可以在每个心动周期期间的多个时间处确定。然后,波速度可以在每个心动周期期间的多个时间处确定和/或波速度可以仅在每个心动周期期间的所选时间处确定。波速度可以在前向波在纵向位置13处占主导的心动周期中的某一点处确定。
根据波速度的测量,可以得出体积元件15的纵向位置13处的流体导管壁弹性的量度。
在替代性布置中,波速度可以根据略微不同的方法来计算。用于确定在导管1的纵向位置13处的作为时间的函数的导管直径d的超声数据可以用于计算作为时间的函数的导管的横截面面积a。用于确定在导管1的纵向位置13处的体积元件15中的作为时间的函数的流体速度的超声测量可以用于计算作为时间的函数的的通过导管的总体流动速率q。再次,表达“作为时间的函数”旨在涵盖通过以已知时间间隔(如单位时间间隔)或可变时间间隔或在所测量到的两种不同特性可以与共同时间点或时间间隔相关的时间处对相关特性(例如,q或a)进行连续测量以及对所述特性的第一时间导数进行瞬时测量所确定的任何变化。在优选的布置中,q和a是根据超声换能器10的帧速率周期性地确定的。测量q和a可以通过假设径向对称根据速度测量u和直径测量d来确定。可替代地,可以用一些最近的3d超声系统来直接获得q和a。在具有跨血管或导管的b模式成像的情况下,流动速率q和面积a将易于计算,并且无需根据单个直径测量进行工作,尽管如果使用m模式或b模式图像中的横截面的一部分可能需要这样做。不需要3d模式。
然后,可以根据流动速率的变化与导管的横截面面积的对应变化之比来确定波速度c,例如c=dq/da。通过导管的流动速率的变化可以基于连续的流体速度测量和导管直径测量。导管的横截面面积的变化可以基于连续的导管直径测量。
因此,波速度c还可以根据流体速度的变化与导管的横截面面积的对应变化之比来确定,例如使用[52]中概述的关系:
c=adu/da=du/dlna,
其中a是横截面面积,da是横截面面积的变化,并且du是流动速度的变化。可以理解的是,如果面积变化与速度变化相比可忽略不计,则c=dq/da表达式[53]将等同于c=adu/da。否则,所述表达式仅大致相同。
由于a和a的变化可以根据d的超声测量来确定,因此这可以被视为导管直径的变化的函数。因此,在一般方面,波速可以根据(i)作为时间的函数的在纵向位置处的流体速度的变化和(ii)作为时间的函数的导管直径的变化的函数来确定,或者波速可以根据作为时间的函数的在纵向位置处的流动速率的变化与作为时间的函数的导管横截面面积的变化之比来确定。应当理解的是,在这种背景下,具有圆形横截面的导管中的横截面面积的变化的量度可以容易地从横截面直径的变化的量度获得。还应当理解的是,对于具有例如非圆形横截面的导管,对直径的多次测量(围绕导管纵向轴线以不同角度)或多次弦测量(可以包含或不包含穿过导管的中心的线的在严格的数学意义上的“直径”)可以用于确定横截面面积并且因此确定横截面面积的变化。
还可以根据如上文所描述的超声测量以及具体地根据所确定的导管直径和流体速度来计算出波强度量度。波强度量度可以是根据以下方程确定的:
其中ndi+是如从非侵入式测量导出的前向波强度,ndi-是如从非侵入式测量导出的后向波强度;d是导管直径;dd是导管直径的变化;c是波速;du是流体速度的对应变化。
还可根据方程ndi=dddu来确定波强度量度,其中ndi是如根据非侵入式测量确定的波强度;dd是导管直径的变化;并且du是流体速度的对应变化。
还可以通过对一段时间内的波强度ndi求积分来确定波能量i量度。所述一段时间可以是从波的开始到波的结束和/或是心动周期的预定部分。确定波能量i对于低强度的持久波可以是有用的。
根据纵向位置13处的波强度量度,可以确定心脏的性能量度。通过对心动周期进行适合的分析(例如通过对反射的分析),尤其是通过计算经过反射的波的强度、反射系数和到反射位点的距离,还可以确定在纵向位置处以及纵向位置13的上游和下游两者的流体导管壁刚度和横截面特性的量度。横截面特性可以包含如壁刚度、壁厚度、血管横截面面积、分支、分叉、壁特性的病理学改变等特性。
体积元件15的纵向范围13可以是提供足够的空间分辨率用于确定流体速度和导管直径或导管横截面面积的任何尺寸,以便实现在必要的空间分辨率下对波速或波强度的确定。实际上,影响流体速度的脉冲的波长可以相当长(例如,超过一米的量级),并且因此体积元件15的纵向范围13可以是厘米量级,条件是可以针对散斑去相关解决散射体移动。
尽管图1的布置示出有被定向成生成具有与流体流动轴线2(z-轴线)正交的束轴线11的激发束12的换能器头10,但是可替代地,只要换能器头10能够基于沿z-轴线的移动分辨散斑去相关并且(如果需要)能够根据同一束确定导管直径或导管横截面面积,所述换能器头就可以被定向成使得束轴线11与流体流动轴线(z-轴线)斜交。类似地,只要换能器头10能够基于沿所述轴线的移动解决散斑去相关并且(如果需要)能够根据同一光束在合适的z位置处确定导管直径或导管横截面面积,所述换能器头就可以被定位在身体外部的位置处与流体流动轴线(z-轴线)同轴。在此类布置中,超声换能器10可以选择如从沿z轴线或与z轴线斜交观察到的选择体积元件15的成像深度。如前所述,体积元件15表示导管沿z-轴线的有限区段,并且可以表示导管在x空间和y空间中的一部分,或者可以代表穿过导管的完整切片(即,导管在x和y之一或两者中的完整宽度)。
参考图2,描述了用于确定波速度、波强度和波能量的示例性设备。
超声换能器10耦接到超声系统模块20。激发模块21或驱动器向换能器10提供信号22以产生用于对流体导管1进行声照射的超声激发信号,特别适于生成来自如图1中所见的流体导管1的纵向位置13处的所选的体积元件15的响应信号。来自换能器10的响应信号23传递到散斑去相关分析模块24和几何结构分析模块25。散斑去相关分析模块24被配置成使用如上文所描述的散斑去相关技术确定连续的流体速度测量(即,确定作为时间的函数的流体速度)。散斑去相关分析模块24还可以或替代地被配置成计算还如上文所讨论的作为时间的函数的通过导管的总体流动速率q。几何结构分析模块25被配置成使用如上文所描述的技术确定连续的导管直径测量(即,确定从来自导管壁的超声响应信号导出的作为时间的函数的导管直径)。几何结构分析模块25还可以被配置成根据连续的直径测量确定导管的连续的横截面面积测量。
作为时间的函数的流体速度和作为时间的函数的导管直径的测量传递到波速度分析模块26和/或波强度分析模块27。
波速度分析模块26被配置成使用如上文所描述的技术在导管的纵向位置13处根据以下中的任一个确定波速度:(i)流体速度的变化与导管直径的对数函数的对应变化之比或(ii)流动速率的变化与导管横截面面积的变化之比。
波强度分析模块27被配置成使用如上文所描述的技术确定作为导管直径的变化和流体速度的对应变化的函数的波强度。
如上文所描述的各个模块(例如,散斑去相关分析模块24、几何结构分析模块25、波速度分析模块26和波强度分析模块27)可以包括被适合地配置成执行所描述的操作的任何一个或多个硬件、固件或软件模块或其组合。功能可以在一个或多个模块内保持分离或组合,例如包含由适合地编程的通用计算机系统实施的功能。
最近已经开发了用于医学应用的超快超声成像系统。所述超快超声成像系统对所有换能器元件进行波束赋形并且并行地而不是逐行地从所述所有换能器元件获取数据,从而产生比常规扫描仪高两个数量级的帧速率。所述技术很可能形成下一代临床扫描仪的基础。出于我们的目的,大幅提高的帧速率使得能够更加准确地跟踪动脉中发生的流量和直径的快速变化,并且其还通过允许对重复测量进行平均降低了信噪比,甚至同时满足严格的时间分辨率要求,。任选地,这些超快超声成像系统可以用于执行如上文所描述的散斑去相关技术。
图2的超声系统模块20可以进一步适于包含实时图形用户界面28,所述实时图形用户界面示出当前的b模式图像和对来自散斑去相关流动测速法的速度的初步估计,从而允许用户选择区域进行分析。此外,通过例如允许超声束中的相位变化或在频域中工作或针对灵敏度的深度方面变化进行调整来评估相关性的更加复杂的算法可以是有利的。
系统模块20可以进一步包含用于监测动脉直径的半自动回声跟踪方法。首先,可以例如使用界面28手动标记上导管壁和下导管壁的腔表面的位置。然后,可以使用rf信号的互相关来跟踪所述腔表面的位置并且因此获得导管直径d的变化。
可以针对准确度和精度对成像和散斑去相关变量(如平面波转向角和散斑去相关窗口大小)进行优化。可以合并rf数据滤波以优化用于进行散斑去相关速度测量的超声信号。在其最基本的形式中,散斑去相关测量不固有地提供流体速度的方向。然而,在需要的情况下,在许多或大部分实例中,流体流动方向将可根据其它感测到的参数(例如,通过测量出的流体速度在其经过零时的的时间变化和对心动周期的了解)推导出或检测到。可替代地,将可以使测量限制在作为流体导管的动脉的流动在其中将更加一致地前向行进的中心区域,或结合散斑去相关技术使用另外的(例如,不成熟的)多普勒超声方法。
出于波反射的效应而校正pwv的最近描述的因素[27]可以结合到系统模块20的控制软件中。
来自系统的所有数据可以传输到数据库29以进行进一步处理。波速度分析模块26和/或波强度分析模块27可以提供为单独的设备,例如用于进行离线处理和计算波速、强度和来自捕获到数据库29的数据的反射。
系统20可以用于使用所描述的非侵入式技术通过监测在心力衰竭患者中改变的波强度的变化来检测人和动物的循环异常。
对内皮功能的评估:已经注意到,具有血管扩张效力的一氧化氮(no)改变压力波或体积波中的重搏切迹(收缩峰值和舒张峰值之间的拐点)的高度。刺激no释放的物质(如乙酰胆碱(ach))降低重搏切迹的高度。抑制no产生的物质(如l-name)相对于波的整体振幅增加重搏切迹的高度。已经示出,这些变化相当特定于no(以及相关的硝基血管扩张剂);这些变化未反映出血管活性剂对外周肤色、血压或心率的一般影响。如图4所展示的,效应可能由于变化的波反射而产生。系统20可以被部署成确定no对波反射的效应。
系统20可以用于检测临床前模型中的心力衰竭、年龄有关的动脉硬化和no依赖性波反射。
用于分析脉搏波的传统方法基于傅立叶分析。结果是在频域中的,这使得难以将所述结果与临床意义的任何特征联系起来。相比之下,波强度分析使波概念化为由在特定时间以已知强度正向或反向行进的无限小的波前构成。以此方式,对脉搏波的击穿使得更容易将所述脉搏波的特征与真实的心脏和血管特性联系起来。
wia可以在评估冠状动脉狭窄的功能意义并且因此确定是否需要干预的程序中使用。wia识别出心动周期期间的自然无波时段。在此类点处,狭窄的上游的压力与狭窄的下游的压力之比可以用于评估所述狭窄引起的阻力。在常规程序中,此些时段未被识别出并且可能必须通过施用血管舒张药物来消除波,这是耗时的、昂贵的、令患者感到不适的并且在一些患者组中是不可行的。本文所描述的技术可以提供无需导液管插入的非侵入式方法。
所述系统可以用于研究心力衰竭。curtiss等人[1]将正常受试者与患有代偿性收缩性心力衰竭的患者进行了比较。在患者中,重新反射的膨胀波(x波)中的能量降低了80%。有趣的是,基于眼压测量法的增强指数(不基于wia的假设的波反射量度)没有变化。takaya等人[37]在运动测试(被接受的用于预测存活的方法)下检查了射血分数正常的患有慢性心力衰竭的患者。经胸超声心动图参数不与任何运动参数显著相关,但是正向膨胀波(w2)的强度与所有运动参数显著相关,这暗示这种简单的非侵入式量度将更好地预测结果。vriz等人[38]对患有心力衰竭且射血分数降低的患者进行了纵向研究,将波参数与左心室功能的超声心动图指标进行了比较。平均随访>3年。在逐步反向多元回归上,只有波参数-w2的强度-是结果的独立预测因子。li和guo[39]评估了wia在区分非阻塞性肥厚型心肌病(nohcm)和继发于高血压的左心室肥厚(lvhsh)中的价值。他们检查了正向行进压缩波(w1)和膨胀波(w2)以及由外围反射产生的负波强度(na)的面积。nohcm中的w2低于lvhsh和正常受试者中的w2。lvhsh中的na高于nohcm和正常受试者中的na。波强度参数在很大程度上不同于经胸回波参数:在nohcm组与lvhsh组之间,w2相差3倍,na几乎相差2倍,而最大的tte变化约为40%。因此,wia有可能对区分不同类型的心力衰竭是有用的。siniawski等人[40]检查了患有末期扩张型心肌病并且等待移植的患者。执行了单变量逻辑回归分析以评估wia的预测值、最大摄氧量(vo2max)、侵入性评估的压力和搏出量以及超声心动图测量的射血分数。事件的最强预测因子是波强度的第一峰值。实际上,只有基于波参数才可以区分两组,这再次表明wia将预测结果。
对测量动脉僵硬度或作为替代的pwv的临床需求是众所周知的-其已得到频繁审查并且是来自专家组的共识或政策文件的主题[41,42]。上文呈现了估计全局pwv的困难和缺点。出于临床目的而评估局部壁刚度引起很多关注并且许多制造商已经因此设计出用于这样做的非侵入式方法。这些方法基于回声跟踪-所述这些方法使用超声来测量动脉直径在心动周期内的变化。为了获得壁刚度,还需要知道局部的收缩压和舒张压。不幸的是,这使得回到上文针对压平眼压测量法所讨论的问题。相比之下,在本文所描述的方法中,局部pwv根据u和d的测量来获得-不需要压力-并且来自可以通过超声成像的所有血管(包含主动脉的实质区段)的测量是可行的。
本文所描述的方法可以通过其对波反射的影响来用于诊断内皮功能障碍。内皮功能障碍-主要以no生物利用度降低为特征-是心血管疾病的强大的风险因素,但很少被评估。这是不幸的,因为许多生活方式的改变已经示出对内皮功能的改善。几种药理学方法还正在研究中[43,44]。这很有可能反映测量此类功能障碍的技术挑战。至少在研究背景下接近接受的唯一方法涉及引起血流介导的扩张:将闭塞性袖带置于前臂周围,充气到收缩压以上持续几分钟,然后释放。反应性充血引起的流量增加增加了肱动脉内皮上的血液动力学剪切应力,从而导致no释放和血管的扩张。直径的增加是根据超声图像评估的[45]。尽管此量度与心血管风险有关[46],但是仍然存在许多技术问题:基线直径的标准化方法引入假像[47];袖带位置、闭塞的持续时间和测量的定时似乎很关键,并且其中一些对no的依赖性是值得怀疑的[48];反应性充血的程度存在个体差异,但是使剪切应力正常化似乎引起另外的问题[49];并且存在需要通过用千分尺可调节的立体定向设备来保持探针而最小化的很大的操作员强依赖性[48]。在本文所描述的方法中,内皮功能可以根据no对脉搏波而不是仅对直径的效应来评估。
当前的超快超声系统可以分辨下至100微米,这对于获得dd项的足够的准确度绰绰有余。此外,此种系统的速度(>1000帧/秒)足以“冻结”在心动周期期间移动的血管的运动。迄今为止,信噪比已经是可接受的并且微泡造影剂可以用于例如通过对微泡发射出的非线性信号和组织发出的线性信号进行区分来进一步改善信噪比。
图5展示了与现有的多普勒技术相比,使用本文所描述的散斑去相关技术进行的血流速度测量。图5a示出了通过“金标准”多普勒方法非侵入式地测量的血流速度(上),图5b示出了通过散斑去相关技术测量的血流速度。两种测量均在同一只经过麻醉的兔子的腹主动脉中进行。示出了三个心跳的数据。由于多普勒系统和b模式系统冲突,因此测量在不同时间处进行。在主峰的两个面板中看到了类似的图案。收缩晚期和舒张晚期期间存在差异,部分可能是因为在这些时期期间存在前向行进的流动和后向行进的流动两者的区域;多普勒方法考虑流动方向,但是散斑去相关方法没有考虑。这对于临床应用而言不是问题,因为(a)测量可以在很少有或没有后向流动的颈动脉中进行,并且(b)感兴趣的两个波强度峰值在心动周期中出现较早(在流动的最大加速和减速期间),其中两种方法给出相同的结果。增加的采样率可以进一步减小上文所提到的差异。错误在心动周期的对诊断心力衰竭感兴趣的一部分(对应于压缩波和膨胀波的峰值的流动的最大加速和减速)之后发生。可以通过滤波和平均化来消除图5b的散斑去相关数据中的噪声。未使用造影剂。
图6展示了与超声图像测速法(uiv)相比,使用本文所描述的散斑去相关技术进行的血流速度测量,从而示出了全面的比较。散斑去相关结果的数据是用与正交于流体导管纵向轴线2(z-轴线)并且具有沿z轴线的束的束宽度尺寸或横向范围的其束轴线11对准的换能器头获取的,。
确定波速和/或确定波强度的方法通常应用于任何非刚性流体导管系统中,特别是在在系统的至少一部分中的壁中展现出弹性行为的系统内。表达“导管”涵盖可以具有变化的直径和横截面轮廓、可以是支化的并且可以具有连接到其的腔室的管和管道。通常,所描述的技术可以应用于对超声具有足够的透明度以使得能够对导管内的流体的流动的连续超声帧中的对象的去相关进行定量测量的任何弹性有壁流体导管中。所述技术可以通常适用于在其中压缩波/减压波可能例如由于系统内的阀门的操作而在流体导管内出现的系统。
上文所描述的用于确定波速、波强度和/或波能量的方程可以被修改用于更准确地考虑系统的其它可测量特性,如流体介质(例如,血液)的粘度、导管壁的粘弹性和其它非线性效应。在一种方法[57]中,这可以通过在沿导管的第二位点处对d或u进行另外的测量(或等效地对a或q进行另外的测量)来实现。用于确定波速的方程可以例如使用如psegers等人[27]导出的校正因子来被修改成将反射纳入考虑。
波强度分析技术(如在本公开中所使用的那些波强度分析技术)可以通过减去“韦德克瑟尔(windkessel)”效应(即,减去由注满血液的弹性血管而不是由波引起的压力[56])来改善,。
用于计算波速的其它方法
使用压力和速度,波速常规地被计算为
c=(1/rho)(dp/du)
其中rho(ρ)是流体密度。当反射可以被认为是可忽略的时,所述方法和本文档先前所示例的那些方法可以在收缩早期使用。
当波不是单向的时,波速还可以使用“平方和”方法来计算[54]:
c=(1/rho)[(σdp2)/(σdu2)]0.5
其中σ是心动周期内的总和。
可以将这个方程转换为基于a(横截面面积)和d(导管直径)的方程,如
c=0.5[(σdu2)/σdlnd2)]0.5
从而还落入(i)作为时间的函数的在纵向位置处的流体速度的变化和(ii)作为时间的函数的导管直径的变化的函数的一般范围内。
其它实施例有意地在所附权利要求的范围内。
参考文献列表
[1]curtis,s等人,《美国生理学杂志:心脏与循环生理学(amjphysiolheartcircphysiol)》2007,293:h557。[2]sugawara,m等人,《医学和生物工程与计算(medbiolengcomput)》2009,47:197。[3]avolio,ap等人,《循环(circulation)》1985,1985:202。[4]laurent,s等人,《欧洲心脏病学杂志(eurheartj)》2006,27:2588。[5]vanpopele,nm等人,《中风(stroke)》2001,32:454。[6]manistyc等人,《美国心脏病学会杂志(jamcollcardiol)》2010,56:24。[7]manisty,ch等人,《高血压(hypertension)》2009,54:724。[8]bradlow,wm等人,《磁共振成像杂志(j.magn.reson.imaging)》2007,25:974。[9]taviani,v等人,《医学磁共振(magnresonmed)》2011,65:261。[10]o'rourke,mf等人,《美国高血压杂志(amjhypertens)》2002,15:426。[11]tsai,w-c等人,《美国高血压杂志》2013,26:770。[12]khiraw等人,《生物力学杂志(jbiomech)》2001,34;1145。[13]parker,kh等人,《心脏血管(heartvessels)》1988,4:241。14http://www.bg.ic.ac.uk/research/k.parker/wave_intensity_web/welcome.html[15]senss等人,《美国心脏病学会杂志》2012,59:1392。[16]beulen,bw等人,《医学和生物学超声(ultrasoundmedbiol)》2011,37:788。[17]feng,j等人,《生物力学杂志》2010,43:455。[18]biglinog等人,《国际人造器官杂志(intjartiforgans.)》2012,35:15。[19]kolyvac等人,《人造器官(artiforgans.)》2012,36:e62。[20]li,y等人,《ieee工程医学和生物学院刊(procieeeengmedbiol)》,2010,2010:5153。[27]segersp等人,《生理学测量(physiolmeas.)》2014,35:847。[28]sardarlou,m.,《动脉波形和内皮功能的非侵入式评估(non-invasiveassessmentofarterialwavespeedandendothelialfunction)》,博士论文,帝国理工学院2013。[29]liy,khiraw.《生物力学期刊》2011,44:1393。[30]alastrueyj等人,《国际生物医学工程的数值方法杂志(intjnumermethodbiomedeng.)》2014,30:249。[31]mehrad,h等人,《医学和生物学超声》2012,38:1391。[32]lee,sc等人,《美国心脏病学会杂志:心血管影像(jamcollcardiolimg)》2010,3:1265。[33]arnolda,l等人,《心血管研究(cardiovascres)》1985,19:378。[34]weinbergpd等人,《英国药理学杂志(brjpharmacol)》2001,133:361。[35]nier,ba等人,《实验生理学(expphysiol)》2008,93:503。[36]morikaway.,《自然(nature)》1967,213(5078):841。[37]takayay等人,《心脏血管(heartvessels)》2013,28:179。[38]vrizo等人,《国际心血管成像杂志(intjcardiovascimaging)》2015,31:1369。[39]liy,guol,《临床超声杂志(jclinultrasound)》2013,41:151。[40]siniawskih等人,《基础与应用物理学杂志(jbasicapplphysics)》2013,2:95。[41]townsendrr等人,《高血压》2015,66:698。[42]laurents等人,《欧洲心脏病学杂志》2006,27:2588。[43]wangq等人,《基于证据的补充和替代医学(evidbasedcomplementalternatmed.)》2014,2014:850312。[44]
- 还没有人留言评论。精彩留言会获得点赞!