细胞毒性药物的结合物和所述结合物的前体药物形式的制作方法
本发明涉及用于治疗癌症和炎性疾病的细胞毒性药物的特定结合物和所述结合物的前体药物形式。
背景技术:
癌症和炎性疾病是当今最常见的疾病。具体来说,癌症是工业化国家中最重要的死亡原因之一,目前被诊断出患有癌症的人数持续增长
迄今为止已经开发出几种治疗方式,然而化学疗法仍然是唯一可用于对抗循环肿瘤例如淋巴瘤和白血病以及转移肿瘤的疗法。
在化学疗法中,一种策略在于抑制微管蛋白的聚合并因此阻止细胞分裂(抗有丝分裂剂)。这可以通过使用尾海兔素(dolastatin)家族的化合物,特别是天然尾海兔素10来实现,所述化合物可以从印度洋海兔dolabellaauricularia中分离,由四个氨基酸构成,其中三个是其特有的。尾海兔素10的合成衍生物例如奥瑞他汀(auristatin)pe、奥瑞他汀e和单甲基奥瑞他汀e(mmae)也已存在,并被证明是有效的抑制剂。这些化合物的主要缺陷在于缺乏对癌细胞的选择性,导致健康组织的破坏和由此严重的副作用,例如脱发或恶心。这些活性药剂的蛋白质-药物结合物的开发,已成为克服选择性缺乏的一种简洁有效的策略。
蛋白质-药物结合物是迄今为止增长最快的一类高效活性药物成分。蛋白质-药物结合物构建物通常包含共价附连到连接物基团一端的蛋白质例如抗体,所述连接物基团的另一端是细胞毒素,即高效灭杀细胞的毒素。所述生物分子的蛋白质组分提供靶特异性。一旦所述结合物进入细胞后,所述毒素通过例如细胞酶的作用而被释放。事实上,大多数蛋白质-药物结合物都针对癌症治疗。除了市售的曲妥珠单抗-emtansine(被称为t-dm1或
这些结合物的活性的主要先决条件之一是在被癌细胞内化后细胞毒性药物的高效释放,而所述蛋白质与药物之间的连接物,在所述连接物到达其生物靶之前在血液循环中应该是稳定的。
在这个方面,通过将可被酶切割的连接物引入到结合物构建中,实现了真正的突破。
因此,wo2015/118497描述了式(i)的β-葡萄糖醛酸酶响应性白蛋白结合型结合物,
其中a通常是mmae。它的马来酰亚胺末端组成部分旨在用于在静脉内给药后提供与循环白蛋白的选择性结合。对葡萄糖醛酸酶敏感的葡萄糖醛酸苷组成部分也存在于所述分子中,并被连接到自反应臂。由于白蛋白在肿瘤中积累并且β-葡萄糖醛酸酶存在于肿瘤环境中,因此所述化合物到达肿瘤部位,在那里所述酶催化所述糖苷键的切割,然后引发药物(mmae)的释放。所述结合物作为两种异构体的1:1混合物存在,其可变立体中心在所述自反应臂上(在式(i)上用星号标注)。
技术实现要素:
本发明人证实,上述结合物的两种异构体,它们不能利用常规技术分离,可以从前期中间体的hplc对映异构体分离来获得。所述两种分离的异构体被证明是稳定的,特别是在人类血浆中,但可变立体中心具有r构型的异构体与另一者相比表现出更高的酶切割动力学。从一种异构体观察到的这种更高的动力学更加出人意料,因为所述立体中心不是被所述酶识别的药效团的一部分。这个出人意料的特点对于具有较低酶表达的患者可能特别有利。
本发明人还已经证明,将自毁性组成部分插入到所述结构中,更具体来说插入到所述细胞毒性药物与所述结合物的其余部分之间,可以提高所述结合物的稳定性,同时保持其被切割(即释放细胞毒性药物)的能力。
本发明涉及的所述异构体是由式(i)及其可药用盐表示的结合物:
其中:
a表示源自于细胞毒性药物的原子团,
g是自毁性组成部分,并且
m是0或1。
本发明还提供了一种制备如上所定义的结合物的方法,所述方法包括下述步骤:
a)从4-羟基-3-硝基苯甲醛制备消旋-4-(1-羟基丁-3-炔-1-基)-2-硝基-苯酚;
b)优选地通过手性高效液相色谱,分离(r)-4-(1-羟基丁-3-炔-1-基)-2-硝基-苯酚;
c)将(r)-4-(1-羟基丁-3-炔-1-基)-2-硝基-苯酚与葡萄糖醛酸衍生物例如乙酰溴代-α-d-葡萄糖醛酸甲酯在碱性条件下反应;
d)将在步骤(c)中获得的化合物与氯代甲酸4-硝基苯基酯反应;
e)将在步骤(d)中获得的化合物与细胞毒性药物或与a-g-h组成部分结合,其中a表示源自于细胞毒性药物的原子团,并且g表示自毁性组成部分;
f)将在步骤(e)中获得的化合物的葡萄糖醛酸苷组成部分去保护,优选地在碱性条件下去保护;并且
g)将在步骤(f)中获得的化合物与式n3-(ch2-ch2-o)10-(ch2)2-nh-(co)-(ch2)5-x的叠氮化物结合,其中x是马来酰亚胺基团。
本发明还涉及一种前体药物,其包含如上所定义的结合物的至少一个分子,所述结合物的分子通过共价键连接到蛋白质分子或其片段或衍生物,所述蛋白质分子优选为白蛋白。
本发明还涉及一种药物组合物,其至少包含有效量的至少一种如上所定义的结合物或至少一种如上所定义的前体药物,以及可药用载体。
本发明还独立地涉及如上所定义的结合物、如上所定义的前体药物或如上所定义的药物组合物用于治疗癌症和/或炎性疾病。
附图说明
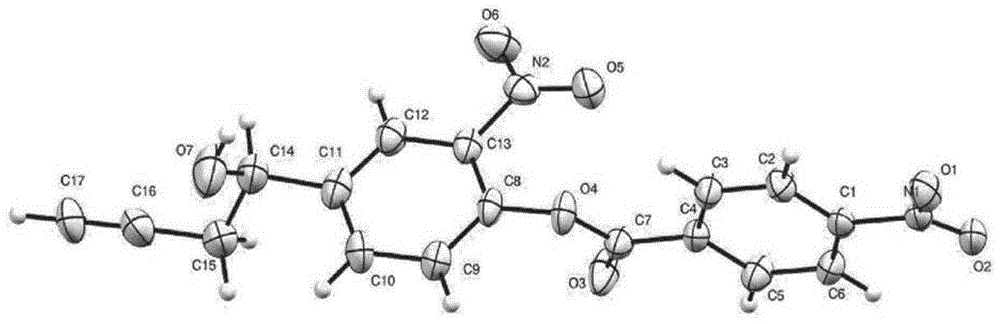
图1示出了化合物r1a的来自于x-射线晶体学的分子结构。位移椭球以50%的概率水平画出。
图2示出了在化合物r5和s5的血浆溶液中β-葡萄糖醛酸酶诱导的mmae释放的动力学。
图3示出了在化合物r6和s6的血浆溶液中β-葡萄糖醛酸酶诱导的mmaf释放的动力学。
图4示出了在化合物r7和s7的血浆溶液中β-葡萄糖醛酸酶诱导的sn-38释放的动力学。
图5示出了在化合物r8和s8的血浆溶液中β-葡萄糖醛酸酶诱导的多柔比星释放的动力学。
图6示出了化合物r5和s5在ph7.4的pbs中的稳定性。
图7示出了化合物r5和s5的血浆结合动力学。
图8示出了白蛋白结合的r5和s5的血浆稳定性。
图9示出了r5与s5的1:1混合物的hplc图谱。
图10示出了r4与s4的1:1混合物的hplc图谱。
发明详述
结合物
本发明涉及一种具有下述式(i)的结合物:
其中:
a表示源自于细胞毒性药物的原子团,
g是自毁性组成部分,并且
m是0或1,
及其可药用盐。
在本发明的情形中,“可药用盐”是指本发明的结合物或前体药物或药物与碱金属、碱土金属或铵的盐,包括使用有机铵碱获得的盐,或本发明的结合物或前体药物或药物与有机酸或无机酸的盐。
更特别适合于本发明的盐可以是钠盐、钾盐、钙盐、镁盐、季铵盐例如四甲基铵或四乙基铵,以及与氨和可药用有机胺例如甲胺、二甲胺、三甲胺、乙胺、三乙胺、乙醇胺或三(2-羟基乙基)胺的加成盐。
本发明的结合物或前体药物或药物与适合于本发明的无机酸的盐,可以使用盐酸、氢溴酸、硫酸、硝酸或磷酸来获得。
本发明的结合物或前体药物或药物与适合于本发明的有机酸的盐,可以使用羧酸和磺酸例如甲酸、乙酸、草酸、柠檬酸、乳酸、苹果酸、琥珀酸、丙二酸、苯甲酸、马来酸、延胡索酸、酒石酸、甲磺酸、苯磺酸或对甲苯磺酸来获得。
根据本发明,“自毁性组成部分”表示将所述源自于细胞毒性药物的原子团与所述结合物的其余部分相连的二价化学基团,并且其在活化(例如葡萄糖醛酸苷残基的酶切割)后变得不稳定,导致游离组成部分、特别是所述细胞毒性药物的释放。自毁性组成部分对于专业技术人员来说是公知的(polym.chem.2011,2,773-790)。
在一个实施方式中,m是0。
在另一个实施方式中,m是1,并且g由选自下述的结构式表示:
在优选实施方式中,g由下述结构式表示:
根据本发明,“源自于细胞毒性药物的原子团”表示由细胞毒性药物构成的组成部分,其已被剥夺其与所述结合物的其余部分反应的官能团之一的一个或多个原子(例如h原子)。
本发明所述的药物是细胞毒性药物。当在本文中使用时,术语“细胞毒性药物”是指当与细胞相接触时,任选地在内化到所述细胞内后,以有害方式改变细胞功能(例如细胞生长和/或增殖和/或分化和/或代谢例如蛋白质和/或dna合成)或导致细胞死亡的分子。当在本文中使用时,术语“细胞毒性药物”涵盖毒素,特别是细胞毒素。原则上,细胞毒性药物被定义为lo1atc分子(“解剖学治疗化学分类系统”(anatomicaltherapeuticchemicalclassificationsystem),其中lo1是定义了抗肿瘤药和免疫调节剂的亚组,其由who药物统计方法学合作中心(whocollaboratingcentrefordrugstatisticsmethodology)定义)。
本发明所述的细胞毒性药物可以选自尾海兔素例如尾海兔素10、尾海兔素15、奥瑞他汀e、奥瑞他汀eb(aeb)、奥瑞他汀efp(aefp)、单甲基奥瑞他汀f(mmaf)、单甲基奥瑞他汀-d(mmad)、单甲基奥瑞他汀e(mmae)、5-苯甲酰基戊酸-ae酯(aevb)或其衍生物。
优选的尾海兔素是mmaf、mmad、mmae或其衍生物。
更优选的尾海兔素是mmae、mmaf或其衍生物。
在特定实施方式中,根据本发明所述的细胞毒性药物是蒽环类化合物例如多柔比星、伊达比星、表柔比星、柔红霉素或戊柔比星,优选为多柔比星。
在另一个特定实施方式中,本发明所述的细胞毒性药物是喜树碱家族的药物(在本文中也被称为“喜树碱类似物”),例如喜树碱、sn-38、拓扑替康、伊立替康、依喜替康、silatecan、cositecan、勒托替康、吉马替康、贝洛替康或鲁比替康,优选为sn-38、依喜替康、贝洛替康,更优选为sn-38。
在优选实施方式中,所述细胞毒性药物选自多柔比星、sn-38、mmae、mmaf、mmad及其衍生物。
尾海兔素是具有至少4个氨基酸、优选具有4个氨基酸的结构的一类化合物,所述氨基酸中的至少3个是其特有的,因为不同于通常天然发现的20种氨基酸。根据本发明,尾海兔素的衍生物具有与尾海兔素家族的至少一种化合物非常相关的化学结构,并表现出相似的抗有丝分裂性质。所述衍生物与尾海兔素家族的化合物之间的结构差异可能在于在至少一个氨基酸的至少一个侧链上被任何适合的通常发现的取代基取代。例如,所述取代基可以是:
-烷基,即直链或支链饱和烃链,例如甲基、乙基、丙基、异丙基、丁基、仲丁基、叔丁基、戊基、己基、庚基、辛基、壬基或癸基;
-杂烷基,即被一个或多个杂原子、主要是o、n和s间断的直链或支链烃链,例如甲氧基或乙氧基;
-芳基,即芳香族碳环基团,例如苯基或萘基,其可以任选地被多达4个基团取代,所述基团包括但不限于:-cooh,-so3h,-och3,-f,-cl,-br,-i,-oh,-nh2,-no2,-cn;
-杂芳基,即含有一个或多个杂原子的芳香族基团,例如吡啶基、噁唑基、呋喃基或噻唑基;或
-卤素原子,例如-f、-cl、-br、-i。
所述结构差异也可以由尾海兔素例如尾海兔素10、尾海兔素15、奥瑞他汀e、奥瑞他汀eb(aeb)、奥瑞他汀efp(aefp)、单甲基奥瑞他汀f(mmaf)、单甲基奥瑞他汀-d(mmad)、单甲基奥瑞他汀e(mmae)或5-苯甲酰基戊酸-ae酯(aevb)的修饰构成,例如在其n-端位置中的叔胺水平上,从而使这个官能团与建立与所考虑的连接物臂的共价键相容。
专业技术人员能够选择用于这些目的的适合的修饰,特别是适合的取代基。
根据另一个实施方式,所述药物可以选自美登素类例如dm1和dm4,蒽环类化合物例如多柔比星、奈莫柔比星和pnu-159682,加利车霉素类,倍癌霉素类例如cc-1065和倍癌霉素a,吡咯并苯并二氮杂卓类,吡咯并苯并二氮杂卓二聚体,吲哚啉并-苯并二氮杂卓类,吲哚啉并-苯并二氮杂卓二聚体,α-鹅膏蕈碱类,艾日布林,阿卡鲁替尼,博来霉素,贝立替尼,克拉屈滨,氯法拉滨,考比替尼,库潘尼西,克唑替尼,阿糖胞苷,达拉非尼,更生霉素,柔红霉素,地西他滨,表柔比星,依鲁替尼,伊达比星,拉帕替尼,来那度胺,丝裂霉素c,米托蒽醌,奈拉滨,尼拉帕尼,紫杉醇,帕比司他,泊马度胺,泼尼松,瑞博西尼,帕博西尼,罗拉吡坦,卢卡帕尼,索尼德吉,他莫苷芬,替西罗莫司,拓扑替康,曲贝替定,戊柔比星,长春花碱,长春新碱,及其可药用盐。
在特定实施方式中,所述细胞毒性药物是sn-38,m是1,并且g是
在另一个特定实施方式中,所述细胞毒性药物是尾海兔素或蒽环类化合物,并且m是0。
方法
术语“溶剂”是指有机溶剂,无机溶剂例如水,或其混合物。有机溶剂的实例包括但不限于脂族烃类例如戊烷或己烷,脂环族烃类例如环己烷,芳香族烃类例如苯、苯乙烯、甲苯、邻二甲苯、间二甲苯或对二甲苯,卤代烃类例如二氯甲烷、氯仿或氯苯,基于氮的溶剂例如吡啶、乙腈或三乙胺,基于氧的溶剂特别是酮例如丙酮,醚例如二乙醚、叔丁基甲基醚(tbme)、环戊基甲基醚(cpme)、四氢呋喃(thf)或甲基四氢呋喃(me-thf),以及醇例如甲醇或乙醇,酯例如乙酸正丁酯,或酰胺例如二甲基甲酰胺(dmf),及其混合物。
“酸性条件”是指在其中使用一种或多种酸的条件。酸的实例包括但不限于盐酸、氢溴酸、氢碘酸、氢氟酸、硝酸、硫酸、六氟磷酸、四氟硼酸、三氟乙酸、乙酸、磺酸例如甲磺酸、单或多羧酸或其混合物,优选为盐酸。
“碱性条件”是指在其中使用一种或多种碱的条件。碱的实例包括但不限于氢氧化锂或氢氧化钠、碳酸盐例如碳酸钾、碳酸钠或碳酸氢钠、醇盐例如甲醇钠、胺例如三乙胺和含氮环状碱例如咪唑、n-甲基咪唑、吡啶或二甲基-氨基-吡啶(dmap),优选为氢氧化锂。
本发明所述的结合物可以从商品化4-羟基-3-硝基苯甲醛通过多步合成来制备,其中包括通过手性高效液相色谱(hplc)对消旋-4-(1-羟基丁-3-炔-1-基)-2-硝基-苯酚中间体进行对映异构体分离的步骤。
下文为每个步骤描述的条件(温度、浓度、溶剂、反应物、反应物的当量),可以由专业技术人员使用其在有机合成中的一般性背景来调整。每种中间体或在步骤结束时获得的产物可以被分离并任选地纯化,或者可以一锅进行几个步骤而不分离所述中间体或产物。下文描述的方法步骤的顺序可以修改。
步骤(a)
在一个实施方式中,消旋-4-(1-羟基丁-3-炔-1-基)-2-硝基-苯酚可以从4-羟基-3-硝基苯甲醛一步制备。所述反应包括通过炔丙基在4-羟基-3-硝基苯甲醛的醛官能团上的加成来引入炔丙基。通常,所述反应可以通过将4-羟基-3-硝基苯甲醛与能够加成到亲电位点上的亲核的炔丙基、即炔丙基的任何阴离子或有机金属形式反应来进行。所述反应可以用催化剂例如hgcl2协助。所述亲核的炔丙基可以从任何炔丙基源例如炔丙基溴原位形成或事先在独立的容器中制备。在优选实施方式中,所述反应使用4-羟基-3-硝基苯甲醛和炔丙基溴在铝金属和hgcl2存在下进行。
步骤(b)
然后,可以利用诸如手性hplc、非对映异构体盐的形成和分离、结晶、催化拆分或酶拆分或其组合的技术,来分离消旋-4-(1-羟基丁-3-炔-1-基)-2-硝基-苯酚的两种对映异构体。优选地,所述两种对映异构体通过手性hplc来分离。手性hplc是固定相为手性的层析技术。所述手性固定相可以是基于直链淀粉、基于环糊精或基于纤维素的相。优选地,所述手性固定相是基于直链淀粉的相。
这个对映异构体分离的步骤允许分离(r)-4-(1-羟基丁-3-炔-1-基)-2-硝基-苯酚。在所述分离步骤后(r)-4-(1-羟基丁-3-炔-1-基)-2-硝基-苯酚的对映异构体纯度在有利情况下高于90%,优选地高于95%。对映异构体纯度可以利用分析型手性hplc来测量。
步骤(c)
为引入葡萄糖醛酸苷组成部分的目的,可以将(r)-4-(1-羟基丁-3-炔-1-基)-2-硝基-苯酚与葡萄糖醛酸衍生物在允许所述苯酚基团的选择性o-葡萄糖醛酸化的条件下反应。优选地,所述葡萄糖醛酸衍生物是全保护的葡萄糖醛酸,通常为乙酰化葡萄糖醛酸酯,并且被官能化以使其可以与苯酚基团反应。所述葡萄糖醛酸衍生物优选为乙酰溴代-α-d-葡萄糖醛酸烷基酯,更优选为乙酰溴代-α-d-葡萄糖醛酸甲酯。在优选实施方式中,所述苯酚基团的o-葡萄糖醛酸化在碱性条件下进行。例如,所述反应可以在ag2co3和hmtta(1,1,4,7,10,10-六甲基三亚乙基四胺)存在下进行。
步骤(d)
可以将在步骤(c)中获得的o-葡萄糖醛酸化产物转化,以用于结合步骤(e)的目的。为此,可以将所述产物的仲醇官能团与氯代甲酸酯、优选为氯代甲酸4-硝基苯基酯反应,导致碳酸酯的形成。所述反应可以由也可充当碱的亲核试剂例如吡啶来催化。
步骤(e)、(f)和(g)
然后在步骤(e)中,将在步骤(d)中获得的化合物连接到如上所定义的细胞毒性药物(例如mmae),或者与a-g-h组成部分相连,其中a表示源自于细胞毒性药物的原子团,并且g表示自毁性组成部分。在其中将所述细胞毒性药物直接连接到在步骤(d)中获得的化合物的第一实施方式中,所述细胞毒性药物的胺基(或羟基)与在步骤(d)中获得的化合物的碳酸酯反应,产生酰胺基团。可以使用活化剂例如hoat、hobt、hoct。优选地,所述活化剂是hobt。
在这个第一实施方式后,如下所述的步骤(f)和(g)的执行产生如上所定义的式(i)的结合物,其中m为0。
在其中将所述细胞毒性药物通过自毁性组成部分连接到在步骤(d)中获得的化合物的第二实施方式中,将所述在步骤(d)中获得的化合物与a-g-h组成部分反应,其中a表示源自于细胞毒性药物的原子团,并且g表示自毁性组成部分。
a-g-h通过官能团连接到在步骤(d)中获得的化合物,所述官能团在有利情况下是-nh2或-nh-。
a-g-h组成部分的实例包括但不限于:
所述a-g-h组成部分通常可以通过将细胞毒性药物与式x-g-h的化合物反应来制备,其中x表示离去基团例如磺酸酯(例如甲磺酸酯、三氟甲磺酸酯、甲苯磺酸酯、硝基苯磺酸酯)或卤素(例如氯、溴、碘)。优选地,x是溴。所述细胞毒性药物通常通过它的(或一个它的)胺基或羟基与x-g-h反应,以形成如上所定义的a-g-h。在特定实施方式中,x-g-h在与所述细胞毒性药物反应时处于被保护形式。“被保护形式”是指其中所述化合物的一个或多个反应性官能团以无反应性形式存在的形式,例如nh2基团以n3基团的形式被保护。在将x-g-h与所述细胞毒性药物反应后,获得a-g-h,并且其也可能处于“被保护形式”。可以将所述a-g-h“去保护”,以便释放出所述反应性官能团(例如将n3基团转变成nh2基团)。
在这个第二实施方式后,如下所述的步骤(f)和(g)的执行产生如上所定义的式(i)的结合物,其中m为1。
在一个实施方式中,然后在步骤(f)中进行葡萄糖醛酸苷组成部分上的乙酰基和酯官能团的去保护,分别成为羟基和羧酸官能团。所述将在步骤(e)中获得的化合物的葡萄糖醛酸苷组成部分去保护的步骤(f),优选地在碱性条件下,更优选地在碱性条件和低温下进行。或者,所述步骤(f)可以在酸性条件下并在任何有机溶剂例如乙腈中进行。然后将在步骤(f)中获得的化合物的炔官能团与其中x是马来酰亚胺基团的式n3-(ch2-ch2-o)10-(ch2)2-nh-co-(ch2)5-x的叠氮化物在公知的点击化学条件下结合,允许选择性形成1,4-双取代的三唑位置异构体,并因此形成本发明的结合物。
所述其中x是马来酰亚胺基团的式n3-(ch2-ch2-o)10-(ch2)2-nh-co-(ch2)5-x的叠氮化物,通常可以通过将n3-(ch2-ch2-o)10-(ch2)2-nh2与6-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)己酸2,5-二氧代吡咯烷-1-基酯反应来获得。
在另一个实施方式中,步骤(f)包括将在步骤(e)中获得的化合物与式n3-(ch2-ch2-o)10-(ch2)2-nh2的叠氮化物在点击化学条件下结合,允许选择性形成所述1,4-双取代的三唑位置异构体。在步骤(g)中,通常通过将在步骤(f)中获得的化合物与6-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)己酸2,5-二氧代吡咯烷-1-基酯反应,将所述-nh2基团转变成在烷基链末端处被马来酰亚胺基团取代的烷基酰胺。然后进行所述在步骤(g)中获得的化合物的葡萄糖醛酸苷组成部分的最终去保护。这种去保护优选在碱性条件下,更优选在碱性条件和低温下进行。
根据本发明所述的方法提供了获得作为单一异构体存在的结合物的途径,所述异构体的纯度在有利情况下高于90%,优选地高于95%。
前体药物
本发明所述的结合物含有马来酰亚胺基团,所述基团对亲核基团,更具体来说对巯基(-sh)具有非常高的反应性。此类基团通常通过迈克尔加成反应被添加在所述马来酰亚胺组成部分上。因此,所述马来酰亚胺是被选择用于将本发明的结合物与大分子结合的反应性基团。在本发明的情形中,所述大分子优选为内源分子。
根据本发明,前体药物是指共价连接到大分子、更具体来说连接到蛋白质的至少一种结合物。所述前体药物能够在生物体中以非活化形式运输细胞毒性药物,并在β-葡萄糖醛酸酶作用下将所述药物释放到器官、组织或细胞中,所述运输和释放是特异性靶向的。所述前体药物可以通过与大分子、更具体来说与蛋白质反应而在体内或体外形成。
具体来说,所述蛋白质选自特异性结合存在于癌细胞膜处的分子的蛋白质,所述分子优选为选自蛋白质、糖蛋白、糖脂、糖类或其组合的分子,甚至更优选地,所述蛋白质特异性结合存在于癌细胞膜处的蛋白质。所述蛋白质能够结合的膜分子是主要或排他性地存在于癌细胞膜处的分子。在特定实施方式中,被所述蛋白质识别的膜分子是在癌细胞膜处过表达的蛋白质。
在优选实施方式中,所述蛋白质可以选自抗体和白蛋白。
当在本文中使用时,术语“抗体”是指免疫球蛋白分子和免疫球蛋白分子的免疫活性部分,即含有免疫特异性结合抗原的抗原结合部位的分子。因此,术语抗体不仅涵盖完整抗体分子,而且涵盖结合抗原的抗体片段以及抗体和抗体片段的变体(包括衍生物)。具体来说,本发明所述的抗体可以对应于单克隆抗体(例如嵌合、人源化或人类抗体)或单克隆抗体的片段。术语抗体是指经典抗体以及重链抗体和片段及其衍生物例如(vhh)2片段和单域抗体。
识别特定表位的抗体片段可以通过已知技术来产生。所述抗体片段是抗体的结合抗原的部分,例如f(ab’)2、fab、fv、scfv等。其他抗体片段包括但不限于:f(ab')2片段,其可以通过抗体分子的胃蛋白酶消化产生;和fab'片段,其可以通过还原f(ab')2片段的二硫桥产生。或者,可以构建fab'表达文库(huse等,1989,science,246:1274-1281),以允许快速且容易地鉴定具有所需特异性的单克隆fab'片段。
本发明所述的抗体可以通过本领域中已知的任何技术来生产,例如但不限于单独或组合的任何化学、生物学、遗传或酶技术。本发明的抗体可以通过生成和培养杂交瘤来获得。对于合成的单域抗体的生成,也参见wo2015/063331。
本发明所述的抗体可以是单体抗体或多聚体抗体,并且它可以包含至少一个可变结构域,特别是当所述抗体是多聚体时。
优选地,本发明所述的抗体是igg,优选为igg1或igg4亚型,例如曲妥珠单抗或利妥昔单抗。
在本发明的最优选实施方式中,所述蛋白质是具有游离巯基官能团的白蛋白分子。可以设想内源或外源白蛋白特别是人血清白蛋白、重组白蛋白或白蛋白的片段。
已知在实体肿瘤的微环境中内源白蛋白通过“epr”(“高通透性和滞留”)效应积累,因此本发明所述的结合物与内源白蛋白分子的原位结合使得可以将由此形成的结合的实体、也被称为前体药物,靶向到肿瘤微环境中,并因此克服某些细胞毒性药物衍生物例如尾海兔素的游离形式的选择性缺失。应该指出,这种“epr”效应适用于发炎组织的微环境。
因此,可以通过所述结合物的反应性马来酰亚胺基团与蛋白质、优选为内源白蛋白分子、更优选为人血清白蛋白或其衍生物的游离且互补的反应性官能团、通常为巯基官能团之间的共价键的体内选择性形成,来获得前体药物。所述前体药物可以包含根据本发明所述的结合物的至少一个分子,其共价连接到蛋白质分子或所述分子的片段或衍生物。
在白蛋白的情况下,可以与白蛋白第34位中半胱氨酸的巯基官能团建立所述共价键。
在特定实施方式中,本发明的前体药物可以在其给药之前制备。本发明的前体药物可以通过至少一个本发明的结合物与蛋白质例如白蛋白分子、重组白蛋白分子或其片段或衍生物的游离且互补的官能团、通常为巯基官能团之间的共价键的形成,在体外形成。可以与白蛋白第34位中半胱氨酸的巯基官能团建立所述共价键。
在本发明的情形中,“白蛋白分子的片段”是指白蛋白分子的片段,其具有足够尺寸,以保证由此产生的前体药物的令人满意的生物可利用性、对肿瘤组织的透过性和对健康组织的内皮屏障的不可透过性。在特定实施方式中,蛋白质分子的片段含有对应于内源白蛋白序列第34位半胱氨酸的半胱氨酸。
根据本发明所述的前体药物可以由式(ii)及其可药用盐表示:
其中a、g和m如上所定义,
prt表示源自于蛋白质的原子团,
n为0.1至16,优选为0.1至8。
在一个特定实施方式中,prt表示源自于抗体的原子团,n是附连到所述抗体的结合物的平均数目并在0.1至16之间,优选地在0.1至8之间。
在另一个特定实施方式中,prt表示源自于白蛋白的原子团,并且n是1。
n可以通过质谱术(ms)和疏水相互作用层析(hic)来测量。
根据本发明,“源自于蛋白质的原子团”是指由蛋白质剥离掉其与结合物的剩余部分反应的官能团之一的一个或多个原子而构成的组成部分。更具体来说,“源自于蛋白质的原子团”是指包含至少一个半胱氨酸组成部分的蛋白质,所述半胱氨酸组成部分已被剥夺了它的-sh基团的氢原子。
药物组合物
本发明的结合物或前体药物可以在药物组合物中递送,所述药物组合物至少包含有效量的至少一种本发明的结合物或至少一种本发明的前体药物,以及可药用载体。所述药物组合物可以处于固体或液体状态,并且可以采取在人类或兽医药物中常用的任何药物形式,例如采取简单或糖包衣片剂、丸剂、菱形片、凝胶胶囊、滴剂、颗粒剂、注射用制剂、软膏、霜剂或凝胶剂的形式。所述药物组合物可以按照常用方法来制备。
当在本文中使用时,术语“可药用载体”是指存在于药物组合物中的除了活性成分之外的任何成分(即赋形剂)。它的添加可能只在为最终产品提供特定的一致性(consistency)或其他物理或味觉性质。赋形剂或可药用载体必须避免与活性成分发生任何相互作用,特别是化学相互作用。可以根据本领域技术人员公知的技术使用常见赋形剂。当在本文中使用时,术语“有效量”是指活性成分的阻止、消除或减少疾病的有害效应的量。
用途
本发明的结合物或本发明的前体药物可用于治疗癌症和/或炎性疾病。
当在本文中使用时,术语“治疗”是指旨在改善患者健康状态的任何行动,例如疾病的治疗、防止、预防和迟滞。在某些实施方式中,该术语是指疾病或与疾病相关的症状的改善或根除。在其他实施方式中,该术语是指由一种或多种治疗剂向患有这种疾病的对象的给药引起的所述疾病的蔓延或恶化的最小化。
当在本文中使用时,术语“对象”、“个体”或“患者”可互换使用,并且是指动物,优选是指哺乳动物,甚至更优选是指人。然而,术语“对象”也可以是指非人类动物,特别是哺乳动物。根据本发明所述的对象是动物,优选为哺乳动物,甚至更优选为人。所述对象可以是非人类动物,特别是选自哺乳动物例如狗、猫、马、奶牛、猪、绵羊和非人的灵长动物等。优选地,所述对象是人,优选为成年人,更优选为至少40岁的成年人,更优选为至少50岁的成年人,甚至更优选为至少60岁的成年人。
本发明还涉及本发明所述的结合物、本发明所述的前体药物或本发明所述的药物组合物在制备药物中的用途。优选地,它涉及本发明所述的结合物、本发明所述的前体药物或本发明所述的药物组合物在制备用于在对象中治疗癌症和/或炎性疾病的药物中的用途。
它还涉及一种在对象中治疗癌症和/或炎性疾病的方法,其中将治疗有效量的本发明所述的结合物、治疗有效量的本发明所述的前体药物或治疗有效量的本发明所述的药物组合物给药到所述患有癌症和/或炎性疾病的对象。
它还涉及一种在对象中治疗癌症和/或炎性疾病的方法,其中将治疗有效量的本发明所述的结合物、治疗有效量的本发明所述的前体药物或治疗有效量的本发明所述的药物组合物与另一种治疗相组合给药到所述患有癌症和/或炎性疾病的对象,所述另一种治疗选自化疗、放疗、使用至少一种抗炎剂的治疗及其组合。
本发明所述的结合物、本发明所述的前体药物或本发明所述的药物组合物可以通过任何方便的途径被给药到需要的对象。例如,它可以通过系统途径,特别是通过皮下、肌肉内、静脉内或真皮内注射,优选地通过静脉内注射给药。本发明所述的结合物、本发明所述的前体药物或本发明所述的药物组合物可以单剂或多剂给药。本发明所述的结合物、本发明所述的前体药物或本发明所述的药物组合物可以在每天至每月之间,优选每周或每两周,更优选每周给药。使用本发明所述的结合物、本发明所述的前体药物或本发明所述的药物组合物的治疗的持续时间优选地在1至20周之间,优选地在1至10周之间。可选地,只要所述疾病的症状仍在,所述治疗就可以持续。本发明所述的结合物、本发明所述的前体药物或本发明所述的药物组合物的待给药的量,必须由本领域普通技术人员通过公知的标准程序来确定。为了确定适合的剂量,必须将患者的生理数据(例如年龄、尺寸和体重)和给药途径考虑在内,以便将治疗有效量给药到所述患者。
癌症
当在本文中使用时,术语“癌症”或“肿瘤”是指具有引起癌症的细胞典型的特征例如不受控制的增殖和/或永生性和/或转移潜力和/或快速生长和/或增殖速率和/或某些特征性形态特点的细胞的存在。该术语是指任何类型的对象中的任何类型的恶性肿瘤(原发或转移肿瘤)。它可以是指实体肿瘤以及造血系肿瘤。
优选地,根据本发明所述的癌症选自前列腺癌、肺癌、乳腺癌、胃癌、肾癌、卵巢癌、肝细胞癌、骨肉瘤、黑素瘤、下咽癌、食道癌、子宫内膜癌、宫颈癌、胰腺癌、肝癌、结肠或结肠直肠癌、神经内分泌肿瘤、肌肉的恶性肿瘤、肾上腺癌、甲状腺癌、子宫癌、皮肤癌、膀胱癌、头颈癌、淋巴瘤和白血病。
本发明的结合物、本发明的前体药物或本发明的药物组合物特别旨在治疗乳腺癌、结肠癌、卵巢癌、前列腺癌、胰腺癌和肺癌。
可以利用本发明的结合物、本发明的前体药物或本发明的药物组合物用于转移肿瘤的预防和/或治疗的用途中。
炎性疾病
当在本文中使用时,术语“炎性疾病”具体来说是指肠的慢性病理状况或类风湿性病理状况。
具体实施方式
实施例
根据下述仅仅出于说明性目的提供的实施例,本发明将被更好地理解。
方法1–制备型hplc
所述制备型hplc系统由两个shimadzulc-8a泵、spd-10avp检测器(shimadzu)、scl-10avp控制器(shimadzu)、sil-10a自动进样器、2ml样品环和sunfirec18柱(150mm×19mmi.d.,5μm,waters)构成。将样品注入到样品环中,并以17ml/min的流速洗脱(50min运行,在254nm处检测;缓冲液a:h2omiliq+0.05%tfa;缓冲液b:乙腈;梯度:40min–从5%至95%b,5min–95%b,5min–5%b)。
方法2–分析型hplc
所述分析型hplc在装备有waters2487uv检测器和gemini-nx,5μm,c18,150x4.6mm柱的waters2695分离模块上进行。流速为1ml/min。溶剂a:0.05%tfa水溶液。溶剂b:0.05%tfa乙腈溶液。梯度运行:0-1min–30%b;1-11min–30%至80%b;11-12min–80至95%b;12-14.5min–95%b;14.5-14.7min–95%至30%b;14.7-17min–30%b。
方法3–lcms
所述lcms在装备有waters2487uv检测器、watersacquityqda质量检测器和cortecs,2.7μm,c18,50x4.6mm柱的waters2695分离模块上运行。流速为1ml/min。溶剂a:0.05%hcooh水溶液。溶剂b:0.05%hcooh乙腈溶液。梯度运行:0-5min–5%至95%b;5-6min–95%b;6-7.8min–5%b。质量检测器在正ms扫描模式中,使用600℃探头温度、1.5kv毛细管电压和10v锥电压运行。
方法4–手性hplc
手性hplc在装备有shimadzusil-10a自动进样器、shimadzuscl-10avpuv检测器(设置到254nm)、两个shimadzulc-8a泵、
方法5–手性hplc
手性hplc在装备有shimadzusil-10a自动进样器、shimadzuscl-10avpuv检测器(设定到254nm)、两个shimadzulc-8a泵、
化合物r1和s1的消旋混合物的合成
在装备有制冷剂和加料漏斗的烧瓶中,将铝粉(6.17eq.,14156mg,524mmol)和催化量的hgcl2(0.00248eq.,57.2mg,0.211mmol)用无水thf(218ml)覆盖。然后逐滴添加炔丙基溴(6.2eq.,78439mg,58.8ml,527mmol)在甲苯中的80%溶液(注意:放热反应;放热曲线的峰及其强度取决于铝粉的分散度)。当添加完成时,将得到的反应混合物回流6小时。然后将所述溶液冷却到0℃,并逐滴添加4-羟基-3-硝基苯甲醛(1eq.,14210mg,85mmol)在thf(109ml)中的溶液。在搅拌30min后,所述醛完全消失(通过tlc控制),并将所述反应冷却到0℃。通过逐滴添加1nhcl(10ml)将所述反应混合物淬灭,然后用etoac萃取3次。将有机层在mgso4上干燥,然后蒸发以得到棕色油状物,将其通过快速层析进行纯化(环己烷/etoac-70/30)。为了消除痕量的wurtz反应副产物,将得到的黄色油状物溶解在dcm(655ml)中,将有机层用1nnaoh溶液萃取3次(每次1/3的dcm体积)。然后向得到的合并水性层添加dcm(等体积)。将反应混合物用浓hcl酸化直至ph1。将水性相用dcm再萃取3次(每次1/3的所述水性溶液体积)。将合并的有机层用mgso4干燥并蒸发,得到(r)-4-(1-羟基丁-3-炔-1-基)-2-硝基苯酚和(s)-4-(1-羟基丁-3-炔-1-基)-2-硝基苯酚混合物的消旋混合物(7927mg,38.3mmol,45%)。
1hnmr(氯仿-d)位移:10.63(s,1h),8.23(s,1h),7.73(dd,j=8.5,1.5hz,1h),7.25(d,j=8.5hz,1h),4.97(t,j=6.1hz,1h),2.67-2.97(m,3h),2.20(t,j=2.5hz,1h)。
13cnmr(氯仿-d)位移:154.6,135.2,135.0,133.3,122.3,120.1,79.6,71.9,70.8,29.3。
ms(esi,方法3)m/z:230.1[m+na]+
对映异构体r1和s1的分离
对映异构体r1和s1使用手性层析来分离。手性层析在装备有shimadzusil-10a自动进样器、shimadzuscl-10avpuv检测器(设定到254nm)、shimadzufrc-10a分部收集器、两个shimadzulc-8a泵、
化合物r1hplc(方法5)rt:6.53min
化合物s1hplc(方法5)rt:16.79min
化合物r2
将hmtta(0.7eq.,2.11g,2.5ml,9.17mmol;1,1,4,7,10,10-六甲基三亚乙基四胺,cas3083-10-1)和ag2co3(3.7eq.,13.4g,48.5mmol)在无水乙腈(20ml)中的溶液在室温下搅拌2h。在0℃下添加(r)-4-(1-羟基丁-3-炔-1-基)-2-硝基苯酚(1eq.,2.71g,13.1mmol)和(2r,3r,4s,5s,6s)-2-溴-6-(甲氧基羰基)四氢-2h-吡喃-3,4,5-三基三乙酸酯(1.1eq.,5.7g,14.3mmol)在乙腈(11.9ml)中的溶液,并将得到的混合物在室温搅拌4h。将所述反应用水淬灭,然后添加etoac(50ml)。将得到的反应混合物搅拌3分钟,然后过滤,以消除银盐。再用et2o进行4次萃取;将合并的有机级分用mgso4干燥并蒸发。将得到的粗材料通过快速层析进行纯化(环己烷/etoac梯度:在20分钟内0-100%的etoac;30个柱体积),得到浅黄色固体的r2甲酯(3428mg,6.55mmol,50%)。
1hnmr(氯仿-d)位移:7.86(dd,j=6.1,1.9hz,1h),7.49-7.65(m,1h),7.36(d,j=8.5hz,1h),5.25-5.39(m,3h),5.17-5.25(m,1h),4.90(t,j=6.1hz,1h),4.21(d,j=8.8hz,1h),3.74(s,3h),2.53-2.70(m,2h),1.98-2.20(m,10h)。
13cnmr(氯仿-d)位移:170.0,169.3,169.3,166.7,148.5,141.2,138.9,131.2,122.6,120.0,99.8,90.3,79.4,72.6,72.0,71.2,70.7,70.2,68.8,53.0,29.4,20.6,20.5。
ms(方法3)m/z:546.2[m+na]+
化合物s2
将hmtta(0.7eq.,3.4g,4ml,14.76mmol;1,1,4,7,10,10-六甲基三亚乙基四胺,cas3083-10-1)和ag2co3(3.7eq.,21.5g,78mmol)在无水乙腈(30ml)中的溶液在室温搅拌2h。在0℃下添加(s)-4-(1-羟基丁-3-炔-1-基)-2-硝基苯酚(1eq.,4.37g,21.1mmol)和(2r,3r,4s,5s,6s)-2-溴-6-(甲氧基羰基)四氢-2h-吡喃-3,4,5-三基三乙酸甲酯(1.1eq.,10g,25.3mmol)在乙腈(20ml)中的溶液,并将得到的混合物在室温搅拌4h。将所述反应用水淬灭,然后添加etoac(80ml)。将得到的反应混合物搅拌3分钟,然后过滤,以消除银盐。再用et2o进行4次萃取;将合并的有机级分用mgso4干燥并蒸发。将得到的粗材料通过快速层析进行纯化(环己烷/etoac梯度:在20分钟内0-100%的etoac;30个柱体积;得到浅黄色固体的s2(6100mg,11.6mmol,55%)。
1hnmr(氯仿-d)位移:7.86(dd,j=6.1,1.9hz,1h),7.49-7.65(m,1h),7.36(d,j=8.5hz,1h),5.25-5.39(m,3h),5.17-5.25(m,1h),4.90(t,j=6.1hz,1h),4.21(d,j=8.8hz,1h),3.74(s,3h),2.53-2.70(m,2h),1.98-2.20(m,10h)。
13cnmr(氯仿-d)位移:170.0,169.3,169.3,166.7,148.5,141.2,138.9,131.2,122.6,120.0,99.8,90.3,79.4,72.6,72.0,71.2,70.7,70.2,68.8,53.0,29.4,20.6,20.5。
ms(方法3)m/z:546.3[m+na]+
化合物r3
在0℃下向r2(1eq.,1600mg,3.05mmol)和氯代甲酸4-硝基苯基酯(2eq.,1230mg,6.1mmol)在无水dcm(30ml)中的溶液添加吡啶(2.5eq.,0.62ml,7.62mmol)。将所述混合物在室温下搅拌1小时,然后用饱和nahco3水溶液淬灭。将所述混合物用dcm(与反应体积相同)萃取3次,并将合并的有机层用mgso4干燥,过滤并真空浓缩。通过快速层析进行的纯化(环己烷/etoac梯度:20分钟内0-100%的etoac;30个柱体积)得到灰白色固体的r3(1469mg,2.13mmol,70%)。
1hnmr(氯仿-d)位移:8.17-8.34(m,2h),7.94(d,j=2.0hz,1h),7.65(dd,j=8.7,2.1hz,1h),7.43(d,j=8.5hz,1h),7.33-7.40(m,2h),5.81(t,j=6.5hz,2h),5.21-5.43(m,4h),4.25(d,j=8.8hz,1h),3.74(s,3h),2.78-3.02(m,2h),2.13(s,3h),2.09-2.12(m,1h),2.02-2.09(m,6h)。
13cnmr(氯仿-d)位移:169.9,169.2,169.1,166.7,155.2,151.5,149.5,145.6,141.2,133.4,132.1,125.3,123.6,121.7,119.9,99.5,72.7,72.5,71.0,70.2,68.6,53.0,26.3,20.6,20.5,20.5。
ms(方法3)m/z:711.2[m+na]+
hplc(方法4)rt:2.77min
化合物s3
在0℃下向s2(1eq.,2600mg,5.0mmol)和氯代甲酸4-硝基苯基酯(2eq.,2000mg,9.9mmol)在无水dcm(50ml)中的溶液添加吡啶(2.5eq.,1ml,12.42mmol)。将所述混合物在室温下搅拌1小时,然后用饱和nahco3水溶液淬灭。将所述混合物用dcm(与反应体积相同)萃取3次,并将合并的有机层用mgso4干燥,过滤并真空浓缩。通过快速层析在环己烷/乙酸乙酯中进行的纯化(环己烷/etoac梯度:20分钟内0-100%的etoac;30个柱体积)得到灰白色固体的s3(2300mg,2.13mmol,68%)。
1hnmr(氯仿-d)位移:8.17-8.34(m,2h),7.94(d,j=2.0hz,1h),7.65(dd,j=8.7,2.1hz,1h),7.43(d,j=8.5hz,1h),7.33-7.40(m,2h),5.81(t,j=6.5hz,2h),5.21-5.43(m,4h),4.25(d,j=8.8hz,1h),3.74(s,3h),2.78-3.02(m,2h),2.13(s,3h),2.09-2.12(m,1h),2.02-2.09(m,6h)。
13cnmr(氯仿-d)位移:170.0,169.3,169.2,166.7,155.2,151.5,149.5,145.6,141.1,133.4,132.1,125.4,123.7,121.7,119.9,99.5,72.6,72.5,71.0,70.2,68.6,53.1,26.2,20.6,20.6,20.5。
ms(方法3)m/z:711.2[m+na]+
hplc(方法4)rt:2.84min
化合物r4
向r3(1eq.,41.3mg,0.06mmol)和mmae(1eq.,43.1mg,0.06mmol)在dmf(1.15ml)中的溶液添加hobt(1eq.,8.11mg,0.06mmol)在吡啶(0.287ml)中的溶液。将所述混合物在室温搅拌24h,然后用meoh(11.5ml)稀释并冷却到0℃。向得到的溶液添加lioh(10eq.,1m,在h2o中,0.6ml,0.6mmol),并将所述混合物在4℃温育16h。将得到的溶液用hcooh(20eq.,1m,在h2o中,1.2ml,1.2mmol)淬灭并在减压下浓缩到3ml。将残留物通过制备型hplc进行纯化(方法1),得到浅黄色固体的r4(41.9mg,0.0372mmol,62%)。
hplc(方法2)rt:7.81min
ms(方法3)m/z:1127.7[m+h]+
化合物s4
向s3(1eq.,37.9mg,0.055mmol)和mmae(1eq.,39.5mg,0.055mmol)在dmf(1.05ml)中的溶液添加hobt(1eq.,7.43mg,0.055mmol)在吡啶(0.263ml)中的溶液。将所述混合物在室温搅拌24h,然后用meoh(10.5ml)稀释并冷却到0℃。向得到的溶液添加lioh(10eq.,1m,在h2o中,0.55ml,0.55mmol),并将所述混合物在4℃温育16h。将得到的溶液用hcooh(20eq.,1m,在h2o中,1.1ml,1.1mmol)淬灭,并在减压下浓缩到3ml。将残留物通过制备型hplc进行纯化(方法1),得到浅黄色固体的s4(36.6mg,0.0325mmol,59%)。
hplc(方法2)rt:7.66min
ms(方法3)m/z:1127.9[m+h]+
化合物r5
向32-叠氮基-3,6,9,12,15,18,21,24,27,30-十氧杂三十二烷-1-胺(1.2eq.,19mg,0.036mmol)在无水dmf(0.5ml)中的溶液添加6-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)己酸2,5-二氧代吡咯烷-1-基酯(1.2eq.,11.1mg,0.036mmol)。将所述混合物在21℃搅拌1小时,然后添加r4(1eq.,33.8mg,0.03mmol)。通过将三[(1-苯甲基-1h-1,2,3-三唑-4-基)甲基]胺(0.2eq.,0.2m,在dmf中,0.03ml,0.006mmol)与五水硫酸铜(0.2eq.,0.2m,在h2o中,0.03ml,0.006mmol)混合并在21℃温育2分钟,制备tbta-cu(ii)络合物。向反应混合物添加所述tbta-cu(ii)络合物(0.2eq.,0.1m,在dmf/h2o50/50中,0.06ml,0.006mmol),然后添加抗坏血酸钠(1eq.,1m,在h2o中,0.03ml,0.03mmol)。将得到的混合物在21℃温育1小时并通过制备型hplc进行纯化,得到白色固体的r5(30.5mg,0.0165mmol,55%)。
hplc(方法2)rt:6.85min
ms(方法3)m/z:924.2[m+2h]2+/2
化合物s5
向32-叠氮基-3,6,9,12,15,18,21,24,27,30-十氧杂三十二烷-1-胺(1.2eq.,15.8mg,0.03mmol)在无水dmf(0.417ml)中的溶液添加6-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)己酸2,5-二氧代吡咯烷-1-基酯(1.2eq.,9.25mg,0.03mmol)。将所述混合物在21℃搅拌1小时,然后添加s4(1eq.,28.2mg,0.025mmol)。通过将三[(1-苯甲基-1h-1,2,3-三唑-4-基)甲基]胺(0.2eq.,0.2m,在dmf中,0.025ml,0.005mmol)与五水硫酸铜(0.2eq.,0.2m,在h2o中,0.025ml,0.005mmol)混合并在21℃温育2分钟,制备tbta-cu(ii)络合物。向反应混合物添加所述tbta-cu(ii)络合物(0.2eq.,0.1m,在dmf/h2o50/50中,0.05ml,0.005mmol),然后添加抗坏血酸钠(1eq.,1m,0.025ml,0.025mmol)。将得到的混合物在21℃温育1小时并通过制备型hplc进行纯化,得到白色固体的s5(26.8mg,0.0145mmol,58%)。
hplc(方法2)rt:6.65min
ms(方法3)m/z:924.1[m+2h]2+/2
化合物r6a
向r3(1eq.,41.5mg,0.06mmol)和mmaf(1eq.,47.5mg,0.06mmol)在dmf(1.3ml)中的溶液添加hobt(1eq.,8.14mg,0.06mmol)在吡啶(0.291ml)中的溶液。将所述混合物在室温搅拌66h,用hcooh(3eq.,6.8μl,0.18mmol)淬灭,并通过制备型hplc(方法1)进行纯化,得到白色固体的r6a(57mg,0.043mmol,71%收率)。
hplc(方法2)rt:6.0min
ms(方法3)m/z:669.5[m+2h]2+/2
化合物s6a
向s3(1eq.,41.5mg,0.06mmol)和mmaf(1eq.,47.5mg,0.06mmol)在dmf(1.3ml)中的溶液添加hobt(1eq.,8.14mg,0.06mmol)在吡啶(0.291ml)中的溶液。将所述混合物在室温搅拌66h,用hcooh(3eq.,6.8μl,0.18mmol)淬灭,并通过制备型hplc(方法1)进行纯化,得到白色固体的s6a(26.6mg,0.02mmol,33%收率)。
hplc(方法2)rt:6.0min
ms(方法3)m/z:669.4[m+2h]2+/2
化合物r6b
向r6a(1eq.26.5mg,0.02mmol)在mecn(233μl)中的溶液添加浓hcl水溶液(233μl),并将所述溶液在40℃搅拌20h。然后将所述混合物用0.5mlmecn稀释并离心以分离沉淀物。将上清液通过制备型hplc(方法1)进行纯化,得到灰白色固体的r6b(6.7mg,5.9μmol,30%收率)。
hplc(方法2)rt:4.4min
ms(方法3)m/z:1141.6[m+h]+
化合物s6b
向s6a(1eq.26.5mg,0.02mmol)在mecn(233μl)中的溶液添加浓hcl水溶液(233μl),并将所述溶液在40℃搅拌20h。然后将所述混合物用0.5mlmecn稀释并离心以分离沉淀物。将上清液通过制备型hplc(方法1)进行纯化,得到灰白色固体的s6b(10.4mg,9.1μmol,46%收率)。
hplc(方法2)rt:4.4min
ms(方法3)m/z:1141.6[m+h]+
化合物r6
向32-叠氮基-3,6,9,12,15,18,21,24,27,30-十氧杂三十二烷-1-胺(1.2eq.,3.53mg,6.7μmol)在无水dmf(0.15ml)中的溶液添加6-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)己酸2,5-二氧代吡咯烷-1-基酯(1.2eq.,2.07mg,6.7μmol)在无水dmf(0.15ml)中的溶液。将所述混合物在21℃搅拌1小时,然后添加在dmso(0.15ml)中的r6b(1eq.,6.4mg,5.6μmol)。通过将三(3-羟基丙基三唑基甲基)胺(1.5eq.,0.1m,在dmf中,0.084ml,8.4μmol)与五水硫酸铜(1.5eq.,0.1m,在h2o中,0.084ml,8.4μmol)混合并在21℃温育1分钟,制备thpta-cu(ii)络合物。向反应混合物添加所述thpta-cu(ii)络合物(1.5eq.,0.05m,在dmf/h2o50/50中,0.168ml,8.4μmol),然后添加抗坏血酸钠(7.46eq.,0.5m,在h2o中,0.084ml,41.5μmol)。将得到的混合物在21℃温育15min并通过制备型hplc(方法1)进行纯化,得到白色固体的r6(3.7mg,1.99μmol,36%)。
hplc(方法2)rt:4.18min
ms(方法3)m/z:931.1[m+2h]2+/2
化合物s6
向32-叠氮基-3,6,9,12,15,18,21,24,27,30-十氧杂三十二烷-1-胺(1.2eq.,4.63mg,8.8μmol)在无水dmf(0.15ml)中的溶液添加6-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)己酸2,5-二氧代吡咯烷-1-基酯(1.2eq.,2.71mg,8.8μmol)在无水dmf(0.15ml)中的溶液。将所述混合物在21℃搅拌1小时,然后添加在dmso(0.15ml)中的s6b(1eq.,8.3mg,7.3μmol)。通过将三(3-羟基丙基三唑基甲基)胺(1.5eq.,0.1m,在dmf中,0.109ml,10.9μmol)与五水硫酸铜(1.5eq.,0.1m,在h2o中,0.109ml,10.9μmol)混合并在21℃温育1分钟,制备thpta-cu(ii)络合物。向反应混合物添加所述thpta-cu(ii)络合物(1.5eq.,0.05m,在dmf/h2o50/50中,0.218ml,10.9μmol),然后添加抗坏血酸钠(7.46eq.,0.5m,在h2o中,0.109ml,54.4μmol)。将得到的混合物在21℃温育15min并通过制备型hplc(方法1)进行纯化,得到白色固体的s6(6.2mg,3.33μmol,46%)。
hplc(方法2)rt:4.14min
ms(方法3)m/z:931.1[m+2h]2+/2
化合物7a
向sn-38(1eq.,72.2mg,0.18mmol)和1-叠氮基-4-(溴甲基)苯(1eq.,39mg,0.18mmol)在dmf(7.22ml)中的溶液添加k2co3(3eq.,76.3mg,0.55mmol)。将所述得到的溶液用氮气吹扫,在室温搅拌1h以允许7a形成。粗品7a(92mg,0.18mmol,96%)不需进一步纯化用于下一步骤中。
ms(方法3)m/z:524.2[m+h]+
化合物7b
向7a(1eq.,96mg,0.18mmol)在dmf(3ml)中的溶液添加三(2-羧乙基)膦盐酸盐(tcep,1.3eq.,68.33mg,0.24mmol),然后添加k2co3(3eq.,76mg,0.55mmol)。将所述混合物搅拌1小时,然后添加5x体积的etoac,然后添加1x体积的水。分离有机层,并将水性层用另外5x体积的etoac萃取。将合并的有机层用mgso4干燥并在真空下浓缩,得到浅黄色固体的7b(90mg,0.18mmol,99%)。粗品7b不需进一步纯化用于下一步骤中。
ms(方法3)m/z:498.2[m+h]+
化合物r7c
将r3(1eq.,82mg,0.12mmol)、7b(1eq.,59mg,0.12mmol)和hobt(1eq.,16mg,0.12mmol)在dmf(2.4ml)中的溶液在25℃搅拌16小时。将得到的混合物通过制备型hplc(方法1)进行纯化,得到浅黄色固体的r7c(45mg,0.043mmol,36%)。
ms(方法3)m/z:1047.3[m+h]+
化合物s7c
将s3(1eq.,82mg,0.12mmol)、7b(1eq.,59mg,0.12mmol)和hobt(1eq.,16mg,0.12mmol)在dmf(2.4ml)中的溶液在25℃搅拌16小时。将得到的混合物通过制备型hplc(方法1)进行纯化,得到浅黄色固体的s7c(63mg,0.06mmol,50%)。
ms(方法3)m/z:1047.3[m+h]+
化合物r7d
向r7c(1eq.,23mg,22μmol)在meoh(20ml)中的溶液添加1mlioh水溶液(200eq.,4.4ml,4.4mmol)。将得到的反应混合物在25℃搅拌4h,并通过制备型hplc进行纯化,得到浅黄色固体的r7d(16mg,0.018mmol,80%)。
ms(方法3)m/z:907.3[m+h]+
化合物s7d
向s7c(1eq.,23mg,22μmol)在meoh(20ml)中的溶液添加1mlioh水溶液(200eq.,4.4ml,4.4mmol)。将得到的反应混合物在25℃搅拌4h,并通过制备型hplc进行纯化,得到浅黄色固体的s7d(13.9mg,0.016mmol,69.6%)。
ms(方法3)m/z:907.3[m+h]+
化合物r7
向32-叠氮基-3,6,9,12,15,18,21,24,27,30-十氧杂三十二烷-1-胺(1.5eq.,5.92mg,11.3μmol)在无水dmf(0.1ml)中的溶液添加6-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)己酸2,5-二氧代吡咯烷-1-基酯(1.5eq.,3.47mg,11.3μmol)在无水dmf(0.1ml)中的溶液。将所述混合物在21℃温育1小时,然后添加在dmso(0.1ml)中的r7d(1eq.,6.8mg,7.5μmol)。通过将三(3-羟基丙基三唑基甲基)胺(0.5eq.,0.1m,在dmf中,37.5μl,3.75μmol)与五水硫酸铜(0.5eq.,0.1m,在h2o中,37.5μl,3.75μmol)混合并在21℃温育1分钟,制备thpta-cu(ii)络合物。向反应混合物添加所述thpta-cu(ii)络合物(0.5eq.,0.05m,在dmf/h2o50/50中,75μl,3.75μmol),然后添加抗坏血酸钠(2.5eq.,0.5m,在h2o中,37.5μl,18.75μmol)。将得到的混合物在21℃温育15min,并通过制备型hplc(方法1)进行纯化,得到白色固体的r7(6.95mg,4.28μmol,57%)。
hplc(方法2)rt:3.92min
ms(方法3)m/z:813.9[m+2h]2+/2
化合物s7
向32-叠氮基-3,6,9,12,15,18,21,24,27,30-十氧杂三十二烷-1-胺(1.5eq.,5.92mg,11.3μmol)在无水dmf(0.1ml)中的溶液添加6-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)己酸2,5-二氧代吡咯烷-1-基酯(1.5eq.,3.47mg,11.3μmol)在无水dmf(0.1ml)中的溶液。将所述混合物在21℃搅拌1小时,然后添加在dmso(0.1ml)中的s7d(1eq.,6.8mg,7.5μmol)。通过将三(3-羟基丙基三唑基甲基)胺(0.5eq.,0.1m,在dmf中,37.5μl,3.75μmol)与五水硫酸铜(0.5eq.,0.1m,在h2o中,37.5μl,3.75μmol)混合并在21℃温育1分钟,制备thpta-cu(ii)络合物。向反应混合物添加所述thpta-cu(ii)络合物(0.5eq.,0.05m,在dmf/h2o50/50中,75μl,3.75μmol),然后添加抗坏血酸钠(2.5eq.,0.5m,在h2o中,37.5μl,18.75μmol)。将得到的混合物在21℃温育15min,并通过制备型hplc(方法1)进行纯化,得到白色固体的s7(7.44mg,4.58μmol,61%)。
hplc(方法2)rt:3.95min
ms(方法3)m/z:813.9[m+2h]2+/2
化合物r8a
向r3(1eq.,317mg,0.46mmol)在乙腈(2ml)中的溶液添加浓hcl(52.2eq.,2ml,24mmol),并将所述混合物在37℃搅拌16h。向得到的混合物添加etoac(8ml),然后添加水(8ml)。分离有机层,并将水性层用etoac萃取三次。将合并的有机层用mgso4干燥并在真空下浓缩,得到粗品r8a(250mg,0.46mmol,99%),其不需进一步纯化用于下一步骤中。
ms(方法3)m/z:549.1[m+h]+
化合物s8a
向s3(1eq.,317mg,0.46mmol)在乙腈(2ml)中的溶液添加浓hcl(52.2eq.,2ml,24mmol),并将所述混合物在37℃搅拌16h。向得到的混合物添加etoac(8ml),然后添加水(8ml)。分离有机层,并将水性层用etoac萃取三次。将合并的有机层用mgso4干燥并在真空下浓缩,得到粗品s8a(247mg,0.45mmol,98%),其不需进一步纯化用于下一步骤中。
ms(方法3)m/z:549.1[m+h]+
化合物r8b
向多柔比星盐酸盐(1eq.,10mg,0.017mmol)在dmf(0.35ml)中的溶液添加tea(2eq.,0.35ml,0.1m,在dmf中,0.035mmol),然后添加r8a(1eq.,9.5mg,0.017mmol)。将得到的混合物在25℃搅拌16h并通过制备型hplc(方法1)进行纯化,得到红色固体的r8b(12.2mg,0.013mmol,74%)。
ms(方法3)m/z:953.3[m+h]+
化合物s8b
向多柔比星盐酸盐(1eq.,10mg,0.017mmol)在dmf(0.35ml)中的溶液添加tea(2eq.,0.35ml,0.1m,在dmf中,0.035mmol),然后添加s8a(1eq.,9.5mg,0.017mmol)。将得到的混合物在25℃搅拌16h并通过制备型hplc(方法1)进行纯化,得到红色固体的s8b(13.2mg,0.014mmol,80%)。
ms(方法3)m/z:953.3[m+h]+
化合物r8
向32-叠氮基-3,6,9,12,15,18,21,24,27,30-十氧杂三十二烷-1-胺(1.5eq.,11.82mg,22.45μmol)在无水dmf(0.2ml)中的溶液添加6-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)己酸2,5-二氧代吡咯烷-1-基酯(1.5eq.,6.92mg,22.45μmol)在无水dmf(0.2ml)中的溶液。将所述混合物在21℃搅拌1小时,然后添加在dmso(0.2ml)中的r8b(1eq.,12mg,14.97μmol)。通过将三(3-羟基丙基三唑基甲基)胺(1eq.,0.1m,在dmf中,150μl,14.97μmol)与五水硫酸铜(1eq.,0.1m,在h2o中,150μl,14.97μmol)混合并在21℃温育1分钟,制备thpta-cu(ii)络合物。向反应混合物添加所述thpta-cu(ii)络合物(1eq.,0.05m,在dmf/h2o50/50中,300μl,14.97μmol),然后添加抗坏血酸钠(2eq.,0.5m,在h2o中,60μl,29.94μmol)。将得到的混合物在21℃温育15min并通过制备型hplc(方法1)进行纯化,得到红色固体的r8(14.35mg,9.43μmol,63%)。
hplc(方法2)rt:3.70min
ms(方法3)m/z:836.9[m+2h]2+/2
化合物s8
向32-叠氮基-3,6,9,12,15,18,21,24,27,30-十氧杂三十二烷-1-胺(1.5eq.,11.82mg,22.45μmol)在无水dmf(0.2ml)中的溶液添加6-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)己酸2,5-二氧代吡咯烷-1-基酯(1.5eq.,6.92mg,22.45μmol)在无水dmf(0.2ml)中的溶液。将所述混合物在21℃搅拌1小时,然后添加在dmso(0.2ml)中的s8b(1eq.,12mg,14.97μmol)。通过将三(3-羟基丙基三唑基甲基)胺(1eq.,0.1m,在dmf中,150μl,14.97μmol)与五水硫酸铜(1eq.,0.1m,在h2o中,150μl,14.97μmol)混合并在21℃温育1分钟,制备thpta-cu(ii)络合物。向反应混合物添加所述thpta-cu(ii)络合物(1eq.,0.05m,在dmf/h2o50/50中,300μl,14.97μmol),然后添加抗坏血酸钠(2eq.,0.5m,在h2o中,60μl,29.94μmol)。将得到的混合物在21℃温育15min并通过制备型hplc(方法1)进行纯化,得到红色固体的s8(15.5mg,10.18μmol,68%)。
hplc(方法2)rt:3.65min
ms(方法3)m/z:836.9[m+2h]2+/2
利用x-射线晶体学通过r1a确定r1的绝对构型
1)r1a的制备
为了确定r1的绝对构型,合成了酯r1a,将其结晶并通过x-射线晶体学进行分析。向冷却至0℃的r1(1eq.,111mg,0.536mmol)和三乙胺(2eq.,108mg,0.149ml,1.07mmol)在thf(3.61ml)中的溶液逐滴添加4-硝基苯甲酰基氯(1.5eq.,149mg,0.804mmol)在thf(3.61ml)中的溶液。将所述得到的溶液升温至室温并放置30分钟。添加乙酸乙酯(22ml),然后添加7ml水。分离有机层并将其用饱和nacl溶液洗涤。将所述有机层蒸发,并将残留物通过快速层析进行纯化(环己烷/etoac梯度:在20分钟内0-100%的etoac;30个柱体积),得到r1a(60.5mg,0.17mmol,88%收率)。
2)通过x-射线晶体学确定r1a的绝对构型
将r1a(60mg)溶解在3ml二氯甲烷中,并用3ml庚烷稀释。允许所述混合物在2周的时间内缓慢蒸发,诱导r1a晶体的形成。将所述晶体放置在油中,并选择尺寸为0.50×0.40×0.18mm的无色片状单晶,将其安装在玻璃纤维上并置于低温n2流中。x-射线衍射数据收集在装备有oxfordcryosystem液n2装置的brukerapexiiduokappa-ccd衍射仪上,使用cu-kα辐射
x-射线晶体学的结果呈现在图1上。
测量β-葡萄糖醛酸酶诱导的mmae释放的动力学
·r异构体的样品溶液通过向990μl人类血浆添加10μlr5(10mm,在dmso中)并在37℃温育20min来制备。
·s异构体的样品溶液通过向990μl人类血浆添加10μls5(10mm,在dmso中)并在37℃温育20min来制备。
·淬灭溶液(q)通过向1.5ml乙腈添加50μl1mhcl水溶液来制备。
·β-葡萄糖醛酸酶溶液(glu)通过向180μlh2o添加20μl来自于大肠埃希氏杆菌(escherichiacoli)的β-葡萄糖醛酸酶的甘油水溶液(6.5mg/ml)来制备。
·参比溶液(ref)通过向990μl人类血浆添加10μlmmae(10mm,在dmso中)并在37℃温育20min来制备。
向1ml每种异构体和参比溶液添加40.9ulglu。将得到的混合物在37℃温育。将45μl每种溶液的等分试样在下述时间点用155μlq淬灭:1min,2min,3min,4min,5min,6min和7min。将淬灭的等分试样以15000g离心5min,并将上清液通过lcms(方法3)进行分析,其中将选择离子记录设置到719da(对应于[mmae+h]+)。在每个时间点释放的mmae的量被计算为(样品峰面积)/(参比峰面积)×100%(图2)。
用于测量β-葡萄糖醛酸酶诱导的细胞毒性药物释放的动力学的通用程序
·r异构体的样品溶液通过向500μl人类血浆与磷酸钾缓冲液(0.1m,ph7.0)的50/50混合物添加5μl化合物r6、r7或r8(10mm,在dmso中)并在37℃温育20min来制备。
·s异构体的样品溶液通过向500μl人类血浆与磷酸钾缓冲液(0.1m,ph7.0)的50/50混合物添加5μl化合物s6、s7或s8(10mm,在dmso中)并在37℃温育20min来制备。
·淬灭溶液(q)通过向1.5ml乙腈添加50μl1mhcl水溶液来制备。
·β-葡萄糖醛酸酶溶液(glu)通过向180μlh2o添加20μl来自于大肠埃希氏杆菌的β-葡萄糖醛酸酶的甘油水溶液(6.5mg/ml)来制备。
·参比溶液(ref)通过向500μl人类血浆与磷酸钾缓冲液(0.1m,ph7.0)的50/50混合物添加5μl相应的游离细胞毒性药物(10mm,在dmso中)并在37℃温育20min来制备。
向每种样品和参比溶液添加10ulglu。将得到的混合物在25℃温育。在曲线图(图3-5)上指示的准确时间点将45μl每种溶液的等分试样用155μlq淬灭。将淬灭的等分试样以15000g离心5min,并将上清液通过lcms(方法3)进行分析,将选择离子记录设置到[m+h]+,其中m对应于游离细胞毒性药剂的分子质量。在每个时间点释放的细胞毒性药剂的量被计算为(样品峰面积)/(参比峰面积)×100%。
结果示出在图2至5中:
图2.在r5和s5的血浆溶液中β-葡萄糖醛酸酶诱导的mmae释放的动力学证实,血浆结合的r5比s5具有明显更快的切割:在温育7分钟后从血浆结合的r5释放出24%的mmae,而从血浆结合的s5仅释放出12%。
图3.在r6和s6的血浆溶液中β-葡萄糖醛酸酶诱导的mmaf释放的动力学证实,血浆结合的r6比s6具有明显更快的切割:在温育40分钟后从血浆结合的r6释放出86%的mmaf,而从血浆结合的s6仅释放出57%。
图4.在r7和s7的血浆溶液中β-葡萄糖醛酸酶诱导的sn-38释放的动力学证实,血浆结合的r7比s7具有明显更快的切割:在温育40分钟后从血浆结合的r7释放出24%的sn-38,而从血浆结合的s7仅释放出18%。
图5.在r8和s8的血浆溶液中β-葡萄糖醛酸酶诱导的多柔比星释放的动力学证实,血浆结合的r8比s8具有明显更快的切割:在温育40分钟后从血浆结合的r8释放出99%的多柔比星,而从血浆结合的s8仅释放出80%。
测量r5和s5在ph7.4的水性缓冲液中的稳定性
·样品溶液r5-pbs通过向180μl磷酸盐缓冲盐水(ph7.4)添加20μlr5(10mm,在dmso中)来制备。
·样品溶液s5-pbs通过向180μl磷酸盐缓冲盐水(ph7.4)添加20μls5(10mm,在dmso中)来制备。
·将样品在25℃温育并通过lcms(方法3)进行分析,其中将选择离子记录设置到924da(对应于[r5+2h]2+/2和[s5+2h]2+/2)和933da(形成的主要杂质,对应于水解产物[r5+h2o+2h]2+/2和[s5+h2o+2h]2+/2)。样品在下述时间点进样:0min,99min,195min,291min,387min,543min,699min,855min,980min。在0min时进样的样品的峰面积被当作参比峰面积。
·峰面积的%被计算为(924da峰面积)/((924da峰面积)+(933da峰面积))×100%。
结果示出在图6中。对于两种样品来说,在ph7.4下观察到化合物(r5或s5)的缓慢水解:30-40%的所述化合物在1000min后水解。
在ph6.0的磷酸盐缓冲盐水中进行了相同的实验。在这些条件下,在任何时间点均未观察到r5或s5的降解。
r5和s5的血浆结合动力学
·淬灭溶液(q)通过向1.5ml乙腈添加50μl1mhcl水溶液来制备。
·样品溶液r-alb通过向990μl人类血浆添加10μlr5(10mm,在dmso中)并在37℃温育来制备。
·样品溶液s-alb通过向990μl人类血浆添加10μls5(10mm,在dmso中)并在37℃温育来制备。
·在下述时间点向155μl淬灭溶液添加45μl每种样品溶液的等分试样:0min,1min,2min,3min,4min,5min,6min,7min。
·将淬灭的等分试样以15000g离心5min,并将上清液通过lcms(方法3)进行分析,其中将选择离子记录设置到924da(对应于[r5+2h]2+/2和[s5+2h]2+/2)。在0min时淬灭的等分试样的峰面积被当作参比峰面积。
·在每个时间点剩余的游离药物的%被计算为(样品峰面积)/(参比峰面积)×100%。
化合物r5和s5两者都经历与血清白蛋白的快速结合反应,导致它们的游离形式的浓度的锐减,如图7中所示。在温育2分钟后,约90%的s5或r5被结合到血清白蛋白,并在4分钟后获得完全转化。
白蛋白结合的r5和s5的血浆稳定性
·样品溶液r5-alb通过向990μl人类血浆添加10μlr5(10mm,在dmso中)来制备。
·样品溶液s5-alb通过向990μl人类血浆添加10μls5(10mm,在dmso中)来制备。
·淬灭溶液(q)通过向1.5ml乙腈添加50μl1mhcl水溶液来制备。
·参比溶液(ref)通过向990μl人类血浆添加10μlmmae(10mm,在dmso中)来制备。
·将样品溶液和参比溶液在37℃温育。
·在下述时间点向155μl淬灭溶液添加45μl每种样品溶液的等分试样:0h,8h,24h,48h,102h,192h。
·将淬灭的等分试样以15000g离心5min,并将上清液通过lcms(方法3)进行分析,其中将选择离子记录设置到719da(对应于[mmae+h]+)。
·在每个时间点释放的mmae的%被计算为(样品峰面积)/(参比峰面积)×100%。
如图8中所示,白蛋白结合的r5和s5在血浆中保持稳定,因为在长期温育后仅有痕量的细胞毒性药物(mmae)被释放(在温育192小时、即8天后少于10%)。
分离试验
按照方法2,通过hplc进行了旨在分离1:1混合物中的化合物r5和s5的试验,但试验被证明是不成功的:正如在图9中所示,获得了6.72和6.83分钟的非常接近的rt。
使用r4和s4的1:1混合物进行了类似试验,但分离也被证明是不成功的,因为获得了7.56和7.72分钟的rt(图10)。
- 还没有人留言评论。精彩留言会获得点赞!