具有直接地相对的感测电极的柔性多臂导管的制作方法
本发明整体涉及医疗探针,并且具体地涉及多电极导管。
背景技术:
各种类型的诊断导管和治疗导管可用于心脏诊断过程。例如,美国专利申请公布2016/0081746描述了一种适于在心房中标测和/或消融的导管,该导管具有篮形电极阵列,该篮形电极阵列具有两个或更多个带有可偏转扩展器的位置传感器。该导管包括导管主体、位于导管主体的远侧端部处的篮形电极组件以及位于导管主体的近侧端部处的控制柄。该篮形电极组件具有多个电极承载脊和扩展器,该扩展器适于相对于导管主体纵向移动,以用于经由延伸经过控制柄的近侧端部部分使组件扩展和塌缩,该控制柄部可由使用者推动或拉动。扩展器还适于响应于控制柄上的致动器而偏转,该致动器允许使用者控制延伸穿过导管主体和扩展器的至少一条牵拉线。
又如,美国专利6669693描述了一种具有可回缩的和可展开的伞状主体的装置。伞状主体包括用于周向接合并消融靶组织的消融元件。伞状主体是可调节的、顺从性锥形构件,其可在很宽的工作直径范围内展开。消融元件附接到脊以及附接到脊的周向环或环段。因此,附接到伞状主体的消融元件可适形于肺静脉口的几何形状并提供周向接触,这允许更准确的消融规程。
国际专利申请公布wo/2016/090175(pct/us/2015/063807)在各种实施方案中描述了用于调节靶向的神经纤维(例如,肝神经调节)或其他组织的系统、装置和方法。这些系统可被配置为进入肝脉管的曲折解剖结构或邻近肝脉管的曲折解剖结构。这些系统可被配置为靶向动脉或其他血管(诸如,肝总动脉)周围(例如,在动脉或其他血管的外膜内或血管周隙内)的神经。
美国专利申请公布2012/0172697描述了一种医疗装置,该医疗装置具有柔性细长主体、连接到细长主体的柄部、连接到细长主体的至少一个脊,以及附接到至少一个脊的柔性片材。该柔性片材在其上具有多个电极,其中该柔性片材和所述多个电极限定用于标测组织中的电信息的标测组件,并且其中所述至少一个脊和该柔性片材能够从塌缩构型移动到展开构型。
技术实现要素:
本发明的实施方案提供了一种医疗器械,该医疗器械包括轴、多个柔性脊和多个电极。轴被配置用于插入患者的身体中。所述多个柔性脊具有连接到轴的远侧端部的相应第一端部和自支撑且未锚定的相应第二端部。这些脊朝近侧弯曲,使得第二端部比第一端部更近侧。柔性脊中的每个包括被配置为致使柔性脊朝近侧弯曲的拉伸层。所述多个电极设置在柔性脊上。
在一些实施方案中,所述多个电极设置在柔性脊的直接地相对的表面上。
在一些实施方案中,柔性脊和电极分别包括电路板基板和设置在电路板基板上的金属元件。
在一些实施方案中,电路板基板被折叠,使得所述多个电极设置在电路板基板的直接地相对的小面上。
在一个实施方案中,拉伸层中的每个包括被配置为致使柔性脊朝近侧弯曲的一个或多个拉伸纤维。在另一个实施方案中,该层的拉伸强度大于相同尺寸的镍钛诺合金层的拉伸强度。在一个示例中,该层的拉伸强度大于完全退火的镍钛诺的极限拉伸强度(在约895mpa下),并且大于加工硬化的镍钛诺的拉伸强度(在约1900mpa下)。
根据本发明的实施方案,还提供了一种制造方法,该制造方法包括生产其上设置有多个电极的多个柔性脊。所述多个柔性脊安装在轴的远侧端部处。所述多个柔性脊具有连接到轴的远侧端部的相应第一端部和自支撑且未锚定的相应第二端部,其中这些脊朝近侧弯曲,使得第二端部比第一端部更近侧。
根据本发明的一个实施方案,还提供了一种制造方法,该制造方法包括在多个柔性电路板上使电极和导线图案化。将成对的柔性电路板与夹置在每对电路板之间的拉伸材料层层合,以便形成柔性脊。所述多个柔性脊安装在轴的远侧端部处。所述多个柔性脊具有连接到轴的远侧端部的相应第一端部和自支撑且未锚定的相应第二端部,其中这些脊朝近侧弯曲,使得第二端部比第一端部更近侧。包括在柔性脊中的每个中的拉伸层被配置为致使柔性脊朝近侧弯曲。
根据本发明的一个实施方案,还提供了一种制造方法,该制造方法包括在多个柔性电路板上使电极和导线图案化。柔性电路板越过由拉伸材料制成的一个或多个纤维沿电路板的相应纵向轴线折叠,使得纤维被夹置在图案化柔性板的两个直接地相对的小面之间,以便形成柔性脊。所述多个柔性脊安装在轴的远侧端部处。所述多个柔性脊具有连接到轴的远侧端部的相应第一端部和自支撑且未锚定的相应第二端部,其中这些脊朝近侧弯曲,使得第二端部比第一端部更近侧。包括在柔性脊中的每个中的拉伸层被配置为致使柔性脊朝近侧弯曲。
结合附图,通过以下对本发明的实施方案的详细描述,将更全面地理解本发明,其中:
附图说明
图1为根据本发明的实施方案的基于导管的电解剖标测系统的示意性图解;
图2是根据本发明的实施方案的柔软多臂导管的示意性图解;
图3a至图3d为根据本发明的一些实施方案的例示包括直接地相对的电极的柔性脊的制造阶段的示意图;并且
图4为根据本发明的实施方案的图2的软多臂导管的示意性详细图解。
具体实施方式
概述
心肌中的电信号可通过设置在诊断心脏导管上的感测电极来记录。此类感测电极可设置在包括刚性主干结构的导管远侧端部处,或者设置在刚性臂上。刚性主干结构可由例如脊制成,所述脊在其两个端部处固定到轴,例如组装成篮形导管。另选地,足够刚性的臂可仅保持在一个端部。
然而,在一些情况下,刚性远侧端部可能存在问题。例如,当标测心肌以获取电信号时,由刚性结构或刚性构件制成的诊断导管可通过与组织机械接触而触发异位心跳(即,由于过早心跳而导致的不规则心律)。还存在心肌被例如刚性脊的边缘穿孔的风险。
下文所述的本发明的实施方案提供了包括多个柔性脊的多臂导管,在下文中称为“柔性多臂导管”。柔性脊包括高密度的直接地相对的感测电极对。多个柔性脊从装配有软导管的轴的远侧端部的中心向外延伸,然后朝向轴向内弯曲,并且在轴的远侧端部上沿近侧方向向后弯曲。每个柔性脊弯曲而不被锚定在其另一个端部处,例如,通过将拉伸材料嵌入脊中。
换句话讲,给定的柔性脊具有连接到轴的远侧端部的相应第一端部和自支撑且未锚定的相应第二端部,其中脊朝近侧弯曲,使得第二端部比第一端部更近侧。
一些公开的实施方案利用柔性电路板来构造脊,该脊在顶侧和底侧上(即,在柔性电路板的直接地相对的表面上)均具有电极。此类几何形状使得能够在每个电极对位置测量来自两个相反方向的信号。当柔性脊完全延伸时,面向轴的电极通常将不与组织接触。当脊仍被部分地推出护套时,当这些“内部”电极仍在外侧上时,这些电极可能具有重要的临床意义,并且感测可在导管仍处于紧凑形式、部分地折叠在护套中时开始。
在一些实施方案中,电路板由柔性材料制成,该柔性材料允许电路板紧密折叠,以便在两个相对侧上形成电极。可将具有高拉伸强度的薄材料诸如
另选地或除此之外,柔性脊可包括一个或多个高拉伸强度纤维以控制其弯曲,诸如由液晶聚合物(lcp)、碳纤维、玻璃纤维和/或uhmwpe制成的纤维。在一些实施方案中,柔性电路具有以保持柔性脊的结构柔性的方式图案化为薄膜和/或嵌入纱线的电极导线。
在一些实施方案中,用于迫使柔性电路板弯曲的材料的拉伸强度大于镍钛诺合金的拉伸强度。即,对于相同的层或相同的纤维厚度,由使用上文列出的材料中的一种的层或纤维施加的张力高于如果由镍钛诺合金中的一种制成时的张力。由镍钛诺合金制成的导管臂的示例为由biosensewebster(irvine,california)制造的
本发明所公开的柔性多臂导管(其臂在从轴的远侧端部悬吊的同时朝近侧和向内自弯曲)可容纳具有高柔性和最小刚度的任何解剖结构。该设计允许医师安全地操纵心腔内的导管,并且以较小的异位搏动或穿孔风险从组织收集信号。因此,软多臂导管扩展了医师诊断某些心脏疾病的能力,尤其是在更易受心导管插入术的上述副作用影响的患者中。此外,柔性多臂设计可增加使用现有设计难以达到的解剖结构部分标测的可达性。
系统描述
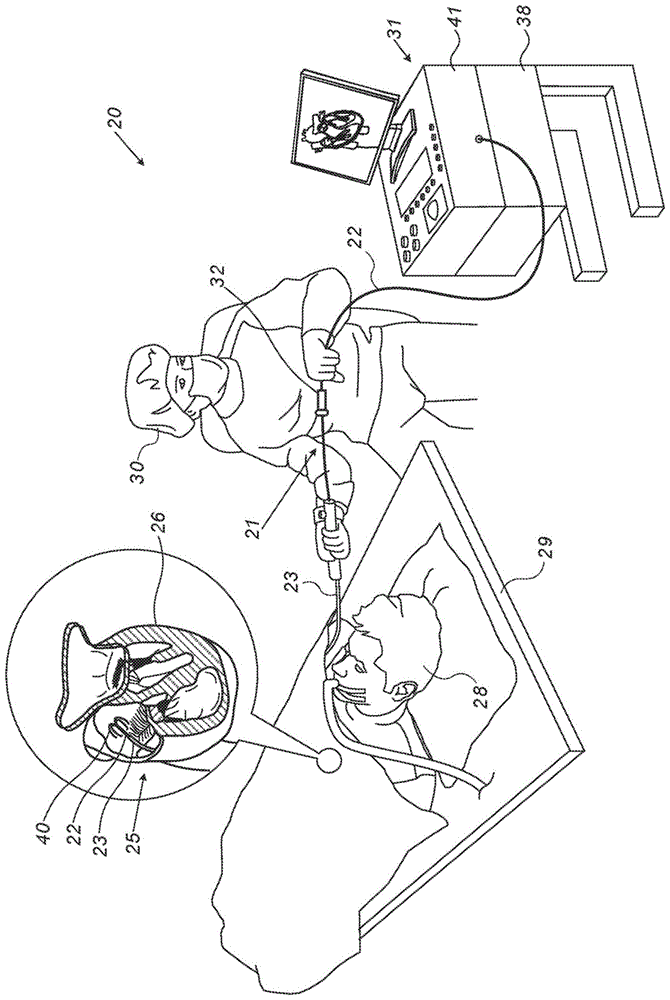
图1为根据本发明的实施方案的基于导管的电解剖标测系统20的示意性图解。系统20包括导管21,其中导管的轴22通过护套23插入患者28的心脏26中。导管21的近侧端部连接到控制台31。在本文所述的实施方案中,导管21可用于任何合适的诊断目的,诸如心脏26中组织的电生理标测和/或电解剖标测。
控制台31包括具有合适前端的处理器38,通常为通用计算机。控制台31还包括接口电路41,该接口电路用于从导管21接收信号,以及用于连接到处理器38控制的系统20的其他部件。
医生30将轴22插入穿过躺在桌子29上的患者28的血管系统。如在插图25中所见,导管21包括装配在轴22的远侧端部处的软多臂感测导管40(在被推出护套23之后)。在轴22的插入期间,软多臂导管40由护套23保持在塌缩构型中。通过将导管40包含在塌缩构型中,护套23还用于使目标位置沿途的血管创伤最小化。医师30通过使用导管的近侧端部附近的操纵器32和/或来自护套23的偏转操纵轴22,来将软多臂导管40导航到心脏26中的目标位置。一旦轴22的远侧端部到达目标位置,医师30回缩护套23,或推进轴22,从而使软多臂感测导管40伸展。然后,医师操作控制台31,以便使用电极24(见图2)感测来自目标位置处的组织的信号。
尽管图示的实施方案具体地涉及软多臂感测导管40用于心脏组织的电生理感测的用途,但系统20的元件和本文所述的方法可另外地应用于控制多电极消融装置,诸如圆形消融导管、球囊消融导管和多臂消融装置。
具有直接地相对的感测电极的软多臂导管
图2是根据本发明的实施方案的软多臂感测导管40的示意性图解。如图所示,软多臂导管40装配在轴22的远侧端部上。导管40由多个柔性脊制成,所述多个柔性脊从轴22的远侧端部的中心沿对角线向外延伸。脊随后在轴22的远侧端部上沿近侧方向向内弯曲,其中脊的另一个端部为自支撑且未锚定的。矩形感测电极24形式的多个金属元件在柔性脊27的两个小面上图案化,从而允许检测来自相反方向的信号。
在脊27被完全推出护套之前,在脊完全伸展之后面向轴的电极24可能仍然具有重要的临床意义。当脊27被部分地推出时,此类内部电极在外侧上,并且感测可在导管仍处于紧凑形式、部分地折叠在护套中时开始。
柔性脊27实际上是半浮动的,以便轻轻地适应脊可能接触的解剖结构。脊27的边缘指向轴22,以便避免脊的边缘与组织的尖锐接触。
脊27被设计成当向内按压时,例如当压靠在组织的表面上时,施加弹性反向力。弹性反向力的强度可在设计和/或制造期间进行调整,以便优化导管40的柔性。在一个实施方案中,使相反的弹性力足够强以确保电极24与组织的牢固接触,但仍然足够弱以最小化导管40的一个或多个脊27与心肌组织机械接触时的不期望事件诸如异位心跳。
图2所示的示例性例证完全是为了概念清晰而选择的。柔性脊的其他构型也是可能的。另选的或附加的图案是可能的,诸如圆形电极,以及装配附加类型的图案化传感器或电极,例如,消融、应变、超声或任何其他合适类型的传感器或电极。柔性脊27的横截面可在形状上变化。可包围柔性脊的电极的分布和数量可变化。例如,环形电极可设置在具有圆形横截面的柔性脊上。
图3a至图3d为根据本发明的一些实施方案的例示包括直接地相对的电极的柔性脊27的制造阶段的示意图。一般来讲,柔性脊和电极分别包括电路板基板和设置在电路板基板上的金属元件。
图3a示出了在被折叠以形成脊27之前的柔性电路板52。感测电极24a和24b在电路板52上图案化,其中折叠线51将它们物理地和电地分开。一旦柔性电路板52将沿折叠线51折叠,电极24a和24b将形成直接地相对的电极几何形状,如下文进一步所述。
图3b示出了折叠的脊27,其通过折叠电路板52制成以实现设置在脊27上的直接地相对的电极。折叠电路板52包裹沿脊的内部延伸的一个或多个可拉伸纤维54,并且提供所需的结构强度和脊27固定在其端部之一上时弯曲的趋势。
图3c示出了另一个实施方案,其中柔性脊27由层合在两个柔性电路板52a和52b之间的拉伸材料50诸如液晶聚合物(lcp)、超高分子量聚乙烯(uhmwpe)、对位芳族聚酰胺、碳纤维或玻璃纤维的层制成(其例如通过沿线51将电路板52切割成两个而制成)。感测电极24在板52a和52b上图案化以面向相反方向。
图3d提供了柔性板65上的电极24的图案化方案的放大剖视图。在一个实施方案中,电极层61由沉积在绝缘聚酰亚胺层64上的铜制成。接着将镍沉积到铜上,最后将金沉积到镍上。在另选的实施方案中,电极层61由溅射到绝缘聚酰亚胺层64上的钛钨(tiw)籽晶层制成。接着将金溅射到籽晶层上,然后在电镀过程中添加最终的金层。用于电极24的导电迹线63嵌入在聚酰亚胺层64下方以便将电极24连接到系统20,其中聚酰亚胺绝缘层64将迹线63与电极层61隔离。在一个实施方案中,导电迹线63由包封在金层66中的铜制成。形成通路62(通孔)(例如,通过蚀刻或钻穿印刷板52)并用金电镀,以便将电极24与导电迹线63电连接。在一个实施方案中,通路62延伸得更深并且一直穿过柔性板65,以连接直接地相对的电极(图3d仅示出了涂覆有电极的一个小面,而对于连接相对的电极,通路延伸得深得多以到达柔性板65的另一个小面上的另一个电极)。
粘合剂层66将聚酰亚胺层64粘结到柔性板65,以便提供额外耐久性并有助于制造多个层。
图3a至图3d中所示的制造设计的示例仅为了概念清楚而选择。在另选的实施方案中,图案化设计可包括不同数量和类型的电极。柔性脊27的不同部分和层的加工技术可变化。
在一个实施方案中,提供了柔性多臂导管,该柔性多臂导管具有在每个柔性脊27上图案化的至多三十二个感测电极24(例如,十六个相对的对)。导管40由八个脊制成,使得设置在导管40处的感测电极的总数多达256个电极。
图4为根据本发明的实施方案的图2的软多臂导管的示意性详细图解。例如,图4中的导管42示出了每个脊27上的12个电极对24,每个电极对24具有背向纵向轴线100的电极24a和面向纵向轴线100的电极24b。脊27被配置为使得当脊27从管状轴22完全延伸时,曲率半径r可与脊的内表面27b的一部分一致。如图所示,脊27相对于轴22的纵向轴线100向外延伸,然后朝近侧和向内弯曲。在一个实施方案中,拉伸材料50被配置为使得柔性脊27以相对于纵向轴线100约0.40英寸的预设曲率半径r(即,柔性脊27具有的近似圆弧形状的半径)自由弯曲,以便使柔性脊27装配到具有类似典型尺寸(例如肺静脉口的尺寸)的弯曲解剖结构中。
一般来讲,在导管40被完全展开之后,电极24a的至少一部分将与组织物理接触。另一方面,电极24b通常将不与组织接触(而是仅与血液接触)。当脊仍被部分地推出护套时,当这些“内部”电极仍在外侧上时,电极24b可能具有重要的临床意义,并且感测可在导管仍处于紧凑形式、部分地折叠在护套中时开始。另外,电极24b可用于收集背景(例如,远场)电生理信号,该处理器41可用于分析来自相应电极24a的组织电生理信号。
在一个实施方案中,电极24a和24b的尺寸在宽度乘以长度上都分别为约0.040×约0.027英寸。相邻电极24之间的间隙34的长度为约0.030英寸。电极和间隙的尺寸被设计成使得其提供医学上所需的心脏内测量的电生理信号的空间分辨率。本文所述和所示的示例性构型允许消除脊中的刚性主干构件诸如镍钛诺线,同时允许通过每个电极对24的外部电极24a和内部电极24b(图4)检测来自脊27的两侧的信号。这可通过将每个脊配置成具有柔性电路基板来实现。基板具有在基板的外表面上的导电表面作为电极。通过使用具有设置在表面之间的合适的拉伸构件(例如,聚合物纤维)的薄柔性电路,医师可操纵心脏中的脊27并收集信号而不管脊27的取向如何,并且降低了由于脊构件引起的并发症的风险。
尽管本文所述的实施方案主要针对心脏电生理标测和/或电解剖标测,但本文所述的方法和系统也可以用于其他应用,诸如耳鼻喉科或神经内科手术中。
因此应当理解,上面描述的实施方案以举例的方式被引用,并且本发明不限于上文特定示出和描述的内容。相反,本发明的范围包括上文描述的各种特征的组合和子组合以及它们的变型和修改,本领域的技术人员在阅读上述描述时将会想到该变型和修改,并且该变型和修改并未在现有技术中公开。以引用方式并入本专利申请的文献被视为本申请的整体部分,不同的是如果这些并入的文献中限定的任何术语与本说明书中明确或隐含地给出的定义相冲突,则应仅考虑本说明书中的定义。
- 还没有人留言评论。精彩留言会获得点赞!