治疗线粒体功能障碍的方法和制剂与流程
治疗线粒体功能障碍的方法和制剂
1.相关申请的交叉引用
2.本申请要求2018年12月31日提交的授予moore等人的名称为“methods and formulations to treat mitochondrial dysfunction”的美国临时申请序列号62/786,970的优先权;该临时申请的公开内容全文以引用方式并入本文。
技术领域
3.本发明涉及治疗原发性和继发性线粒体功能障碍的治疗方法和药物制剂。
背景技术:
4.先前研究的候选药物是常规的amp依赖性ampk激活剂,其作用机制需要通过rc抑制(例如,二甲双胍、白藜芦醇)或转化为amp模拟物(例如,aicar)来引起amp升高。涉及rc抑制的间接机制不适用于潜在的线粒体功能障碍的情况,而ampk的amp依赖型激活导致其他amp调节的酶的激活,从而实现复合多效性。此外,先前的研究已确定直接的、非amp依赖性ampk激动剂用于治疗糖尿病、肥胖症和代谢综合征的目的。
5.原发性线粒体疾病是一组在临床上具有异质性的病症,其通常是进行性、多系统性的,并且与儿童的高死亡率相关。它们是由线粒体呼吸链(rc)的遗传性缺陷引起的,从而导致活性氧和氮物质(ros和rns)的产量增加,以及总能量产量不足。这些导致的代谢失衡会导致细胞损伤,并最终导致细胞死亡。
6.目前尚无针对原发性线粒体疾病的治愈性治疗。仅支持性治疗可用,并涉及治疗特定症状(例如,糖尿病、心脏病和下垂症)和由维生素辅因子和抗氧化剂组成的“线粒体混合物”。不幸的是,元分析表明,可用的支持性干预缺乏功效,突显了对新型治疗的需求(参见例如,pfeffer等人,cochrane database sys rev.,2012年4月18;4;chinnery等人,2006,cochrane database sys rev.,2006年1月25日;(1);所述文献的公开内容全文以引用方式并入本文)。
7.继发性线粒体疾病也表现出线粒体功能障碍,但与原发性线粒体疾病不同,它不是由与线粒体呼吸链相关的基因引起的。继发性线粒体疾病诸如帕金森氏病或阿尔茨海默病是由于由间接破坏线粒体的其他疾病、疾患或环境因素引起的获得性线粒体异常所致。因此,针对原发性线粒体疾病确定的任何治疗都有望同样有益于与继发性线粒体功能障碍相关的病症和疾患,包括神经变性病症、神经肌肉病症和肌肉萎缩病症。
技术实现要素:
8.本文公开了根据本发明的实施方案的治疗线粒体功能障碍的方法和制剂。
9.在一个实施方案中,一种治疗患有线粒体功能障碍的患者的方法包括识别个体的线粒体功能障碍并将ampk激动剂提供给该个体。
10.在另一个实施方案中,线粒体功能障碍是原发性线粒体功能障碍。
11.在另一个实施方案中,原发性线粒体功能障碍选自由以下项组成的组:常染色体
显性视神经萎缩(adoa)、阿尔佩斯
‑
胡滕洛赫尔综合征(ndna缺陷)、共济失调神经病变综合征(ndna缺陷)、巴斯综合征/致死性婴儿心肌病(lic)、辅酶q缺乏症、复合体i、复合体ii、复合体iii、复合体iv和复合体v缺乏症(单一缺乏症或缺乏症的任何组合)、慢性进行性眼外肌麻痹(cpeo)、糖尿病和耳聋、卡恩斯
‑
塞尔综合征(mtdna缺陷)、伴脑干和脊髓受累及乳酸升高的脑白质病(lbsl
‑
脑白质营养不良)、莱氏综合征(mtdna和ndna缺陷)、莱伯氏遗传性视神经病变(lhon)、拉夫特病、线粒体肌病、脑病、乳酸酸中毒和卒中综合征(melas)(mtdna缺陷)、线粒体烯酰辅酶a还原酶蛋白相关神经变性(mepan)、肌阵挛性癫痫伴破碎红纤维(merrf)、线粒体隐性共济失调综合征(miras)、mtdna缺失综合征、mtdna耗竭综合征、mtdna维持病症、mtdna/rna翻译缺陷、线粒体trna合成酶缺乏症、线粒体肌病、线粒体神经胃肠型脑病综合征(mngie)、神经源性肌无力、共济失调和色素性视网膜炎(narp)、皮尔森综合征、丙酮酸脱氢酶复合物缺乏症(pdcd/pdh)、dna聚合酶γ缺乏症(polg)、丙酮酸羧化酶缺乏症和胸苷激酶2缺乏症(tk2)。
12.在另一个实施方案中,线粒体功能障碍是继发性线粒体功能障碍。
13.在另一个实施方案中,继发性线粒体功能障碍选自由以下项组成的组:肌萎缩性脊髓侧索硬化症(als)、阿尔茨海默病(ad)和其他痴呆症、弗里德希共济失调(fa)、亨廷顿氏病(hd)、运动神经元病(mnd)、n
‑
聚糖酶缺乏症(ngly1)、有机酸血症、帕金森氏病(pd)和pd相关病症、朊病毒病、脊髓性肌肉萎缩症(sma)、脊髓小脑性共济失调(sca)、贝克型肌营养不良、先天性肌营养不良、杜兴型肌营养不良、埃默里
‑
德雷弗斯肌营养不良、面肩胛肱型肌营养不良、肌强直性营养不良、眼咽型肌营养不良、夏柯
‑
马利
‑
杜斯氏病、先天性肌病、远端肌病、内分泌性肌病(甲状腺功能亢进性肌病、甲状腺功能减退性肌病)、巨轴索神经病、遗传性痉挛性截瘫、炎性肌病(皮肌炎、包涵体肌炎、多肌炎)、代谢性肌病、神经肌肉接头疾病、自闭症、癌症、糖尿病、代谢综合征、慢性疲劳综合征、炎性病症、关节炎和衰老。
14.在另一个实施方案中,ampk激动剂是直接ampk激动剂。
15.再次,在另一个实施方案中,直接ampk激动剂选自由以下项组成的组:pt1、etc
‑
1002、水杨酸盐、c991、c13、d561
‑
0775、mt 63
‑
78、a
‑
769662、zln024、c24、mk
‑
8722、pf
‑
739和pf
‑
06409577。
16.再次,在另一个实施方案中,ampk激动剂是amp依赖性激动剂。
17.在另一个实施方案中,amp依赖性激动剂选自由二甲双胍、白藜芦醇和aicar组成的组。
18.在另一个实施方案中,ampk激动剂以药物制剂的形式提供。
19.在又一个实施方案中,药物制剂包含ampk激动剂以及由粘结剂、润滑剂、缓冲剂和包衣组成的组中的至少一者。
20.在又一个实施方案中,提供步骤包括向个体口服施用ampk激动剂。
21.再次,在另一个实施方案中,提供步骤包括每天施用ampk激动剂,持续至少一周。
22.再次,在另一个实施方案中,该方法还包括评估ampk激动剂在个体中的功效。
23.在另一个实施方案中,提供步骤通过由以下项组成的组中的至少一种施用ampk激动剂来完成:口服施用、皮下施用、静脉内施用、腹膜内施用、鼻内施用、皮肤施用和吸入。
24.在另一个实施方案中,一种治疗线粒体病症的方法包括识别个体的病症并调节个体中的ampk活性。
25.再次,在又一个实施方案中,调节步骤通过激活个体中的ampk来完成。
26.在又一个实施方案中,激活步骤通过使ampk磷酸化或为ampk提供激动剂来完成。
27.在又一个实施方案中,调节步骤通过抑制个体中的ampk来完成。
28.在又一个实施方案中,病症与线粒体功能障碍相关。
29.再次,在另一个实施方案中,线粒体功能障碍是原发性线粒体功能障碍。
30.再次,在另一个实施方案中,线粒体功能障碍是继发性线粒体功能障碍。
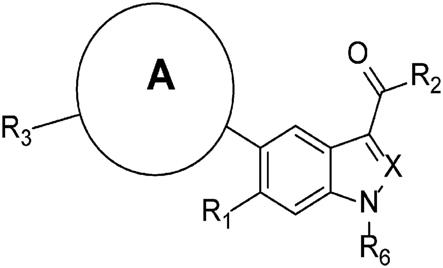
31.再次,在又一个实施方案中,ampk激动剂包含式
32.的分子,
33.其中:
34.a选自未取代或被一个或多个c1‑6烷基或氟取代基取代的5元环杂环
35.x为cr5或n;
36.r1为h、cf3或卤代基;
37.r2为or5、nhoh、nhso2r4、och2ocor4,或者cor2为c连接的四唑,
38.r3为未取代或被一至三个选自卤代基、oh和ocor7的取代基取代的c1‑
10
烷基、c3‑7环烷基、c4‑
12
烷基环烷基、c4‑
10
环烷基烷基、c3‑7杂环烷基、c4‑
12
烷基杂环烷基、c4‑
10
杂环烷基烷基、芳基或杂芳基;
39.r4为未取代或被一至三个卤素取代基取代的c1‑
10
烷基、c3‑7环烷基、c4‑
12
烷基环烷基、c4‑
10
环烷基烷基;
40.r5为r4或h;
41.r6为h、c1‑6烷基、c3‑6环烷基或两个r6基团与它们所连接的氮原子一起可形成四至七元杂环烷基环,所有这些环可任选地被1至3个氟原子取代;并且
42.r7为未取代或被一至三个选自氟、c1‑
10
烷基和nr6、r6的取代基取代的c1‑
10
烷基、c3‑7环烷基、c4‑
12
烷基环烷基。
43.再次,在又一个实施方案中,a选自由以下项组成的组:
[0044][0045]
在又一个实施方案中,a选自由以下项组成的组:
[0046][0047]
在又一个实施方案中,a选自由以下项组成的组:
[0048][0049]
再次,在又一个实施方案中,x为ch,r6为h,r1为cl,并且r2为oh。
[0050]
再次,在又一个实施方案中,该分子具有如图13a
‑
13z和图14a
‑
14o中的一者所示的式。
[0051]
再次,在又一个实施方案中,该分子具有下式:
[0052][0053]
再次,在又一个实施方案中,ampk激动剂包含下式的分子:
[0054][0055]
其中:
[0056]
x为ch或n;
[0057]
r1为小烷基(c1
‑
c4)或卤素(例如,cl、br或f);
[0058]
r2为苯基、烷基c1
‑
c10、环烷基(c3
‑
c10)、羟烷基(c1
‑
c6)、杂芳族(例如,吡啶基、吡唑基、吡咯基、嘧啶基、噻吩基、呋喃基或三唑)或杂环c4
‑
c6;
[0059]
其中苯基任选地被卤素(例如,cl、br或f)取代,
[0060]
其中烷基为直链或支链的并且任选被oh、ome、oet取代,
[0061]
其中环烷基任选地被一个或多个oh取代,
[0062]
其中羟烷基为直链或支链的
[0063]
其中杂芳族任选地被小烷基(c1
‑
c6)或羟烷基(c1
‑
c6)取代,其中烷基和羟烷基为直链或支链的,
[0064]
其中杂环中的杂原子任选地为o、s或nr4,其中r4为直链或支链的c1
‑
c6烷基或羟烷基;并且
[0065]
r4为直链或支链的c1
‑
c6烷基或羟烷基。
[0066]
在另一个实施方案中,该分子具有下式:
[0067][0068]
在另一个实施方案中,ampk激动剂包含下式的分子:
[0069][0070]
其中:
[0071]
a为稠环(例如,c3
‑
c10环烷基);
[0072]
x为ch或n;
[0073]
y为o、s、nh、nr3;
[0074]
r1为小烷基(c1
‑
c4)或卤素(例如,cl、br或f);
[0075]
r2为苯基、烷基c1
‑
c10、环烷基(c3
‑
c10)、羟烷基(c1
‑
c6)、杂芳族(例如,吡啶基、吡唑基、吡咯基、嘧啶基、噻吩基、呋喃基或三唑)或杂环c4
‑
c6;
[0076]
其中苯基任选地被卤素(例如,cl、br或f)取代,
[0077]
其中烷基为直链或支链的并且任选被oh、ome、oet取代,
[0078]
其中环烷基任选地被一个或多个oh取代,
[0079]
其中羟烷基为直链或支链的
[0080]
其中杂芳族任选地被小烷基(c1
‑
c6)或羟烷基(c1
‑
c6)取代,其中烷基和羟烷基为直链或支链的,
[0081]
其中杂环中的杂原子任选地为o、s或nr4;
[0082]
r3为c1
‑
c6烷基(直链或支链的);并且
[0083]
r4为直链或支链的c1
‑
c6烷基或羟烷基。
[0084]
在又一个实施方案中,a选自c6苯环或以下中的一者:
[0085][0086]
再次,在另一个实施方案中,该分子具有下式:
[0087]
附图说明
[0088]
参考以下详细描述并结合附图来考虑,将更好地理解本发明的这些和其他特征和优点,其中:
[0089]
图1a示出了根据各种实施方案的由ampk激活和抑制的途径。
[0090]
图1b
‑
1d示出了根据各种实施方案的ampk激动剂的结构。
[0091]
图2a
‑
2f示出了根据各种实施方案的在各种处理下的细胞活力测定的结果。
[0092]
图3a
‑
3n示出了根据各种实施方案的在各种处理下的成纤维细胞的细胞形态。
[0093]
图4a示出了根据各种实施方案的在敲低试验中的pampk浓度。
[0094]
图4b示出了根据各种实施方案的用各种处理进行的敲低研究中的细胞活力结果。
[0095]
图4c
‑
4f示出了根据各种实施方案的用各种处理进行的敲低研究中的细胞形态结果。
[0096]
图5a示出了根据各种实施方案的处理试验后的pampk浓度。
[0097]
图5b
‑
5d示出了根据各种实施方案的处理试验后的基因表达水平。
[0098]
图6a
‑
6h示出了根据各种实施方案的在各种缺陷型成纤维细胞系上进行处理和未
进行处理的细胞呼吸结果。
[0099]
图7a
‑
7c示出了根据各种实施方案的在处理和不处理各种缺陷型成纤维细胞系的情况下的atp浓度。
[0100]
图7d
‑
7f示出了根据各种实施方案的在处理和不处理各种缺陷型成纤维细胞系的情况下的活性氧物质(ros)浓度。
[0101]
图8a示出了根据各种实施方案的对照和ngly1缺陷型成纤维细胞系中的脂褐素水平。
[0102]
图8b示出了根据各种实施方案的在ngly1缺陷型成纤维细胞系中以及在处理和不处理的情况下的脂褐素水平。
[0103]
图9a示出了根据各种实施方案的在对照和诱导的amd模型中在处理和不处理的情况下的视网膜的眼底镜检查图像。
[0104]
图9b示出了根据各种实施方案的在对照和诱导的amd模型中在处理和不处理的情况下的视网膜的视网膜节段图像。
[0105]
图9c示出了根据各种实施方案的在对照和诱导的amd模型中在处理和不处理的情况下的视网膜的onl厚度测量结果。
[0106]
图9d示出了根据各种实施方案的在对照和诱导的amd模型中在处理和不处理的情况下的视网膜的视网膜电图图像。
[0107]
图9e示出了根据各种实施方案的在用ampk激动剂处理后减少的视网膜退化。
[0108]
图10a示出了根据各种实施方案的在经处理的和未经处理的缺血组织中的梗塞组织的百分比。
[0109]
图10b和图10c示出了根据各种实施方案的在经处理的和未经处理的缺血组织中具有梗塞组织的脑片。
[0110]
图11a
‑
11c示出了根据各种实施方案的经处理的和未经处理的小鼠的运动表现。
[0111]
图11d和图11e示出了根据各种实施方案的经处理的和未经处理的小鼠中的线粒体功能和糖原贮存。
[0112]
图11f和图11g示出了根据各种实施方案的对经处理的和未经处理的小鼠进行的acc磷酸化测定的结果。
[0113]
图12a示出了根据各种实施方案的ampk激动剂的一般结构。
[0114]
图12b
‑
12d示出了根据各种实施方案的合成ampk激动剂的图示方法。
[0115]
图13a
‑
13z示出了根据各种实施方案的ampk激动剂的结构。
[0116]
图14a
‑
14o示出了根据各种实施方案的ampk激动剂的结构。
[0117]
图15a
‑
15b示出了根据各种实施方案的ampk激动剂的一般结构。
[0118]
图15c示出了根据各种实施方案的合成ampk激动剂的方法的示意图。
[0119]
图15d示出了根据各种实施方案的ampk激动剂的结构。
[0120]
图16a示出了根据各种实施方案的对线粒体缺陷细胞进行的acc磷酸化测定的结果。
[0121]
图16b示出了根据各种实施方案的用于确定ec50的ampk激动剂的ampk活性。
[0122]
图17示出了根据各种实施方案的治疗个体的方法。
[0123]
图18示出了根据各种实施方案的在个体中调节ampk活性的方法。
具体实施方式
[0124]
现在转到数据和说明,描述了被配置为治疗线粒体病症、疾病和/或功能障碍的治疗方法和药物制剂。在各种实施方案中,所述方法和制剂使用amp激活的蛋白激酶(ampk)的激动剂。ampk是细胞能量稳态的主要调节剂,在能量不足时被激活以恢复三磷酸腺苷(atp)的水平。一般来讲,ampk通过激活atp产生途径(例如,糖酵解、线粒体生物发生)和抑制atp消耗途径(例如,糖异生和脂肪酸合成)来恢复能量稳态。ampk促进的其他途径或过程包括抗氧化酶、自噬、脂肪酸代谢和肌肉再生。图1示出了由ampk激活或抑制的多种途径。ampk对葡萄糖和脂肪酸途径的调节使其成为糖尿病、肥胖症和代谢综合征的有吸引力的治疗靶标,从而确定ampk激动剂用于此目的。
[0125]
为了克服ampk间接激动剂的缺陷,某些实施方案涉及直接的、非amp依赖性ampk激动剂,以治疗具有潜在的线粒体功能障碍的病症和疾患。ampk直接激活化合物包括pt1、etc
‑
1002、水杨酸盐、c991、c13、d561
‑
0775、mt 63
‑
78、a
‑
769662、zln024、c24、mk
‑
8722(图1b)、pf
‑
739(图1c)和pf
‑
06409577(图1d),其通过直接结合到α或β亚基来变构激活ampk,并且在一些情况下被证明能改善体内脂质和葡萄糖分布(参见例如,cool等人,cell metab.,2006年6月,3(6):403
‑
16;pang等人,j biol chem.,2008年6月6日,283(23):16051
‑
60;hawley等人,science.,2012年5月18日,336(6083):918
‑
22;li等人,toxicol appl pharmacol.,2013年12月1日,273(2):325
‑
34;zhang等人,plos one.,2013年8月20日,8(8);xiao等人,nat commun.,2013年,4:3017;zadra等人,embo mol med.,2014年4月,6(4):519
‑
38;hunter等人,chem biol.,2014年7月17日,21(7):866
‑
79;pinkosky等人,nat commun.,2016年11月28日,7:13457;cameron等人,2016年9月8日,59(17):8068
‑
81;myers等人,science.,2017年8月4日,357(6350):507
‑
511;cokorinos等人,cell metab.,2017年5月2日,25(5):1147
‑
1159;xi等人,oncotarget.,2017年11月10日,8(56):96089
–
96102;这些文献的公开内容全文以引用方式并入本文)。
[0126]
使用直接ampk激动剂的各种实施方案进行的治疗提高了细胞呼吸和atp水平并且降低氧化应激,从而导致患有原发性和继发性线粒体疾病(包括与继发性线粒体功能障碍相关的多种病症和疾患)的患者的细胞活力得到持续有效的改善。与原发性和继发性线粒体功能障碍相关的疾病和病症分别列于表1和表2中。此外,直接ampk激动剂可预防年龄相关性黄斑变性(amd)中的视网膜变性,对缺血性卒中提供神经保护作用,并且足以增强运动表现。另外,直接ampk激动剂能在原发性和继发性线粒体病症中减轻与线粒体功能障碍相关的已知负面影响,诸如视网膜损伤、神经元变性和肌肉萎缩。这样,某些实施方案涉及n
‑
聚糖酶(ngly1)缺乏症、年龄相关性黄斑变性(amd)、缺血性卒中、肌营养不良(例如,杜兴型和贝克型)、弗里德希共济失调(fa)、自身免疫性病症伴肌肉受累(例如,包涵体肌炎、多肌炎和皮肌炎)和/或神经变性病症(例如,肌萎缩性脊髓侧索硬化症(als)、帕金森氏病和阿尔茨海默病)的治疗。此外,心脏组织中的ampk激活可导致可逆的心脏肥大,因此各种实施方案涉及与扩张型心肌病相关的疾病的治疗(参见例如,arad等人,circ res.,2007年3月2日,100(4):474
‑
88;myers等人,science,2017年8月4日,357(6350):507
‑
511;所述文献的公开内容全文以引用方式并入本文)。
[0127][0128]
[0129]
[0130][0131]
ampk激动剂特性的表征
[0132]
下面提供了所选ampk激动剂的特性,以表征本发明的示例性实施方案的性能。尽管讨论了一些特定的激动剂,但应当理解,结果仅是为了提供激动剂功能的概述,并非旨在进行限制。
[0133]
直接ampk激动剂对细胞活力和形态的影响
[0134]
各种实施方案利用直接ampk激动剂增加患有线粒体功能障碍的个体的细胞活力和形态。图2a
‑
2f示出了一些实施方案的直接ampk激动剂对细胞活力的影响。图2a
‑
2d示出了在四个缺乏细胞色素c氧化酶组装因子(surf1,图2a)、血红素a:法尼基转移酶细胞色素c氧化酶组装因子(cox10,图2b)、线粒体复合体i(ci,图2c)和线粒体dna聚合酶γ(polg,图2d)的成纤维细胞系中的细胞活力。在图2a中,各种实施方案的四种直接ampk激动剂pt1、a
‑
769662、zln024和c24证明与未经处理的细胞(例如,用媒介物dmso处理的细胞)相比,活力增加了35%
‑
55%。图2b
‑
2d示出了线粒体功能障碍对细胞活力的影响,包括呼吸链和线粒体dna(mtdna)复制机制的组成部分。转到图2b
‑
2d,尽管基因缺陷的致病机制不同,但直接ampk激动剂pt1提高了这些突变株的存活率。另外,其余化合物在突变株之间显示出不同的响应:a
‑
769662提高了ci和polg缺陷型细胞的存活率,zln024提高了ci缺陷型细胞的存活率,并且c24提高了surf1缺陷型细胞的存活率而并非其他细胞系中任一种的存活率。此外,ampk间接激动剂aicar不能增加除surf1之外的其他任何细胞系的细胞活力(图2a),表明aicar不如直接ampk激动剂有效。直接ampk激动剂pt1在表现出ngly
‑
1缺陷的成纤维细胞中显示出相似的结果,如图2e所示。图2e示出了从三个个体中分离的缺乏ngly
‑
1的成纤维细
胞。与未经处理的(
‑
pt1)细胞相比,用pt1(+pt1)处理的成纤维细胞表现出提高至多60%的活力。此外,图2f示出了各种实施方案的三种新型ampk激动剂对细胞活力的影响。在图2f中,ampk激动剂mk
‑
8722、pf
‑
739和pf
‑
06409577显示出surf1缺陷型成纤维细胞的细胞活力的水平呈剂量依赖性变化。因此,各种实施方案的直接ampk激动剂在一系列原发性和继发性线粒体疾病病因学范围内提高了细胞活力。
[0135]
转到图3a
‑
3n,根据许多实施方案,示出了具有各种缺陷的成纤维细胞的细胞形态。具体地,图3a和图3b示出了缺乏surf1的成纤维细胞,其中图3a示出了未经处理(仅dmso)的细胞形态,而图3b示出了用pt1处理的surf1缺陷型成纤维细胞显示出比图3a中未经处理的细胞改善的细胞形态。类似地,图3c
‑
3j示出了当用pt1处理时的细胞形态的相似结果,其中图3c和图3d示出了缺乏cox10的成纤维细胞,图3e和图3f示出了缺乏ci的成纤维细胞,图3g和图3h示出了缺乏polg的成纤维细胞,并且图3i和图3j示出了缺乏ngly
‑
1的成纤维细胞。类似地,图3c、图3e、图3g和图3i示出了未经处理的缺陷型成纤维细胞,而图3d、图3f、图3h和图3j示出了用pt1处理的成纤维细胞。此外,图3k
‑
3n示出了新开发的ampk激动剂mk
‑
8722、pf
‑
739和pf
‑
06409577对surf1缺陷型成纤维细胞的影响。具体地,图3k示出了仅用媒介物dmso处理的surf1缺陷型成纤维细胞,而图3l示出了用mk
‑
8722处理后改善的细胞形态,图3m示出了用pf
‑
739处理后改善的细胞形态,并且图3n示出了用pf
‑
06409577处理后改善的细胞形态。因此,各种实施方案的直接ampk激动剂在一系列原发性和继发性线粒体疾病病因学内改善了细胞形态。
[0136]
现在转到图4a
‑
4f,某些实施方案的直接ampk激动剂对ampk激活具有特异性,而不是非特异性相互作用。图4a示出了磷酸化ampk(pampk)的蛋白质印迹(western印迹),显示出用小干扰rna(sirna)转染cox10缺陷型成纤维细胞后的处理后pampk与微管蛋白的相对水平。与用作对照的用非特异性sirna转染的细胞(sicnt)相比,特异于ampkα亚基基因prkaa1的sirna导致pampk水平降低。图4b示出了在进行和未进行pt1处理以及进行和未进行sirna转染的情况下cox10缺陷型成纤维细胞的细胞活力,表明与未经处理的细胞(dmso)和用pt1处理并用siampk转染的细胞(siampk+pt1)相比,单独的pt1处理(pt1)和pt1处理与非特异性sicnt的组合(sicnt+pt1)增加了活力。此外,与对照条件(sicnt+pt1)相比,用pt1处理并选择性敲低ampk(siampk+pt1)导致pampk水平降低63%并且细胞活力降低41%,这与对pt1的细胞响应由ampk激活介导的理念一致。图4c
‑
4f示出了与图4b相同的条件下的细胞形态。具体地,图4c示出了未经处理的cox10缺陷型成纤维细胞;图4d示出了用pt1处理的cox10缺陷型成纤维细胞;图4e示出了用siampk转染并用pt1处理的cox10缺陷型成纤维细胞;并且图4f示出了用对照sicnt转染并用pt1处理的cox10缺陷型成纤维细胞。
[0137]
转到图5a
‑
5d,直接ampk激动剂的某些实施方案解决了由线粒体功能障碍引起的代谢干扰。图5a示出了在用pt1处理0小时、2小时、24小时和48小时的surf1缺陷型成纤维细胞中归一化至肌动蛋白的pampk水平。图5a示出了pampk水平在pt1处理后2小时内增加,并在pt1处理后24小时达到峰值。此外,pt1处理后48小时后,pampk水平恢复到基线位置。在图5b
‑
5d中,根据各种实施方案,pt1处理的效果增加了线粒体生物合成和抗氧化基因的基因表达。图5b示出了过氧化物酶体增殖物激活的受体γ共激活因子1
‑
α(pgc
‑
1α)的表达增加2.4倍,而图5c和图5d分别示出了锰超氧化物歧化酶(sod2)的表达增加1.3倍并且过氧化氢酶的表达增加1.5倍。
[0138]
直接ampk激动剂对细胞呼吸的影响
[0139]
各种实施方案改善了患有线粒体功能障碍的个体的细胞呼吸。如上所述,某些实施方案增加了pgc
‑
1α表达。与具有累积的继发mtdna突变和活性氧物质(ros)的衰老线粒体相比,pgc
‑
1α刺激了具有增强的呼吸功能的新线粒体的生物发生。转到图6a
‑
6h,示出了由一些实施方案的直接ampk激动剂引起的改善的呼吸功能。图6a
‑
6c分别示出了surf1、polg和ngly1缺陷型成纤维细胞的基础耗氧率(ocr)。根据各种实施方案,尽管每个基因的病因学差异,但与未经处理细胞(dmso)相比,surf1、polg和ngly1缺陷型成纤维细胞在用pt1处理后,surf1和polg缺陷型成纤维细胞的基础呼吸改善了约30%,并且ngly1缺陷型成纤维细胞的基础呼吸改善了16%。此外,图6d和图6e示出了surf1(图6d)和polg(图6e)缺陷型成纤维细胞中用于atp合成(atp耦合呼吸)的基础线粒体耗氧量。在这种情况下,与未经处理的(dmso)成纤维细胞相比,用pt1进行的处理显示出surf1缺陷型成纤维细胞改善了约40%(图6d),并且polg缺陷型成纤维细胞改善了30%(图6e),这与某些实施方案一致。此外,根据一些实施方案,用pt1进行的处理改善了最大呼吸能力,这反映了细胞对增加的atp需求作出响应的能力,如图6f
‑
6h所示。在图6f中,与未经处理的(dmso)成纤维细胞相比,surf1缺陷型成纤维细胞在用直接ampk激动剂pt1处理的细胞中显示出最大呼吸改善约50%。类似地,图6g示出了与未经处理的(dmso)成纤维细胞相比,polg缺陷型成纤维细胞在用直接ampk激动剂pt1处理的细胞中显示出最大呼吸改善约20%。而且,图6h示出了与未经处理的(dmso)成纤维细胞相比,当用直接ampk激动剂pt1处理时,ngly1缺陷型成纤维细胞的最大呼吸改善约40%。
[0140]
直接ampk激动剂对氧化应激和能量状态的影响
[0141]
现在转到图7a
‑
7f,各种实施方案在线粒体功能障碍中提高了atp产量并降低了活性氧物质(ros)水平。具体地,图7a、图7b和图7c分别示出了与未经处理的(dmso)成纤维细胞相比,用直接ampk激动剂pt1处理时,surf1缺陷型成纤维细胞的atp产量增加35%,polg缺陷型成纤维细胞的atp产量增加36%,并且ngly1缺陷型成纤维细胞的atp产量增加40%。另外,图7d、图7e和图7f分别示出了与未经处理的(dmso)成纤维细胞相比,用直接ampk激动剂pt1处理时,surf1缺陷型成纤维细胞的ros水平降低10%,polg缺陷型成纤维细胞的ros水平降低15%,并且ngly1缺陷型成纤维细胞的ros水平降低18%。线粒体功能障碍导致通过呼吸链(rc)的电子传递不完全,从而导致atp合成减少和活性氧物质(ros)过量产生(参见例如,atkuri等人,proc natl acad sci u s a.,2009年3月10日,106(10):3941
‑
5;enns等人,plos one.,2014年6月18日;9(6);所述文献的公开内容全文以引用方式并入本文)。atp和ros含量反映细胞能量和氧化状态,这两者均取决于有效的atp耦合呼吸和整体线粒体功能。细胞对这些代谢干扰的响应涉及激活途径,该激活途径可改善细胞呼吸(例如,线粒体生物发生)并上调内源性抗氧化剂的表达以中和ros并降低氧化应激。因此,如图7a
‑
7f所示,atp产量的提高和ros水平的降低显示了各种实施方案改善线粒体功能障碍的氧化应激和能量状态的能力。
[0142]
直接ampk激动剂对脂褐素水平的影响
[0143]
一些实施方案减少了异常糖蛋白的积累,如图8a
‑
8b所示。某些线粒体功能障碍,包括由ngly1缺陷引起的功能障碍,会导致被称为脂褐素的蛋白质和脂质的积累(参见例如,jobst等人,j clin pathol.,1991年5月;44(5):437
–
438;该文献的公开内容全文以引
用方式并入本文)。如图8a所示,与正常成纤维细胞(对照)相比,ngly1缺陷型成纤维细胞表现出高约60%的脂褐素水平。图8b示出了根据各种实施方案,用直接ampk激动剂pt1进行的处理将ngly1缺陷型成纤维细胞中的脂褐素水平降低约36%。
[0144]
ampk激活减轻amd的视网膜变性
[0145]
现在转到图9a
‑
9e,各种实施方案减轻了由线粒体功能障碍引起的视网膜损伤。具体地,图9a示出了根据某些实施方案,用和不用碘酸钠(si)以及用和不用直接ampk激动剂pt1处理的视网膜的眼底镜检查图像。si是一种能选择性诱导视网膜色素上皮(rpe)中的氧化应激和线粒体功能障碍的毒素。因此,经si处理的组织模拟了由线粒体功能障碍引起的视网膜病症,诸如amd。如图9a所示,使用和未使用pt1(+pt1和
‑
pt1)的未进行si处理(
‑
si)的组织具有相似的正常组织。然而,用si处理但未使用pt1的组织(+si;
‑
pt1)显示出视网膜变性的迹象,包括白色沉积物。然而,同时用si和pt1处理的组织(+si;+pt1)显示出改善的视网膜变性迹象。因此,表明各种实施方案的直接ampk激动剂减轻了视网膜变性。类似地,图9b示出了视网膜节段的h&e染色的相似结果。如图所示,未经si处理的组织(
‑
si;
‑
pt1和
‑
si,+pt1)具有相似的外观。然而,
–
si;+
‑
pt1组织显示出视网膜变性的迹象,包括光感受器外核水平(onl)变薄,内层和光感受器外段/内段(is/os)紊乱以及黑色素碎屑的存在。通过在经si处理的组织中的pt1处理,这些疾病的适应症有所减轻,包括对onl变薄的保护(白色条),光感受器形态的改变以及黑色素碎屑的减少(黑色箭头)。onl厚度的测量结果如图9c所示,其中未用si处理的组织(si
‑
,pt1
‑
和si
‑
,pt1+)以及经si和pt1处理的组织(si+,pt1+)显示出比未进行pt1处理的经si处理的组织(si+,pt1
‑
)更大的厚度。另外,图9d展示了与用si且不用pt1处理的组织(pt1
‑
;si+)相比,用si和pt1处理的视网膜组织(pt1+;si+)的改善的电响应达到与正常组织(pt1
‑
;si
‑
和pt1+;si
‑
)相似的水平。
[0146]
另外,图9e示出了野生型小鼠(wt/wt)的视网膜厚度,因为这些小鼠具有细胞色素c氧化酶组装蛋白sco2的敲除和/或敲入等位基因,其中敲入等位基因代表sco2蛋白上的e129k突变。具体地,小鼠是杂合敲入和野生型(ki/wt)小鼠或杂合敲除和敲入(ko/ki)小鼠。图9e示出了与仅用媒介物(veh)处理的小鼠相比,经处理(mk8722)的小鼠如何表现出更少的退化。
[0147]
线粒体疾病患者的眼中的线粒体功能障碍会导致诸如视网膜病和视神经萎缩的眼科表现,并且线粒体功能受损也已被证明与年龄相关性黄斑变性(amd)相关。鉴于眼睛是人体中最具能量依赖性的组织之一,具有眼科发现的原发性和继发性线粒体疾病都有望受益于ampk激活(参见例如,calaza等人,neurobiol aging.,2015年10月,36(10):2869
‑
76;该文献的公开内容全文以引用方式并入本文)。因此,各种实施方案的直接ampk激动剂将用于治疗患有与线粒体功能障碍相关的眼科疾病的患者。
[0148]
缺血性卒中的神经保护
[0149]
一些实施方案在患有缺血性卒中的个体中提供神经保护。神经元中线粒体能量代谢的受损是缺血性卒中和许多神经变性病症(包括某些原发性线粒体疾病、ad、pd和als)的关键致病因素(schon等人,j clin invest.,2003年2月1日;111(3):303
–
312;该文献的公开内容全文以引用方式并入本文)。图10a
‑
10c展示了直接ampk对患有缺血性卒中的个体的神经保护作用。具体地,图10a示出了患有缺血性卒中的脑组织中梗塞组织的百分比。如图10a所示,与仅用媒介物dmso(媒介物)处理的个体相比,用pt1进行的处理显示出显著的改
善。转到图10b和图10c,示出了tcc染色的脑片,其中仅用媒介物处理的个体(图10b)以白色显示高水平的缺血组织,而根据各种实施方案,用pt1处理的个体(图10c)显示出白色的缺血组织的量要少得多。
[0150]
ampk激动剂对运动表现和骨骼肌的影响
[0151]
各种实施方案将用于改善患有线粒体功能障碍以及肌肉萎缩疾病诸如肌营养不良和自身免疫性肌炎病症的个体的运动表现。图11a
‑
11c示出了根据各种实施方案的使用ampk激动剂mk
‑
8722的肌肉性能的改善。图11a示出了在用ampk激动剂和仅用递送媒介物处理的sco2基因中,具有各种基因型的小鼠在活动室中行进的距离。具体地,图11a示出了仅用媒介物处理的杂合敲入和野生型小鼠(1102),仅用媒介物处理的杂合敲入和敲除小鼠(1104),用ampk激动剂处理的杂合敲入和野生型小鼠(1106),以及用ampk激动剂处理的杂合敲入和敲除小鼠(1108)。如图11a所示,杂合敲入和野生型小鼠无论用ampk激动剂(1106)还是仅用媒介物(1102)处理都显示出相似的活动水平,而杂合敲除和敲入等位基因的小鼠在仅用媒介物处理(1104)时显示出降低的活动,但是用ampk激动剂处理(1108)的敲除/敲入小鼠的活动恢复到与敲入/野生型相当的水平。
[0152]
图11b示出了使用ampk激动剂的敲除/敲入小鼠(1108)相比于仅用媒介物处理的敲除/敲入小鼠(1104)的转棒表现改善。此外,使用ampk激动剂的敲除/敲入小鼠(1108)显示出比用ampk激动剂(1106)或用媒介物(1102)处理的敲入/野生型小鼠更高的水平。类似地,图11c示出了来自挂线试验的结果,表明许多实施方案的ampk激动剂改善了肌肉性能。具体地,ampk激动剂能够将敲除/敲入小鼠(1108)的挂线时间改善到比敲入/野生型小鼠(1102、1106)以及经媒介物处理的敲除/敲入小鼠(1104)更高的水平。总的来说,图11a
‑
11c示出了来自许多实施方案的ampk激动剂的ampk激活可增强与线粒体功能障碍相关的肌肉变性病症的强度、耐力和整体运动功能。
[0153]
许多实施方案还能够提高骨骼肌中的线粒体功能和/或糖原贮存,如图11d
‑
11e所示。图11d示出了指示线粒体细胞色素c氧化酶(ctyoc)和琥珀酸脱氢酶(sdh)活性的组织学染色。与较浅染色的仅经媒介物处理的样品相比,在用ampk激动剂处理的实施方案中的较深染色指示活性增加。类似地,图11e中糖原的较深染色说明在用ampk激动剂的实施方案处理的样品中贮存的糖原的存在增加。提高的线粒体功能和糖原含量的组合表明实施方案能够使骨骼肌内的能量水平正常化,从而防止变性和虚弱。
[0154]
转到图11f
‑
11g,骨骼肌中acc的磷酸化增加。具体地,图11f示出了在仅用媒介物处理的小鼠(ki/ko veh)中以及在用许多实施方案的ampk激动剂处理的小鼠(ki/ko mk8722)中的磷酸化acc(pacc)的蛋白质印迹。图11g汇总了通过在仅用媒介物处理的小鼠(ki/ko veh)和用许多实施方案的ampk激动剂处理的小鼠(ki/ko mk8722)中将pacc归一化至1的蛋白质印迹。因此,图11f
‑
11g表明许多实施方案的ampk激动剂能够激活骨骼肌中的ampk。
[0155]
ampk激动剂的实施方案
[0156]
许多实施方案涉及ampk的高效、选择性和稳定的小分子激动剂。许多此类实施方案涉及具有如图12a所示的一般结构的分子。许多实施方案将修改图12a中的一般结构,以基于图12a中的结构生成衍生物分子。可通过本领域已知或本文描述的多种方式测试衍生分子的活性,诸如测量样品中的pacc,以作为增加ampk活性的指标。通过改变某些片段、r基
团等,可以对每个片段如何影响ampk活性形成系统的理解。
[0157]
某些实施方案的衍生物分子由12a中的结构开发而来。在许多实施方案中,部分、r基团或其他片段可被以下中的一者或多者取代:
[0158]
·
a选自未取代或被一个或多个c1‑6烷基或氟取代基取代的5元环杂环;
[0159]
·
x为cr5或n;
[0160]
·
r1‑
为h、cf3‑
或卤代基;
[0161]
·
r2为or5、nhoh、nhso2r4、och2ocor4,或者cor2为c连接的四唑,
[0162]
·
r3为未取代或被一至三个选自卤代基、oh和ocor7的取代基取代的c1‑
10
烷基、c3‑7环烷基、c4‑
12
烷基环烷基、c4‑
10
环烷基烷基、c3‑7杂环烷基、c4‑
12
烷基杂环烷基、c4‑
10
杂环烷基烷基、芳基或杂芳基;
[0163]
·
r4为未取代或被一至三个卤素取代基取代的c1‑
10
烷基、c3‑7环烷基、c4‑
12
烷基环烷基、c4‑
10
环烷基烷基;
[0164]
·
r5为r4或h;
[0165]
·
r6为h、c1‑6烷基、c3‑6环烷基或两个r6基团与它们所连接的氮原子一起可形成四至七元杂环烷基环,所有这些环可任选地被1至3个氟原子取代;
[0166]
·
r7为未取代或被一至三个选自氟、c1‑
10
烷基和nr6、r6的取代基取代的c1‑
10
烷基、c3‑7环烷基、c4‑
12
烷基环烷基。
[0167]
在许多实施方案中,a选自由以下项组成的组:
[0168][0169]
多种实施方案可诸如通过使用如图12b
‑
12d所示的方法来制造或合成。图12b示出
了合成图13a所示的化合物的方法。具体地,图12b示出了将环丁酮与2,5
‑
二溴噻吩结合以生成1
‑
(5
‑
溴噻吩
‑2‑
基)环丁
‑1‑
醇的步骤1。在步骤2处,将双联频哪醇硼酸酯添加到步骤1的结果中以生成1
‑
(5
‑
(4,4,5,5
‑
四甲基
‑
1,3,2
‑
二氧杂环戊硼烷
‑2‑
基)噻吩
‑2‑
基)环丁
‑1‑
醇。步骤3将该产物与5
‑
溴
‑6‑
氯
‑
1h
‑
吲哚
‑3‑
羧酸甲酯和k2co3结合以生成6
‑
氯
‑5‑
(5
‑
(1
‑
羟基环丁基)噻吩
‑2‑
基)
‑
1h
‑
吲哚
‑3‑
羧酸甲酯。最后,步骤4通过将步骤3的产物与naoh和乙醇结合,生成6
‑
氯
‑5‑
(5
‑
(1
‑
羟基环丁基)噻吩
‑2‑
基)
‑
1h
‑
吲哚
‑3‑
羧酸(图13a)。尽管图12b的过程生成了图13a所示的化合物,但应当指出的是,可以类似的方式(例如,图12c
‑
12d所示的过程)生成另外的化合物,诸如图13b
‑
13z和图14a
‑
14o所示的化合物。
[0170]
另外的实施方案将通过图12c所示的方法制备,使得硼基团首先连接到这些实施方案的吲哚环,然后耦合到a环(如图12a所示)。
[0171]
另外的实施方案将通过图12d的方法制备,其中a环含有四个氮原子。
[0172]
另外的实施方案可具有不同的结构,同时仍然保持激活ampk的能力。一些实施方案将具有一般结构,诸如图15a
‑
15b所示。
[0173]
某些实施方案的衍生物分子由15a中的结构开发而来。在许多实施方案中,部分、r基团或其他片段可被以下中的一者或多者取代:
[0174]
·
x为ch或n;
[0175]
·
r1为小烷基(c1
‑
c4)或卤素(例如,cl、br或f);
[0176]
·
r2为苯基、烷基c1
‑
c10、环烷基(c3
‑
c10)、羟烷基(c1
‑
c6)、杂芳族(例如,吡啶基、吡唑基、吡咯基、嘧啶基、噻吩基、呋喃基或三唑)或杂环c4
‑
c6;
[0177]
ο其中苯基任选地被卤素(例如,cl、br或f)取代,
[0178]
ο其中烷基为直链或支链的并且任选被oh、ome、oet取代,
[0179]
ο其中环烷基任选地被一个或多个oh取代,
[0180]
ο其中羟烷基为直链或支链的
[0181]
ο其中杂芳族任选地被小烷基(c1
‑
c6)或羟烷基(c1
‑
c6)取代,其中烷基和羟烷基为直链或支链的,
[0182]
ο其中杂环中的杂原子任选地为o、s或nr4,其中r4为直链或支链的c1
‑
c6烷基或羟烷基;并且
[0183]
·
r4为直链或支链的c1
‑
c6烷基或羟烷基。
[0184]
某些实施方案的衍生物分子由15b中的结构开发而来。在许多实施方案中,部分、r基团或其他片段可被以下中的一者或多者取代:
[0185]
·
a为稠环(例如,c3
‑
c10环烷基);
[0186]
·
x为ch或n;
[0187]
·
y为o、s、nh、nr3;
[0188]
·
r1为小烷基(c1
‑
c4)或卤素(例如,cl、br或f);
[0189]
·
r2为苯基、烷基c1
‑
c10、环烷基(c3
‑
c10)、羟烷基(c1
‑
c6)、杂芳族(例如,吡啶基、吡唑基、吡咯基、嘧啶基、噻吩基、呋喃基或三唑)或杂环c4
‑
c6;
[0190]
ο其中苯基任选地被卤素(例如,cl、br或f)取代,
[0191]
ο其中烷基为直链或支链的并且任选被oh、ome、oet取代,
[0192]
ο其中环烷基任选地被一个或多个oh取代,
[0193]
ο其中羟烷基为直链或支链的
[0194]
ο其中杂芳族任选地被小烷基(c1
‑
c6)或羟烷基(c1
‑
c6)取代,其中烷基和羟烷基为直链或支链的,
[0195]
ο其中杂环中的杂原子任选地为o、s或nr4;
[0196]
·
r3为c1
‑
c6烷基(直链或支链的);并且
[0197]
·
r4为直链或支链的c1
‑
c6烷基或羟烷基。
[0198]
在多种实施方案中,a为c6苯环。在许多实施方案中,a选自由以下项组成的组:
[0199][0200]
转到图15c,示出了合成实施方案的方法。具体地,图15c示出了合成图15d所示的实施方案(也称为ev8017)的方法。虽然图15c的过程生成了图15d所示的化合物,但应当指出的是,另外的化合物可以类似的方式生成。
[0201]
转到图16a,示出了图13a所示的新型ampk激动剂的生物效应。具体地,图16a示出了用图13a所示的实施方案处理的线粒体缺陷患者细胞(标记为ev8016)和仅用媒介物处理的细胞(标记为dmso)中的磷酸化acc(pacc)的蛋白质印迹。如上所述,关于图11f,acc的磷酸化指示ampk激活,因此表明根据许多实施方案的化合物能够激活ampk。
[0202]
转到图16b,可确定ampk激动剂的各种实施方案的ec50。在示例性实施方案ev8016(图13a)中,ec50被确定为232nm,而pf
‑
06409577实施方案(图1d)被确定为96nm。本领域技术人员将认识到并理解如何确定另外的实施方案的ec50。
[0203]
用ampk激动剂治疗个体的方法
[0204]
现在转到图17,各种实施方案涉及在过程1700中治疗个体的线粒体功能障碍。在一些实施方案中,在步骤1702处,识别个体的线粒体功能障碍。在某些实施方案中,患有功能障碍的个体通过表现出的症状被发现,诸如n
‑
聚糖酶(ngly1)缺乏症、年龄相关性黄斑变性(amd)、缺血性卒中、肌营养不良(例如,杜兴型和贝克型)、弗里德希共济失调(fa)、自身免疫性疾病伴肌肉受累(例如,包涵体肌炎、多肌炎和皮肌炎)、神经变性病症(例如,肌萎缩性脊髓侧索硬化症(als)、帕金森氏病和阿尔茨海默病)、糖尿病、代谢病症和/或肥胖症。在其他实施方案中,线粒体功能障碍将基于疾病或功能障碍的分子标记进行识别,使得蛋白质印迹(western印迹)、聚合酶链反应(pcr)、使用遗传标志物(例如,单核苷酸多态性(snp)、表达序列标签(est)、简单序列重复标记(ssr)等)的基因分型将识别个体中存在的特定疾病或功能障碍。
[0205]
在各种实施方案中,在步骤1704处,用ampk激动剂治疗个体。在一些实施方案中,ampk激动剂是直接的(或非amp依赖性的)激动剂,而在其他实施方案中,ampk激动剂是amp依赖性激动剂。直接激动剂的实例包括pt1、etc
‑
1002、水杨酸盐、c991、c13、d561
‑
0775、mt 63
‑
78、a
‑
769662、zln024、c24、mk
‑
8722、pf
‑
739和pf
‑
06409577。atp依赖性激动剂的实例包括二甲双胍、白藜芦醇和aicar。在某些实施方案中,以治疗有效剂量向个体提供ampk激动剂,其中在治疗开始期间和/或之后,治疗有效剂量减少、消除或减轻线粒体功能障碍的后果。在一些实施方案中,ampk激动剂通过口服、皮下、静脉内、腹膜内注射、鼻内施用、皮肤施用、经由吸入、眼内(包括玻璃体内)和/或提供治疗效果的任何方法来提供。在某些实施方
案中,ampk激动剂被配制为提供治疗效果。在一些实施方案中,ampk制剂包括粘结剂、润滑剂、缓冲剂和/或包衣,该包衣允许ampk激动剂的药代动力学释放以提供治疗效果。
[0206]
另外,ampk激动剂和/或制剂将以适当的剂量和给药方案提供给个体,以提供治疗效果。在一些实施方案中,ampk激动剂将以单剂量提供,而一些实施方案将在一段时间内提供多剂量。在各种实施方案中,剂量将以总体积的浓度的形式来实现,使得剂量将为10nm、30nm、100nm、1μm、100μm或更高,具体取决于治疗效果。在另外的实施方案中,给药将以ampk激动剂的质量与所治疗个体的质量的比率进行,使得剂量将为1mg/kg、5mg/kg、10mg/kg、20mg/kg、50mg/kg、100mg/kg或更高,具体取决于治疗效果。在多次给药的实施方案中,给药方案可为1剂/天、2剂/天、3剂/天或更多,并且可以持续必要的时间,使得给药可以持续1周、2周、3周、4周、5周、10周、20周,或在个人的生命期内永久存在。
[0207]
在其他实施方案中,剂量和/或给药方案将在治疗过程中根据各种因素而变化,包括达到酶活性的阈值。在一些实施方案中,将使用较高的剂量治疗个体,并且将在一段时间后降低,使得在各种实施方案中,将在一段时间(诸如1周、2周、4周或更长时间)内使用100μm的日剂量,然后将减少剂量以继续治疗个人。在某些实施方案中,给药方案将改变,使得剂量之间的时间将在治疗过程中改变。例如,某些实施方案将在一段时间(例如,1周、2周、4周等)内向个体提供ampk激动剂日剂量,然后将增加剂量之间的时间量,使得随后的剂量在剩余的治疗过程中每半周、每周或每月发生一次。
[0208]
在步骤1706处,各种实施方案将评估个体的ampk激动剂功效。在某些实施方案中,该步骤通过评估疾病症状来完成,诸如针对步骤1702列出的那些症状,而在其他实施方案中,该步骤将通过查看分子概况诸如基因分型、基因表达和参考步骤1702所公开的其他方法来完成。
[0209]
调节ampk活性的方法
[0210]
现在转到图18,各种实施方案涉及调节ampk活性以治疗个体的疾病或病症,如过程1800所示。在一些实施方案中,在步骤1802处,识别与线粒体功能障碍相关的病症或疾病。这些疾病和/或病症的实例包括表1
‑
表2中列出的疾病和病症,使得该疾病和/或病症与线粒体功能障碍诸如原发性线粒体功能障碍和/或继发性线粒体功能障碍相关。在各种实施方案中,基于个体表现出的症状来识别疾病和病症,而在一些实施方案中,将基于疾病或功能障碍的分子标记来识别疾病和病症,诸如蛋白质印迹(western印迹)、聚合酶链反应(pcr)、使用遗传标志物(例如,单核苷酸多态性(snp)、表达序列标签(est)、简单序列重复标记(ssr)等)的基因分型。
[0211]
在步骤1804处,各种实施方案将调节ampk活性。调节ampk活性可激活ampk或抑制ampk活性。在某些实施方案中,ampk活性将通过使ampk磷酸化或提供ampk激动剂而被激活。在某些实施方案中,调节通过抑制ampk活性来完成。ampk的抑制可使用竞争性抑制剂或变构抑制剂来完成,这会防止ampk催化反应。
[0212]
在步骤1806处,各种实施方案将评估个体的治疗功效。在某些实施方案中,该步骤通过评估疾病症状来完成,诸如针对步骤1802列出的那些症状,而在其他实施方案中,该步骤将通过查看分子概况诸如基因分型、基因表达和参考步骤1802所公开的其他方法来完成。
[0213]
示例性实施方案
[0214]
进行实验以证明根据实施方案的测定和抑制剂的能力。这些结果和讨论并非旨在进行限制,而仅仅是提供操作装置及其特征的实例。
[0215]
材料与方法
[0216]
本研究使用先前得自四名原发性线粒体疾病患者(surf1、complex i、cox10、polg)、三名ngly1缺乏症患者和四名正常对照的成纤维细胞。所有样品均在获得知情同意的情况下获得,并得到stanford irb的批准。成纤维细胞在37℃、5%co2下维持在dmem培养基中,该培养基含有8.3mm葡萄糖并补充有10%胎牛血清(fbs)(fisher scientific)、1%青霉素
‑
链霉素(10,000u/ml)(life technologies)、1%glutamax(life technologies)、1%尿苷(5mg/ml)和1%丙酮酸盐(11mg/ml)。
[0217]
为了筛选各种化合物,将15x103个细胞/500ul培养基以四联组接种在24孔微量滴定板上。第二天,去除培养基,用pbs洗涤孔,并替换为线粒体胁迫培养基,该培养基含有dmem、1%青霉素
‑
链霉素(10,000u/ml)(life technologies)、10%fcs(fisher scientific)、1mm半乳糖(sigma aldrich)和25μm叠氮化钠,含或不含以下化合物:1mm aicar(medchem express)、1mm二甲双胍(sigma aldrich)、100μm pt1(santa cruz biotechnology)、100μm a
‑
769662(medchem express)、100μm c24(medchem express)。用各种化合物处理后,分析组织培养物的生长、耗氧率和atp水平。
[0218]
实施例1:细胞生长和活力
[0219]
方法:使用钙黄绿素乙酰甲酯(anaspec)通过荧光法测量细胞生长。去除线粒体胁迫培养基,用pbs洗涤孔,然后在37℃、5%co2下与500ul/孔的800nm钙黄绿素乙酰甲酯在pbs中温育30分钟。通过flouroskan ascent微孔板荧光计(thermo scientific)使用485nm激发获得的值来测量细胞活力。
[0220]
细胞atp含量通过lc
‑
ms来测量。将细胞用胰蛋白酶处理,用冷pbs洗涤,并使用nh4ac(0.05m ph6)裂解。将裂解物转移至分子量截止过滤器(chromsystems),并在4℃、800xg下旋转20分钟。离心后,使用nanodrop nd
‑
1000(nanodrop technologies)对上清液进行dna定量分析,并通过6400系列三重四极杆lc/ms系统(agilent technologies)进行atp定量。
[0221]
用leica dm irb显微镜通过相差显微术以10倍的放大倍率观察组织培养物中的成纤维细胞,并用hamamatsu orca
‑
er相机拍摄图像。
[0222]
通过双尾学生t检验计算统计学显著性(p<0.05)。
[0223]
结果:对surf1缺陷型成纤维细胞测试ampk的四种直接激活剂pt1、a
‑
769662、zln024和c24。先前被证明能改善体外线粒体功能的amp类似物aicar(golubitzky等人,plos one.,2011年;6(10);该文献的公开内容全文以引用方式并入本文;)包含在研究设计中作为阳性对照。与未经处理的细胞(即,用媒介dmso处理的细胞)相比,用直接ampk激动剂处理的突变细胞显示出活力增加35%
‑
55%(图2a),其中pt1显示出最大的改善。与相应的未经处理的对照(即,用pbs处理的细胞)相比,在用aicar处理的surf1细胞也观察到较小但仍很显著的效果,平均细胞存活率提高了57%。
[0224]
为了评估这些发现是否扩展到surf1缺乏症以外的线粒体病症,使用来自缺乏线粒体复合体i(ci)、血红素a:法尼基转移酶细胞色素c氧化酶组装因子(cox10)和线粒体dna聚合酶γ(polg)的患者的成纤维细胞进行类似研究。因此,这些研究评估了广泛范围的线
粒体破坏,包括呼吸链和mtdna复制机制的不同组分。尽管致病机制不同,但一种化合物pt1持续且显著地提高了所有突变株的存活率(图2b
‑
2d)。其余化合物在突变株之间显示出不同的响应:a
‑
769662提高了ci和polg缺陷型细胞的存活率,zln024提高了ci缺陷型细胞的存活率,并且c24提高了surf1缺陷型细胞的存活率而并非其他细胞系中任一种的存活率。有趣的是,aicar治疗也没有提高除surf1外其他任何细胞系的存活率。用来自nlgy
‑
1缺乏症患者的成纤维细胞观察到相似的结果,活力提高至多60%(图2e)。此外,对新开发的ampk激动剂mk
‑
8722、pf
‑
739和pf
‑
04609577进行了测试,并且表明它们与pt1类似地改善了surf1患者细胞的活力,并且这种改善是以剂量依赖性方式发生的(图2e)。此外,与未经处理的细胞(图3a、图3c、图3e、图3g和图3i)相比,在surf1(图3b)、cox10(图3d)、ci(图3f)、polg(图3h)和ngly1(图3j)缺陷型成纤维细胞上进行pt1处理后,细胞形态得到了改善,其中未经处理的细胞显示出明亮的凋亡细胞。此外,与未经处理的成纤维细胞(图3k)相比,mk
‑
8722(图3l)、pf
‑
739(图3m)和pf
‑
04609577(图3n)改善了surf1缺陷型成纤维细胞的细胞形态,其中未经处理的细胞显示出明亮的凋亡细胞。
[0225]
结论:这些结果表明,直接ampk激活能在一系列原发性和继发性线粒体疾病病因内提高细胞活力,这得到在用pt1处理的突变细胞中观察到与用dmso处理的细胞相比改善的细胞形态的支持。
[0226]
实施例2:在ampk上测量ampk激动剂
[0227]
方法:进行蛋白质印迹以确定用pt1处理的细胞中的pampk水平。用补充有原钒酸钠、pmsf和蛋白酶抑制剂混合物的ripa缓冲液裂解细胞。将全细胞提取物通过sds
‑
page分级分离,并使用转移装置根据制造商的方案(bio
‑
rad)转移至聚偏二氟乙烯膜上。与5%脱脂奶在tbst(10mm tris,ph 8.0,150mm nacl,0.5%tween 20)中温育60分钟后,将膜用tbst洗涤一次,并与针对ampk(1:1,000)、pampk(1:1,000)、肌动蛋白(1:10,000)的抗体一起在4℃下温育过夜。将膜洗涤三次,持续5分钟,并与辣根过氧化物酶缀合的抗小鼠或抗兔抗体的1:10,000稀释液一起温育2小时。将印迹用tbst洗涤三次,并根据制造商的方案用ecl系统(thermo scientific)显影。
[0228]
为了测试对pt1的细胞响应是ampk激活本身的结果,还是仅仅是非特异性相互作用的结果,使用sirna敲低策略。将prkaa1的sirna(s101)和阴性对照(life technologies)与hiperfect试剂(qiagen)在含有dmem、1%青霉素
‑
链霉素(10,000u/ml)(life technologies)、1%glutamax(life technologies)但不含血清的培养基中温育,并且使其在室温下复合10分钟。然后将复合物添加到6孔微量滴定板中的cox10患者组织培养物(每种sirna的最终sirna浓度为10nm),并且在37℃、5%co2下温育72小时。在温育期结束时,通过蛋白质印迹分析(参见上述方案)分析细胞的ampk和pampk水平,或者将细胞与pt1(或dmso,作为未经处理的对照)再温育六天,并通过钙黄绿素乙酰甲酯评估活力。用pt1和siampk或sicnt处理cox10缺陷型成纤维细胞,并且通过蛋白质印迹评估响应的pampk蛋白质表达(图4a),通过钙黄绿素乙酰甲酯荧光测定评估细胞活力(图4b),并通过相差显微术评估细胞形态(图4c
‑
4f)。
[0229]
结果:将来自surf1缺陷患者细胞的培养成纤维细胞用pt1处理0小时、2小时、24小时和48小时,并测量pampk水平。pampk水平到pt1处理后2小时增加,并在24小时达到峰值,并在48小时恢复到基线(图5a)。与对照条件(pt1+sicnt)相比,用pt1处理并选择性敲低
ampk(pt1+siampk)导致pampk水平降低63%并且细胞活力降低41%,这与对pt1的细胞响应由ampk激活介导的理念一致。用pt1处理48小时后,过氧化物酶体增殖物激活的受体γ共激活因子1
‑
α(pgc
‑
1α)(线粒体生物发生的主要调节剂)增加了2.4倍(图5b)。类似地,过氧化氢酶和锰超氧化物歧化酶(sod2)(受ampk调控的两个主要抗氧化基因)分别增加了1.3倍和1.5倍(图5c
‑
5d)。
[0230]
结论:pt1的作用机制解决了线粒体功能障碍引起的主要代谢破坏;因此刺激线粒体生物发生并通过ampk激活触发氧化应激响应。
[0231]
实施例3:耗氧量和细胞呼吸
[0232]
背景:为了确定通过pt1处理上调pgc
‑
1是否与线粒体呼吸的改善相关,在surf1和polg患者的成纤维细胞两者中评估耗氧率(ocr)。
[0233]
方法:使用xf96细胞外流量分析仪(seahorse biosciences)测量耗氧率(ocr)。将成纤维细胞在37℃、5%co2下以10x103个细胞/孔接种在xf 96孔板上的100ul培养基中,该培养基含有8.3mm葡萄糖并补充有10%胎牛血清(fbs)(fisher scientific)、1%青霉素
‑
链霉素(10,000u/ml)(life technologies)、1%glutamax(life technologies)、1%尿苷(5mg/ml)和1%丙酮酸盐(11mg/ml)。第二天,将培养基替换为含或不含pt1、a
‑
769662和aicar的线粒体胁迫培养基(如上文所详述)。48小时后,将胁迫培养基替换为175μl非缓冲xf基础dmem培养基(fisher scientific),其成分与线粒体胁迫培养基相同,并且在测量前于37℃温育30分钟以达到平衡。测量ocr基线测量值三次,每五分钟一次。在实验后,通过钙黄绿素乙酰甲酯荧光强度(fi)估计细胞含量,并以ocr除以fi来计算ocr。
[0234]
结果:尽管病因学差异明显,但用pt1处理的surf1和polg患者细胞均显示出基础呼吸改善大约30%(图6a
‑
6b),而pt1则显示出ngly1患者细胞中的基础ocr增加16%(图6c)。
[0235]
用于atp合成(atp耦合呼吸)的基础线粒体耗氧量分数也在surf1中提高了40%并且在polg中提高了30%,表明pt1对氧化磷酸化的耦合效率具有积极作用(图6d
‑
6e)。
[0236]
在surf1和polg细胞两者中,最大呼吸能力(反映细胞对增加的atp需求的响应能力)均得到了改善,分别增加了50%和20%(图6f
‑
6g),而pt1在ngly1患者细胞中显示出最大ocr增加40%(图6h)。
[0237]
结论:通过非amp依赖性机制激活ampk可能是靶向线粒体功能障碍的更适合的机制。
[0238]
实施例4:测量氧化应激和能量状态
[0239]
背景:atp和ros含量反映细胞能量和氧化状态,这两者都取决于有效的atp耦合呼吸作用和整体线粒体功能。线粒体功能障碍导致通过rc的电子传递不完全,从而导致atp合成减少和活性氧物质(ros)过量产生。(atkuri等人,proc natl acad sci usa.,2009年3月10日;106(10):3941
‑
5;enns等人,plos one.,2014年6月18日;9(6);所述文献的公开内容全文以引用方式并入本文。)
[0240]
方法:surf1、polg和ngly1患者细胞补充有pt1或dmso(未经处理的对照),保持48小时(n=3)并通过celltiter
‑
glo atp测定或者保持72小时(n=3)来测量atp水平,并通过cellrox deep red流式细胞术测定来测量ros水平。将结果归一化至总蛋白质浓度。数据表示为平均值+平均值的标准误差。统计显著性测量为p<0.05。
[0241]
结果:随着处理,surf1中的atp含量增加了35%,polg中的atp含量增加了36%,并且ngly1患者细胞中的atp含量增加了40%,并且与经dmso处理的细胞相比,ros水平分别降低了10%、15%和18%(图7a
‑
7f)。
[0242]
结论:与观察到的上调atp耦合呼吸以及抗氧化剂过氧化氢酶和sod2的表达(实施例2;图5c
‑
5d)一致,通过pt1处理,原发性或继发性线粒体功能障碍患者细胞中的能量不足和氧化应激均得到改善。
[0243]
实施例5:对amd的测量影响
[0244]
方法:为生成amd模型,在si(或媒介物)处理之前的24小时和12小时对小鼠进行100mg/kg pt1(或媒介物)处理,然后在si后每24小时处理一次,持续3天。pt1和si两者均通过腹膜内(ip)注射递送,并且在si施用3天后对动物进行表型分析。
[0245]
麻醉小鼠,并使用1%硫酸阿托品、2.5%盐酸去氧肾上腺素和0.5%盐酸丙美卡因使其瞳孔放大。使用micron iii小动物视网膜成像ad相机(phoenix research laboratories,inc)进行眼底镜检查。
[0246]
通过记录暗适应和明适应的erg(espion e2 system,diagnosys llc)来评估视网膜功能。在erg记录之前,使小鼠暗适应过夜,并且所有程序均在黑暗或暗红色光下进行。麻醉小鼠,并如上所述使其瞳孔放大。对于erg记录,将电极置于角膜中心上。将接地针状电极置于尾巴的基部中,并且将参考针状电极置于两眼之间的皮下。从基线到a波的波谷测量a波振幅,并且从a波的波谷到b波的波峰测量b波振幅。
[0247]
结果:与未经处理的小鼠(+si;
‑
pt1)相比,在经pt1处理的小鼠(+si;+pt1)中观察到更少的白色沉淀(每组n=5只小鼠)。仅pt1处理(
‑
si;+pt1)不改变眼底镜检查结果,与对照小鼠(
‑
si;
‑
pt1)非常相似(图9a)。视网膜节段的h&e染色显示,与未经处理的小鼠(+si;
‑
pt1)相比,pt1处理(+si;+pt1)防止onl变薄(白色条),阻止光感受器is/os形态改变并且减少黑色素碎屑(黑色箭头)(每组n=5只小鼠)(图9b)。经pt1处理的小鼠(+si;+pt1)中的onl厚度与对照小鼠(
‑
si;
‑
pt1)相似,并且与未经处理的小鼠(+si;
‑
pt1)相比显著改善。仅pt1处理不会改变onl厚度(
‑
si;+pt1对比
‑
si;
‑
pt1)(每组n=3
‑
4只小鼠)(图9c)。视网膜电图显示,与未经处理的小鼠(+si;
‑
pt1)相比,经pt1处理的小鼠(+si;+pt1)的视杆响应(暗视a波和b波)显著增加(每组n=3
‑
4只小鼠)(图9d)。
[0248]
结论:pt1表现出显示amd的视网膜的改善,因此表明ampk激动剂可积极用于amd的治疗。
[0249]
实施例6:缺血性卒中的神经保护
[0250]
方法:为生成缺血性卒中模型,通过短暂阻塞大脑中动脉45分钟,然后再灌注,来诱导缺血性病变。然后在阻塞后1小时和24小时以两个剂量向小鼠腹膜内注射100mg/kg的pt1或媒介物,并在一小时后处死以用于终末组织收集。
[0251]
将分离的大脑置于冷盐水中20分钟,切成七个冠状切片(2mm厚),并在37℃的盐水中的1.0%2,3,5
‑
三苯基氯化四氮唑(ttc)溶液中染色30分钟。将染色的脑组织固定在磷酸盐缓冲盐水中的10%福尔马林中。使用ccd相机(panasonic corporation,japan)捕获图像,并将未染色的受损区域定义为梗塞组织,并使用image pro plus 4.1软件(media cybernetics,silver spring,md)进行定量。
[0252]
结果:与用媒介物处理的小鼠相比,用pt1处理的小鼠的tcc染色的脑切片显示出
梗塞区域(白色)大小的减小(图10b
‑
10c)。
[0253]
结论:与未经处理的对照相比,pt1处理显示出用pt1处理的小鼠的脑切片中缺血(卒中)区域的显著减少。
[0254]
实施例7:运动表现的增强
[0255]
背景:作为高能量需求器官,眼睛特别容易受到线粒体损伤的后果的影响。类似地,骨骼肌也是依赖于氧化磷酸化和糖酵解两者来产生能量的高能量器官。
[0256]
方法:为了检测ampk激动剂对体内具有线粒体功能障碍的系统的影响,使用mk8722处理线粒体疾病的小鼠模型。这些小鼠具有因细胞色素c氧化酶组装蛋白sco2不足而引起的线粒体复合体iv缺乏症,并携带在第129位表达e
→
k突变(e129k)的sco2敲除(ko)等位基因和sco2敲入(ki)等位基因。e129k突变对应于几乎所有人类sco2突变患者中存在的e140k突变(参见例如,yang等人,analysis of mouse models of cytochrome c oxidase deficiency owing to mutations in sco2.hum mol genet.,2010年1月1日;19(1):170
‑
80;该文献的公开内容全文以引用方式并入本文)。sco2缺陷型小鼠的主要表型是运动功能降低和眼缺陷,这都是原发性线粒体疾病患者中的常见发现。将sco2小鼠分为四个处理组:sco2 ki/ko+mk8722、sco2ki/ko+dmso(媒介物)、对照ki/wt+mk8722、对照ki/wt+dmso,每组7
‑
9只小鼠。1.5个月大的sco2小鼠通过经口灌注用mk8722(10mg/kg)或媒介物(dmso)每天处理一次,持续14周。使用活动室、转棒和挂线测试评估运动功能,并使用光学相干断层扫描(oct)评估眼结构。
[0257]
结果:由于这种对线粒体功能障碍敏感,通过光学相干断层扫描(oct)在体内测量的眼结构显示sco2 ki/ko以及杂合ki/wt同窝仔中都存在视网膜缺陷。与wt/wt对照相比,sco2 ki/ko和ki/wt小鼠中的视网膜神经纤维层(rnfl)厚度减小(ki/ko veh:74.1μm和ki/wt veh:72.7μm,对比wt/wt veh:76.2μm)。相比之下,经mk8722处理的小鼠中的rnfl厚于经媒介物处理的sco2 ko/ki和ki/wt小鼠(ki/ko veh:74.1μm,对比ki/ko mk8722:77μm和ki/wt veh:72.7μm,对比ki/wt mk8722:74.7μm)(参见图9e)。
[0258]
在评价肌肉性能的运动功能研究中,经mk8722处理的sco2ki/ko突变小鼠在活动室(参见图11a)、转棒测试(参见图11b)和前肢挂线测试(参见图11c)中表现均优于经媒介物处理的sco2 ki/ko突变小鼠。如图11a所示,与ki/wt同窝仔对照相比,经媒介物处理的sco2 ki/ko小鼠在活动室内移动的距离更短,并且mk8722处理8周恢复了其活动至对照水平(ko/ki veh:1516.7cm;ko/ki mk8722:2337.8cm;ki/wt veh:2337cm)。图11b示出了与经媒介物处理的小鼠相比,mk8722处理也将ki/ko突变小鼠的转棒时间改善到与对照相似的水平(ko/ki veh:176.1sec;ko/ki mk8722:248.1sec;ki/wt veh:235.7sec)。对于挂线测试,图11c示出了mk8722处理增加了sco2 ko/ki突变小鼠可用其四肢悬挂的时间长度,至甚至超过了ki/wt对照的水平(ko/ki veh:173.2sec;ko/ki mk8722:312.5sec;ki/wt veh:145.5sec)。
[0259]
图11d示出了与经媒介物处理的突变小鼠相比,经mk8722处理的sco2 ki/ko突变小鼠的骨骼肌组织中指示线粒体细胞色素c氧化酶(cytoc)和琥珀酸脱氢酶(sdh)活性的组织学染色的强度增加。类似地,图11e示出了与未经处理的小鼠相比,在用mk8722处理的sco2 ki/ko突变小鼠中,通过骨骼肌的组织学评估,糖原含量增加。运动功能(图11a
‑
11c)和线粒体功能(图11d
‑
11e)的提高与acc磷酸化的增加相关,如图11f所示。
[0260]
结论:视网膜研究(图9e)表明ampk的激活可改善和/或预防与线粒体功能障碍相关的眼损伤。此外,运动研究(图11a
‑
11c)表明ampk激活可以增强与线粒体功能障碍相关的肌肉变性病症的强度、耐力和整体运动功能。另外,提高的线粒体功能(图11d)和糖原含量(图11e)可能在骨骼肌中使能量水平正常化的作用机制中起着不可或缺的作用,从而防止变性和虚弱。这些结果与指示增加的ampk激活的增加的acc磷酸化相结合,证明了许多实施方案的ampk激动剂具有许多药理学益处的能力。
[0261]
实施例8:合成6
‑
氯
‑5‑
(5
‑
(1
‑
羟基环丁基)噻吩
‑2‑
基)
‑
1h
‑
吲哚
‑3‑
羧酸及其类似物
[0262]
背景:图12a示出了能够激活ampk的化合物的一般结构。该实施例中描述了四种衍生物的合成(图13a
‑
13b和图14j
‑
14k)。
[0263]
方法:该实施例的图解例示在图12b中进行了说明,而该实施例示出了图13a所示的化合物的合成,本领域的技术人员将会知道使用不同的试剂、反应物、条件等生成衍生化合物,包括图13b
‑
13z和图14a
‑
14o所示的那些。
[0264]
步骤1:1
‑
(5
‑
溴噻吩
‑2‑
基)环丁
‑1‑
醇—向
‑
78℃的2,5
‑
二溴噻吩(0.95g,3.922mmol)在无水thf中的搅拌溶液中在
‑
78℃下逐滴添加正丁基锂(2.69ml,4.314mmol),并将混合物在相同温度下再搅拌30分钟。然后在2分钟内缓慢添加环丁酮(0.27g,3.922mmol)的溶液,并将反应混合物在
‑
78℃下搅拌1小时,然后用氯化铵猝灭。将产物萃取到乙酸乙酯中,经硫酸钠干燥,减压蒸发,然后通过快速柱色谱(230
–
400目,10%ea的pe溶液)纯化,得到呈无色液体的1
‑
(5
‑
溴噻吩
‑2‑
基)环丁
‑1‑
醇(0.6g;66%)。
[0265]
步骤2:1
‑
(5
‑
(4,4,5,5
‑
四甲基
‑
1,3,2
‑
二氧杂环戊硼烷
‑2‑
基)噻吩
‑2‑
基)环丁
‑1‑
醇—将步骤1的产物(2.0g,8.579mmol)、双联频哪醇硼酸酯(3.2g,12.87mmol)和koac(2.25g,25.7mmol)在1,4
‑
二噁烷(20ml)中的混合物用n2气体吹扫5分钟,然后添加pd(dppf)cl2(0.32g,0.429mmol)。在90℃下搅拌16小时后,通过减压蒸发去除溶剂,并将残余物通过柱色谱用弗罗里硅土纯化,用0
‑
10%ea/pe洗脱,得到呈粘性固体的1
‑
(5
‑
(4,4,5,5
‑
四甲基
‑
1,3,2
‑
二氧杂环戊硼烷
‑2‑
基)噻吩
‑2‑
基)环丁
‑1‑
醇(0.6g;25%)。
[0266]
步骤3:6
‑
氯
‑5‑
(5
‑
(1
‑
羟基环丁基)噻吩
‑2‑
基)
‑
1h
‑
吲哚
‑3‑
羧酸甲酯—将步骤2的产物(0.275g,0.977mmol)、5
‑
溴
‑6‑
氯
‑
1h
‑
吲哚
‑3‑
羧酸甲酯(0.282g,0.977mmol)、k2co3(0.40g,2.931mmol)在1,4
‑
二噁烷(5ml)和水(1ml)中的混合物用n2气体吹扫5分钟。然后添加pd(dppf)cl2.dcm(0.04g,0.048mmol),并将所得溶液在100℃下搅拌16小时。通过减压蒸发去除溶剂,并将残余物通过柱色谱用弗罗里硅土纯化,用0
‑
10%ea/pe洗脱,得到呈灰白色固体的6
‑
氯
‑5‑
(5
‑
(1
‑
羟基环丁基)噻吩
‑2‑
基)
‑
1h
‑
吲哚
‑3‑
羧酸甲酯(0.15g;91%)。
[0267]
步骤4:6
‑
氯
‑5‑
(5
‑
(1
‑
羟基环丁基)噻吩
‑2‑
基)
‑
1h
‑
吲哚
‑3‑
羧酸—将步骤3的产物(0.150g,0.414mmol)在乙醇和6n naoh溶液(10ml)中的搅拌溶液在80℃下搅拌16小时。通过减压蒸发去除溶剂,并将残余物用柠檬酸酸化,并将产物萃取到乙酸乙酯中。在用水洗涤萃取物并用硫酸钠干燥后,减压去除溶剂,并通过制备型hplc纯化粗残余物,得到呈灰白色粉末的6
‑
氯
‑5‑
(5
‑
(1
‑
羟基环丁基)噻吩
‑2‑
基)
‑
1h
‑
吲哚
‑3‑
羧酸(0.06g;42%)。
[0268]
通过改变某些试剂,还使用上文关于图12b所述的方法生成6
‑
氯
‑5‑
(5
‑
(1
‑
羟基环丁基)噻吩
‑3‑
基)
‑
1h
‑
吲哚
‑3‑
羧酸(图13b)、6
‑
氯
‑5‑
(1
‑
甲基
‑
1h
‑
吡唑
‑4‑
基)
‑
1h
‑
吲哚
‑3‑
羧酸(图14j)和6
‑
氯
‑5‑
(1
‑
苯基
‑
1h
‑
吡唑
‑4‑
基)
‑
1h
‑
吲哚
‑3‑
羧酸(图14k)。
[0269]
结果:步骤1产生了具有以下特征的1
‑
(5
‑
溴噻吩
‑2‑
基)环丁
‑1‑
醇:1h nmr(400mhz,cdcl3):δ6.91(d,j=3.6hz,1h),6.81(d,j=4.0hz,1h),2.49
–
2.36(m,4h),2.21(s,1h),1.96
–
1.91(m,1h),1.76
–
1.69(m,1h)。lcms:97.6%(217.07,m
‑
18)。
[0270]
步骤3产生了具有以下特征的6
‑
氯
‑5‑
(5
‑
(1
‑
羟基环丁基)噻吩
‑2‑
基)
‑
1h
‑
吲哚
‑3‑
羧酸甲酯:1h nmr(400mhz,cdcl3):δ8.56(bs,1h),8.29(s,1h),7.93(d,j=2.8hz,1h),7.54(s,1h),7.16(d,j=3.6hz,1h),7.06(d,j=3.6hz,1h),3.92(s,3h),2.65
–
2.58(m,2h),2.51
–
2.44(m,2h),2.31(s,1h),1.99
–
1.91(m,1h),1.84
–
1.80(m,1h)。lcms:95.63%(344.23,m
‑
18)。
[0271]
步骤4产生了具有以下特征的6
‑
氯
‑5‑
(5
‑
(1
‑
羟基环丁基)噻吩
‑2‑
基)
‑
1h
‑
吲哚
‑3‑
羧酸:1h nmr(400mhz,dmso
‑
d6):δ12(br s,1h),8.12(s,1h),8.07(s,1h),7.63(s,1h),7.12(d,j=3.6hz,1h),7.06(d,j=3.6hz,1h),5.96(s,1h),2.45
–
2.31(m,4h),1.91
–
1.82(m,1h),1.78
–
1.68(m,1h)。lcms:99.06%(465.30[m+h]+),熔点范围:228
‑
232℃。
[0272]
图13b示出了6
‑
氯
‑5‑
(5
‑
(1
‑
羟基环丁基)噻吩
‑3‑
基)
‑
1h
‑
吲哚
‑3‑
羧酸,其具有1h nmr(400mhz,dmso
‑
d6):δ11.90(bs,1h),8.04(s,1h),7.60(s,1h),7.42(d,j=1.2hz,1h),7.20(d,j=1.6hz,1h),5.96(s,1h),2.44
–
2.32(m,4h),1.91
–
1.82(m,1h),1.77
–
1.70(m,1h),lcms:97.92%(346.51[m+h]+)和熔点范围:248
‑
252℃。
[0273]
图14j示出了6
‑
氯
‑5‑
(1
‑
甲基
‑
1h
‑
吡唑
‑4‑
基)
‑
1h
‑
吲哚
‑3‑
羧酸,其具有1h nmr(400mhz,dmso
‑
d6):δ12.09(s,1h),11.87(s,1h),8.04(d,j=2.4hz,2h),8.01(s,1h),7.67(s,1h),7.59(s,1h),3.90(s,1h),lcms:99.32%(276.31[m+h]+)和熔点范围:241
‑
245℃。
[0274]
图14k示出了6
‑
氯
‑5‑
(1
‑
苯基
‑
1h
‑
吡唑
‑4‑
基)
‑
1h
‑
吲哚
‑3‑
羧酸,其具有1h nmr(400mhz,dmso
‑
d6):δ11.86(br s,1h),8.77(s,1h),8.20(br s,1h),8.00(s,2h),7.93(d,j=7.6hz,1h),7.63(s,1h),7.52(t,2h),7.33(t,1h),lcms:97.20%(338.13[m+h]+)和熔点范围:245
‑
249℃。
[0275]
结论:实施方案能够合成新型ampk激动剂及其衍生物,诸如图13b
‑
13z和图14a
‑
14o所示的那些。
[0276]
实施例9:合成ev8016的类似物(图13a)
[0277]
背景:图12a示出了能够激活ampk的化合物的一般结构。该实施例中描述了其他衍生物的合成(图13f和图14l
‑
14m)。
[0278]
方法:该实施例的图解例示在图12c中进行了说明,而该实施例示出了图14l所示的化合物的合成,本领域的技术人员将会知道使用不同的试剂、反应物、条件等生成衍生化合物,包括图13a
‑
13z和图14a
‑
14o所示的那些。
[0279]
结果:图13f示出了6
‑
氯
‑5‑
(5
‑
(1
‑
(羟甲基)环丙基)噻吩
‑2‑
基)
‑
1h
‑
吲哚
‑3‑
羧酸,其具有1h nmr(400mhz,dmso
‑
d6):δ11.65(bs,1h),8.24(bs,1h),7.89(bs,1h),7.55(d,j=9.2hz,1h),705(s,1h),6.88(d,j=3.6hz,1h),4.90(s,1h),3.57(s,2h),,1.00
–
0.87(m,4h)和lcms:99.06%(465.30[m+h]
+
)。
[0280]
图14l示出了6
‑
氯
‑5‑
(2
‑
苯基噁唑
‑5‑
基)
‑
1h
‑
吲哚
‑3‑
羧酸,其具有1h nmr(400mhz,dmso)δ12.08(s,2h),8.53(s,1h),8.13(s,1h),8.06(d,j=6.6hz,2h),7.81(s,1h),7.72(s,1h),7.59(t,j=7.1hz,3h),lcms:91.95%(339.35[m+h]+)和熔点范围:261
‑
265℃。
[0281]
图14m示出了6
‑
氯
‑5‑
(4
‑
苯基噻吩
‑2‑
基)
‑
1h
‑
吲哚
‑3‑
羧酸,其具有1h nmr(400mhz,dmso
‑
d6):δ11.77(bs,1h),8.31(s,1h),7.91(s,1h),7.88(s,1h),7.76(d,j=7.6hz,2h),7.66(d,j=1.2hz,1h),7.61(s,1h),7.43(t,2h),7.31(t,1h),lcms:99.55%(354.10[m+h]
+
)和熔点范围:195
–
199℃。
[0282]
结论:实施方案能够合成新型ampk激动剂及其衍生物,诸如图13a
‑
13z和图14a
‑
14o所示的那些。
[0283]
实施例10:合成ev8016的其他类似物(图13a)
[0284]
背景:图12a示出了能够激活ampk的化合物的一般结构。该实施例中描述了其他衍生物的合成(图14n
‑
14o)。
[0285]
方法:该实施例的图解例示在图12d中进行了说明,而该实施例示出了图14n
‑
14o所示的化合物的合成,本领域的技术人员将会知道使用不同的试剂、反应物、条件等生成衍生化合物,包括图13a
‑
13z和图14a
‑
14o所示的那些。
[0286]
结果:图14n示出了6
‑
氯
‑5‑
(1h
‑
四唑
‑5‑
基)
‑
1h
‑
吲哚
‑3‑
羧酸甲酯,其为图12d的步骤2之后的产物。该化合物具有1h nmr(400mhz,dmso
‑
d6):δ12.03(br s,1h),8.25(s,1h),8.15(s,1h),7.60(s,1h),7.01
‑
7.00(br s,1h),3.81(s,3h)和lcms:93.9%(278.07[m+h]+)。
[0287]
图14o示出了6
‑
氯
‑5‑
(1h
‑
四唑
‑5‑
基)
‑
1h
‑
吲哚
‑3‑
羧酸,其为图12d的步骤3的产物。该化合物具有1h nmr(400mhz,dmso
‑
d6):δ16.73(s,1h),12.34(s,1h),12.21(s,1h),8.36(s,1h),8.19(d,j=2.9hz,1h),7.78(s,1h)和熔点范围:268
‑
272℃。
[0288]
结论:实施方案能够合成新型ampk激动剂及其衍生物,诸如图13a
‑
13z和图14a
‑
14o所示的那些。
[0289]
实施例11:合成(3r,3ar,6r,6ar)
‑6‑
((5
‑
([1,1'
‑
联苯]
‑4‑
基)
‑
1h
‑
萘并[1,2
‑
d]咪唑
‑2‑
基)氧基)六氢呋喃并[3,2
‑
b]呋喃
‑3‑
醇
[0290]
方法:该实施例的图解例示如图15a所示。另外,虽然该实施例说明了图15b所示化合物的合成,但本领域技术人员将会知道使用不同的试剂、反应物、条件等生成衍生化合物。
[0291]
步骤1:合成n
‑
(4
‑
溴萘
‑1‑
基)乙酰胺(化合物2)—在室温下,向化合物
‑
1(5.0g,22.520mmol)在甲醇中的搅拌溶液中添加乙酸(4.2ml,45.040mmol),并且将反应混合物在70℃下搅拌2小时。通过tlc监测反应进展。完成后,将反应混合物倒入冰冷的水中,并滤出沉淀的固体,在真空下干燥,得到呈黄色固体的化合物
‑
2(4.5g,75%)。
[0292]
步骤2:合成n
‑
(4
‑
溴
‑2‑
硝基萘
‑1‑
基)乙酰胺(化合物3)—在室温下,向化合物2(4.0g,15.150mmol)在乙酸(40ml)中的搅拌溶液中添加发烟hno3(0.72ml,16.660mmol),并将该反应混合物在75℃下搅拌2小时。通过tlc监测反应进展。完成后,将反应混合物倒入冰冷的水中,滤出沉淀的固体,用大量水洗涤,并在真空下干燥,得到呈黄色固体的化合物3(3.52g,72%)。
[0293]
步骤3:合成n
‑
(4
‑
([1,1'
‑
联苯]
‑4‑
基)
‑2‑
硝基萘
‑1‑
基)乙酰胺(化合物5):
[0294]
向化合物3(20.0g,64.720mmol)和化合物4(19.2g,97.080mmol)在二噁烷和水(9:1)中的搅拌溶液中添加k2co3(22.30g,161.800mmol),将反应混合物用氮气吹扫15分钟,然后添加pd(pph3)4(3.73g,3.230mmol),并再次用氮气吹扫10分钟,然后将反应混合物在90
℃下搅拌2小时。通过tlc监测反应进展。反应完成后,将反应混合物通过硅藻土过滤,在减压下浓缩滤液,将残余物用水研磨,并过滤沉淀的固体。固体从2
‑
丙醇中重结晶,将所得固体过滤并真空干燥,得到呈黄色固体的化合物
‑
5(11.1g,40%)。化合物5原样用于步骤6中。
[0295]
步骤4:合成4
‑
([1,1'
‑
联苯]
‑4‑
基)
‑2‑
硝基萘
‑1‑
胺(化合物6)—向化合物5(5.0g,13.089mmol)在1,4
‑
二噁烷(500ml)中的搅拌溶液中添加浓hcl(50ml),并将反应混合物在100℃下搅拌48小时。通过tlc监测反应进展。反应完成后,将二噁烷减压蒸发,用冰冷的水稀释含水残余物,并过滤沉淀的固体。用大量水洗涤固体,并在真空下干燥,得到呈黄色固体的化合物
‑
6(4.05g,91.0%)。将该化合物不经进一步纯化用于下一步骤。
[0296]
步骤5:合成4
‑
([1,1'
‑
联苯]
‑4‑
基)萘
‑
1,2
‑
二胺(化合物7)—向化合物
‑
6(5.0g,14.662mmol)在thf(400ml)和乙醇(100ml)的混合物中的溶液中添加10%w/w的湿pd
‑
c(1.0g),将所得的反应混合物在parr装置中在80psi的氢气压力下于室温氢化16小时。通过tlc监测反应的进展。反应完成后,通过硅藻土过滤,并且将滤液在减压下浓缩。将粗产物用正戊烷研磨,并过滤沉淀的固体,真空干燥,得到呈黄色固体的化合物
‑
7(3.5g粗品)。将该化合物立即用于下一步骤。
[0297]
步骤6:合成5
‑
([1,1'
‑
联苯]
‑4‑
基)
‑
1,3
‑
二氢
‑
2h
‑
萘并[1,2
‑
d]咪唑
‑2‑
硫酮(化合物8)—在0℃下,向化合物7(3.5g,11.290mmol)在thf(70ml)中的搅拌溶液中添加dmap(2.75g,22.80mmol),然后添加二氯硫化碳(0.89ml,11.290mmol),并将所得的反应混合物在室温下搅拌3小时。通过tlc监测反应进展。反应完成后,减压蒸发溶剂,将残余物在乙酸乙酯和水之间分配。将有机层用盐水洗涤,经无水na2so4干燥,过滤并减压浓缩,得到呈黄色固体的粗化合物8(3.2g)。
[0298]
步骤7:合成5
‑
([1,1'
‑
联苯]
‑4‑
基)
‑2‑
(甲硫基)
‑
1h
‑
萘并[1,2
‑
d]咪唑(化合物9)—在0℃下,向化合物8(3.0g,8.522mmol)在丙酮(100ml)中的搅拌溶液中添加k2co3(1.41g,10.226mmol),搅拌10
–
15分钟,添加碘甲烷(0.55ml,8.522mmol),并将所得的反应混合物在室温下搅拌3小时。通过tlc监测反应进展。反应完成后,减压蒸发溶剂,并且将残余物在乙酸乙酯和水之间分配。将有机层用盐水洗涤,经无水na2so4干燥,过滤并减压浓缩,得到粗品。将粗品通过快速柱色谱(230x400目,15%
–
20%ea的pe溶液)纯化,得到1.1g(35.3%)呈黄色固体的化合物9。
[0299]
步骤8:合成5
‑
([1,1'
‑
联苯]
‑4‑
基)
‑2‑
(甲基磺酰基)
‑
1h
‑
萘并[1,2
‑
d]咪唑(化合物10)—在0℃下,向化合物9(1.0g,2.732mmol)在二氯甲烷(30ml)中的搅拌溶液中添加3
‑
氯过氧苯甲酸(1.41g,8.196mmol),并将所得的反应混合物在室温下搅拌2小时。通过tlc监测反应进展。反应完成后,将反应混合物用二氯甲烷稀释,用10%nahco3水溶液、10%硫代硫酸钠溶液然后用盐水洗涤。将有机层经无水na2so4干燥、过滤并在减压下浓缩,得到3.5g粗制黄色固体化合物10。
[0300]
步骤9:合成5
‑
([1,1'
‑
联苯]
‑4‑
基)
‑2‑
(甲基磺酰基)
‑1‑
((2
‑
(三甲基甲硅烷基)乙氧基)甲基)
‑
1h
‑
萘并[1,2
‑
d]咪唑(化合物11)—在0℃下,向化合物
‑
10(1.3g,3.266mmol)在二氯甲烷(50ml)中的搅拌溶液中添加三乙胺(0.68ml,4.899mmol),然后添加sem氯化物(0.65g,3.919mmol),并将所得的反应混合物在室温下搅拌2小时。通过tlc监测反应进展。反应完成后,用二氯甲烷稀释,用10%nahco3水溶液洗涤,然后用盐水洗涤。将有机层经无水na2so4干燥,过滤并在减压下浓缩。粗产物通过快速柱色谱(230x 400目,10%
–
15%ea的pe溶液)纯化,得到化合物11(0.35g,20%)。
[0301]
步骤10:合成5
‑
([1,1'
‑
联苯]
‑4‑
基)
‑2‑
(((3r,3ar,6r,6as)
‑6‑
((叔丁基二甲基甲硅烷基)氧基)六氢呋喃并[3,2
‑
b]呋喃
‑3‑
基)氧基)
‑1‑
((2
‑
(三甲基甲硅烷基)乙氧基)甲基)
‑
1h
‑
萘并[1,2
‑
d]咪唑(13)—在0℃下,向化合物12(0.34g,1.325mmol)在四氢呋喃(5ml)中的搅拌溶液中添加叔丁醇钾(0.15g,1.325mmol),并将所得的反应混合物在0℃下搅拌1小时。在0℃下向该反应混合物中添加化合物11在四氢呋喃中的溶液,并将所得的反应混合物在室温下搅拌2小时。通过tlc监测反应进展。反应完成后,减压蒸发溶剂,并且将残余物在乙酸乙酯和水之间分配。将有机层用盐水洗涤,经无水na2so4干燥,过滤并减压浓缩,得到呈棕色粘性固体的粗化合物13(0.6g)。
[0302]
步骤11:合成(3r,3ar,6r,6ar)
‑6‑
((5
‑
([1,1'
‑
联苯]
‑4‑
基)
‑
1h
‑
萘并[1,2
‑
d]咪唑
‑2‑
基)氧基)六氢呋喃并[3,2
‑
b]呋喃
‑3‑
醇(化合物ev8017)—向化合物13(0.6g,0.846mmol)在甲酸(12ml)中的搅拌溶液中添加khso4(0.11g,0.846mmol)的水(1.0ml)溶液,并将所得的反应混合物在60℃下搅拌16小时。通过tlc和lcms监测反应进展。反应完成后,冷却至0℃,用2n naoh水溶液通过将ph调节至12
–
13来进行碱化,将溶液在0℃下再搅拌1小时,用2n hcl中和并用乙酸乙酯萃取。将合并的有机层用盐水洗涤,经无水na2so4干燥,过滤并减压浓缩。通过快速柱色谱(c
‑
18柱,80%meoh的水溶液)纯化粗产物,得到呈灰白色固体的化合物ev8017(0.14g,35.7%)。
[0303]
结果:步骤1产生了具有以下特征的化合物2:lcms:98.8%(266.06m+h
+
&264.06m
‑
h
+
);1h nmr(400mhz,cdcl3):δ8.31(d,j=8.4hz,1h),7.88(d,j=8.0hz,1h),7.82
–
7.80(m,2h),7.67
–
7.61(m,2h),7.47(br s,1h),2.36(s,3h)。
[0304]
步骤2产生了具有以下特征的化合物3:lcms:94.0%(309.12m
‑
h
+
);1h nmr(400mhz,cdcl3):δ8.72(br s,1h),8.38(s,1h),8.30(d,j=8.4hz,1h),8.06(d,j=8.4hz,1h),7.82
–
7.78(m,1h),7.71
–
7.67(m,1h),2.37(s,3h)。
[0305]
步骤3产生了具有以下特征的化合物5:lcms:91.85%(381.31m
‑
h
+
)。
[0306]
步骤4产生了具有以下特征的化合物6:lcms:90.48%(341.29,m+h
+
)。
[0307]
步骤5产生了具有以下特征的化合物7:lcms:52.0%(311.3[m+h]
+
)。
[0308]
步骤6产生了具有以下特征的化合物8:lcms:52.0%(353.2[m+h]
+
)。
[0309]
步骤7产生了具有以下特征的化合物9:lcms:77.6.0%(367.29[m+h]
+
)。
[0310]
步骤8产生了具有以下特征的化合物10:lcms:76.9%(397.29[m
‑
h]
+
)。
[0311]
步骤9产生了具有以下特征的化合物11:lcms:88.0%(529.40[m+h]
+
);1h nmr(400mhz,cdcl3):δ8.75(d,j=7.6hz,1h),8.00(s,1h),7.75(d,j=6.4hz,2h),7.71(m,3h),7.67(s,1h),7.60(d,j=8.4hz,1h),7.54
–
7.40(m,4h),6.04(s,2h),3.70(t,j=8.0hz,2h),0.93(t,j=8.0hz,2h),
‑
0.47(s,9h)。
[0312]
步骤10产生了具有以下特征的化合物13:lcms:84.8%(709.70[m+h]
+
)。
[0313]
步骤11产生了具有以下特征的化合物ev8017:lcms:99.89%(465.30[m+h]
+
);hplc:99.86%;熔点:158
‑
162℃;1h nmr(400mhz,dmso
‑
d6):δ13
‑
12(br s,1h),8.29(br s,1h),7.87(d,j=8.4hz,1h),7.83
–
7.77(m,4h),7.59
–
7.50(m,6h),7.42
–
7.35(m,2h),5.52(d,j=5.6hz,1h),4.98(d,j=6.8hz,1h),4.89(t,j=4.8hz,1h),4.41(t,j=4.8hz,1h),4.23
–
4.16(m,2h),3.88(q,j=6.8hz,1h),3.82(t,j=6.8hz,1h),3.48(t,j=8.4hz,1h)。
[0314]
结论:实施方案能够合成新型ampk激动剂及其衍生物,诸如图15b所示的那些。
[0315]
等同原则
[0316]
虽然以上描述包含本发明的许多特定实施方案,但是这些不应解释为对本发明范围的限制,而应被解释为其一个实施方案的实例。因此,本发明的范围不应由所例示的实施方案来确定,而应由所附权利要求书及其等同形式来确定。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1