诊疗一体化细胞纳米探针、制备方法及用途与流程
本发明属于纳米生物技术领域,具体涉及一种诊疗一体化细胞纳米探针、制备方法及用途。
背景技术:
癌症是一种严重威胁人类生命的疾病之一,对人类的正常生产和生活产生了巨大的影响;传统的治疗方法如外科切除术、化学疗法、放射疗法等可以一定程度地降低死亡率,但是治疗效果却非常有限;此外,治疗后期肿瘤的复发和转移是一个非常严峻的问题;提高诊断和治疗疾病手段成为一项迫在眉睫的工作。
近年来,肿瘤干细胞的提出和相关研究为癌症的治疗打开了一道大门,经过研究者长期的实验探究,证明肿瘤干细胞是肿瘤生长的源头,具有自我更新能力、增值分化潜能,以及强大的耐药抗凋亡能力。在肿瘤的生长、转移和复发过程中发挥着极其重要的作用;因此,针对肿瘤干细胞的靶向治疗有望是根除癌症的有效途径。
在肿瘤治疗方面,近年来涌现出各种新颖的治疗方法;其中光热和光动力疗法由于在细胞层面针对肿瘤进行精准治疗,因此得到了越来越多的关注,光热治疗是利用金属或者金属化合物纳米粒子在光照条件下产生热疗,使肿瘤组织局部温度升高,超过癌细胞的耐受阈值,从而是细胞凋亡的一种疗法;光动力治疗是利用光敏剂在光照时产生活性氧物种,与细胞中的分子发生反应使细胞凋亡的一种方法,这两种疗法相比于化疗和放疗来讲,具有极小的副作用,因此在肿瘤诊断和治疗方面具有广阔的应用前景。
技术实现要素:
有鉴于此,本发明的主要目的在于提供一种诊疗一体化细胞纳米探针、制备方法及用途。
为达到上述目的,本发明的技术方案是这样实现的:
本发明实施例提供一种诊疗一体化细胞纳米探针,由以下各项组成:
核为表面钝化并且具有两个等离激元共振峰的贵金属纳米粒子;
中间为羟基乙酸偶联金丝桃素光敏剂;
最外层为聚乳酸修饰的石墨烯类材料保护层。
上述方案中,所述表面钝化的具有两个等离激元共振峰的贵金属纳米粒子为金、银、铜中的一种或多种构成,通过对其形貌控制或者与其他介质进行耦合,使其具有两个等离激元共振峰;所述贵金属纳米粒子的表面通过氧化物、高分子聚合物、生物大分子进行钝化。
上述方案中,所述石墨烯类材料采用单层或多层石墨烯、氧化石墨烯以及氧化还原石墨烯中的一种。
本发明实施例还提供一种如上述方案中任意一项所述的诊疗一体化细胞纳米探针的制备方法,所述方法包括以下步骤:
步骤1,贵金属纳米粒子的表面修饰:将贵金属纳米粒子与表面修饰剂溶液混合,搅拌反应,通过超滤膜过滤,重新分散在磷酸缓冲盐溶液(pbs)中,获得功能化的贵金属纳米粒子(nmnps)分散液;
步骤2,nmnps与金丝桃素的偶联:将羟基乙酸分散液与nmnps混合,加热,加入金丝桃素溶液,搅拌反应,通过超滤膜过滤,重新分散在pbs中,获得金丝桃素偶联的贵金属纳米粒子(h-nmnps)分散液;
步骤3,h-nmnps与石墨烯材料的复合:将石墨烯材料分散液与聚乳酸溶液混合,搅拌反应,通过超滤膜过滤,重新分散在pbs中;然后加入h-nmnps分散液,搅拌反应,离心,除去上清液,将剩余部分溶液加入到pbs中,最终得到石墨烯稳定的h-nmnps(g-h-nmnps)纳米探针的分散液。
上述方案中,所述步骤1中,表面修饰剂为含有巯基(-sh)、且含有羧基(-cooh)或/和氨基(-nh2)的化合物;表面修饰剂溶液的浓度为0.001~10000mmol/l;贵金属纳米粒子与表面修饰剂溶液混合时,贵金属纳米粒子与表面修饰剂的摩尔比为1:1~1:500;搅拌反应的时间为0.5~48h;所述超滤膜的截留分子量(mwco)为300~100000;得到的功能化的贵金属纳米粒子(nmnps)的pbs分散液中,nmnps的浓度为1nmol/l~1000mmol/l。
上述方案中,所述步骤2中,羟基乙酸溶液的浓度为0.001~10000mmol/l;羟基乙酸溶液和nmnps分散液混合时,g-nmnps与羟基乙酸的摩尔比为1:1~1:500,加热的温度为10~80℃;金丝桃素溶液的浓度为0.01~50mg/ml;金丝桃素与羟基乙酸的质量比为1:1~1:10000;所述的超滤膜的截留分子量(mwco)为300~100000;得到的h-nmnps分散液中,h-nmnps的浓度为1nmo/l~1000mmol/l。
上述方案中,所述步骤3中,石墨烯材料分散液的浓度为0.01~100mg/ml;聚乳酸的分子量为1000~200000,聚乳酸溶液的溶剂为二甲基甲酰胺,浓度为0.001~10000mmol/l;所述的超滤膜的截留分子量(mwco)为300~100000;h-nmnps分散液与石墨烯材料分散液混合时,石墨烯材料与h-nmnps的质量比为1:100~1:1000000;搅拌反应温度为10~80℃;离心转速为8000~15000rpm,时间为0.1~6h,除去上清液的体积占总体积的3/4。
本发明实施例还提供一种上述方案中任意一项所述的诊疗一体化细胞纳米探针或者如上述方案中任意一项制备方法制备的诊疗一体化细胞纳米探针,用于荧光标记、或者纳米治疗剂、或者纳米材料/药物载体的用途。
与现有技术相比,本发明利用双吸收峰的贵金属纳米粒子来同时提高诊断和治疗效率;利用聚乳酸修饰的石墨烯材料来提高贵金属纳米粒子核的稳定性;通过羟基乙酸将光敏剂和石墨烯偶联起来,具有制备简单、可重复性高等优点;此外,本发明提供的纳米探针可以同时实现对癌细胞的定位和杀灭,具有重要的临床应用价值。
附图说明
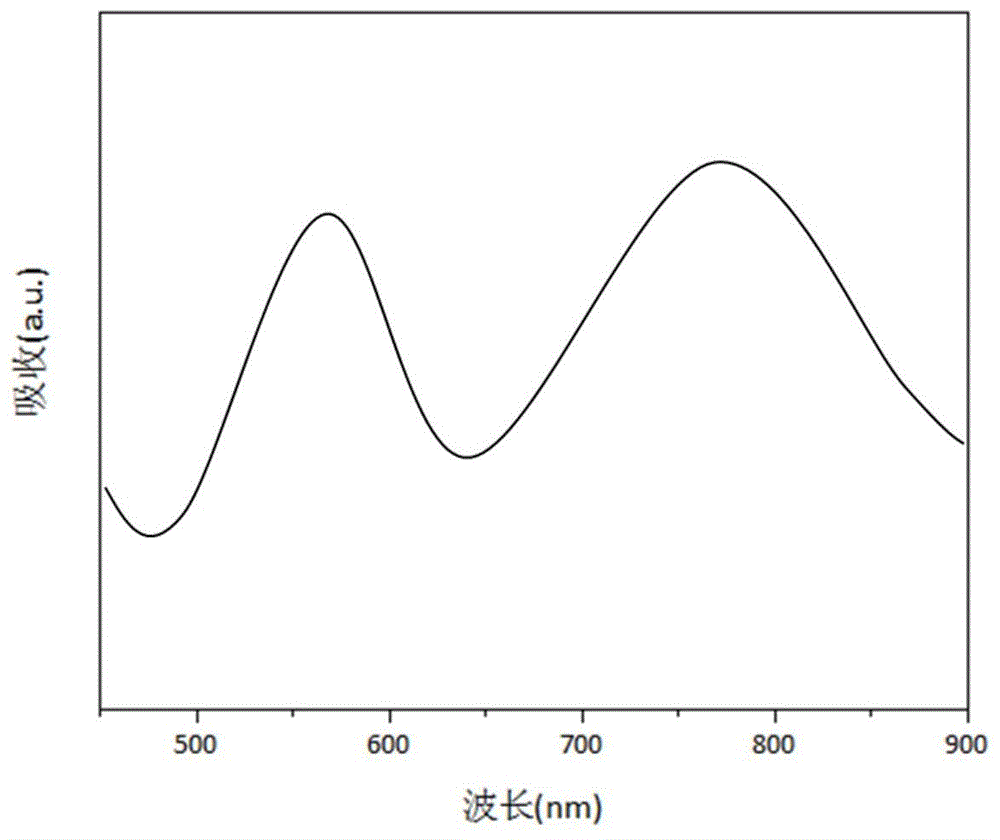
图1为根据本发明的一个实施方案的诊疗一体化细胞纳米探针的吸收谱;
图2为根据本发明的一个实施方案的诊疗一体化细胞纳米探针的荧光谱;
图3为根据本发明的一个实施方案的诊疗一体化细胞纳米探针分散液在光照下的升温曲线;
图4为根据本发明的一个实施方案的诊疗一体化细胞纳米探针孵育下的细胞存活率图。
具体实施方式
为了使本发明的目的、技术方案及优点更加清楚明白,以下结合附图及实施例,对本发明进行进一步详细说明。应当理解,此处所描述的具体实施例仅仅用以解释本发明,并不用于限定本发明。
本发明实施例提供一种诊疗一体化细胞纳米探针,其由表面钝化的具有两个等离激元共振峰的贵金属纳米粒子的核、中间为羟基乙酸偶联金丝桃素光敏剂和最外层聚乳酸修饰的石墨烯类材料保护层。
所述的表面钝化的具有两个等离激元共振峰的贵金属纳米粒子的核为金、银、铜等物质中的一种或多种构成;所述的石墨烯类材料包括单层或多层石墨烯、氧化石墨烯以及氧化还原石墨烯等具有石墨烯结构的物质。
本发明实施例还提供一种诊疗一体化细胞纳米探针的制备方法,该制备方法通过以下步骤实现:
步骤1,贵金属纳米粒子的核的表面修饰:将贵金属纳米粒子与表面修饰剂溶液混合,搅拌反应,用超滤膜过滤,重新分散在磷酸缓冲盐溶液(pbs)中,得到功能化的贵金属纳米粒子(nmnps)分散液。
步骤2,nmnps与金丝桃素的偶联:将羟基乙酸分散液与nmnps混合,加热,加入金丝桃素溶液,搅拌反应,用超滤膜过滤,重新分散在pbs中,得到金丝桃素偶联的nmnps(h-nmnps)分散液。
步骤3,h-nmnps与石墨烯材料的复合:将石墨烯材料分散液与聚乳酸溶液混合,搅拌反应,用超滤膜过滤,重新分散在磷酸缓冲盐溶液(pbs)中;然后加入h-nmnps分散液,搅拌反应,离心,除去上清液,将剩余部分溶液加入到pbs中,最终得到石墨烯稳定的h-nmnps(g-h-nmnps)纳米探针的分散液。
以下通过实施例对优选实施方式作具体阐释。
实施例中贵金属纳米粒子的核为金纳米棒;表面修饰剂为巯基丙酸,其浓度为1mmol/l;超滤膜的截留分子量为10000;石墨烯材料为氧化石墨烯,聚乳酸分子量为10000。
实施例1:
(1)将金纳米棒分散液与巯基丙酸溶液混合,使金纳米棒与巯基丙酸的摩尔比为1:50;搅拌反应1h,用超滤膜过滤,重新分散在pbs缓冲液中,得到功能化的金纳米棒(nmnps)分散液,其浓度为1mmol/l。
(2)将浓度为1mmol/l的羟基乙酸分散液与nmnps混合,使nmnps与羟基乙酸的摩尔比为1:10,加热到60℃;加入浓度为0.1mg/ml的金丝桃素溶液,使金丝桃素与羟基乙酸的质量比为1:100搅拌反应,用超滤膜过滤,重新分散在pbs中,得到h-nmnps,浓度为1mmol/l
(3)将浓度为1mg/ml的氧化石墨烯分散液与浓度为1mmol/l的聚乳酸溶液混合,搅拌30min,用超滤膜过滤,重新分散在pbs中;再加入将步骤(2)中的h-nmnps分散液,使氧化石墨烯与h-nmnps的质量比为1:100;在50℃下搅拌反应,然后10000rpm转速下离心1h,除去3/4体积的上清液;将剩余部分溶液加入到pbs中,最终得到纳米探针的分散液,低温避光保存。
实施例2:
(1)将金纳米棒分散液与巯基丙酸溶液混合,使金纳米棒与巯基丙酸的摩尔比为1:50;搅拌反应1h,用超滤膜过滤,重新分散在pbs缓冲液中,得到功能化的金纳米棒(nmnps)分散液,其浓度为1mmol/l。
(2)将浓度为1.1mmol/l的羟基乙酸分散液与nmnps混合,使nmnps与羟基乙酸的摩尔比为1:10,加热到60℃;加入浓度为0.1mg/ml的金丝桃素溶液,使金丝桃素与羟基乙酸的质量比为1:100搅拌反应,用超滤膜过滤,重新分散在pbs中,得到h-nmnps,浓度为1mmol/l
(3)将浓度为1mg/ml的氧化石墨烯分散液与浓度为1mmol/l的聚乳酸溶液混合,搅拌30min,用超滤膜过滤,重新分散在pbs中;再加入将步骤(2)中的h-nmnps分散液,使氧化石墨烯与h-nmnps的质量比为1:100;在50℃下搅拌反应,然后10000rpm转速下离心1h,除去3/4体积的上清液;将剩余部分溶液加入到pbs中,最终得到纳米探针的分散液,低温避光保存。
实施例3:
(1)将金纳米棒分散液与巯基丙酸溶液混合,使金纳米棒与巯基丙酸的摩尔比为1:50;搅拌反应1h,用超滤膜过滤,重新分散在pbs缓冲液中,得到功能化的金纳米棒(nmnps)分散液,其浓度为1.2mmol/l。
(2)将浓度为1mmol/l的羟基乙酸分散液与nmnps混合,使nmnps与羟基乙酸的摩尔比为1:10,加热到60℃;加入浓度为0.11mg/ml的金丝桃素溶液,使金丝桃素与羟基乙酸的质量比为1:100搅拌反应,用超滤膜过滤,重新分散在pbs中,得到h-nmnps,浓度为1mmol/l。
(3)将浓度为1mg/ml的氧化石墨烯分散液与浓度为1mmol/l的聚乳酸溶液混合,搅拌30min,用超滤膜过滤,重新分散在pbs中;再加入将步骤(2)中的h-nmnps分散液,使氧化石墨烯与h-nmnps的质量比为1:100;在50℃下搅拌反应,然后10000rpm转速下离心1h,除去3/4体积的上清液;将剩余部分溶液加入到pbs中,最终得到纳米探针的分散液,低温避光保存。
实施例4:
(1)将金纳米棒分散液与巯基丙酸溶液混合,使金纳米棒与巯基丙酸的摩尔比为1:50;搅拌反应1h,用超滤膜过滤,重新分散在pbs缓冲液中,得到功能化的金纳米棒(nmnps)分散液,其浓度为1mmol/l。
(2)将浓度为1mmol/l的羟基乙酸分散液与nmnps混合,使nmnps与羟基乙酸的摩尔比为1:10,加热到60℃;加入浓度为0.12mg/ml的金丝桃素溶液,使金丝桃素与羟基乙酸的质量比为1:100搅拌反应,用超滤膜过滤,重新分散在pbs中,得到h-nmnps,浓度为1mmo/l。
(3)将浓度为1mg/ml的氧化石墨烯分散液与浓度为2mmol/l的聚乳酸溶液混合,搅拌30min,用超滤膜过滤,重新分散在pbs中;再加入将步骤(2)中的h-nmnps分散液,使氧化石墨烯与h-nmnps的质量比为1:100;在50℃下搅拌反应,然后10000rpm转速下离心1h,除去3/4体积的上清液;将剩余部分溶液加入到pbs中,最终得到纳米探针的分散液,低温避光保存。
实施例5:
(1)将金纳米棒分散液与巯基丙酸溶液混合,使金纳米棒与巯基丙酸的摩尔比为1:50;搅拌反应1h,用超滤膜过滤,重新分散在pbs缓冲液中,得到功能化的金纳米棒(nmnps)分散液,其浓度为1.5mmol/l。
(2)将浓度为1mmol/l的羟基乙酸分散液与nmnps混合,使nmnps与羟基乙酸的摩尔比为1:10,加热到60℃;加入浓度为0.1mg/ml的金丝桃素溶液,使金丝桃素与羟基乙酸的质量比为1:100搅拌反应,用超滤膜过滤,重新分散在pbs中,得到h-nmnps,浓度为1.5mmol/l。
(3)将浓度为1mg/ml的氧化石墨烯分散液与浓度为1mmol/l的聚乳酸溶液混合,搅拌30min,用超滤膜过滤,重新分散在pbs中;再加入将步骤(2)中的h-nmnps分散液,使氧化石墨烯与h-nmnps的质量比为1:102;在50℃下搅拌反应,然后10000rpm转速下离心1h,除去3/4体积的上清液;将剩余部分溶液加入到pbs中,最终得到纳米探针的分散液,低温避光保存。
所述诊疗一体化细胞纳米探针的性能测试:
使用紫外-可见吸收光度计测试实施例1得到的探针的吸收谱,结果如图1所示,可以看到,探针有两个明显的吸收峰。
使用荧光光度计测试实施例2得到的探针的荧光光谱,结果如图2所示。可以看到,探针在可见光波段具有明显的荧光峰。
采用本领域公知的方法对实施例3得到的探针的进行光热实验,结果如图3所示,可以看到,在808nm激光照射下,探针分散液的温度有明显的提高,说明探针具有良好的光热效果。
采用本领域公知的方法对实施例4得到的探针的进行细胞存活率实验,结果如图4所示,可以看到,在探针与乳腺癌细胞孵育24h后,细胞的存活率依然高于90%。
以上所述,仅为本发明的较佳实施例而已,并非用于限定本发明的保护范围。
- 还没有人留言评论。精彩留言会获得点赞!