一种索法地尔冻干粉针剂的制备方法及其产品和用途与流程
1.本发明属于药物制剂技术领域,涉及一种索法地尔冻干粉针剂的制备方法,通过该方法制备的索法地尔冻干粉针剂产品,以及该产品的医药用途。
背景技术:
2.索法地尔(salfaprodil),化学名为2-羟基-5-[2,3,5,6-四氟-4-(三氟甲基)苄氨基]苯甲酸钾,其结构式如下所示。
[0003][0004]
索法地尔是一种中等强度的n-甲基-d-天冬氨酸(nmda)受体拮抗剂,也是一种强力的抗氧化剂,具备双重神经保护作用,可同时阻断nmda受体介导的兴奋毒性和机体的氧化应激反应,其保护神经功能的效果可持续28天以上,提供了广泛的神经保护作用,扩大了治疗时间窗。
[0005]
cn1309703c公开了索法地尔可用于治疗脑血管和神经系统疾病和症状中的常规或病理性神经性疾病。具体而言,索法地尔用于预防和治疗血栓栓塞、缺血性中风、出血性中风、脑血管痉挛、脑老化、外伤性脑损伤、外伤性脊髓损伤、心搏停止、动脉低血压、低血糖症、缺氧症和组织缺氧。索法地尔还可以有效地用于缓解神经变性疾病,如亨廷顿氏症、阿尔茨海默氏症、小脑退化症、肌萎缩性脊髓侧索硬化症、帕金森氏症、唐氏综合征、癫痫、多发梗塞性痴呆和脑炎。
[0006]
现有的冻干制剂工艺种类繁多,并且广泛应用于各种注射用粉针药物当中。然而,当通过现有技术中其他品种所使用的工艺(例如,cn104771369b中磷酸氟达拉滨的冻干工艺)制备注射用索法地尔时,由于不同药效活性成分在冷冻时的结晶行为存在差异,导致产品在冻干时不易形成均一细致的结晶形态。另外,产品在复溶后产生沉淀,存在稳定性差、外观有明显分层现象等缺陷。因此,亟需开发一种适于注射用索法地尔的冻干制剂工艺。
技术实现要素:
[0007]
发明要解决的问题
[0008]
为克服使用现有冻干技术制备注射用索法地尔存在的缺陷,本发明提供一种成型性良好,冻干前溶液外观澄清,冻干品复溶性好,复溶后澄明度好,杂质含量低,稳定性好,质量可控的注射用索法地尔的制备方法以及通过该方法制备的产品。
[0009]
用于解决问题的方案
[0010]
本发明是通过以下方案实现的:
[0011]
第一方面,本发明提供了一种索法地尔冻干粉针剂的制备方法,其包括如下步骤:将索法地尔加入到注射用水中,溶清后过滤,滤液用碱性物质水溶液调节ph值,再加入注射
用水定容,充入惰性气体保护,除菌过滤后得到索法地尔溶液,冻干,即得。
[0012]
优选地,在上述制备方法中,所述过滤和所述除菌过滤使用的滤膜的孔径各自独立地为0.2~1.0μm。
[0013]
更优选地,在上述制备方法中,所述过滤和所述除菌过滤使用的滤膜的材质各自独立地为聚醚砜(pes)、聚四氟乙烯(ptfe)、尼龙(n6/n66)或聚偏氟乙烯(pvdf)。
[0014]
优选地,在上述制备方法中,所述碱性物质选自氢氧化钾、碳酸钾、碳酸氢钾、氢氧化钠、碳酸钠和碳酸氢钠。
[0015]
优选地,在上述制备方法中,所述碱性物质水溶液的浓度为0.1~1.0m。
[0016]
优选地,在上述制备方法中,所述ph值被调节至8.0~10.0。
[0017]
优选地,在上述制备方法中,所述惰性气体为氩气或氮气。
[0018]
优选地,在上述制备方法中,所述除菌过滤在所述定容之后的16小时内进行。
[0019]
优选地,在上述制备方法中,所述索法地尔溶液的质量体积浓度为5~20w/v%。
[0020]
优选地,在上述制备方法中,所述冻干在冻干机中进行,并且包括预冻阶段、回温阶段、再次降温阶段、一次干燥a阶段、一次干燥b阶段和解析干燥阶段。
[0021]
更优选地,在所述预冻阶段中,所述冻干机的板层温度降至-50~-30℃,保温1~3小时。
[0022]
更优选地,在所述回温阶段中,所述冻干机的板层温度升至-5~5℃,保温1~3小时。
[0023]
更优选地,在所述再次降温阶段中,所述冻干机的板层温度降至-50~-30℃,保温1~3小时。
[0024]
更优选地,在所述一次干燥a阶段中,所述冻干机的板层温度升至-30~-25℃,保温10~30小时,真空度为5~20pa。
[0025]
更优选地,在所述一次干燥b阶段中,所述冻干机的板层温度升至5~20℃,保温10~30小时,真空度为5~20pa。
[0026]
更优选地,在所述解析干燥阶段中,所述冻干机的板层温度升至10~40℃,保温10~30小时,真空度为5~20pa。
[0027]
优选地,上述制备方法还包括灌装、压塞、轧盖和/或包装等步骤。
[0028]
第二方面,本发明提供了一种索法地尔冻干粉针剂,其通过上述制备方法制得。
[0029]
优选地,在上述索法地尔冻干粉针剂中,索法地尔为唯一的药效活性成分。
[0030]
第三方面,本发明提供了上述索法地尔冻干粉针剂在制备用于预防和/或治疗神经变性疾病的药物中的用途。
[0031]
优选地,在上述用途中,所述神经变性疾病选自亨廷顿病、阿尔茨海默病、皮克病、柯萨可夫综合征、小脑退化症、肌萎缩性脊髓侧索硬化症、帕金森病、唐氏综合征、戊二酸血症、癫痫、多发梗塞性痴呆和脑炎中的一种或多种。
[0032]
第四方面,本发明提供了上述索法地尔冻干粉针剂在制备用于预防和/或治疗脑血管和神经系统疾病和症状的药物中的用途。
[0033]
优选地,在上述用途中,所述脑血管和神经系统疾病和症状选自血栓栓塞、缺血性中风、出血性中风、脑血管痉挛、脑老化、外伤性脑损伤、外伤性脊髓损伤、心搏停止、动脉低血压、低血糖症、缺氧症和组织缺氧中的一种或多种。
[0034]
发明的效果
[0035]
与现有技术相比,本发明具有下列有益效果:
[0036]
(1)通过本发明的方法进行冻干粉针剂生产时,冻干前的溶液澄清,无可见异物;
[0037]
(2)本发明的冻干粉针剂为类白色粉末,粉体细致,结构均一;
[0038]
(3)本发明的冻干粉针剂的复溶性好,复溶后的溶液为浅黄色,澄明度良好;
[0039]
(4)本发明的冻干粉针剂的水分含量低;
[0040]
(5)与原料相比,本发明的冻干粉针剂的杂质含量没有增加,能够得到有效控制;
[0041]
(6)本发明的冻干粉针剂在6个月加速试验前后的各项参数均能保持大体一致,稳定性表现良好。
具体实施方式
[0042]
首先,本发明提供了一种索法地尔冻干粉针剂的新型制备方法。
[0043]
除非另有说明,本发明中所使用的术语“索法地尔”是指以任意一种或多种物理形态存在的2-羟基-5-[2,3,5,6-四氟-4-(三氟甲基)苄氨基]苯甲酸钾(potassium2-hydroxyl-5-[2,3,5,6-tetrafluoro-4-(trifluoromethyl)benzylamino]benzoate)或其药学上可接受的盐、水合物或溶剂化物。
[0044]
除非另有说明,本发明中所使用的术语“冻干粉针剂”是指在无菌环境下,将一种或多种药效活性成分(或原料药)掺入一种或多种辅料中或溶于一种或多种溶剂(或溶媒)中,经过一定的加工处理(例如,冷冻干燥)而制成的固体粉末状制剂。
[0045]
具体而言,上述制备方法包括如下步骤:
[0046]
将索法地尔加入到注射用水中,溶清后过滤,滤液用碱性物质水溶液调节ph值,再加入注射用水定容,充入惰性气体保护,除菌过滤后得到索法地尔溶液,冻干,即得。
[0047]
除非另有说明,本发明中所使用的术语“注射用水”是指符合中国药典(或者作为备选的美国药典、欧洲药典或日本药典)中“注射用水”项下相关规定的水。
[0048]
除非另有说明,本发明中所使用的术语“溶清”(或其全称“溶解澄清”)是指待溶解样品在溶剂中溶解至澄清或者无肉眼可见的浑浊或沉淀的操作或过程。
[0049]
除非另有说明,本发明中所使用的术语“过滤”是指在外力作用下,使包含固体颗粒的多相分散系(例如,混悬液或固体颗粒气溶胶)中的连续相(例如,混悬液中的液体或固体颗粒气溶胶中的气体)透过特定的分离介质(例如,滤纸或滤膜),同时分散相(例如,多相分散系中的固体颗粒)被截留,从而使两相分离的操作或过程。当上述多项分散系为混悬液时,透过分离介质的液态连续相即为“滤液”,被分离介质截留的固态分散相即为“滤饼”,除非另有说明,本发明中所使用的术语“滤液”和“滤饼”的含义如上所述。
[0050]
在一些优选的实施方案中,上述制备方法中的过滤通过滤膜来完成。
[0051]
在一些更优选的实施方案中,上述过滤用滤膜的孔径为0.2~1.0μm,优选0.2~0.5μm,更优选0.45μm。
[0052]
在一些更优选的实施方案中,上述过滤用滤膜的材质选自pes、ptfe、n6/n66和pvdf中的任意一种或多种。
[0053]
在一些优选的实施方案中,上述制备方法利用碱性物质水溶液来调节滤液的ph值。
[0054]
在一些更优选的实施方案中,上述制备方法中的碱性物质选自氢氧化钾、碳酸钾、碳酸氢钾、氢氧化钠、碳酸钠和碳酸氢钠,优选氢氧化钾、碳酸钾或碳酸氢钾,更优选氢氧化钾。
[0055]
在一些更优选的实施方案中,上述碱性物质水溶液的摩尔浓度为0.1~1.0mol/l,优选0.1~0.5mol/l。
[0056]
在一些更优选的实施方案中,上述碱性物质水溶液将滤液的ph值调节至8.0~10.0。
[0057]
除非另有说明,本发明中所使用的术语“定容”是指当使用固定容量的容器(例如,容量瓶)来溶解或稀释物质至一定浓度时,最终借助液体转移设备(例如,滴管或移液管)将溶剂准确且精密地加至容器的刻度线的操作或过程;简言之,定容就是调整至固定容量。
[0058]
除非另有说明,本发明中所使用的术语“惰性气体”或“化学惰性气体”是指在常规试验环境下表现出化学反应惰性的气态物质,既包括位于元素周期表中的0族且被统称为“稀有气体”的氦气(he)、氖气(ne)、氩气(ar)、氪气(kr)、氙气(xe)和氡气(rn),也包括在一般条件下不表现出化学反应活性的氮气(n2)和二氧化碳(co2)。
[0059]
在一些优选的实施方案中,上述制备方法中的惰性气体保护步骤使用惰性气体对定容后的物料提供惰性气氛。
[0060]
在一些更优选的实施方案中,上述制备方法中的惰性气体保护步骤使用氩气或氮气对定容后的物料提供惰性气氛。
[0061]
除非另有说明,本发明中所使用的术语“除菌过滤”或“过滤除菌”是指通过过滤的方式除去待处理样品中的细菌,以达到无菌目的的操作或过程。通常,除菌过滤需要使用具有微小孔径的滤菌设备,包括薄膜滤菌器(又称滤菌滤膜,有时也简称滤膜,孔径主要有0.45μm和0.22μm两种,且后者的除菌效果更佳)、陶瓷滤菌器、石棉滤菌器、烧结玻璃滤菌器等。
[0062]
在一些优选的实施方案中,上述制备方法中的除菌过滤同样通过滤膜来完成。
[0063]
在一些更优选的实施方案中,上述除菌过滤用滤膜的孔径为0.20~0.22μm。
[0064]
在一些更优选的实施方案中,上述除菌过滤用滤膜的材质同样选自pes、ptfe、n6/n66和pvdf中的任意一种或多种。
[0065]
在一些更优选的实施方案中,上述除菌过滤在定容步骤完成之后的16小时内进行,优选在12小时内进行,更优选在8小时内进行。
[0066]
在一些优选的实施方案中,上述制备方法中的索法地尔溶液具有适宜的质量体积浓度,以便顺利进行后续的冻干步骤。
[0067]
除非另有说明,本发明中所使用的术语“质量体积浓度”(或其简称“质量浓度”)是指单位体积(例如,1m3或1l)的溶液中所含溶质的质量数(例如,1g或1mg),单位通常以g/m3或mg/l来表示。除非另有说明,本发明中所使用的术语“w/v%”表示每百毫升溶液中所含溶质的克数,即“g/100ml”。
[0068]
在一些更优选的实施方案中,上述适宜的质量体积浓度为5~20w/v%。
[0069]
在一些优选的实施方案中,上述制备方法中的冻干在冻干机中进行,并且包括预冻阶段、回温阶段、再次降温阶段、一次干燥(在一次干燥中,根据温度变化细分为a阶段和b阶段)和解析干燥阶段。
disease,pd)、柯萨可夫综合征(korsakov’s syndrome,ks)、小脑退化症(olivopontocerebellar degeneration)、肌萎缩性脊髓侧索硬化症(amyotrophic lateral sclerosis,als)、帕金森病(parkinson’s disease,pd)、唐氏综合征(down’s syndrome,ds)、戊二酸血症(glutaric acidaemia)、癫痫、多发梗塞性痴呆(multi-infarct dementia)和脑炎中的一种或多种。
[0084]
最后,本发明提供了上述索法地尔冻干粉针剂在制备用于预防和/或治疗脑血管和神经系统疾病和症状的药物中的用途。
[0085]
在一些优选的实施方案中,上述用途中的脑血管和神经系统疾病和症状选自血栓栓塞、缺血性中风、出血性中风、脑血管痉挛、脑老化、外伤性脑损伤、外伤性脊髓损伤、心搏停止、动脉低血压、低血糖症、缺氧症和组织缺氧中的一种或多种。
[0086]
下面结合具体实施例对本发明作进一步的说明,以下具体实施例为了更好地理解本发明的技术方案,但本领域的技术人员应当认识到,本发明并不限于这些实施例。本领域技术人员可以对本发明做各种修改而不背离本发明的精神和范围,这些等同形式的修改同样落在本发明的保护范围之内。除非另有说明,下列实施例中所使用的药品、试剂、材料及仪器等均可通过常规商业手段获得。
[0087]
实施例1:索法地尔的制备。
[0088]
按照cn1309703c中所述的方法,制备2-羟基-5-[2,3,5,6-四氟-4-(三氟甲基)苄氨基]苯甲酸:
[0089]
在室温和氮气保护下,将5-氨基水杨酸(102g)和三乙胺(100ml)溶于干燥的dmf(8000ml)中,向溶液中加入2,3,5,6-四氟-4-三氟甲基苄基溴(123g)。将反应混合物在室温条件下搅拌2小时,然后在真空下除去溶剂。用乙酸乙酯/水萃取,有机层用水和盐水洗涤,无水硫酸镁干燥,蒸馏除去溶剂,残余物在醚/正己烷(1:10)中溶析结晶,得白色固体2-羟基-5-[2,3,5,6-四氟-4-(三氟甲基)苄氨基]苯甲酸(160g)。
[0090]
向无水乙醇(500ml)中加入2-羟基-5-[2,3,5,6-四氟-4-(三氟甲基)苄氨基]苯甲酸(100g),在搅拌条件下升温至50℃,直至完全溶解,将所得溶液冷却至10℃,用氢氧化钾无水乙醇溶液将上述溶液的ph值调节至6.8-7.0,室温搅拌2小时,析出晶体,过滤,干燥,得类白色粉末状索法地尔(102g),经hplc检测,纯度≥99.7%。
[0091]
实施例2:索法地尔冻干粉针剂的制备。
[0092]
将索法地尔(3000g)溶于注射用水(30l)中,溶清,用0.45μm孔径的pes材质滤膜过滤,滤液用0.1mol/l的氢氧化钾水溶液调节ph值至8.2,再加入注射用水定容至60l,溶液充氩气保护,在8小时内用0.22μm孔径的pes材质滤膜进行除菌过滤,得索法地尔溶液。
[0093]
将上述索法地尔溶液灌装于西林瓶中,灌装结束后,将玻璃瓶放入冻干机,在30分钟内将冻干机的板层温度降至-50℃,保温1小时;然后将板层温度升至-5℃,保温1小时;再将板层温度降至-50℃,保温1小时。接着,将板层温度升至-30℃,保持真空度为5pa,保温10小时;再将板层温度升至5℃,保持真空度为5pa,保温10小时;继续将板层温度升至10℃,保持真空度为5pa,保温10小时。充氮气至40kpa,压塞,轧盖,包装,即得。
[0094]
实施例3:索法地尔冻干粉针剂的制备。
[0095]
将索法地尔(1500g)溶于注射用水(13l)中,溶清,用0.45μm孔径的pvdf材质滤膜过滤,滤液用0.5mol/l的氢氧化钾水溶液调节ph值至9.0,再加入注射用水定容至18l,溶液
充氩气保护,在4小时内用0.22μm孔径的pvdf材质滤膜进行除菌过滤,得索法地尔溶液。
[0096]
将上述索法地尔溶液灌装于西林瓶中,灌装结束后,将玻璃瓶放入冻干机,在60分钟内将冻干机的板层温度降至-40℃,保温2小时;然后将板层温度升至0℃,保温2小时;再将板层温度降至-40℃,保温2小时。接着,将板层温度升至-25℃,保持真空度为10pa,保温20小时;再将板层温度升至10℃,保持真空度为10pa,保温20小时;继续将板层温度升至25℃,保持真空度为10pa,保温20小时。充氮气至65kpa,压塞,轧盖,包装,即得。
[0097]
实施例4:索法地尔冻干粉针剂的制备。
[0098]
将索法地尔(3750g)溶于注射用水(15l)中,溶清,用0.45μm孔径的ptfe材质滤膜过滤,滤液用0.8mol/l的氢氧化钾水溶液调节ph值至9.8,再加入注射用水定容至19l,溶液充氮气保护,在2小时内用0.22μm孔径的ptfe材质滤膜进行除菌过滤,得索法地尔溶液。
[0099]
将上述索法地尔溶液灌装玻璃瓶中,灌装结束后,将玻璃瓶放入冻干机,在90分钟内将冻干机的板层温度降至-30℃,保温3小时;然后将板层温度升至5℃,保温3小时;再将板层温度降至-30℃,保温3小时。接着,将板层温度升至-20℃,保持真空度为20pa,保温30小时;再将板层温度升至5℃,保持真空度为20pa,保温30小时;继续将板层温度升至40℃,保持真空度为20pa,保温30小时。充氮气至90kpa,压塞,轧盖,包装,即得。
[0100]
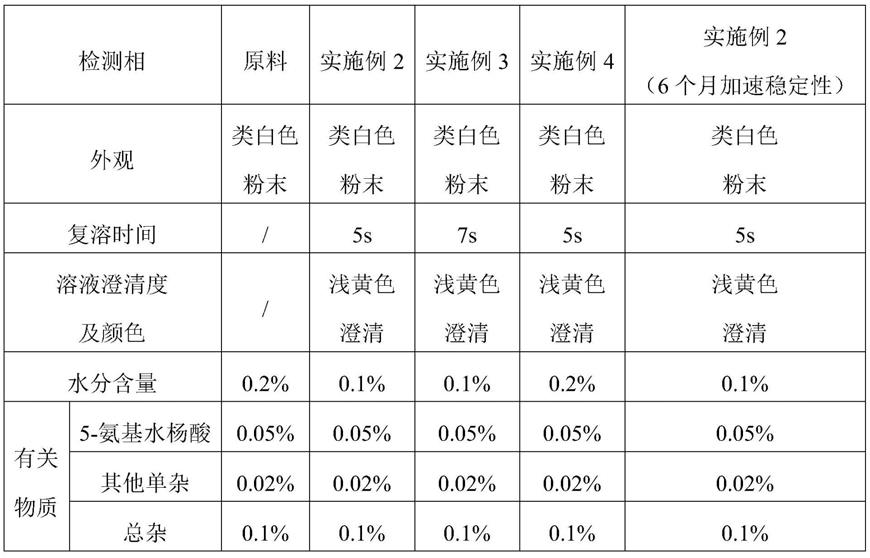
考察实施例2~4中索法地尔冻干粉针剂的外观(《中国药典》2015年版四部通则)、复溶时间、溶液的澄清度及颜色(《中国药典》2015年版附录ix b)、水分(《中国药典》2015年版四部通则0832)、有关物质(《中国药典》2015年版四部通则0512)、稳定性等项目,其结果如表1所示。
[0101]
表1.索法地尔冻干粉针剂性质考察结果
[0102][0103]
通过上述实施例2~4,本发明制备了三个不同批次的索法地尔冻干粉针剂,所有批次的产品均可实现下列效果:
[0104]
(1)通过本发明的方法进行冻干粉针剂生产时,冻干前的溶液澄清,无可见异物;
[0105]
(2)本发明的冻干粉针剂为类白色粉末,粉体细致,结构均一;
[0106]
(3)本发明的冻干粉针剂的复溶性好(复溶时间在10s以内),复溶后的溶液为浅黄色,澄明度良好;
[0107]
(4)本发明的冻干粉针剂的水分含量低(0.2%以下);
[0108]
(5)与原料相比,本发明的冻干粉针剂的杂质含量没有增加,能够得到有效控制;
[0109]
(6)本发明的冻干粉针剂在6个月加速试验前后的各项参数均能保持大体一致,稳定性表现良好。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1