化合物在制备抗A6型柯萨奇病毒药物中的应用的制作方法
本发明属于医药技术领域,具体涉及化合物青蒿酸、青蒿素、绿原酸、栀子苷和木犀草苷在制备抗a6型柯萨奇病毒药物中的应用。
背景技术:
a6型柯萨奇病毒(coxsackievirus,cv-a6),是柯萨奇病毒中的重要类别。2008年以来,cv-a6开始在全世界范围内流行,从欧洲逐渐传播到了亚洲,cv-a6感染致手足口病发病率呈上升趋势。2008年,cv-a6阳性手足口病首次暴发于芬兰,2009年中国台湾、2010年西班牙、2011年日本、2013年我国广东深圳、2014年法国等地相继暴发了cv-a6感染所致手足口病疫情。2013年以来,cv-a6成为手足口病暴发流行的主要病原之一。国内cv-a6感染致手足口病发病率呈上升趋势,cv-a6感染手足口病患者构成比由2009年的8.2﹪上升到2012年的27.4﹪。2013—2017年我国大陆地区手足口病疫情的监测数据表明,cv-a6已成为大部分地区的主要流行株,部分地区超越了ev71和cv-a16,成为引起手足口病的首位病原体,如2013年浙江省检测样本中cv-a6阳性率为51.3%。
cv-a6感染发病的平均年龄为(2.91±2.12)岁,除了感染儿童,也可以感染免疫功能正常的成年人。cv-a6引起的临床症状由早年的疱疹性咽峡炎向皮疹分布广泛及伴随脱甲转变。puenpaj等对vp1基因的分析表明,cv-a6基因组的重组提高了序列间的遗传差异。贝叶斯系统发育分析表明,目前的重组分组(rf-e,-f,--h,-j和-k)均可溯源到一个共同的祖先(rf-a)。39个不同rfs的全长基因均在2a-2c和5’utr之间发生重组。gaunt等[92]的研究表明,截至2014年cv-a6出现了8种重组形式,重组发生在2a-2c区、vp3内部、非编码区和vp1区,且非结构区的重组可能是cva6导致临床症状改变的潜在原因。bian等根据基因组序列的不同,将cv-a6划分为a~e五个分支,e基因型又分为e1和e2亚簇。目前,世界上主流行的cv-a6为e2亚簇。董兆鹏通过ml法建立系统发育树,分析发现从1992年至今山东省cv-a6的流行亚型发生了明显的更替,更替模式为:1992年b亚型→1996年c亚型→2010年d亚型→至今e2亚型,cv-a6的流行实现了由非优势株向优势株的转变。e2亚簇cva6感染往往导致严重的呼吸系统和神经系统疾病,如疱疹性咽峡炎、无菌性脑膜炎、脑干脑炎和急性弛缓性麻痹等。
但是,cv-a6的相关研究目前较少,亟需抗cv-a6药物的研究。
银花青蒿栀子方方源于名老中医经验方,组方为金银花、青蒿和栀子,具有清热解毒、疏风解表之功效。该方成功的开发成热毒宁注射液(rdn)等中药制剂,广泛应用于上呼吸道感染(外感风热证)的治疗,取得了良好的社会和经济效益。但其目前尚未有关于抗cv-a6的研究报道。
青蒿素(artemisinin),商品名黄花蒿素、黄蒿素。主要用于间日疟、恶性疟的症状控制,以及耐氯喹虫株的治疗,也可用以治疗凶险型恶性疟,如脑型、黄疸型等。青蒿素分子式c15h22o5,分子量282,结构式为
青蒿酸英文名artemisicacid,分子式c15h22o2,分子量234,结构式为
绿原酸分子式c16h18o9,分子量354,结构式为
栀子苷英文名geniposide,分子式c17h24o11,分子量404,结构式为
木犀草苷英文名luteoloside,分子式c21h20o11,分子量448,结构式为
技术实现要素:
本发明人通过大量的体外细胞试验研究及不懈探索后发现,青蒿酸、青蒿素、绿原酸、栀子苷和木犀草苷对cv-a6的抑制率显著高于对照药利巴韦林。
本发明的目的在于提供化合物在制备抗a6型柯萨奇病毒药物中的应用,所述化合物为青蒿酸、青蒿素、绿原酸、栀子苷和木犀草苷中的一种或多种,所述青蒿酸、青蒿素、绿原酸、栀子苷和木犀草苷均为银花青蒿栀子方的有效成分。
本发明的另一目的在于提供青蒿酸在制备抗a6型柯萨奇病毒药物中的应用。
本发明的另一目的在于提供青蒿素在制备抗a6型柯萨奇病毒药物中的应用。
本发明的另一目的在于提供绿原酸在制备抗a6型柯萨奇病毒药物中的应用。
本发明的另一目的在于提供栀子苷在制备抗a6型柯萨奇病毒药物中的应用。
本发明的另一目的在于提供木犀草苷在制备抗a6型柯萨奇病毒药物中的应用。
与现有技术相比,本发明首次发现青蒿酸、青蒿素、绿原酸、栀子苷和木犀草苷的抗a6型柯萨奇病毒药生物活性,并对其与病毒靶点蛋白之间的相互作用进行了研究,揭示了其抗a6型柯萨奇病毒机理。
附图说明
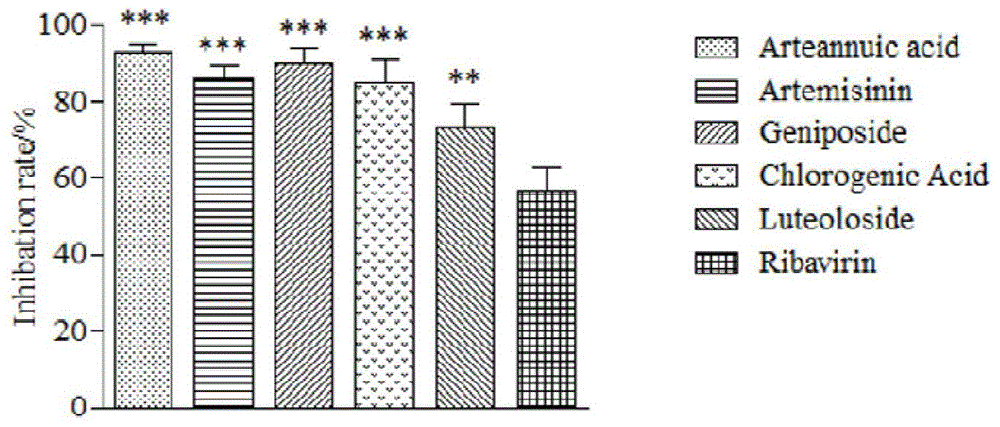
图1为不同化合物对cv-a6的抑制率.n=3,
图2为分子对接的二维与三维示意图(图中,1-绿原酸;2-栀子苷;3-青蒿酸;4-青蒿素;5-木犀草苷)。
具体实施方式
下面结合附图和具体实施方式来对本发明作更进一步的说明,以便本领域的技术人员更了解本发明,但并不以此限制本发明。
实施例1青蒿酸、青蒿素、绿原酸、栀子苷和木犀草苷的抗a6型柯萨奇病毒实验
1.1药材
金银花药材为忍冬科忍冬属植物忍冬lonicerajaponicathunb.的干燥花蕾;青蒿药材为菊科蒿属植物黄花蒿artemisiaannual.的干燥地上部分;栀子药材为茜草科栀子属植物栀子gardeniajasminoideselis的干燥果实。以上药材购自泰安市金泰联药店。
1.2病毒、细胞和动物
cv-a6引自中国疾病预防控制中心病毒病预防控制所毒种室;人横纹肌瘤(rhabdomyoma,rd)细胞,引自中国预防医学研究所病毒研究室。
1.3溶液的配制
细胞培养液:mem培养基:胎牛血清:双抗=89:10:1。
细胞维持液:mem培养基:胎牛血清:双抗=97:2:1。
细胞冻存液:胎牛血清:dmso:mem=1:1:8。
分别称取青蒿酸、青蒿素和木犀草苷各20mg,加二甲亚砜溶解,得到浓度为20mg·ml-1的储备液。取青蒿酸、青蒿素的储备液适量,加细胞维持液稀释,得到2.5-100μg·ml-1共7个不同浓度溶液。取木犀草苷的储备液适量,加细胞维持液稀释,得到2.0-20μg·ml-1共7个不同浓度溶液。
分别称取绿原酸和栀子苷各20mg,加pbs溶解,得到浓度为10mg·ml-1的储备液。取储备液适量,加细胞维持液稀释,得到10-320μg·ml-1共7个不同浓度溶液。
2实验方法
2.1细胞的培养
2.1.1细胞复苏
将细胞冻存管从液氮中取出,立即置于37℃水浴中快速振摇至完全解冻,室温1000r/min离心5min。弃上清,加入细胞培养液,缓慢吹打重悬,置于37℃、5%co2的细胞培养箱中,12h后更换新的培养液。
2.1.2细胞传代
细胞生长至细胞瓶底面积的90%以上时弃培养液,加0.01mpbs洗2次,加入1ml0.25%胰蛋白酶,置于37℃、5%co2的细胞培养箱中1min。弃胰蛋白酶,置于37℃、5%co2的细胞培养箱中,倒置显微镜下观察至细胞间隙明显加入培养液,吹打细胞至均匀分散,调整细胞密度至2×104/ml,置于37℃、5%co2的细胞培养箱。
2.1.3细胞冻存
丰度大于90%、处于对数生长期的细胞经胰酶消化后,加入细胞生长液吹打分散均匀。调整细胞密度至4×106/ml,1000r/min离心10min,弃上清,加预冷的冻存液重悬细胞,转移至冻存管中。按照4℃20min、-20℃30min、-80℃过夜进行梯度降温,转移入液氮中保存。
2.2细胞存活率的测定
采用cck8法测定细胞存活率。96孔板弃液,加pbs洗涤2次,每孔加入100μl维持液、10μlcck8,置于37℃、5%co2的细胞培养箱中培养1h,酶标仪测定450nm的od值,计算细胞存活率。
细胞存活率=(od实验组-od空白组)/(od正常细胞对照-od空白组)×100%。
2.3病毒的繁育
处于对数生长期的rd细胞丰度达80%左右时弃液,加0.01mpbs洗2次。加入2ml维持液和200μlcv-a6病毒液,充分混匀,37℃、5%co2的细胞培养箱中培养2h。补加维持液2ml,置于37℃5%co2的细胞培养箱中继续培养。当75%以上细胞出现病变时,吸取上清液置于无菌离心管中,8000r/min离心5min,上清经0.22μm微孔滤膜过滤,滤液分装,-80℃冻存。
2.4病毒毒力测定
取对数生长期的rd细胞,经胰酶消化加入生长液调整密度至5×104/ml,接至96孔板中(100μl/孔),置于37℃、5%co2的细胞培养箱中培养24h。用维持液将cv-a6病毒液进行稀释,稀释度为10-1~10-10,每孔100μl,每个稀释度8个复孔,同时设置正常细胞对照,置于37℃、5%co2的细胞培养箱孵育2h。弃上清,每孔加维持液100μl,置于37℃、5%co2的细胞培养箱培养,每隔24h换液一次。于接毒后72h观察细胞形态变化,记录特征性细胞病变(cytopathiceffect,cpe)的孔数,根据reed-muench法计算cv-a6在rd细胞中的tcid50。
2.5细胞毒性测定
收集对数期细胞,用细胞生长液调整细胞密度为5×104/ml,接种到96孔板,每孔100μl。置于37℃含5%co2的细胞培养箱中培养24h,弃液,pbs洗2次。将不同组方提取物的药物溶液和对照利巴韦林溶液加入到细胞中,每孔100μl,对照组加入维持液,置于37℃含5%co2的细胞培养箱中培养48h,按照“2.2”项下方法测定细胞存活率,计算最大无毒浓度。
2.6体外抗病毒作用
2.6.1病毒感染和药物作用方式
收集对数期rd细胞,用生长液调整细胞密度为5×104/ml,接到96孔板,每孔100μl,置于37℃含5%co2的细胞培养箱中培养24h。弃液,pbs洗2次。将50μg/ml的药液和病毒液1:1混合,加入到96孔板,每孔100μl(moi=1),同时设置正常细胞对照组和病毒对照组。置于37℃含5%co2的细胞培养箱中培养1h。弃液,加入维持液,每孔100μl,置于37℃含5%co2的细胞培养箱孵育至48hpi。
2.6.2评价指标
显微镜下观察细胞病变情况,按照“2.2”项下方法测定细胞存活率,计算病毒抑制率。
病毒抑制率%=(样品组od-病毒对照组od)/(细胞对照组od-病毒对照组od)*100%
3.结果
3.1病毒毒力测定
cv-a6感染rd细胞72h的cpe情况见表1。
表1cv-a6感染rd细胞72h的cpe
距离比例=(大于50﹪的阳性百分比-50)/(大于50﹪的阳性比-小于50﹪的阳性百分比)
logtcid50=高于50﹪的病毒稀释度的对数+距离比例×稀释系数的对数
cv-a6在rd细胞中的tcid50为10-8.41/0.1ml。
3.2化合物的细胞毒性
青蒿酸、青蒿素、栀子苷、绿原酸和木犀草苷对rd细胞的最大无毒浓度tc0结果见表2。
表2化合物对rd细胞的细胞毒性
3.3化合物的抗病毒活性
青蒿酸、青蒿素、绿原酸、栀子苷和木犀草苷的病毒抑制率结果见图1。
由图1可见,青蒿酸、青蒿素、绿原酸、栀子苷和木犀草苷对cv-a6的抑制率显著高于对照利巴韦林(p<0.01或0.001),具有良好的抗cv-a6作用。
3.4活性成分与病毒靶点蛋白之间的相互作用
cv-a6属于小核糖核酸病毒科的evsa组,病毒颗粒基因组编码的多聚蛋白水解为3个蛋白前体(p1~p3)。p1进一步水解为4个结构蛋白(vp1~vp4),共同构成病毒衣壳。vp4位于病毒衣壳内侧,vp1~vp3位于衣壳表面,是抗原决定簇存在的主要部位。其中,vp1的surface-exposedloops和c端结构是主要的免疫原性位点,作为分子对接的结合部位。将化合物的二维结构转变成三维结构,作为配体与受体蛋白进行对接,分子对接的二维作用示意图和三维结构示意图见图2。
由图2可见,绿原酸分子和vp1蛋白的asn、tyr等6个氨基酸残基之间存在氢键作用,栀子苷分子与met、asp等7个氨基酸之间形成氢键,亲和力强。青蒿酸分子和氨基酸arg、glu之间形成氢键,和asp、tyr等多个残基之间存在范德华引力。木犀草苷分子与asn、cys等5个氨基酸之间存在氢键作用,同时与其他氨基酸存在碳氢键、范德华引力、pi-sulfur等相互作用。上述化合物分子与氨基酸残基之间的相互作用使二者具有良好的亲和力,使化合物起到抑制vp1蛋白的作用。
分子对接结果表明,青蒿酸、青蒿素、绿原酸、栀子苷和木犀草苷分子均与cv-a6衣壳蛋白存在多个氢键、范德华引力等作用,具有良好的亲和力,生成的复合物稳定,可抑制病毒衣壳蛋白,发挥抗病毒作用。
- 还没有人留言评论。精彩留言会获得点赞!