贴剂的制作方法
1.本发明涉及一种贴剂。
现有技术
2.贴剂等经皮吸收制剂由于可使药物透过皮肤直接到达血管,因此可避免消化道酶的分解、肝脏的首过效应等经口给药的缺点,具备减少给药次数、提高服药依从性、可容易地进行给药的切换等优点。在使用者为老年人或儿童时,贴剂等经皮吸收制剂的优点变得特别重要。
3.但是,经皮吸收制剂由于药物与皮肤直接接触而有时出现搔痒、红斑、发疹、疼痛、湿疹、皮炎等症状(以下也称为“皮肤刺激”)。因此,研究了各种各样的制剂。例如,作为贴剂的结构,可举出:由支持体层、贮药层、粘合剂层等多个层构成的多层型贴剂(例如,参照专利文献1、2);以及粘合剂层含有药物的双层型贴剂(例如,参照专利文献3)。
4.在多层型贴剂中,含有药物的贮药层与皮肤被粘合剂层隔开,即使在应用于皮肤时,也不易出现由药物引起的皮肤刺激。但是,多层型贴剂由于贴剂整体的厚度增加,因此产生在使用中容易脱落、附着在保存用包装材料的内层上等新的问题。
5.现有技术文献
6.专利文献
7.专利文献1:国际公开第2007/064407号
8.专利文献2:国际公开第2015/087926号
9.专利文献3:国际公开第2010/098230号
技术实现要素:
10.发明要解决的课题
11.因此,本发明的目的在于鉴于上述情况,提供一种减少由药物引起的皮肤刺激和皮肤萎缩的贴剂。
12.解决课题的手段
13.[1]贴剂,其在支持体上具备粘合剂层,粘合剂层含有粘合基剂、皮肤刺激性药物或其药学上可接受的盐、和戊酸二氟可龙,戊酸二氟可龙的含量以粘合剂层的总质量为基准,为0.0009~0.08质量%。
[0014]
[2]如[1]所述的贴剂,其中,粘合基剂包含选自橡胶系粘合基剂、丙烯酸系粘合基剂和有机硅系粘合基剂中的至少1种粘合基剂。
[0015]
[3
‑
1]如[1]或[2]所述的贴剂,其中,皮肤刺激性药物或其药学上可接受的盐为阿塞那平或其药学上可接受的盐,阿塞那平或其药学上可接受的盐的含量在换算为阿塞那平游离体的质量时,以粘合剂层的总质量为基准,为1~25质量%。
[0016]
[3
‑
2]如[1]或[2]所述的贴剂,其中,皮肤刺激性药物或其药学上可接受的盐为利凡斯的明,利凡斯的明的含量以粘合剂层的总质量为基准,为6~30质量%。
[0017]
[3
‑
3]如[1]或[2]所述的贴剂,其中,皮肤刺激性药物或其药学上可接受的盐为罗替戈汀,罗替戈汀的含量以粘合剂层的总质量为基准,为5~15质量%。
[0018]
[3
‑
4]如[1]或[2]所述的贴剂,其中,皮肤刺激性药物或其药学上可接受的盐为美金刚或其药学上可接受的盐,美金刚或其药学上可接受的盐的含量在换算为美金刚游离体的质量时,以粘合剂层的总质量为基准,为0.1~50质量%。
[0019]
[3
‑
5]如[1]或[2]所述的贴剂,其中,皮肤刺激性药物或其药学上可接受的盐为氨氯地平或其药学上可接受的盐,氨氯地平或其药学上可接受的盐的含量在换算为氨氯地平游离体的质量时,以粘合剂层的总质量为基准,为0.1~40质量%。
[0020]
[3
‑
6]如[1]或[2]所述的贴剂,其中,皮肤刺激性药物或其药学上可接受的盐为罗匹尼罗或其药学上可接受的盐,罗匹尼罗或其药学上可接受的盐的含量在换算为罗匹尼罗游离体的质量时,以粘合剂层的总质量为基准,为0.5~50质量%。
[0021]
[4
‑
1]如[1]、[2]或[3
‑
1]所述的贴剂,其中,皮肤刺激性药物或其药学上可接受的盐为马来酸阿塞那平,粘合剂层中含有的戊酸二氟可龙的含量以粘合剂层的总质量为基准,为0.0009~0.08质量%。
[0022]
[4
‑
2]如[1]、[2]或[3
‑
2]所述的贴剂,其中,皮肤刺激性药物或其药学上可接受的盐为利凡斯的明,粘合剂层中含有的戊酸二氟可龙的含量以粘合剂层的总质量为基准,为0.0009~0.08质量%。
[0023]
[4
‑
3]如[1]、[2]或[3
‑
3]所述的贴剂,其中,皮肤刺激性药物或其药学上可接受的盐为罗替戈汀,粘合剂层中含有的戊酸二氟可龙的含量以粘合剂层的总质量为基准,为0.0005~0.08质量%。
[0024]
[4
‑
4]如[1]、[2]或[3
‑
4]所述的贴剂,其中,皮肤刺激性药物或其药学上可接受的盐为盐酸美金刚,粘合剂层中含有的戊酸二氟可龙的含量以粘合剂层的总质量为基准,为0.0009~0.08质量%。
[0025]
[4
‑
5]如[1]、[2]或[3
‑
5]所述的贴剂,其中,皮肤刺激性药物或其药学上可接受的盐为苯磺酸氨氯地平,粘合剂层中含有的戊酸二氟可龙的含量以粘合剂层的总质量为基准,为0.0005~0.08质量%。
[0026]
[4
‑
6]如[1]、[2]或[3
‑
6]所述的贴剂,其中,皮肤刺激性药物或其药学上可接受的盐为盐酸罗匹尼罗,粘合剂层中含有的戊酸二氟可龙的含量以粘合剂层的总质量为基准,为0.0009~0.08质量%。
[0027]
[5
‑
1]如[1]、[2]或[3
‑
1]所述的贴剂,其中,皮肤刺激性药物或其药学上可接受的盐为马来酸阿塞那平,粘合剂层中含有的马来酸阿塞那平与戊酸二氟可龙的质量比为12.5:1~27778:1。
[0028]
[5
‑
2]如[1]、[2]或[3
‑
2]所述的贴剂,其中,皮肤刺激性药物或其药学上可接受的盐为利凡斯的明,粘合剂层中含有的利凡斯的明与戊酸二氟可龙的质量比为75:1~33333:1。
[0029]
[5
‑
3]如[1]、[2]或[3
‑
3]所述的贴剂,其中,皮肤刺激性药物或其药学上可接受的盐为罗替戈汀,粘合剂层中含有的罗替戈汀与戊酸二氟可龙的质量比为62.5:1~20000:1。
[0030]
[5
‑
4]如[1]、[2]或[3
‑
4]所述的贴剂,其中,皮肤刺激性药物或其药学上可接受的盐为盐酸美金刚,粘合剂层中含有的盐酸美金刚与戊酸二氟可龙的质量比为1.25:1~
55556:1。
[0031]
[5
‑
5]如[1]、[2]或[3
‑
5]所述的贴剂,其中,皮肤刺激性药物或其药学上可接受的盐为苯磺酸氨氯地平,粘合剂层中含有的苯磺酸氨氯地平与戊酸二氟可龙的质量比为1.25:1~44444:1。
[0032]
[5
‑
6]如[1]、[2]或[3
‑
6]所述的贴剂,其中,皮肤刺激性药物或其药学上可接受的盐为盐酸罗匹尼罗,粘合剂层中含有的盐酸罗匹尼罗与戊酸二氟可龙的质量比为6.25:1~55556:1。
[0033]
发明效果
[0034]
根据本发明,可提供一种减少由药物引起的皮肤刺激和皮肤萎缩的贴剂。
具体实施方式
[0035]
本说明书中,“皮肤刺激”是指在将含有任意药物的贴剂应用于皮肤时,在该应用部位产生的皮肤刺激,具体地,表现为搔痒、红斑、发疹、疼痛、湿疹、皮炎等皮肤症状。另外,皮肤刺激的程度例如可以通过对红斑和浮肿的程度评分,以此为基准来评价。
[0036]
本说明书中,“皮肤萎缩”是指在将甾体化合物应用于皮肤时,应用部位的表皮与通常的表皮(不受甾体化合物的影响的状态下的表皮的厚度)相比变薄的症状。另外,皮肤萎缩的程度例如可以以将贴剂应用于皮肤后的表皮的厚度与通常的表皮的厚度相比是否为50%以下为基准来评价。
[0037]
本发明中的“皮肤刺激的降低”和“皮肤萎缩的降低”例如通过实施例中所述的方法,相对地评价。
[0038]
本发明一实施方式的贴剂是在支持体上具备粘合剂层的贴剂,粘合剂层含有:粘合基剂、皮肤刺激性药物或其药学上可接受的盐、和戊酸二氟可龙。
[0039]
支持体是物理上支持粘合剂层的层。支持体的材质只要是通常可用于贴剂的材质,就没有限定。作为支持体的材质,例如可举出:聚乙烯、聚丙烯、聚丁二烯等聚烯烃;聚对苯二甲酸乙二醇酯、聚对苯二甲酸丁二醇酯、聚萘二甲酸乙二醇酯等聚酯;和乙烯
‑
乙酸乙烯酯共聚物、乙酸乙烯酯
‑
氯乙烯共聚物、聚氯乙烯、聚酰胺、尼龙、纤维素衍生物、聚氨酯等合成树脂。支持体的性状可以为膜、片、片状多孔质体、片状发泡体、织布、编织布、无纺布或它们的层叠体。
[0040]
粘合剂层含有粘合基剂、皮肤刺激性药物或其药学上可接受的盐、和戊酸二氟可龙。但是,本说明书中,皮肤刺激性药物并非奥昔布宁。
[0041]
粘合基剂只要是通常可用于贴剂的粘合基剂即可,例如可举出:橡胶系粘合基剂、丙烯酸系粘合基剂和有机硅系粘合基剂。也可以组合使用多种粘合基剂。优选的粘合基剂为橡胶系粘合基剂、丙烯酸系粘合基剂或它们的混合物。
[0042]
橡胶系粘合基剂可以是以天然或合成橡胶为主体的高分子,例如为聚异戊二烯、聚异丁烯、聚丁二烯、苯乙烯
‑
异戊二烯
‑
苯乙烯嵌段共聚物(sis嵌段共聚物)、苯乙烯
‑
丁二烯
‑
苯乙烯嵌段共聚物、苯乙烯
‑
丁二烯橡胶、或苯乙烯
‑
异戊二烯橡胶。
[0043]
作为丙烯酸系粘合基剂,例如可举出:(甲基)丙烯酸烷基酯的聚合物或(甲基)丙烯酸烷基酯与共聚单体的共聚物。在此,“(甲基)丙烯酸”及其类似表述是指丙烯酸、甲基丙烯酸、和这两者,烷基为碳数1~20的烷基,优选为碳数3~12的烷基。作为(甲基)丙烯酸烷
基酯,例如可举出:(甲基)丙烯酸丁酯、(甲基)丙烯酸异丁酯、(甲基)丙烯酸己酯、(甲基)丙烯酸辛酯、(甲基)丙烯酸2
‑
乙基己酯、和(甲基)丙烯酸癸酯。(甲基)丙烯酸烷基酯可单独使用或组合使用2种以上。作为共聚单体,例如可举出:(甲基)丙烯酸羟基烷基酯、乙烯、丙烯、苯乙烯、乙酸乙烯酯、n
‑
乙烯基吡咯烷酮、和(甲基)丙烯酰胺。共聚单体可单独使用或组合使用2种以上。作为丙烯酸系粘合基剂,具体地可举出含有共聚物的丙烯酸系粘合基剂,该共聚物含有选自丙烯酸丁酯、丙烯酸2
‑
乙基己酯、乙酸乙烯酯、甲基丙烯酸、丙烯酸羟乙酯、甲基丙烯酸缩水甘油基酯、丙烯酸甲氧基乙酯和丙烯酸中的至少2种。作为具体例,可举出:duro
‑
tak87
‑
2097、87
‑
2194、87
‑
2196、87
‑
2287、87
‑
2516、和87
‑
2852(商品名,汉高公司);mas811(商品名,
コスメディ
制药(株)制);plastoid b(商品名,rohm pharm polymers公司制)以及nissetsu kp
‑
77和as
‑
370(商品名,日本电石工业(株))。
[0044]
丙烯酸系粘合基剂可以为不具有官能团的丙烯酸系粘合基剂,也可以为具有官能团的丙烯酸粘合基剂。“官能团”是指含有除碳原子和氢原子以外的元素的基团,例如为羟基、烷氧基、羧基(也包括盐)、2
‑
氧代吡咯烷基、乙酰氧基、酰胺基、缩水甘油基、氨基、单烷基氨基、二烷基氨基、季铵。这样的官能团主要来自共聚单体的化学结构。
[0045]
作为有机硅系粘合基剂,例如可举出:二甲基聚硅氧烷、二甲基聚硅氧烷与硅酸盐树脂的缩合反应物等有机聚硅氧烷。作为有机硅系粘合基剂,具体地可举出bio
‑
psa x7
‑
4201、bio
‑
psa q7
‑
4501、360medical fluid 1000cs、和mdx4
‑
4210(商品名,道康宁公司)。
[0046]
粘合基剂的含量例如以粘合剂层的总质量作为基准,优选为5~90质量%,更优选为10~50质量%,进一步优选为10~30质量%。
[0047]
皮肤刺激性药物只要是显示皮肤刺激性和经皮吸收性的药物(游离体),就没有特别限定。本发明中“皮肤刺激性药物或其药学上可接受的盐”如后述的试验例1所述,是指将贴剂贴附于hwy:slc大鼠后,在将贴剂剥离0.5小时后的时间点,基于draize等人的判定基准(参考文献:draize jh等人,j.pharmacol.exp.ther.1944:82:377
‑
390)的平均得分为0.1~2.0的药物。
[0048]
作为皮肤刺激性药物或其药学上可接受的盐,例如可举出:解热消炎镇痛药(吲哚美辛等)、抗炎药(辣椒素、辣椒提取物等)、精神神经用药(氢溴酸西酞普兰、马来酸阿塞那平、利培酮等)、局部麻醉药(盐酸利多卡因等)、泌尿器官用药(托特罗定等)、抗帕金森病药(盐酸罗匹尼罗、罗替戈汀等)、戒烟辅助药(烟碱等)、循环器官用药(苯磺酸氨氯地平等)、抗过敏药(富马酸酮替芬等)、抗阿尔兹海默症药(盐酸多奈哌齐、利凡斯的明、盐酸美金刚等)、骨骼肌脂环药(盐酸替扎尼定等)、前列腺环素受体激动剂(赛乐西帕等)、兴奋/清醒剂(去氧麻黄碱盐酸盐、盐酸哌醋甲酯等)。这些药物或其药学上可接受的盐可以仅为相应药物的游离体、也可以仅为相应药物的药学上可接受的盐,或者也可以为它们的混合物。
[0049]
皮肤刺激性药物或其药学上可接受的盐的含量只要是可确保该药物的有效血药浓度的量即可。在皮肤刺激性药物的含量小于规定范围的下限时,有皮肤透过量减少的倾向,因此需要增大贴剂的面积,另一方面,当超过上述上限时,有产生皮肤刺激等局部的副作用,或者对皮肤的附着力、粘性等粘合物性下降的倾向。
[0050]
当皮肤刺激性药物的药学上可接受的盐为马来酸阿塞那平时,其含量在换算为阿塞那平游离体的质量时,以粘合剂层的总质量为基准,可以为1~25质量%、1~15质量%、1.5~12质量%、2~10质量%、3~8质量%、或4~7质量%。
[0051]
当皮肤刺激性药物为利凡斯的明时,其含量以粘合剂层的总质量为基准,可以为6~30质量%、10~30质量%、或20~30质量%。
[0052]
当皮肤刺激性药物为罗替戈汀时,其含量以粘合剂层的总质量为基准,可以为5~15质量%、7~12质量%、或8~10质量%。
[0053]
当皮肤刺激性药物的药学上可接受的盐为盐酸美金刚时,其含量在换算为美金刚游离体的质量时,以粘合剂层的总质量为基准,可以为0.1~50质量%、5~45质量%、10~40质量%、10~30质量%、11~20质量%、或12~15质量%。
[0054]
当皮肤刺激性药物的药学上可接受的盐为苯磺酸氨氯地平时,其含量在换算为氨氯地平游离体的质量时,以粘合剂层的总质量为基准,可以为0.1~40质量%、0.2~30质量%、0.5~20质量%、0.6~10质量%、0.8~8质量%、或1~5质量%。
[0055]
当皮肤刺激性药物的药学上可接受的盐为盐酸罗匹尼罗时,其含量在换算为罗匹尼罗游离体的质量时,以粘合剂层的总质量为基准,可以为0.5~50质量%、5~30质量%、10~20质量%、或12~20质量%。
[0056]
戊酸二氟可龙也称为6α,9
‑
二氟
‑
11β
‑
羟基
‑
21
‑
戊酰氧基
‑
16α
‑
甲基
‑
1,4
‑
孕甾二烯
‑
3,20
‑
二酮。戊酸二氟可龙是具有合成肾上腺皮质激素作用的甾体化合物的一种,与其他甾体化合物同样地具有抗炎作用。根据日本的特应性皮肤炎诊疗指南2018,戊酸二氟可龙属于甾体化合物的5个分类中的ii类(非常强)。
[0057]
戊酸二氟可龙的含量只要以粘合剂层的总质量为基准,为0.0009~0.08质量%即可,优选为0.0009~0.05质量%。当戊酸二氟可龙的含量为0.0009质量%以上时,存在更容易减轻由药物引起的皮肤刺激的倾向。当戊酸二氟可龙的含量为0.08质量%以下时,更不易产生贴附部位的皮肤萎缩。
[0058]
当皮肤刺激性药物的药学上可接受的盐为马来酸阿塞那平时,戊酸二氟可龙的含量只要以粘合剂层的总质量为基准,为0.0009~0.08质量%即可,优选为0.0009~0.05质量%。当戊酸二氟可龙的含量为0.0009质量%以上时,存在更容易减轻由药物引起的皮肤刺激的倾向。当戊酸二氟可龙的含量为0.08质量%以下时,更不易产生贴附部位的皮肤萎缩。
[0059]
当皮肤刺激性药物为利凡斯的明时,戊酸二氟可龙的含量只要以粘合剂层的总质量为基准,为0.0009~0.08质量%即可,优选为0.0009~0.05质量%。当戊酸二氟可龙的含量为0.0009质量%以上时,存在更容易减轻由药物引起的皮肤刺激的倾向。当戊酸二氟可龙的含量为0.08质量%以下时,更不易产生贴附部位的皮肤萎缩。
[0060]
当皮肤刺激性药物为罗替戈汀时,戊酸二氟可龙的含量以粘合剂层的总质量为基准,为0.0005~0.08质量%即可,优选为0.0005~0.05质量%。当戊酸二氟可龙的含量为0.0005质量%以上时,存在更容易减轻由药物引起的皮肤刺激的倾向。当戊酸二氟可龙的含量为0.08质量%以下时,更不易产生贴附部位的皮肤萎缩。
[0061]
当皮肤刺激性药物的药学上可接受的盐为盐酸美金刚时,戊酸二氟可龙的含量只要以粘合剂层的总质量为基准,为0.0009~0.08质量%即可,优选为0.0009~0.05质量%。当戊酸二氟可龙的含量为0.0009质量%以上时,存在更容易减轻由药物引起的皮肤刺激的倾向。当戊酸二氟可龙的含量为0.08质量%以下时,更不易产生贴附部位的皮肤萎缩。
[0062]
当皮肤刺激性药物的药学上可接受的盐为苯磺酸氨氯地平时,戊酸二氟可龙的含
量只要以粘合剂层的总质量为基准,为0.0005~0.08质量%即可,优选为0.0005~0.05质量%。当戊酸二氟可龙的含量为0.0005质量%以上时,存在更容易减轻由药物引起的皮肤刺激的倾向。当戊酸二氟可龙的含量为0.08质量%以下时,更不易产生贴附部位的皮肤萎缩。
[0063]
当皮肤刺激性药物的药学上可接受的盐为盐酸罗匹尼罗时,戊酸二氟可龙的含量只要以粘合剂层的总质量为基准,为0.0009~0.08质量%即可,优选为0.0009~0.05质量%。当戊酸二氟可龙的含量为0.0009质量%以上时,存在更容易减轻由药物引起的皮肤刺激的倾向。当戊酸二氟可龙的含量为0.08质量%以下时,更不易产生贴附部位的皮肤萎缩。
[0064]
另外,粘合剂层中含有的皮肤刺激性药物与戊酸二氟可龙的质量比优选为以下范围。当粘合剂层含有皮肤刺激性药物的药学上可接受的盐时,将该盐的含量以该盐整体的分子量为基准换算为该药物的游离体的质量,计算该游离体与戊酸二氟可龙的质量比。
[0065]
当皮肤刺激性药物的药学上可接受的盐为马来酸阿塞那平时,粘合剂层中含有的马来酸阿塞那平(换算为阿塞那平游离体的质量)与戊酸二氟可龙的质量比优选为:12.5:1~27778:1、12.5:1~16667:1、18.75:1~13333:1、40:1~10000:1、70:1~9000:1、或100:1~8000:1、或110:1~7000:1。
[0066]
当皮肤刺激性药物为利凡斯的明时,粘合剂层中含有的利凡斯的明与戊酸二氟可龙的质量比优选为:75:1~33333:1、125:1~33333:1、300:1~30000:1、400:1~30000:1、或400:1~26000:1。
[0067]
当皮肤刺激性药物为罗替戈汀时,粘合剂层中含有的罗替戈汀与戊酸二氟可龙的质量比优选为:62.5:1~20000:1、62.5:1~18000:1、62.5:1~16667:1、87.5:1~13333:1、100:1~12000:1、150:1~11000:1、或160:1~10000:1。
[0068]
当皮肤刺激性药物的药学上可接受的盐为盐酸美金刚时,粘合剂层中含有的盐酸美金刚(换算为美金刚游离体的质量)与戊酸二氟可龙的质量比优选为:1.25:1~55556:1、62.5:1~50000:1、140:1~45000:1、200:1~40000:1、220:1~25000:1、或250:1~15000:1。
[0069]
当皮肤刺激性药物的药学上可接受的盐为苯磺酸氨氯地平时,粘合剂层中含有的苯磺酸氨氯地平(换算为氨氯地平游离体的质量)与戊酸二氟可龙的质量比优选为:1.25:1~44444:1、6.25:1~22222:1、20:1~5000:1、20:1~2000:1、或20:1~1600:1。
[0070]
当皮肤刺激性药物的药学上可接受的盐为盐酸罗匹尼罗时,粘合剂层中含有的盐酸罗匹尼罗(换算为罗匹尼罗游离体的质量)与戊酸二氟可龙的质量比优选为:6.25:1~55556:1、62.5:1~33333:1、200:1~30000:1、或200:1~15000:1。
[0071]
粘合剂层还可以含有其他成分(增粘剂、增塑剂、填充剂、稳定剂、药物的经皮吸收促进剂、香料等)。
[0072]
作为增粘剂,例如可举出:萜烯树脂、萜烯酚醛树脂、松香酯树脂、氢化松香酯树脂、脂环族饱和烃树脂、和石油系树脂。萜烯树脂优选为经氢化的萜烯树脂。萜烯树脂优选为氢化的萜烯树脂。作为萜烯树脂,例如可举出:α
‑
蒎烯树脂、β
‑
蒎烯树脂、芳族改性萜烯树脂、和萜烯酚醛树脂。
[0073]
作为增塑剂,例如可举出:石蜡油(液体石蜡等);角鲨烷、角鲨烯、植物油类(橄榄
油、山茶油、蓖麻油、妥尔油、花生油、薄荷油、桉油、荷荷芭油、白樟油、葵花籽油、橙油等);脂类(邻苯二甲酸二丁酯、邻苯二甲酸二辛酯等);和液态橡胶(液态聚丁烯、液态异戊二烯橡胶等)。
[0074]
作为填充剂,例如可举出:金属化合物(氧化铝、氢氧化铝、氧化锌、氧化钛、碳酸钙等)、陶瓷(滑石、粘土、高岭土、二氧化硅、羟基磷灰石、合成硅酸铝、硅酸铝镁等)或有机化合物(纤维素粉末、硬脂酸盐等)的粉末或含有它们的树脂的短纤维。
[0075]
经皮吸收促进剂只要为以往已知具有在皮肤上的经皮吸收促进作用的化合物即可。作为经皮吸收促进剂,例如可举出:有机酸及其盐(例如,碳数6~20的脂族羧酸(以下,也称为“脂肪酸”)及其盐、肉桂酸及其盐)、有机酸酯(例如,脂肪酸酯、肉桂酸酯)、有机酰胺(例如,脂肪酰胺)、脂肪醇、多元醇、醚(例如,脂肪醚、聚氧乙烯烷基醚)等。这些吸收促进剂可以具有不饱和键,也可以为环状、直链状或支链状的化学结构。另外,经皮吸收促进剂可以为单萜烯系化合物、倍半萜烯系化合物、和植物油(例如,橄榄油)。这些经皮吸收促进剂可以单独使用1种或组合使用2种以上。
[0076]
作为上述有机酸,可举出:脂族(单、二或三)羧酸(例如,乙酸、丙酸、柠檬酸(包括柠檬酸酐)、异丁酸、己酸、辛酸、脂肪酸、乳酸、马来酸、丙酮酸、草酸、琥珀酸、酒石酸等)、芳族羧酸(例如,邻苯二甲酸、水杨酸、苯甲酸、乙酰水杨酸等)、肉桂酸、链烷磺酸(例如,甲磺酸、乙磺酸、丙磺酸、丁磺酸)、烷基磺酸衍生物(例如,聚氧乙烯烷基醚磺酸、n
‑2‑
羟基乙基哌嗪
‑
n'
‑2‑
乙磺酸)、胆酸衍生物(例如,去氢胆酸等)。这些有机酸可以为钠盐等碱金属盐。其中,优选为脂族羧酸、芳族羧酸或它们的盐,特别优选为乙酸、乙酸钠或柠檬酸。
[0077]
作为脂肪酸,例如可举出:月桂酸、肉豆蔻酸、棕榈酸、硬脂酸、异硬脂酸、油酸、亚油酸、亚麻酸。
[0078]
作为有机酸酯,例如可举出:乙酸乙酯、乙酸丙酯、乳酸鲸蜡基酯、乳酸月桂基酯、水杨酸甲酯、水杨酸乙二醇酯、肉桂酸甲酯、脂肪酸酯。作为脂肪酸酯,例如可举出:月桂酸甲酯、月桂酸己酯、肉豆蔻酸异丙酯、肉豆蔻酸肉豆蔻酯、肉豆蔻酸辛基十二烷基酯、棕榈酸鲸蜡基酯。脂肪酸酯可以为甘油脂肪酸酯、丙二醇脂肪酸酯、山梨糖醇酐脂肪酸酯、聚乙二醇山梨糖醇酐脂肪酸酯、聚乙二醇脂肪酸酯、蔗糖脂肪酸酯、或聚氧乙烯氢化蓖麻油。作为脂肪酸酯的具体例,可举出:单辛酸甘油酯、单癸酸甘油酯、单月桂酸甘油酯、单油酸甘油酯、山梨糖醇酐单月桂酸酯、蔗糖单月桂酸酯、聚山梨酯20(商品名)、丙二醇单月桂酸酯、聚乙二醇单月桂酸酯、聚乙二醇单硬脂酸酯、司盘20、司盘40、司盘60、司盘80、司盘120(商品名)、吐温20、吐温21、吐温40、吐温60、吐温80(商品名)、nikkol hco
‑
60(商品名)。
[0079]
作为有机酰胺,例如可举出:脂肪酰胺(例如,月桂酸二乙醇酰胺)、六氢
‑1‑
十二烷基
‑
2h
‑
吖庚因
‑2‑
酮(也称为氮酮)及其衍生物、焦硫代癸烷。
[0080]
脂肪醇是指碳数6~20的脂族醇。作为脂肪醇,例如可举出:月桂醇、肉豆蔻醇、油醇、异硬脂醇、鲸蜡醇。作为多元醇,例如可举出:丙二醇。
[0081]
作为聚氧乙烯烷基醚,例如可举出:聚氧乙烯月桂基醚。
[0082]
作为单萜烯系化合物,例如可举出:香叶醇、百里香酚、丁香酚、萜品醇、l
‑
薄荷醇、龙脑、d
‑
柠檬烯、异丁香酚、异龙脑、橙花醇、dl
‑
樟脑。
[0083]
更优选为油醇、月桂醇、异硬脂醇、月桂酸二乙醇酰胺、单辛酸甘油酯、单癸酸甘油酯、单油酸甘油酯、山梨糖醇酐单月桂酸酯、丙二醇单月桂酸酯、聚氧乙烯月桂基醚或焦硫
代癸烷。优选为脂肪酸,特别优选为油酸。
[0084]
粘合剂层可以在与支持体相反一侧的与皮肤接触的面上具备剥离衬垫。剥离衬垫是在使用贴剂时被除去的衬垫,只要是通常可用于贴剂的衬垫,就没有限定。作为剥离衬垫的材质,可举出:聚酯(聚对苯二甲酸乙二醇酯(pet)等)、聚烯烃(聚丙烯、聚乙烯等)、及纤维素化合物(纸等)。剥离衬垫可以是由上述材质的层叠体构成的片状。剥离衬垫的表面优选通过有机硅或含氟聚烯烃等进行过离型处理。
[0085]
本实施方式的贴剂例如可通过以下方法制造。
[0086]
1)称取粘合剂层的成分,根据需要进行加温和添加溶剂,混合而使之均匀化。
[0087]
2)在剥离衬垫的离型面上以一定厚度延展得到的粘合剂组合物,根据需要进行干燥以除去溶剂成分,形成粘合剂层。
[0088]
3)在粘合剂层上层叠支持体。
[0089]
4)剪裁成特定的形状(例如,短边为3cm~14cm且长边为7cm~20cm的长方形、或直径为1cm~10cm的圆形)。
[0090]
实施例
[0091]
以下,使用实施例和比较例更详细地说明本发明的贴剂。
[0092]
<贴剂的制造>
[0093]
根据各表的记载,混合特定量的各成分,得到均匀的粘合剂组合物。将得到的粘合剂组合物在聚对苯二甲酸乙二醇酯制的膜(剥离衬垫)上延展,形成粘合剂层。在粘合剂层上层叠聚对苯二甲酸乙二醇酯膜(支持体),裁剪为特定的形状,得到实施例、比较例或参考例的贴剂。另外,各表中,只要没有特别说明,数值表示质量%。
[0094]
试验例1:皮肤刺激和皮肤萎缩的评价
[0095]
hwy:购入slc大鼠(6~7周龄,雌性),驯化6天以上。在驯化期间在大鼠背部实施剪毛和剃毛处理。从所有大鼠中选拔一般状态和皮肤状态良好的大鼠,以体重均等的方式实施分组。对各组的大鼠应用任一种贴剂和作为对照的比较例1的贴剂。具体地,在贴附日在大鼠的背部皮肤(剃毛区域)设定贴附部位(约1.5cm
×
1.5cm或约1cm
×
1cm的长方形),在其四角作标记。将上述得到的贴剂分别贴附在所标记的贴附部位。贴附后,以覆盖贴附部位的方式贴附网状粘合绷带,进而覆盖纱布并用粘合性伸缩绷带固定。贴附24小时后,将纱布、粘合绷带和贴剂除去,评价各组大鼠的皮肤刺激的程度。另外,评价皮肤刺激的程度后,摘取贴附部位的皮肤,制作皮肤切片标本,评价皮肤萎缩的程度。
[0096]
皮肤刺激的评价是在剥离贴剂0.5小时后,以draize等人的判定基准(参考文献:draize jh等人,j.pharmacol.exp.ther.1944:82:377
‑
390)为参考来实施。具体地,通过观察剥离了0.5小时后的贴附部位的皮肤,从(1)红斑和痂皮形成、和(2)浮肿形成的方面,根据以下基准进行评分,对各组计算出平均值。并且,计算实施例的平均得分相对于对应的参考例(不含甾体化合物的贴剂)的平均得分的相对值。即,皮肤刺激的评价记录为基于对应的参考例的贴剂的平均得分的相对值。
[0097]
将实施例或比较例的平均得分以对应的参考例的平均得分为基准为60%以下的情况评价为“a”、超过60%的情况评价为“b”。
[0098]
<draize等人的判定基准>
[0099]
(1)红斑和痂皮形成
[0100]
0:无红斑
[0101]
1:非常轻微的红斑(勉强可识别的程度)
[0102]
2:明显的红斑
[0103]
3:中度或高度的红斑
[0104]
4:高度红斑(beet redness)至轻微痂皮的形成(深部损伤)
[0105]
(2)浮肿形成
[0106]
0:无浮肿
[0107]
1:非常轻微的浮肿(勉强可识别的程度)
[0108]
2:轻度浮肿(可识别因明显的隆起引起的明确边缘的程度)
[0109]
3:中度浮肿(约1mm的隆起)
[0110]
4:高度浮肿(1mm以上的隆起并扩散到暴露范围之外)
[0111]
皮肤萎缩的评价对皮肤刺激的评价后的大鼠(每组2只)实施。对每只动物在异氟烷吸入麻醉下从腹部主动脉采全血。采血后,采取含有各贴附部位的皮肤的表皮切片,将得到的表皮切片用10%福尔马林液固定。切出固定后的表皮切片中的贴附部位的中央部,包埋石蜡后,进行苏木精
‑
曙红染色(he染色),使用显微镜(商品名:bx50,olympus公司制)观察得到的标本。使用图像分析软件(商品名:winroof ver7.3,三谷商事(株)制)对用显微镜拍摄的标本图像进行分析,计测表皮的厚度。对各表皮切片,在5处测定表皮的厚度,计算出平均值。
[0112]
将贴附部位的表皮厚度超过未贴附部位(正常皮肤)的表皮厚度的50%的情况评价为“a”,将50%以下的情况评价为“b”。
[0113]
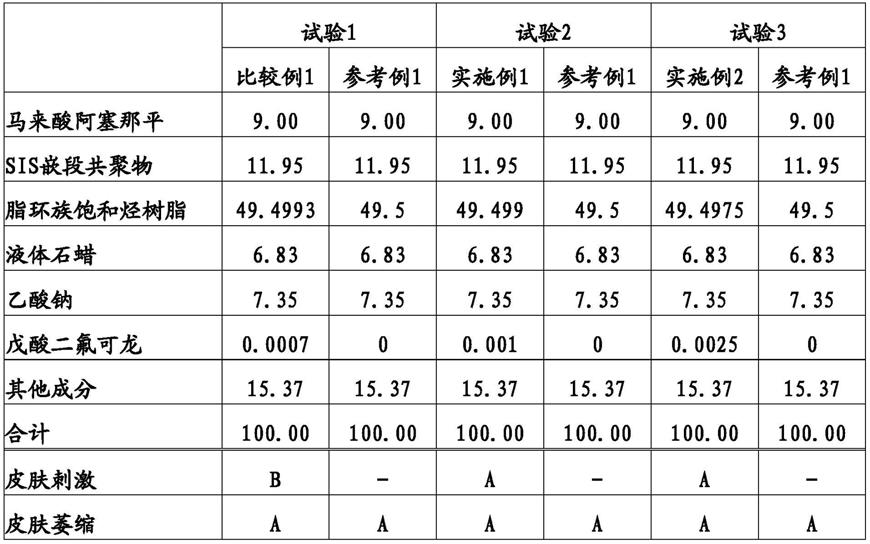
关于含有马来酸阿塞那平的贴剂,将试验1~6的结果示于表1和表2。在比较例1的贴剂中,不能充分抑制由马来酸阿塞那平引起的皮肤刺激。在比较例2的贴剂中,观察到皮肤萎缩。
[0114]
[表1]
[0115]
[0116]
[表2]
[0117][0118]
关于含有罗替戈汀的贴剂,将试验7~10的结果示于表3和表4。在比较例3的贴剂中,观察到皮肤萎缩。
[0119]
[表3]
[0120][0121]
[表4]
[0122][0123]
关于含有罗替戈汀的贴剂,将试验33的结果示于表5。
[0124]
[表5]
[0125][0126]
关于含有利凡斯的明的贴剂,将试验11~16的结果示于表6和表7。丙烯酸系粘合基剂x是不含官能团的丙烯酸系粘合基剂,丙烯酸系粘合基剂y是含有羧基的丙烯酸系粘合基剂。在比较例4的贴剂中,观察到皮肤萎缩。
[0127]
[表6]
[0128][0129]
[表7]
[0130][0131]
关于含有盐酸美金刚的贴剂,将试验17~20的结果示于表8和表9。在比较例5的贴剂中,观察到皮肤萎缩。
[0132]
[表8]
[0133][0134]
[表9]
[0135][0136]
关于含有盐酸美金刚的贴剂,将试验29的结果示于表10。在比较例8和9的贴剂中,皮肤刺激未充分降低。
[0137]
[表10]
[0138][0139]
关于含有苯磺酸氨氯地平的贴剂,将试验21~24的结果示于表11和表12。在比较例6的贴剂中,观察到皮肤萎缩。
[0140]
[表11]
[0141][0142]
[表12]
[0143][0144]
关于含有苯磺酸氨氯地平的贴剂,将试验30的结果示于表13。在实施例22和23的贴剂中,皮肤刺激降低,未观察到皮肤萎缩。
[0145]
[表13]
[0146][0147]
关于含有盐酸罗匹尼罗的贴剂,将试验25~28的结果示于表14和表15。在比较例7的贴剂中,观察到皮肤萎缩。
[0148]
[表14]
[0149][0150]
[表15]
[0151][0152]
关于含有盐酸罗匹尼罗的贴剂,将试验31和32的结果示于表16和表17。在比较例10~12的贴剂中,皮肤刺激未充分降低。
[0153]
[表16]
[0154][0155]
[表17]
[0156]
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1