一种负载布地奈德的丝素蛋白/壳聚糖复合多孔支架的制作方法
本发明属于生物医学材料领域,具体说涉及一种组织工程生物材料,尤其是涉及一种负载布地奈德的丝素蛋白/壳聚糖复合多孔支架。
背景技术:
慢性鼻窦炎(chronicrhinosinusitis,crs)是一种常见的累及鼻腔、鼻窦黏膜的慢性炎症性疾病,我国发病率可达2%~8%,涉及1亿多人口,需要接受手术治疗的约为6.1%,对生活质量、社会经济都有严重影响。所有需要接受手术治疗的患者中约10-20%crs为难治性鼻窦炎,具有术后高复发性,术后3年复发率甚至高达99%。迄今为止,鼻内镜鼻窦手术(endoscopicsinussurgery,ess)被广泛认为是手术治疗crs的标准方法,但crs患者ess的成功与否很大程度上取决于术后瘢痕、水肿和结痂的减少,因为这些会抑制自然纤毛功能和窦道引流。
内镜术后鼻腔鼻窦粘连、窦口狭窄、感染和炎症复发使crs的治疗策略复杂化,而术后鼻腔鼻窦填塞缓释糖皮质激素支架被认为是解决这些问题的合理选择。嗜酸粒细胞浸润可能是炎症严重程度的一种客观指标,嗜酸粒细胞浸润越广泛,鼻窦黏膜越容易出现肿胀和息肉形成。考虑到鼻用激素是治疗鼻腔鼻窦黏膜慢性炎症最有效的药物,糖皮质激素能抑制鼻黏膜中嗜酸性粒细胞的活化,具有较强的抗炎作用,可加快鼻窦黏膜功能恢复。特别针对于难治性鼻窦炎反复发作,国内外公认激素的抗炎治疗是病因和具有1a级循证医学证据的治疗方法。但由于鼻腔解剖结构的因素,鼻用激素喷剂难以喷到额窦、蝶窦等区域,且多数喷鼻药物由于鼻腔黏液纤毛传输系统的作用而无法长期停留在鼻腔鼻窦黏膜表面,另因需长期每日喷鼻导致患者对治疗的依从性明显下降等等都导致药物治疗的疗效显著下降。
可降解鼻窦药物系统带来的支架式缓释激素抗炎新技术,克服了传统给药方式的弊端,给临床实现长期优化手术结局提供了新的可能性。可降解鼻窦药物系统做到了精准、持续可控、安全的给药方式,是革命性的治疗方案,能够将药物释放到鼻窦局部黏膜、支撑窦口,防止窦口闭锁、抑制炎症等多重功效。显著减少患者术后再次接受药物治疗和手术治疗的几率,也相应减少患者支出,降低医患矛盾的发生。因此,包括欧洲鼻窦炎和鼻息肉意见书(theeuropeanpositionpaperonrhinosinusitis,epos)和国际关于鼻窦炎的共识声明(theinternationalconsensusstatementonrhinosinusitis,icar)等都强烈建议在crs手术中使用可降解鼻窦支架以取得良好治疗效果。
但是目前国内外临床使用的可降解鼻窦支架品种单一,且价格昂贵,单价高达3000元每个,严重制约其在临床上的广泛应用。因此,临床上需要更多具有价格低廉且具有同样甚至更好效果的鼻窦支架。理想的药物缓释生物材料应具有生物可吸收性、生物相容性和药物缓释的有效性。研究发现天然生物大分子由于其固有的可再生、无毒、生物相容性、生物降解性、血液循环时间长、靶向性等生化和生物物理特性,越来越受到生物医学的重视。近年来对丝素蛋白、壳聚糖等天然生物大分子的生物学功能的认识和对生物药物载体的研究进展表明,生物药物载体在半衰期、稳定性、安全性和易于制造等方面要优于合成材料载体。这些天然材料来自于自然,容易获取,价格低廉,可成为潜在的用于鼻窦炎术后的载药填充材料。
丝素蛋白是一种不溶性蛋白,由蚕、蜘蛛或其他昆虫分泌大量疏水结构域,可作为无丝素的丝素基生物材料而易于纯化。丝素蛋白因其高适应性、良好的生物相容性和温和的体内异物反应而被用作典型的支架材料。丝素可自组装成机械坚固的材料结构,同时也具有生物降解性和非细胞毒性,丝素蛋白在支架材料的选择中被广泛应用。但是作为单独支架使用时溶失率高、生物性能差,究其原因可能与材料内部空间较小、细胞无法长入有关。壳聚糖作为载药材料最为常见,是一种天然的碱性多糖聚合物,具有抗菌性能,及独特的生物粘附性、生物相容性、生物可降解性、无毒性、低免疫原性以及易加工等特性,能够在生物体中酶解成易被活体吸收、无毒副作用的小分子物质,不会残留在活体内,使其广泛的应用在制药和生物医学领域。壳聚糖分子上氨基和羧基的存在为化学修饰提供很大的可能,通过化学修饰能使壳聚糖产生两亲性,此双亲分子可以形成自组装纳米粒子,纳米粒子可以封装一定量的药物并随着降解而将药物缓慢地释放。壳聚糖单独作为支架材料也存在不足,如干燥时易碎裂、降解较慢等,但可通过与其他材料复合来提高降解速率,降低其脆性。
丝素蛋白与壳聚糖作为组织工程常用的支架材料,将两者混合使用可以互为改性,充分发挥优点,可获取理想的复合,这也是本申请的研究方向。
技术实现要素:
本发明的目的在于克服现有技术的不足之处而提供一种负载布地奈德的壳聚糖/丝素蛋白复合多孔支架,本发明制备的支架具有药物缓释功能,能够提高布地奈德的药物利用度。特别地,本发明制备的支架是一种可用于鼻窦的缓释支架,能够将药物释放到鼻窦局部黏膜、支撑窦口,防止窦口闭锁、抑制炎症等多重功效。
根据本发明一个方面,本发明提供了一种负载布地奈德的丝素蛋白/壳聚糖复合多孔支架,所述复合多孔支架包括多孔支架以及负载于其上的布地奈德;所述多孔支架的主要成分包括丝素蛋白、生物可降解的高聚物。优选地,所述多孔支架的主要成分还包括聚乙二醇。
进一步,生物可降解的高聚物包括聚乳酸、聚羟基乙酸、聚乳酸与聚羟基乙酸共聚物、聚氰代丙烯酸酯、聚己内酯、聚对二氧杂环己酮及其共聚物、聚酸酐、聚原酸酯、聚膦腈、聚羟基丁酸、其他线性脂肪族聚酯、聚氨基酸、甲壳素、壳聚糖或其衍生物、纤维素、聚乙烯醇、聚氧乙烯。
优选地,生物可降解的高聚物是壳聚糖或其衍生物。
更优选地,壳聚糖衍生物是羧化壳聚糖。
进一步,复合多孔支架中聚乙二醇、丝素蛋白与羧化壳聚糖的质量比是2:3:5。
进一步,复合多孔支架中布地奈德与聚乙二醇、丝素蛋白与羧化壳聚糖构成的混合物的质量比是1:1000。
根据本发明另一个方面,本发明还提供了前面所述的复合多孔支架的制备方法,所述制备方法包括如下步骤:
(1)制备壳聚糖溶液;
(2)制备丝素蛋白溶液;
(3)制备聚乙二醇溶液;
(4)将聚乙二醇溶液、丝素蛋白溶液与壳聚糖溶液混合,混合后的溶液中聚乙二醇、丝素蛋白与羧化壳聚糖的质量比为2:3:5;
(5)制备布地奈德溶液,将其缓慢滴加到步骤(4)制备的溶液中,搅拌;
(6)将步骤(5)的混合溶液注入模型中,冷冻干燥。
优选地,壳聚糖溶液的质量浓度为35g/l。
优选地,步骤(1)的具体过程如下:将羧化壳聚糖溶于浓度为1%的冰乙酸,制备成质量浓度为35g/l的壳聚糖溶液。
优选地,步骤(5)搅拌1h。
优选地,布地奈德溶液制备方法如下:称取35mg布地奈德溶于50ml四氢呋喃制备布地奈德溶液。
进一步,步骤(5)的具体过程如下:称取35mg布地奈德(与壳聚糖、聚乙二醇及丝素蛋白复合物质量比1:1000)溶于50ml四氢呋喃,缓慢滴加到步骤(4)获得的混合后的溶液中,持续搅拌1h。
优选地,步骤(2)的具体过程如下:将丝素蛋白20g溶于蒸馏水100ml,制备丝素蛋白溶液。
优选地,步骤(3)的具体过程如下:将聚乙二醇(1500)20g溶于蒸馏水100ml,制备聚乙二醇溶液。
更优选地,所述制备方法还包括去除四氢呋喃的步骤。
去除四氢呋喃的步骤如下所示:在水浴50℃中搅拌使四氢呋喃挥发。
根据本发明另一个方面,本发明提供了前面所述的制备方法获得的负载布地奈德的丝素蛋白/壳聚糖复合多孔支架。
根据本发明另一个方面,本发明提供了前面所述的复合多孔支架在制备组织和创面的填充和修复材料或器械、组织工程材料或器械、药物缓释材料或器械中的应用。
具体地,本发明提供了前面所述的复合多孔支架在制备鼻窦药物缓释系统中的应用。
更具体地,本发明提供了前面所述的复合多孔支架在制备鼻窦药物缓释支架中的应用。
本发明的优点和有益效果:
本发明的复合多孔支架具有丝素蛋白优异的机械性能,并且还具有壳聚糖的止血和吸水能力,其强度高,组织相容性好,吸水性好,可以用来制备组织和创面的填充和修复材料或器械、组织工程材料或器械、药物释放材料或器械。特别地,本发明的复合多孔支架可放入鼻窦作为鼻窦药物缓释系统,发挥药物释放到鼻窦局部黏膜、支撑窦口,防止窦口闭锁、抑制炎症等多重功效。
本发明的制备工艺简单、材料来源广泛,生产效率高,成本低,可应用于工业化大生产。
本发明负载布地奈德的丝素蛋白/壳聚糖复合多孔支架主要通过氢键的结合而形成,当丝素蛋白与壳聚糖混合后,在壳聚糖中活性氨基团会形成氢键,不仅与壳聚糖中本身的羧基团结合,还与丝素蛋白羧基团结合。这使得纯丝素蛋白的水溶性α螺旋结构或盘状结构转变为β-折叠的稳定结构,从而使丝素蛋白形成稳定的、各方面性能良好的复合生物支架。
附图说明
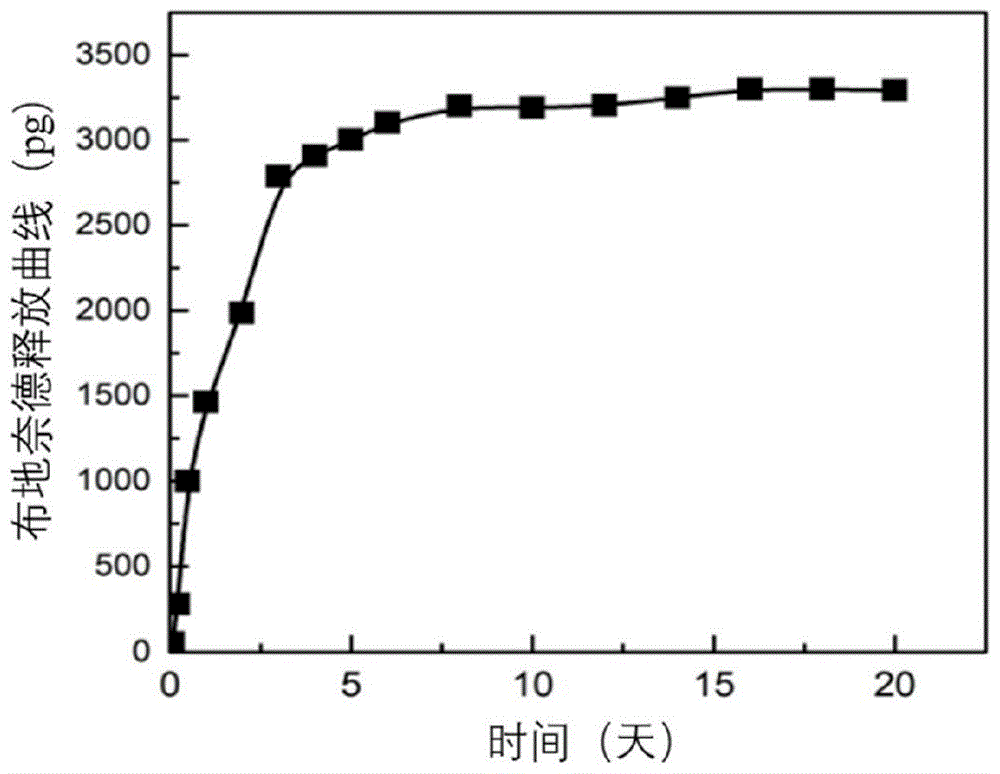
图1显示本发明的载药支架体外缓释布地奈德曲线图;
图2显示药物释放前后本发明的载药支架的形态图,其中a:释放前;b:释放后。
具体实施方式
为更好地说明本发明的目的、技术方案和优点,下面将结合附图和具体实施例对本发明进一步说明。本领域技术人员应当理解,此处所描述的具体实施例仅用以解释本发明,并不用于限定本发明。
下述实施例中所使用的试验方法如无特殊说明,均为常规方法;下述实施例中所使用的材料、试剂等,如无特殊说明,均可从商业途径得到。
实施例1负载布地奈德的复合多孔支架的制备
1、将羧化壳聚糖溶于浓度为1%的冰乙酸,制备成质量浓度为35g/l的壳聚糖溶液;
2、将丝素蛋白20g溶于蒸馏水100ml,制备丝素蛋白溶液;
3、将聚乙二醇(1500)20g溶于蒸馏水100ml,制备聚乙二醇溶液;
4、将上述聚乙二醇溶液、丝素蛋白溶液、壳聚糖溶液混合,混合后的溶液中聚乙二醇、丝素蛋白与羧化壳聚糖的质量比为2:3:5;
5、称取35mg布地奈德(与壳聚糖、聚乙二醇及丝素蛋白复合物质量比1:1000)溶于50ml四氢呋喃,缓慢滴加到步骤4获得的混合后的溶液中,持续搅拌1h;
6、在水浴50℃中搅拌使四氢呋喃挥发;
7、将步骤6获得的混合溶液注入模型中,最后通过冷冻干燥得到负载布地奈德的丝素蛋白/壳聚糖复合多孔支架。
实施例2负载布地奈德的丝素蛋白/壳聚糖复合多孔支架性能测定
1、支架缓释药物实验
取实施例1制备的载药支架(平均141mg)装入透析袋内,透析袋截留分子量为14000。将透析袋置于200ml的释放介质(ph6.2磷酸盐缓冲液/乙醇=80/20),于37.0℃慢速震荡下进行体外释放实验。在固定时间点取出5ml(并用相同体积释放介质替换),采用紫外分光光度法,在248nm波长下测定释放出的布地奈德含量。获得累积药物释放百分比随时间变化的曲线图,以确定复合支架的体外药物释放情况。药物在缓冲溶液中的释放行为如图1所示,药物从载药支架中缓释3d后基本达到平衡,持续缓释大于20天。释放前支架形态和释放后支架形态见图2。
2、体外细胞毒性实验
取实施例1制备的载药支架,加成纤维细胞l929培养液10ml,于37℃培养箱浸提24h,取浸提液备用。在96孔板中每孔接种100μl的细胞悬液。将培养板在37℃,5%co2的条件,在培养箱预培养24h。而后向培养板加入10μl的浸提液,将培养板在培养箱孵育24h。随后向每孔加入10μlcck-8溶液,再将培养板在培养箱内孵育4h。用酶标仪测定孔板在450nm处的吸光度。设置阳性和阴性对照,且96孔板四周不放样品,为空白孔板。样品重复3次实验。结果:细胞毒性等级为1级。
最后所应当说明的是,以上实施例仅用以说明本发明的技术方案而非对本发明保护范围的限制,尽管参照较佳实施例对本发明作了详细说明,本领域的普通技术人员应当理解,可以对本发明的技术方案进行修改或者等同替换,而不脱离本发明技术方案的实质和范围。
- 还没有人留言评论。精彩留言会获得点赞!