具有降血糖血脂功效的茶色素胶囊及其制备方法与流程
1.本发明涉及中医药领域,具体涉及一种具有降血糖血脂功效的茶色素胶囊及其制备方法。
背景技术:
2.糖尿病是一种以糖代谢紊乱为主要特征的内分泌代谢综合疾病,是胰岛素相对或绝对不足,或利用缺陷而引起的,表现为高血糖和糖尿,多伴有眼、肾、神经、皮肤、血管和心脏病等组织、器官的慢性并发症,糖尿病属中医学“消渴”“消癣”等范畴。中国古代对该病早有认识,一般称为消渴病,并以消渴、消痒、消中等不同的名称保留在古代文献中。
3.糖尿病的病因和发病机制非常复杂,现代医学至今尚缺乏针对病因的有效治疗手段。传统的治疗方法包括药物治疗、健康教育、饮食控制、运动疗法、自我监测五大措施,其中药物治疗是糖尿病治疗中的重要手段。
4.西药治疗糖尿病具有降血糖作用强、起效快的特点,但往往缺乏整体的协调性,且具有明显的副作用,不利于患者的长期使用。而中药通过多途径多靶点降低血糖、减轻糖尿病对机体损害及控制、延缓糖尿病并发症,且中药有效成分具有疗效稳定、毒性小、不良反应少、服用方便等优点,尤其适用于防治糖尿病并发症。因此,中药在糖尿病及其并发症的防治方面,有着不可替代的优势。
5.中国发明专利cn102727743b公开了一种具有降血糖、血脂功效的茶色素胶囊及其制备方法,利用黄精、荞麦、桑椹、茶色素、吡啶甲酸铬、糊精、硬脂酸镁混合,先将黄精、荞麦、桑椹净药材置于罐中,加水,加热,过滤,滤渣再加水煎煮,得稠膏,将茶色素过筛,取吡啶甲酸铭和茶色素混合,将混合粉装入胶囊中即得。该发明采用黄精、荞麦、桑椹为原料,提取、浓缩、干燥,添加茶色素、吡啶甲酸铬和适宜的辅料,从中医理论入手择方,有降血糖和血脂的功能。但是该方法制得的茶色素胶囊降血糖与化学药相比,效果有待进一步提高,且其药材的利用率低,未发挥其最大的药效。
技术实现要素:
6.针对现有技术的不足,本发明提供一种具有降血糖、降血脂功效的茶色素胶囊及其制备方法,其疗效显著,药材利用率高,副作用小。
7.本发明的目的是通过以下技术方案实现的:
8.一种具有降血糖血脂功效的茶色素胶囊,按照重量份数计,所述茶色素胶囊的原料包括如下组分:茶色素5
‑
10份、黄精10
‑
20份、荞麦10
‑
20份、桑葚5
‑
10份、吡啶甲酸铬0.001
‑
0.005份、土大黄20
‑
30份、白子菜25
‑
35份和乳酸杆菌。
9.优选地,所述茶色素胶囊的原料包括如下组分:茶色素8
‑
10份、黄精15
‑
20份、荞麦10
‑
15份、桑葚8
‑
10份、吡啶甲酸铬0.001
‑
0.002份、土大黄20
‑
25份、白子菜25
‑
30份和乳酸杆菌。
10.优选地,所述乳酸杆菌为质量比1:5
‑
10的嗜酸乳杆菌和干酪乳杆菌合的混合物。
11.优选地,所述茶色素胶囊还包括药学上可接受的辅料。
12.优选地,药学上可接受的辅料为糊精和硬脂酸镁。
13.本发明的再一目的是提供上述茶色素胶囊的制备方法,包括如下步骤:
14.(1)将黄精和桑葚加水提取,过滤,浓缩得浓缩液,加入乙醇醇沉得上清液和沉淀物,将沉淀物冷冻干燥得多糖;将上清液过聚酰胺柱,用乙醇溶液和丙酮溶液依次洗脱,合并得洗脱液;浓缩干燥得干膏粉;
15.(2)将荞麦、白子菜和土大黄加6
‑
8倍量的水煎煮,过滤,浓缩得浓缩液,将浓缩液115℃下灭菌40分钟;
16.(3)将乳酸杆菌接种于液体培养基中,在35
‑
38℃下厌氧发酵24
‑
72h,得乳酸杆菌液;将体积比为0.5
‑
1.0%乳酸杆菌的菌液加入到步骤(2)中的浓缩液中,在35
‑
38℃下厌氧发酵30
‑
40h,得发酵液,冷冻干燥得冻干粉;
17.(4)将多糖、干膏粉、冻干粉、茶色素、吡啶甲酸铬和药学上可接受的辅料混合均匀,装入胶囊即得。
18.优选地,步骤(1)中所述加入水的体积与黄精和桑葚的总质量比为5
‑
10:1;所述提取的次数为1
‑
3次,每次提取0.5
‑
1.5h。
19.优选地,步骤(1)中所述醇沉为分级沉淀,具体操作为:将浓缩液中加入乙醇至浓缩液终浓度为25%乙醇,醇沉得沉淀物1和上清液1,将上清液1再加入乙醇至终浓度为45%乙醇,醇沉得沉淀物2和上清液2,将上清液2再加入95%乙醇至终浓度为75%乙醇,醇沉得沉淀物3和上清液3,合并沉淀物1、沉淀物2和沉淀物3为沉淀物,上清液3为上清液。
20.优选地,步骤(1)中所述洗脱为用1
‑
2倍柱体积的40
‑
50%乙醇、3
‑
5倍柱体积的75
‑
85%乙醇和5
‑
8倍柱体积的45
‑
55%丙酮水溶液依次洗脱,所述洗脱液以0.5
‑
1ml/min的流速流出。
21.优选地,步骤(2)中,所述煎煮的的次数为1
‑
3次,每次提取时间为1
‑
2h;所述浓缩为浓缩至原滤液体积的1/3
‑
1/5。
22.优选地,步步骤(3)中所述液体培养的组分包括胨化乳、酵母浸粉、磷酸二氢钾、葡萄糖、吐温
‑
80和琼脂。
23.本发明还有一个目的是提供上述茶色素胶囊在制备降血糖血脂产品中的应用。
24.本发明的有益效果:
25.(1)本发明白子菜和土大黄与其他药味相配伍,对降血糖、降血脂作用显著;
26.(2)本发明采用一定浓度的乙醇进行分级沉淀,所得到的多糖成分浓度高,可以有效提高组合物的降糖效果;
27.(3)本发明进一步通过将荞麦、土大黄和白子菜混合提取,可相互作用,促进酸碱等药效成分的溶出,极大地提高了活性成分的浓度,增强了降糖效果;本发明采用特定组分的乳酸杆菌,本身可通过协同作用抑制肠道内α
‑
葡萄糖苷酶等酶的作用,来调节体内血糖的浓度,还可以通过在提取液中发酵,促进提取液新活性产物的生成及和活性成分的转化,使得药效作用更强。
具体实施方式
28.下面结合实施例对本发明技术方案做进一步阐述。
29.以下实施例中各原料均为市售常规材料,其中乳酸杆菌为已有菌株,可自中国普通微生物菌种保藏管理中心(cgmcc)或中国典型培养物保藏中心(cctcc)采购。
30.实施例1
31.本实施例茶色素胶囊的原料包括如下组分:茶色素5份、黄精10份、荞麦10份、桑葚5份、吡啶甲酸铬0.001份、土大黄20份、白子菜25份,乳酸杆菌为质量比1:5的嗜酸乳杆菌和干酪乳杆菌的混合物;辅料为糊精和硬脂酸镁。
32.本实施例的制备方法如下:
33.(1)将黄精和桑葚加药材质量5倍量的水溶液提取3次,每次提取0.5h,过滤,浓缩至原滤液体积的1/3得浓缩液,将浓缩液中加入乙醇至浓缩液终浓度为25%乙醇,醇沉得沉淀物1和上清液1,将上清液1再加入乙醇至终浓度为45%乙醇,醇沉得沉淀物2和上清液2,将上清液2再加入95%乙醇至终浓度为75%乙醇,醇沉得沉淀物3和上清液3,合并沉淀物1、沉淀物2和沉淀物3为沉淀物,上清液3为上清液。将沉淀物冷冻干燥得多糖;将上清液过聚酰胺柱,用1倍柱体积的50%乙醇、3倍柱体积的85%乙醇和5倍柱体积的45%丙酮水溶液依次洗脱,控制洗脱液的流速为0.5ml/min,合并得洗脱液,浓缩干燥得干膏粉;
34.(2)将荞麦、白子菜和土大黄加6倍量水煎煮3次,每次煎煮1h,过滤,浓缩至原滤液体积的1/5得浓缩液,115℃下灭菌40分钟;
35.(3)将乳酸杆菌接种于液体培养基中,在36℃下厌氧发酵24h,得乳酸杆菌液;将体积比为0.5%乳酸杆菌菌液加入到步骤(2)中的浓缩液中,在36℃下厌氧发酵40h,得发酵液,冷冻干燥得冻干粉;其中液体培养基是乳酸杆菌琼脂培养基加水制备而成;具体方法为称取乳酸杆菌琼脂培养基47.5g,加热溶解于1000ml蒸馏水中,分装,121℃高压灭菌15分钟,冷至50℃左右时,倾入无菌平皿即可。乳酸杆菌琼脂培养基购自青岛海博生物有限公司。
36.(4)将多糖、干膏粉、冻干粉、茶色素和吡啶甲酸铬混合为混合粉,再加入30%混合粉的糊精和0.02%混合粉的硬脂酸镁,混合均匀,装入胶囊即得。
37.实施例2
38.本实施例茶色素胶囊的原料包括如下组分:茶色素10份、黄精20份、荞麦20份、桑葚10份、吡啶甲酸铬0.005份、土大黄30份、白子菜35份,乳酸杆菌为质量比1:8的嗜酸乳杆菌和干酪乳杆菌的混合物;辅料为糊精和硬脂酸镁。
39.本实施例的制备方法如下:
40.(1)将黄精和桑葚加药材质量10倍量的水溶液提取1.5h,过滤,浓缩至原滤液体积的1/3得浓缩液,将浓缩液中加入乙醇至浓缩液终浓度为25%乙醇,醇沉得沉淀物1和上清液1,将上清液1再加入乙醇至终浓度为45%乙醇,醇沉得沉淀物2和上清液2,将上清液2再加入95%乙醇至终浓度为75%乙醇,醇沉得沉淀物3和上清液3,合并沉淀物1、沉淀物2和沉淀物3为沉淀物,上清液3为上清液。将沉淀物冷冻干燥得多糖;将上清液过聚酰胺柱,用2倍柱体积的40%乙醇、5倍柱体积的75%乙醇和8倍柱体积的50%丙酮水溶液依次洗脱,控制洗脱液的流速为1.0ml/min,合并得洗脱液,浓缩干燥得干膏粉;
41.(2)将荞麦、白子菜和土大黄加8倍量水煎煮2h,过滤,浓缩至原滤液体积的1/5得浓缩液,115℃下灭菌40分钟;
42.(3)将乳酸杆菌接种于液体培养基中,在36℃下厌氧发酵72h,得乳酸杆菌液;将体
积比为1.0%乳酸杆菌菌液加入到步骤(2)中的浓缩液中,在36℃下厌氧发酵30h,得发酵液,冷冻干燥得冻干粉;其中液体培养基是乳酸杆菌琼脂培养基加水制备而成;具体方法为称取乳酸杆菌琼脂培养基47.5g,加热溶解于1000ml蒸馏水中,分装,121℃高压灭菌15分钟,冷至50℃左右时,倾入无菌平皿即可。乳酸杆菌琼脂培养基购自青岛海博生物有限公司。
43.(4)将多糖、干膏粉、冻干粉、茶色素和吡啶甲酸铬混合为混合粉,再加入30%混合粉质量的糊精和0.02%混合粉的硬脂酸镁,混合均匀,装入胶囊即得。
44.实施例3
45.本实施例茶色素胶囊的原料包括如下组分:茶色素8份、黄精15份、荞麦15份、桑葚8份、吡啶甲酸铬0.002份、土大黄25份、白子菜30份,乳酸杆菌为质量比1:10的嗜酸乳杆菌和干酪乳杆菌的混合物;辅料为糊精和硬脂酸镁。
46.本实施例的制备方法如下:
47.(1)将黄精和桑葚加药材质量8倍量的水溶液提取2次,每次提取1h,过滤,浓缩至原滤液体积的1/3得浓缩液,将浓缩液中加入乙醇至浓缩液终浓度为25%乙醇,醇沉得沉淀物1和上清液1,将上清液1再加入乙醇至终浓度为45%乙醇,醇沉得沉淀物2和上清液2,将上清液2再加入95%乙醇至终浓度为75%乙醇,醇沉得沉淀物3和上清液3,合并沉淀物1、沉淀物2和沉淀物3为沉淀物,上清液3为上清液。将沉淀物冷冻干燥得多糖;将上清液过聚酰胺柱,用1倍柱体积的50%乙醇、5倍柱体积的85%乙醇和5倍柱体积的55%丙酮水溶液依次洗脱,控制洗脱液的流速为0.5ml/min,合并得洗脱液,浓缩干燥得干膏粉;
48.(2)将荞麦、白子菜和土大黄加6倍量水煎煮2次,每次煎煮1h,过滤,浓缩至原滤液体积的1/3得浓缩液,115℃下灭菌40分钟;
49.(3)将乳酸杆菌接种于液体培养基中,在37℃下厌氧发酵30h,得乳酸杆菌液;将体积比为0.8%乳酸杆菌菌液加入到步骤(2)中的浓缩液中,在37℃下厌氧发酵35h,得发酵液,冷冻干燥得冻干粉;其中液体培养基是乳酸杆菌琼脂培养基加水制备而成;具体方法为称取乳酸杆菌琼脂培养基47.5g,加热溶解于1000ml蒸馏水中,分装,121℃高压灭菌15分钟,冷至50℃左右时,倾入无菌平皿即可。乳酸杆菌琼脂培养基购自青岛海博生物有限公司。
50.(4)将多糖、干膏粉、冻干粉、茶色素和吡啶甲酸铬混合为混合粉,再加入30%混合粉的糊精和0.02%混合粉质量的硬脂酸镁,混合均匀,装入胶囊即得。
51.对比例1
52.本对比例与实施例3的区别是将黄精去掉,土大黄的份数调整为40份,其余与实施例3保持一致。具体为:
53.本对比例茶色素胶囊的原料包括如下组分:茶色素8份、荞麦15份、桑葚8份、吡啶甲酸铬0.002份、土大黄40份、白子菜30份,乳酸杆菌为质量比1:10的嗜酸乳杆菌和干酪乳杆菌的混合物;辅料为糊精和硬脂酸镁。
54.本对比例的制备方法如下:
55.(1)将桑葚加药材质量8倍量的水溶液提取2次,每次提取1h,过滤,浓缩至原滤液体积的1/3得浓缩液,将浓缩液中加入乙醇至浓缩液终浓度为25%乙醇,醇沉得沉淀物1和上清液1,将上清液1再加入乙醇至终浓度为45%乙醇,醇沉得沉淀物2和上清液2,将上清液
2再加入95%乙醇至终浓度为75%乙醇,醇沉得沉淀物3和上清液3,合并沉淀物1、沉淀物2和沉淀物3为沉淀物,上清液3为上清液。将沉淀物冷冻干燥得多糖;将上清液过聚酰胺柱,用1倍柱体积的50%乙醇、5倍柱体积的85%乙醇和5倍柱体积的70%丙酮水溶液依次洗脱,控制洗脱液的流速为0.5ml/min,合并得洗脱液,浓缩干燥得干膏粉;
56.(2)将荞麦、白子菜和土大黄加6倍量水煎煮2次,每次煎煮1h,过滤,浓缩至原滤液体积的1/3得浓缩液,115℃下灭菌40分钟;
57.(3)将乳酸杆菌接种于液体培养基中,在37℃下厌氧发酵30h,得乳酸杆菌液;将体积比为0.8%乳酸杆菌菌液加入到步骤(2)中的浓缩液中,在37℃下厌氧发酵35h,得发酵液,冷冻干燥得冻干粉;其中液体培养基是乳酸杆菌琼脂培养基加水制备而成;具体方法为称取乳酸杆菌琼脂培养基47.5g,加热溶解于1000ml蒸馏水中,分装,121℃高压灭菌15分钟,冷至50℃左右时,倾入无菌平皿即可。乳酸杆菌琼脂培养基购自青岛海博生物有限公司。
58.(4)将多糖、干膏粉、冻干粉、茶色素和吡啶甲酸铬混合为混合粉,再加入30%混合粉的糊精和0.02%混合粉质量的硬脂酸镁,混合均匀,装入胶囊即得。
59.对比例2
60.本对比例与实施例3的区别是将不加入土大黄,黄精的份数调整为40份,其余与实施例3保持一致。具体为:
61.本对比例茶色素胶囊的原料包括如下组分:色素8份、荞麦15份、桑葚8份、吡啶甲酸铬0.002份、黄精40份、白子菜30份,乳酸杆菌为质量比1:10的嗜酸乳杆菌和干酪乳杆菌的混合物;辅料为糊精和硬脂酸镁。
62.本对比例的制备方法如下:
63.(1)将黄精和桑葚加药材质量8倍量的水溶液提取2次,每次提取1h,过滤,浓缩至原滤液体积的1/3得浓缩液,将浓缩液中加入乙醇至浓缩液终浓度为25%乙醇,醇沉得沉淀物1和上清液1,将上清液1再加入乙醇至终浓度为45%乙醇,醇沉得沉淀物2和上清液2,将上清液2再加入95%乙醇至终浓度为75%乙醇,醇沉得沉淀物3和上清液3,合并沉淀物1、沉淀物2和沉淀物3为沉淀物,上清液3为上清液。将沉淀物冷冻干燥得多糖;将上清液过聚酰胺柱,用1倍柱体积的50%乙醇、5倍柱体积的85%乙醇和5倍柱体积的70%丙酮水溶液依次洗脱,控制洗脱液的流速为0.5ml/min,合并得洗脱液,浓缩干燥得干膏粉;
64.(2)将荞麦和白子菜加6倍量水煎煮2次,每次煎煮1h,过滤,浓缩至原滤液体积的1/3得浓缩液,115℃下灭菌40分钟;
65.(3)将乳酸杆菌接种于液体培养基中,在37℃下厌氧发酵30h,得乳酸杆菌液;将体积比为0.8%乳酸杆菌菌液加入到步骤(2)中的浓缩液中,在37℃下厌氧发酵35h,得发酵液,冷冻干燥得冻干粉;其中液体培养基是乳酸杆菌琼脂培养基加水制备而成;具体方法为称取乳酸杆菌琼脂培养基47.5g,加热溶解于1000ml蒸馏水中,分装,121℃高压灭菌15分钟,冷至50℃左右时,倾入无菌平皿即可。乳酸杆菌琼脂培养基购自青岛海博生物有限公司。
66.(4)将多糖、干膏粉、冻干粉、茶色素和吡啶甲酸铬混合为混合粉,再加入30%混合粉的糊精和0.02%混合粉质量的硬脂酸镁,混合均匀,装入胶囊即得。
67.对比例3
68.本对比例与实施例3的区别是制备方法不同。具体制备方法如下:
69.(1)将黄精和桑葚加药材质量8倍量的水溶液提取2次,每次提取1h,过滤,浓缩至原滤液体积的1/3得浓缩液,将浓缩液中加入乙醇至浓缩液终浓度为35%乙醇,醇沉得沉淀物1和上清液1,将上清液1再加入乙醇至终浓度为55%乙醇,醇沉得沉淀物2和上清液2,将上清液2再加入95%乙醇至终浓度为65%乙醇,醇沉得沉淀物3和上清液3,合并沉淀物1、沉淀物2和沉淀物3为沉淀物,上清液3为上清液。将沉淀物冷冻干燥得多糖;将上清液过聚酰胺柱,用3倍柱体积的20%乙醇、8倍柱体积的45%乙醇和3倍柱体积的90%乙醇水溶液依次洗脱,控制洗脱液的流速为1.5ml/min,合并得洗脱液,浓缩干燥得干膏粉;
70.(2)将荞麦加6倍量水煎煮2次,每次煎煮1h,过滤,得滤液2;将白子菜和土大黄加6倍量水煎煮2次,每次煎煮1h,过滤,得滤液3,合并滤液1和2,浓缩至原滤液体积的1/3得浓缩液,115℃下灭菌40分钟;
71.(3)将乳酸杆菌接种于液体培养基中,在37℃下厌氧发酵30h,得乳酸杆菌液;将体积比为0.8%乳酸杆菌菌液加入到步骤(2)中的浓缩液中,在37℃下厌氧发酵35h,得发酵液,冷冻干燥得冻干粉;其中液体培养基是乳酸杆菌琼脂培养基加水制备而成;具体方法为称取乳酸杆菌琼脂培养基47.5g,加热溶解于1000ml蒸馏水中,分装,121℃高压灭菌15分钟,冷至50℃左右时,倾入无菌平皿即可。乳酸杆菌琼脂培养基购自青岛海博生物有限公司。
72.(4)将多糖、干膏粉、冻干粉、茶色素和吡啶甲酸铬混合为混合粉,再加入30%混合粉的糊精和0.02%混合粉质量的硬脂酸镁,混合均匀,装入胶囊即得。
73.对比例4
74.本对比例与实施例3的区别是乳酸杆菌为质量比1:1的嗜酸乳杆菌和干酪乳杆菌的混合物;制备方法中步骤(3)发酵时间不同。具体如下:
75.茶色素胶囊的原料包括如下组分:黄精15份、荞麦15份、桑葚8份、茶色素3份、吡啶甲酸铬0.002份、土大黄25份、白子菜30份,乳酸杆菌为质量比1:1的嗜酸乳杆菌和干酪乳杆菌的混合物;辅料为糊精和硬脂酸镁。
76.制备方法如下:
77.(1)将黄精和桑葚加药材质量8倍量的水溶液提取2次,每次提取1h,过滤,浓缩至原滤液体积的1/3得浓缩液,将浓缩液中加入乙醇至浓缩液终浓度为25%乙醇,醇沉得沉淀物1和上清液1,将上清液1再加入乙醇至终浓度为45%乙醇,醇沉得沉淀物2和上清液2,将上清液2再加入95%乙醇至终浓度为75%乙醇,醇沉得沉淀物3和上清液3,合并沉淀物1、沉淀物2和沉淀物3为沉淀物,上清液3为上清液。将沉淀物冷冻干燥得多糖;将上清液过聚酰胺柱,用1倍柱体积的50%乙醇、5倍柱体积的85%乙醇和5倍柱体积的70%丙酮水溶液依次洗脱,控制洗脱液的流速为0.5ml/min,合并得洗脱液,浓缩干燥得干膏粉;
78.(2)将荞麦、白子菜和土大黄加6倍量水煎煮2次,每次煎煮1h,过滤,浓缩至原滤液体积的1/3得浓缩液,115℃下灭菌40分钟;
79.(3)将乳酸杆菌接种于液体培养基中,在37℃下厌氧发酵25h,得乳酸杆菌液;将体积比为0.8%乳酸杆菌菌液加入到步骤(2)中的浓缩液中,在37℃下厌氧发酵45h,得发酵液,冷冻干燥得冻干粉;其中液体培养基是乳酸杆菌琼脂培养基加水制备而成;具体方法为称取乳酸杆菌琼脂培养基47.5g,加热溶解于1000ml蒸馏水中,分装,121℃高压灭菌15分
钟,冷至50℃左右时,倾入无菌平皿即可。乳酸杆菌琼脂培养基购自青岛海博生物有限公司。
80.(4)将多糖、干膏粉、冻干粉、茶色素和吡啶甲酸铬混合为混合粉,再加入30%混合粉的糊精和0.02%混合粉质量的硬脂酸镁,混合均匀,装入胶囊即得。
81.效果例1本发明茶色素胶囊对高血糖小鼠的治疗作用
82.1.1目的:探讨本发明茶色素胶囊对高血糖小鼠的降血糖及降血脂作用效果的影响。
83.1.2药物:实施例1
‑
3与对比例1
‑
4制备得到的茶色素胶囊。
84.1.3动物分组
85.健康雄性昆明小鼠,清洁级,均购于北京维通利华实验动物技术有限公司,体重20
±
5g;标准饲料、自来水喂养于恒温25℃、恒湿55
±
5%动物实验室一周。
86.按照随机数表法随机分组,分别为空白对照组、模型对照组、阳性对照组、实施例1至3组、对比例1至4组。每组10只。
87.1.4高血糖小鼠动物模型的制备及给药
88.将选取的80只小鼠禁食12h,然后按200mg/kg腹腔注射2%四氧嘧啶,72h后测定血糖,若小鼠空腹血糖浓度>16.0mmol/l,判断制备高血糖小鼠动物模型造模成功。
89.给药方式:
90.实施例1至3组、对比例1至4组灌胃给药,每天1次,连续给药7天,给药0.5g/kg,给药体积为0.1ml/10g。空白对照组、模型对照组分别给予等量的蒸馏水;阳性对照组给予盐酸二甲双胍混悬液130mg/kg,给药2周。
91.1.5试验方法
92.各组动物给药2周后,每组小鼠禁食不禁水12h后,剪尾取血测定血糖值。并取血测定血清中总甘油三酯、总胆固醇、低密度脂蛋白的水平。实验数据均用spss13.0软件进行统计学处理,血糖值以均数
±
标准差表示,组间比较采用t检验。
93.1.5结果与分析
94.(1)本发明茶色素胶囊的降血糖作用结果见表1。
95.表1茶色素胶囊降血糖作用
96.组别小鼠数量(只)给药前(mmol/l)给药后(mmol/l)空白组106.84
±
1.76
a
7.03
±
1.99
a
模型组1023.86
±
2.35
b
23.79
±
1.83
b
阳性组1024.17
±
2.83
b
12.29
±
2.05
d
实施例11024.03
±
1.56
b
10.34
±
2.65
c
实施例21023.89
±
1.18
b
10.27
±
1.58
c
实施例31023.73
±
1.85
b
10.21
±
1.71
c
对比例11024.06
±
1.02
b
12.35
±
2.38
d
对比例21023.92
±
1.96
b
13.36
±
1.79
d
对比例3102409
±
1.69
b
12.68
±
1.93
d
对比例41024.16
±
1.04
b
11.84
±
1.07
d
97.注:同一列不同字母表示相应组之间具有统计学差异,p<0.05。
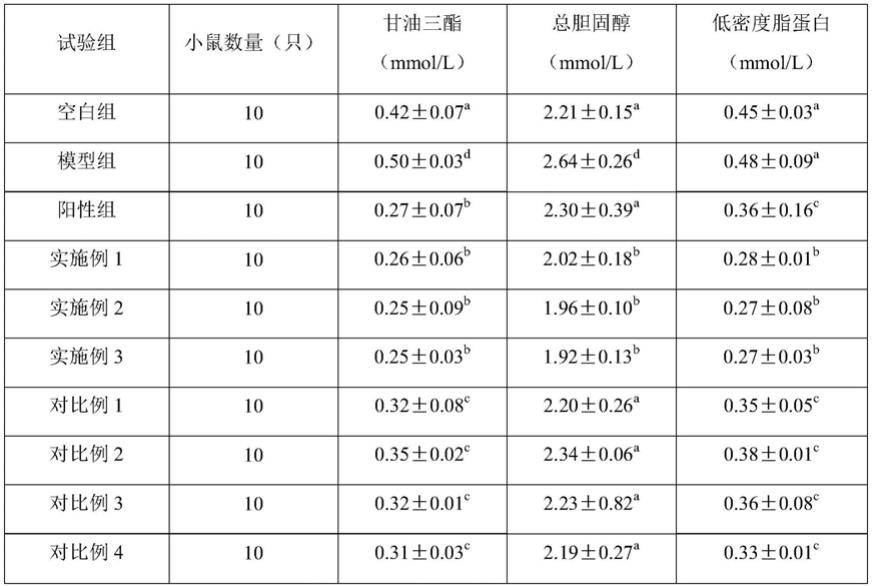
98.(2)本发明茶色素胶囊改善血脂代谢的实验结果见表2。
99.表2茶色素胶囊改善血脂代谢的作用
[0100][0101]
注:同一列不同字母表示相应组之间具有统计学差异,p<0.05。
[0102]
由表1中模型组可知,模型小鼠给药前血糖值为23.86
±
2.35mmol/l,相比空白组,血糖明显升高,且二者之间具有显著的统计学差异,表明造模成功。各组模型组小鼠在给药前血糖无统计学差异。给药2周后,阳性组、实施例1
‑
3组与对比例1
‑
4组、模型组间的血糖值具有显著的统计学差异(p<0.05),由表2可知,本发明茶色素胶囊在显著降低小鼠血糖的同时,还具有改善糖尿病小鼠血脂的作用,本发明茶色素胶囊在医药、保健品领域具有良好的应用前景。
[0103]
上述详细说明是针对本发明其中之一可行实施例的具体说明,该实施例并非用以限制本发明的专利范围,凡未脱离本发明所为的等效实施或变更,均应包含于本发明技术方案的范围内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1