白术内酯Ⅰ在制备妊娠合并糖尿病胚胎发育保护药物中的应用
白术内酯ⅰ在制备妊娠合并糖尿病胚胎发育保护药物中的应用
技术领域
1.本发明属于中药领域,具体涉及白术内酯ⅰ在制备妊娠合并糖尿病胚胎发育保护药物中的应用。
背景技术:
2.近年来,随着人们生活水平的提高,饮食习惯及生活方式的改变,妊娠合并糖尿病的发病率在全球都呈逐年上升的趋势,成为各国的公共健康问题。葡萄糖可以通过胎盘屏障,妊娠合并糖尿病的胚胎实质是处于一个高葡萄糖的环境。
3.妊娠合并糖尿病的发生率在全球肥胖病流行的背景下逐年增长。现代诊断标准细化以及更新,将进一步增加这种疾病的患病率。近年来,中国随着三胎政策开放后,孕妇及高龄产妇的数量在逐渐增长,13%的孕妇患有妊娠糖尿病,而高龄产妇得妊娠合并糖尿病的几率更高。在妊娠期间,由于母体的葡萄糖可以穿过胎盘,在母体高血糖的情况下,过量的血糖通过胎盘传给胚胎,将导致胚胎胰岛素的分泌增加,导致胚胎循环出现高胰岛素血和高血糖。此外,子宫内高血糖的暴露可能对胚胎的血管基因表达造成不良的影响,进而导致了胚胎的血管功能发生变化,使子代患有心血管疾病的风险明显增高。调查显示:糖尿病孕产妇的主要先天性异常患病率为46/1000例(1型糖尿病为48/1000例;2型糖尿病为43/1000例)。这种增加是由神经系统和心血管系统异常引起的,特别是神经管缺陷(4.2倍)和先天性心脏病(3.4倍),在产前诊断出65%的后代异常。
4.妊娠糖尿病患者是一类特殊的人群,主要治疗措施是胰岛素治疗来降低体内血糖浓度。由于胚胎的肝脏发育不完善,药物及降解产物排泄延,且排除的部分代谢产物,可因“羊水肠道循环”被胚胎重吸收,容易在体内蓄积,影响胚胎组织器官的发育。在妊娠期间,即使对母体无严重的不良反应的药品也可能对胚胎产生毒性作用。当前治疗糖尿病的口服药物包括二甲双胍,甲糖宁及氯磺丙脲等都明确说明了孕妇不宜使用。
5.祖国医学中,服用中药保护胚胎正常生长发育,防止流产、早产、畸形已有悠久的历史,积累了丰富的临床经验,在临床治疗方面突出了自身的优势。白术为传统安胎名药,药源广泛,价格低廉,无明显毒副作用。白术适合妊娠期服用,妊娠糖尿病常用的中药复方有七味白术散,四君子汤加减方等等,临床研究表明这些复方可以有效控制血糖,并减少母体并发症和后代先天性疾病的发生情况,但是以上均为复方,难以清楚具体有效成分。
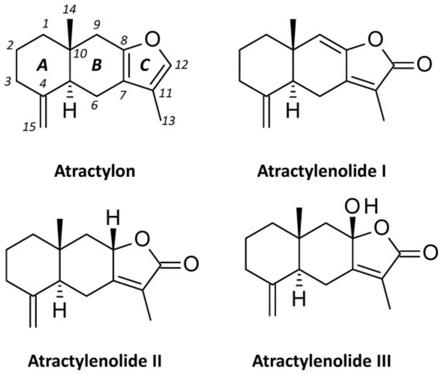
6.白术内酯i、ii和iii和苍术酮的化学式如图1所示,苍术酮的a,b,c是它们具有共同的三环结构。白术内酯ⅲ与白术内酯ⅱ的不同之处在于8位置存在羟基,而白术内酯ⅰ在b环的8
‑
9位置具有双键。近年来发现白术内酯具有抵抗炎症,抗氧自由基以及抗癌的作用[8],但不同的白术内酯分型作用不完全一样,白术内酯i对孕妇及哺乳期妇女用药并不明确。白术内酯的专利多集中在提取技术、抗肿瘤和免疫调节上,例如:中国专利文献cn103254164a(申请号:201310194450.4)公开了一种白术内酯i的制备方法,中国专利文献cn102218056a(申请号:201110098273.0)公开了白术内酯i在防治免疫性肝损伤药物中的
应用,中国专利文献cn 108478557a(申请号:201810119529.3)公开了白术内酯ⅰ在制备抗肝癌药物中的应用。
[0007]
白术内酯i、ii、iii的作用不尽相同,其应用也各有差异,白术内酯i具有较强的增强唾液淀粉酶活性,促进肠管吸收,调节肠道功能,在妊娠合并糖尿病患者胚胎心脏发育保护方面的应用尚未开发。
[0008]
当前治疗妊娠糖尿病主要采用胰岛素治疗,但是价格相对高,有的患者会存在过敏反应,会导致新生儿低血糖症。口服降糖药包括二甲双胍,甲糖宁及氯磺丙脲等都明确说明了孕妇不宜使用。因此当前并无安全的口服药物保护妊娠糖尿病胚胎的发育。
技术实现要素:
[0009]
针对现有技术的不足之处,本发明提供了白术内酯ⅰ在制备妊娠合并糖尿病胚胎发育保护药物中的应用。
[0010]
本发明的目的是提供一种白术内酯ⅰ的新用途,白术虽然为传统安胎药,但是提取物白术内酯ⅰ对于妊娠期糖尿病胚胎发育的保护作用尚不明确。本发明通过大量实验发现一定浓度的白术内酯ⅰ不会导致胚胎发育畸形,并且能够有效缓解高糖环境诱导的胚胎心血管系统和神经系统发育不良现象,提供白术内酯ⅰ及其作为先导化合物合成出来的修饰物可以保护妊娠合并糖尿并胚胎心血管系统和神经系统发育的新用途。
[0011]
应用鸡胚建立妊娠糖尿病胚胎的模型(cell cycle:14(5):772
‑
783.2015),为本发明提供了一个良好的研究保护妊娠糖尿病胚胎发育药物的在体模型。
[0012]
本发明中的“起效浓度”是指药品成分被体内脏腑器吸收后,在作用组织产生作用的浓度。
[0013]
本发明的技术方案
[0014]
白术内酯ⅰ作为有效成分在制备预防和/或治疗妊娠合并糖尿病引起胚胎发育疾病的药物中的应用。
[0015]
根据本发明优选的,白术内酯ⅰ作为有效成分在制备妊娠合并糖尿病胚胎心脏发育保护药物中的应用。
[0016]
根据本发明优选的,白术内酯ⅰ作为有效成分在制备预防和/或治疗妊娠合并糖尿病导致的胚胎死亡和/或胚胎发育畸形药物中的应用。
[0017]
根据本发明优选的,白术内酯ⅰ作为有效成分在制备预防和/或治疗妊娠合并糖尿病导致的胚胎心血管系统发育不良药物中的应用。
[0018]
进一步优选的,所述胚胎心血管系统发育不良包括:胚胎血管发育不良、胚胎心管畸形、胚胎心肌细胞过度凋亡。
[0019]
进一步优选的,所述胚胎心管畸形包括胚胎心管细胞增殖不足、胚胎心管细胞过度凋亡、胚胎心管基因表达不良。
[0020]
根据本发明优选的,白术内酯ⅰ作为有效成分在制备预防和/或治疗妊娠合并糖尿病导致的胚胎神经系统发育不良药物中的应用。
[0021]
进一步优选的,白术内酯ⅰ作为有效成分在制备预防和/或治疗妊娠合并糖尿病导致的神经管畸形药物中的应用。
[0022]
进一步优选的,白术内酯ⅰ作为有效成分在制备预防和/或治疗妊娠合并糖尿病导
致的神经管细胞增殖不足药物中的应用。
[0023]
根据本发明优选的,上述应用中,所述药物还可含有以白术内酯ⅰ作为先导化合物合成得到的修饰物
[0024]
根据本发明优选的,上述应用中,白术内酯ⅰ的起效浓度为15μm以下。
[0025]
进一步优选的,上述应用中,白术内酯ⅰ的起效浓度为7.5
‑
15μm。
[0026]
更有优选的,上述应用中,白术内酯ⅰ的起效浓度为15μm。
[0027]
根据本发明优选的,上述应用中,所述药物含有一种或多种药学上可接受的载体或辅剂。
[0028]
进一步优选的,所述的辅料为缓释剂、赋形剂、填充剂、粘合剂、湿润剂、崩解剂、吸收促进剂、表面活性剂或润滑剂中的至少一种。
[0029]
根据本发明优选的,上述应用中,所述药物的剂型为胶囊、丸剂、片剂、口服液、颗粒剂、酊剂或注射剂。
[0030]
进一步优选的,上述应用中,所述药物的剂型为能够使起效时的浓度为15μm以下的剂型。
[0031]
进一步优选的,上述应用中,所述药物的剂型为能够使起效时的浓度为7.5
‑
15μm的剂型。
[0032]
进一步优选的,上述应用中,所述药物的剂型为能够使起效时的浓度为15μm的剂型。
[0033]
一种预防和/或治疗妊娠合并糖尿病引起胚胎发育疾病的药物,所述药物的有效成分包含白术内酯ⅰ。
[0034]
根据本发明优选的,所述药物中白术内酯ⅰ的起效浓度为15μm以下;
[0035]
进一步优选的,所述药物中白术内酯ⅰ的起效浓度为7.5
‑
15μm;
[0036]
进一步优选的,所述药物中白术内酯ⅰ的起效浓度为15μm。
[0037]
根据本发明优选的,所述药物的剂型为能够使起效时的浓度为15μm以下的剂型。
[0038]
进一步优选的,所述药物的剂型为能够使起效时的浓度为7.5
‑
15μm的剂型。
[0039]
进一步优选的,所述药物的剂型为能够使起效时的浓度为15μm的剂型。
[0040]
根据本发明优选的,所述妊娠合并糖尿病引起胚胎发育疾病包括胚胎心血管系统发育不良、胚胎神经系统发育不良。
[0041]
进一步优选的,胚胎心血管系统发育不良包括:胚胎血管发育不良、胚胎心管畸形、胚胎心肌细胞过度凋亡;神经系统发育不良包括神经管畸形。
[0042]
进一步优选的,胚胎心管畸形包括胚胎心管细胞增殖不足、胚胎心管细胞过度凋亡、胚胎心管基因表达不良。
[0043]
进一步优选的,神经管畸形包括神经管细胞增殖不足。
[0044]
有益效果
[0045]
本发明扩大了白术内酯ⅰ的应用范围,提高了白术内酯ⅰ的应用价值,有助于进一步开发新药,本研究首次发现白术内酯ⅰ能够有效缓解高糖环境诱导的胚胎心血管系统和神经系统发育不良现象,提供白术内酯ⅰ及其作为先导化合物合成出来的修饰物可以保护妊娠合并糖尿影响胚胎心血管系统和神经系统发育的新用途。
[0046]
说明书附图
[0047]
图1白术内酯主要的分型图;
[0048]
图2白术内酯ⅰ对胚胎发育影响的实验图;
[0049]
图3白术内酯ⅰ在高糖环境下对胚胎发育影响的实验图;
[0050]
图4白术内酯ⅰ在高糖环境下对胚胎血管发育影响的实验图;
[0051]
图5白术内酯ⅰ在高糖环境下对神经管和细胞增殖影响的实验图;
[0052]
图6白术内酯ⅰ在高糖环境下对心管发育影响的实验图;
[0053]
图7白术内酯ⅰ在高糖环境下对心管细胞增殖影响的实验图;
[0054]
图8白术内酯ⅰ在高糖环境下对心肌细胞过度凋亡影响的实验图;
[0055]
图9白术内酯ⅰ在高糖环境下对h9c2(大鼠心肌母细胞)的过度凋亡影响的实验图;
[0056]
图10白术内酯ⅰ在高糖环境下对心管形成关键基因的表达影响的实验图;
[0057]
图11白术内酯ⅱ、ⅲ在高糖环境下对胚胎和心肌细胞影响的实验图。
具体实施方式
[0058]
下面结合实施例及附图对本发明作进一步详细的阐述,但本发明的保护范围不限于此。
[0059]
实施例中未详加说明的内容均按本领域现有技术。
[0060]
本发明所述的中药单体白术内酯ⅰ购自成都曼思特生物技术有限公司(货号:a0372),分子式为c
15
h
18
o2,分子量为230.13,具有图1的结构。
[0061]
附图中的符号含义:*
/#
表示p<0.05,视为有显著性差异;**
/##
表示p<0.01,视为非常有显著性差异;***
/###
表示p<0.001,视为极具显著性差异。
[0062]
实施例1
[0063]
一定浓度的白术内酯ⅰ不会影响胚胎发育
[0064]
为了确定白术内酯ⅰ是否对胚胎发育有细胞毒性作用,采用early chick culture(ec culture)的方法培养早期鸡胚。发明人将生理盐水加入培养基中作为对照组;实验组中培养基的白术内酯ⅰ终浓度分别为7.5μm,15μm,30μm,孵育0期(hh0)的鸡胚,在36小时收获(图2a)。用胚胎长度和体节对数目(判断鸡胚早期发育阶段的标志性结构),发明人发现7.5μm和15μm的白术内酯ⅰ对鸡胚的发育没有造成明显影响,但是30μm的白术内酯ⅰ处理显着降低了胚胎发育的长度和体节对数(p值<0.05,p值<0.001,每组胚胎n=6,图2b
‑
c)。同时,发明人观察到7.5μm和15μm的白术内酯ⅰ对胚胎畸形无明显影响,但暴露在30μm浓度的白术内酯ⅰ下有较高影响(30μm时严重畸形率为40%,每组胚胎n=6,图2e),严重畸形种可见神经管缺陷(黑色虚线箭头,图2d)。
[0065]
实验证实,在鸡胚模型中,15μm以下浓度的白术内酯ⅰ不影响胚胎早期发育。
[0066]
实施例2
[0067]
白术内酯ⅰ显著改善高糖环境导致的胚胎死亡及发育畸形
[0068]
基于发明人已经建立的妊娠糖尿病鸡胚模型(cell cycle:14(5):772
‑
783.2015),发明人设立鸡胚对照组(生理盐水),高糖组(50mm葡萄糖),白术内酯ⅰ低浓度组(50mm葡萄糖+7.5μm白术内酯ⅰ),白术内酯ⅰ中浓度组(50mm葡萄糖+15μm白术内酯ⅰ)共4组,在4组ec culture中培养鸡胚至hh10期,进行发育时期和畸形率的统计。发明人通过比较在鸡胚发育第36小时,暴露于生理盐水、高糖和/或7.5μm、15μm的白术内酯ⅰ中原肠胚鸡胚的
发育情况(图3a),发明人发现高糖环境会对胚胎发育造成影响,高糖显着降低原肠胚鸡胚的长度和体节对数(图3b
‑
c,p值<0.01,p值<0.05,n=6)。然而,高糖+15μm白术内酯ⅰ的组合,在第36小时,发明人观察到胚胎的发育没有明显的被抑制(与高糖组相比,p值<0.05)。同时,高糖+15μm白术内酯ⅰ组的畸形胚胎的数量比高糖组少(图3d),重度畸形:对照组0%,高糖组50%,高糖+7.5μm白术内酯ⅰ组40%,高糖+15μm白术内酯ⅰ组25%;n=6。
[0069]
实验证实,在鸡胚模型中,15μm浓度的白术内酯ⅰ能显著改善高糖环境导致的胚胎发育不良。
[0070]
实施例3
[0071]
白术内酯ⅰ改善高糖导致的胚胎血管不良
[0072]
发明人使用了鸡胚ysm(yolk sac membrane)模型来研究白术内酯ⅰ是否能够保护血管生成,使其免受高糖(50mm葡萄糖)抑制(图4a
‑
d)。发明人设立鸡胚对照组(生理盐水),高糖组(50mm葡萄糖),白术内酯ⅰ组(15μm白术内酯ⅰ),高糖+白术内酯ⅰ组(50mm葡萄糖+15μm白术内酯ⅰ)共4组,将0天的受精鸡蛋孵育2.5天,取橡胶圈贴于ysm上,分组加入以上溶液到鸡胚ysm的胶圈上。再培养36小时后,发明人发现与对照组中ysm的血管生成相比(图4a1
‑
d1),高糖组的血管密度明显降低(p值<0.01,图4e),15μm白术内酯ⅰ组的血管密度没有改变(p值>0.05),高糖+15μm白术内酯ⅰ的组合显着比高糖组的血管密度高(p值<0.05,与高糖组组相比;n=6)。
[0073]
实验证实,在鸡胚模型中,15μm浓度的白术内酯ⅰ处理可以在一定程度上保护血管发生,改善高糖导致的胚胎血管不良。
[0074]
实施例4
[0075]
白术内酯ⅰ缓解高糖导致的神经管畸形和细胞增殖不足
[0076]
发明人设立鸡胚对照组(生理盐水),高糖组(50mm葡萄糖),白术内酯ⅰ组(15μm白术内酯ⅰ),高糖+白术内酯ⅰ组(50mm葡萄糖+15μm白术内酯ⅰ)共4组,在4组ec culture中培养鸡胚至hh10期,采用(ph3)phospho
‑
histone h3与dapi共标记的整胚免疫荧光对鸡胚神经管形态和增殖情况进行观察(白色箭头为ph3在神经管上的表达)。发明人可以看到对照组和15μm白术内酯ⅰ处理的胚胎在hh11躯干部神经管均呈现闭合状态(图5a、c,白色箭头为神经管上表达的phospho
‑
histone h3阳性细胞),而高糖处理组严重畸形的胚胎出现了神经管闭合不全(图5b,*为神经管闭合不全处),高糖环境下,15μm的白术内酯ⅰ处理的胚胎,其神经管呈现闭合状态(图5d)。对神经管上表达的phospho
‑
histone h3阳性细胞数量进行统计,发现高糖组phospho
‑
histone h3相对表达量比对照组减少(n>6,p值<0.01,图5e)。高糖+15μm白术内酯ⅰ组的phospho
‑
histone h3相对表达量有所增加(与高糖组比,p值<0.05)。
[0077]
实验证实,在鸡胚模型中,15μm的白术内酯ⅰ改善了高糖环境导致的胚胎神经管畸形和神经管细胞增殖不足。
[0078]
实施例5
[0079]
白术内酯ⅰ缓解高糖导致的心管畸形
[0080]
发明人设立鸡胚对照组(生理盐水),高糖组(50mm葡萄糖),白术内酯ⅰ组(15μm白术内酯ⅰ),高糖+白术内酯ⅰ组(50mm葡萄糖+15μm白术内酯ⅰ)共4组,在4组ec culture中培养鸡胚至hh11期,通过mf20免疫荧光标记心管,对鸡胚心管形态进行观察(图6a
‑
d),进行冰
冻切片获得心管的横截面(图6a1
‑
d1),荧光显微镜观察拍照显示,在对照和15μm白术内酯ⅰ组(正常心管发生率:100%,n>6,图6a
‑
a1,c
‑
c1,e)中可观察到正常的环状心管;高糖会导致心管不融合发生率的增高(异常心管发生率:33%,图6b
‑
b1),高糖+15μm白术内酯ⅰ组的心管畸形率有所降低(异常心管发生率:20%,图6d
‑
d1)。
[0081]
实验证实,在鸡胚模型中,15μm的白术内酯ⅰ缓解了高糖环境导致的胚胎心管发育畸形。
[0082]
实施例6
[0083]
白术内酯ⅰ缓解高糖导致的心管细胞增殖不足
[0084]
为了探究早期心管发育中,白术内酯ⅰ对高糖暴露的心肌细胞的增殖是否有影响,发明人设立鸡胚对照组(生理盐水),高糖组(50mm葡萄糖),白术内酯ⅰ组(15μm白术内酯ⅰ),高糖+白术内酯ⅰ组(50mm葡萄糖+15μm白术内酯ⅰ)共4组,在4组ec culture中培养鸡胚至hh11期,采用mf20和phospho
‑
histone h3双标免疫荧光染色,同时对其心管切面进行观察拍照(图7a
‑
d)。对心管上表达的phospho
‑
histone h3阳性细胞数量进行统计(图7e),发现高糖组phospho
‑
histone h3阳性细胞比对照组减少(n>6,p值<0.05)。高糖+15μm白术内酯ⅰ组的phospho
‑
histone h3阳性细胞有所增加(与高糖组比,p值<0.05)。
[0085]
实验证实,在鸡胚模型中,15μm的白术内酯ⅰ缓解了高糖环境导致的心肌细胞增殖不足。
[0086]
实施例7
[0087]
白术内酯ⅰ缓解高糖导致的心肌细胞过度凋亡
[0088]
为了探究白术内酯ⅰ对高糖暴露的心肌细胞的凋亡是否有影响,发明人设立鸡胚对照组(生理盐水),高糖组(50mm葡萄糖),白术内酯ⅰ组(15μm白术内酯ⅰ),高糖+白术内酯ⅰ组(50mm葡萄糖+15μm白术内酯ⅰ)共4组,在4组ec culture中培养鸡胚至hh11期,采用mf20和c
‑
caspase3双标免疫荧光染色,同时对其心管切面进行观察拍照(图8a
‑
d)。对心管上表达的c
‑
caspase3阳性细胞数量进行统计,发现高糖组c
‑
caspase3阳性细胞个数比对照组增多(n>6,p值<0.01,图8e)。高糖+15μm白术内酯ⅰ组的c
‑
caspase3阳性细胞有所减少(与高糖组比,p值<0.01)。
[0089]
实验证实,在鸡胚模型中,15μm的白术内酯ⅰ缓解了高糖环境导致的心肌细胞过度凋亡。
[0090]
实施例8
[0091]
白术内酯ⅰ缓解高糖导致h9c2(大鼠心肌母细胞)的过度凋亡
[0092]
发明人设立h9c2心肌细胞对照组,高糖组(50mm葡萄糖),白术内酯ⅰ组(15μm白术内酯ⅰ),高糖+白术内酯ⅰ组(50mm葡萄糖+15μm白术内酯ⅰ)共4组,通过体外大鼠心肌母细胞h9c2实验:c
‑
caspase3阳性细胞和hoechst双染实验检测心肌细胞的凋亡情况(图9a
‑
d),结果显示高糖组c
‑
caspase3阳性细胞的相对比率增多(与对照组相比,n>6,p值<0.001,图9e),而高糖+15μm白术内酯ⅰ组的c
‑
caspase3阳性细胞相对比率减少(与高糖组比,p值<0.01)。发明人通过流式细胞技术检测h9c2心肌细胞凋亡情况(图9f
‑
i),趋势与细胞免疫荧光表达类似(图9j)。高糖组早期和晚期凋亡细胞比率增高(与对照组比,p值<0.001),高糖+白术内酯ⅰ组早期凋亡和晚期凋亡比率有所减低(与高糖组相比,p值<0.01)。
[0093]
实验证实,在细胞模型中,15μm的白术内酯ⅰ缓解了高糖导致的大鼠心肌细胞h9c2
(大鼠心肌母细胞)过度凋亡。
[0094]
实施例9
[0095]
白术内酯ⅰ改善高糖导致心管形成关键基因的表达不良
[0096]
发明人设立鸡胚对照组(生理盐水),高糖组(50mm葡萄糖),白术内酯ⅰ组(15μm白术内酯ⅰ),高糖+白术内酯ⅰ组(50mm葡萄糖+15μm白术内酯ⅰ)共4组,在ec culture中培养鸡胚至hh11期,发明人采用q
‑
pcr检测早期心脏发育关键基因的表达情况(图10a),在高糖暴露的环境下,心管形成的关键基因:血管内皮生长因子vegfa、碱性成纤维细胞生长因子fgf2、心肌转录调节因子gata4和nkx2.5在高糖组中下调(与对照组相比,p值<0.01,p值<0.05,p值<0.001,p值<0.05),而在高糖+白术内酯ⅰ组中vegfa、fgf2、gata4和nkx2.5得到恢复(与高糖组相比,p值<0.05,p值<0.05,p值<0.01,p值<0.05)。骨形成蛋白因子bmp2、bmp4在高糖组中上调(与对照组相比,p值<0.001,p值<0.001),而在高糖+白术内酯ⅰ组bmp2、bmp4得到恢复(与高糖组相比,p值<0.001,p值<0.001)。采用western blot的方法,发明人检测了gata4的表达情况(图10b),发明人发现15μm白术内酯ⅰ对gata4的蛋白水平并没有明显影响(p值>0.05),而高糖环境会抑制gata4表达(p值<0.05)。在高糖环境下,15μm白术内酯ⅰ干预可以显著恢复gata4的表达水平(p值<0.05)。
[0097]
实验证实,在鸡胚模型中,15μm白术内酯ⅰ显著改善了高糖环境导致的心管发育重要基因表达不良。
[0098]
对比例
[0099]
白术内酯ⅱ、ⅲ对高糖环境下的胚胎和心肌细胞的影响
[0100]
为探究白术内酯ⅱ与白术内酯ⅲ对于高糖暴露下鸡胚发育的影响,发明人通过比较鸡胚对照组(生理盐水),高糖组(50mm葡萄糖),白术内酯ⅱ/ⅲ低浓度组(50mm葡萄糖+7.5μm白术内酯ⅱ/ⅲ),白术内酯ⅱ/ⅲ中浓度组(50mm葡萄糖+15μm白术内酯ⅱ/ⅲ),在ec culture中培养鸡胚至hh10期,在第36小时鸡胚的发育情况。
[0101]
通过比较第36小时鸡胚的体长和体节数量(图11a
‑
f),发明人发现白术内酯ⅱ和白术内酯ⅲ对于高糖暴露下鸡胚的发育无明显影响。(与高糖组相比,p值<0.05;n=6,图11a
‑
d)。高糖+7.5μm白术内酯ⅱ的畸形胚胎的数量与高糖组一样,高糖+15μm白术内酯ⅱ的畸形胚胎的数量比高糖组少(重度畸形:对照组0%,高糖组50%,高糖+7.5μm白术内酯ⅱ组50%,高糖+15μm白术内酯ⅱ组33%;n=6,图11e)。同时,高糖+7.5μm白术内酯ⅲ的畸形胚胎的数量与高糖组一样,高糖+15μm白术内酯ⅲ的畸形胚胎的数量比高糖组少(重度畸形:对照组0%,高糖组50%,高糖+7.5μm白术内酯ⅲ组50%,高糖+15μm白术内酯ⅲ组40%;n>6,图11f)。发明人设立h9c2心肌细胞对照组,高糖组(50mm葡萄糖),白术内酯ⅱ/ⅲ组(15μm白术内酯ⅱ/ⅲ),高糖+白术内酯ⅱ/ⅲ组(50mm葡萄糖+15μm白术内酯ⅱ/ⅲ),温育h9c2细胞12、24、36和48小时。然后使用cck
‑
8检测细胞增殖和活力,细胞活力实验表明白术内酯ⅱ和白术内酯ⅲ对高糖暴露的心肌细胞的增殖与活力无明显影响。(与高糖组相比,p值>0.05;n=6,图11g
‑
h)。
[0102]
综上,本研究首次发现白术内酯ⅰ能够缓解高糖环境诱导的胚胎心血管系统和神经系统发育不良现象,而白术内酯ⅱ和白术内酯ⅲ的作用效果与白术内酯ⅰ的作用效果有显著差异,白术内酯ⅰ对于缓解高糖环境诱导的胚胎心血管系统和神经系统发育不良现象具有特异性作用,本发明扩大了白术内酯ⅰ的应用范围,提高了白术内酯ⅰ的应用价值,有助
于进一步开发新药,提供白术内酯ⅰ及其作为先导化合物合成出来的修饰物可以保护妊娠合并糖尿影响胚胎心血管系统和神经系统发育的新用途。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1