一种天然高分子有机纳米复合的可注射可二次力学增强的双网络水凝胶的制备方法
1.本发明属于材料科学领域、纳米材料领域、生物医学工程领域,具体是一种天然高分子有机纳米复合的颗粒组装的水凝胶材料及其在组织工程中的应用,公开了一种由非共价键和共价键双重交联的、可注射、可塑形、可打印的双网络水凝胶材料及其制备方法和应用
背景技术:
2.随着我国经济水平的飞速发展以及人口的老龄化的加剧,人们对健康以及医疗的需求日益加强,然而许多外伤造成的创伤是不可逆的,对这种组织来说创伤会在数年内都一直保留下来,进一步退化并最终引发疾病,如骨关节炎,导致关节功能受损,生活质量下降。目前的治疗策略包括自体或异体器官移植植入,这些方法大大改善了缺陷修复的结果,然而有一定的缺陷,可能会导致免疫排斥反应以及引发伦理问题,以及配型供不应求,无法作为长期的临床解决方案面向广大群体普遍应用。因此,迫切需要有潜力的的替代治疗方法。
3.通过三维(3d)打印模拟复合组织结构的挤出式增材制造因其快速原型设计和创建复杂配方而在组织工程中越来越受欢迎。能够制造患者特定的解剖结构,以满足个性化再生医学的需求。生物墨水需要满足的几个基本标准包括适当的粘度,用于控制在生物打印过程中创建独立结构的灵活性,以及生物打印后保持建筑完整性。此外,剪切变稀用于在低喷嘴压力下挤出生物墨水,以保护细胞免受物理压力源的影响,适配新组织生成的生物降解性,仿生特性以及其结构和机械稳定性是同样重要的标准。为解决传统的胶体凝胶力学强度差的问题,双网络水凝胶的设计策略提供了新的手段。双网络水凝胶是一类具有高机械强度和韧性的水凝胶材料。其通过将两种可独立形成水凝胶网络的高分子复合在同一水凝胶中实现优异的机械性能。目前报道的双网络水凝胶往往基于高分子组成,不具有可注射的性能,颗粒水凝胶是一种基于“自下而上”设计理念,以微、纳米颗粒为基本单元,形成具有精细微观结构和稳定宏观结构的新型水凝胶材料。以天然高分子有机微纳米颗粒为基本结构单元,通过自下而上的组装策略,控制基本结构单元之间的相互作用如:磁力、疏水相互作用、静电力、空间位阻等诱导其自组装形成的支架。由于物理“交联”的胶体颗粒间作用的可逆性保障双网络水凝胶力学强度增强的同时具有优异的剪切变稀自修复性能满足3d打印的需求。
技术实现要素:
4.本发明开发了一种天然高分子有机纳米复合的可注射可二次力学增强的双网络水凝胶的制备方法。本发明以聚乙烯醇和有机高分子明胶纳米颗粒为基本机构单元构建了双网络水凝胶,明胶颗粒具有优异的生物相容性以及rgd多肽序列为细胞提供黏附位点,并且可以组装形成胶体凝胶网络。由于明胶颗粒表面具有带有正电荷的氨基和负电荷的羧基
和羟基,有明显的非共价相互作用形成第二重网络,聚乙烯醇是一种极安全的高分子有机物,对人体无毒,无副作用,具有良好的生物相容性,尤其在医疗中的如其水性凝胶在眼科、伤口敷料和人工关节方面的有广泛应用,保证了有机纳米复合凝胶在生物医学领域应用的可行性。通过氢键相互作用,使有机纳米复合凝胶更加稳定。通过二次交联的方法,有机纳米复合凝胶在未进行二重交联时具有剪切变稀、自修复的优异力学性能,可以用于可注射填充材料用于微创手术以及3d生物打印墨水用于生物制造。然后,通过控制聚合交联网络后,得到的有机纳米复合凝胶具有稳定和优异的力学强度的。进一步通载细胞生物打印3d生物打印,我们证实了通过3d生物制造将胶体凝胶加工成具有精细结构的三维细胞支架。
5.有益效果
6.本发明通过一种新型的有机纳米复合水凝胶的概念,将明胶有机纳米颗粒引入传统的聚合物网络,构建了一种区别去传统复合水凝胶材料的有机纳米复合材料,基于明胶纳米颗粒之间丰富的静电相互作用,氢键作用等可逆的非共价相互作用,赋予了这种复合凝胶材料优异的剪切变稀自修复特性,反映到材料来说就是良好的的精细的的一种可塑型性,同时可进行二次交联二次力学增强,用以匹配不同组织部位组织工程的需求,本发明精细的探究了聚乙烯醇与明胶纳米颗粒共混时,通过共聚焦显微镜观察了颗粒与聚合物之间的排空力诱导胶体网络的形成过程以及最终胶体凝胶网络结构。这种有机纳米复合凝胶材料提高了传统的生物打印墨水的力学性能,实现了高强度生物打印墨水的开发。制备简单,极大的扩宽了可注射材料和3d打印支架的应用领域。
7.本专利所述的双网络水凝胶具有良好的生物相容性和生物降解性,可作为细胞二维培养或三维培养的基质,实现对细胞三维环境的构建,并支持细胞的生长繁殖等功能,可作为载细胞的三维可注射凝胶支架和3d打印支架用于组织工程和再生医学的应用。
附图说明
8.图1是高分子网络未形成时,水凝胶粘度随剪切速率变化趋势,表明水凝胶具有剪切变稀的力学性能,且光学图像表明水凝胶的可注射性能。
9.图2是高分子网络未形成时,水凝胶模量经受剪切应变后恢复曲线,表明水凝胶具有自修复的力学性能,且光学图像表明水凝胶的自修复性能;
10.图3是实施例2中双网络水凝胶,聚乙烯醇高分子网络聚合过程,双网络水凝胶模量的变化
11.图4是实施例2和对比例2双网络水凝胶和明胶胶体凝胶微观结构的扫描电镜图;
12.图5是实施例3中明胶颗粒组装成网络结构的共聚焦显微镜图片;
13.图6是实施例10中双网络水凝胶作为载小鼠间充质干细胞支架细胞培养实验结果;
具体实施方式
14.以下结合具体实施例对本发明作进一步说明,但不以任何方式限制本发明。
15.实施例1
16.1.明胶颗粒的制备:5ga型明胶溶解在100ml去离子水溶液中,并保持加热到 40℃,得到澄清透明的明胶水溶液,滴加盐酸将溶液ph值调节至2.5,分别将240,350ml的丙酮
溶液滴加至上述明胶水溶液中并保持加热40℃和持续搅拌(1000rpm),滴加总时间为20min,向上述纳米颗粒悬液中加入74μl 的交联剂戊二醛(25wt%水溶液),交联时间12hrs,待反应结束后,向混合物中加入100mm浓度的甘氨酸,终止未反应完全的戊二醛的端基。将纳米颗粒悬浮液反复离心和在去离子水中重悬。将悬浊液在-60℃下冷冻干燥,得到明胶纳米颗粒干粉。通过纳米粒度仪测试明胶颗粒的颗粒尺寸和表面电荷。 (表1)
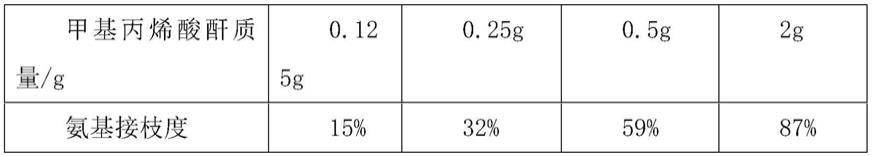
17.2.光交联基团改性明胶纳米颗粒的制备:在50℃下将5g明胶a型粉末溶于 100ml去离子水中得到明胶溶液。分别加入0.0625,0.125,0.25,0.5,2g的甲基丙烯酸酐于高温下反应两小时,甲基丙烯酸酐与蛋白质分子链上游离的氨基发生亲核取代反应,同时产生等摩尔的甲基丙烯酸。用盐酸调节ph至7,并加入原溶液2倍体积的丙酮,破坏蛋白质分子表面的水化层,甲基丙烯酸酯明胶(gelma)沉淀析出,使用去离子水反复清洗后,进行冷冻干燥,得到冻干的甲基丙烯酸酯明胶样品。通过核磁共振氢谱测试明胶表面的氨基的接枝度;根据相应基团谱图变化计算出的接枝度如表1所示;
18.表1
[0019][0020]
3.将5g上述不同接枝度的改性明胶重新溶于40℃100ml的去离子水中,并调节ph至2.5,在30min内加入300ml丙酮,并快速搅拌,使蛋白质分子缓慢脱水卷曲形成纳米级球体。随后加入165μl交联剂戊二醛,搅拌12hrs。用氢氧化钠将颗粒悬浮液ph调节至7后,得到改性明胶纳米颗粒,其尺寸和表面电荷如表2所示。将纳米颗粒悬浮液反复离心和在去离子水中重悬。将悬浊液在-60℃下冷冻干燥,得到明胶纳米颗粒干粉。
[0021]
表2
[0022] 改性明胶颗粒颗粒尺寸416nm表面电荷11.9mv
[0023]
实施例2
[0024]
1.改性明胶纳米颗粒颗粒的制备:使用实施例1方案1中制备的改性明胶纳米颗粒
[0025]
2.使用分子量为6kda的聚乙烯醇(购买自中国西格玛-奥德里奇化学试剂公司) 将0.1g的6kda的聚乙烯醇和0.005g的2-羟基-4
′‑
(2-羟乙氧基)-2-甲基苯丙酮光引发剂溶解在1ml水性溶液中与0.2g明胶颗粒通过鲁尔转接头注射器反复吹打10次,得到预聚合胶体凝胶,其可注射和自修复性能如图1,2 所示,表1明预聚合胶体凝胶具有优异的可注射性和自修复性能;
[0026]
表1
[0027][0028]
3.上述预聚合胶体凝胶在365nm,50mw/cm2紫外光下交联30s,得到双网络水凝胶,成胶过程中凝胶强度通过流变仪监控如图3所示,随着第二重聚合物网络的交联,水凝胶的储能模量和损耗模量显著增加。形成的双网络水凝胶的微观结构如图4所示,可以观察到多空聚合物网络的内部分布着相互堆积的明胶颗粒;
[0029]
4.上述二次交联后双网络水凝胶的储能模量和损耗模量(表2)使用旋转流变仪的时间扫描模式得到,其中频率为1hz,应变为0.5%。压缩力学应变和断裂强度通过力学测试机获得,其中压缩速率为0.0211/s。
[0030]
表2
[0031][0032]
实施例3
[0033]
1.明胶颗粒的制备:使用实施例1方案二制备的明胶纳米颗粒;
[0034]
2.聚乙烯醇聚合基团的接枝:使用分子量为6kda的聚乙烯醇二丙烯酸酯(购买自中国西格玛-奥德里奇化学试剂公司)
[0035]
3.将0.05g得到的6kda的聚乙烯醇二丙烯酸酯和0.005g的2-羟基-4
′‑
(2
‑ꢀ
羟乙氧基)-2-甲基苯丙酮光引发剂溶解在1ml水性溶液中与0.2g明胶颗粒通过鲁尔转接头注射器反复吹打10次,得到可注射,自修复预聚合胶体凝胶;
[0036]
[0037]
4.上述预聚合胶体凝胶在365nm,50mw/cm2紫外光下交联30s,得到双网络水凝胶
[0038]
5.上述双网络水凝胶的储能模量和损耗模量(表4)使用旋转流变仪的时间扫描模式得到,其中频率为1hz,应变为0.5%。压缩力学应变和断裂强度通过力学测试机获得,其中压缩速率为0.0211/s。
[0039][0040]
实施例4
[0041]
1.明胶颗粒的制备:使用实施例1方案1制备的明胶纳米颗粒
[0042]
2.聚乙二醇聚合基团的接枝使用分子量为20kda的叠氮端基修饰聚乙二醇和炔烃修饰聚乙二醇(购买自中国厦门赛诺邦格生物科技有限公司);
[0043]
3.将0.05g20kda的叠氮端基修饰聚乙二醇和0.05g20kda炔烃修饰聚乙二醇以相同质量比在水性溶液混合均匀,再与0.2g明胶颗粒通过鲁尔转接头注射器反复吹打10次,室温等待1hrs,形成双网络水凝胶;
[0044][0045]
4.上述预聚合胶体凝胶在365nm,50mw/cm2紫外光下交联30s,得到双网络水凝胶;
[0046]
5.上述双网络水凝胶的储能模量和损耗模量(表4)使用旋转流变仪的时间扫描模式得到,其中频率为1hz,应变为0.5%。压缩力学应变和断裂强度通过力学测试机获得,其中压缩速率为0.0211/s。
[0047]
[0048]
实施例5
[0049]
1.点击化学明胶高分子制备:在50℃下将5g明胶a型粉末溶于100ml去离子水中得到明胶溶液。将上述溶液加入反应催化剂0.01g的edc/nhs,同时加入0.1g的叠氮亚胺或丙炔胺反应2hrs,叠氮亚胺和丙炔胺与明胶链上游离的羧基发生亲核取代反应,分别得到叠氮基团封端的明胶和炔烃封端的明胶;
[0050]
2.改性明胶纳米颗粒制备:用盐酸调节ph至7,并加入原溶液2倍体积的丙酮,破坏明胶分子表面的水化层,叠氮基团封端的明胶和炔烃封端的明胶作为沉淀析出,将叠氮基团封端的明胶和炔烃封端的明胶的沉淀分别重新溶于 40℃100ml的去离子水中,并调节ph至2.5,在30min内加入300ml丙酮,并快速搅拌,使蛋白质分子缓慢脱水卷曲形成纳米级球体。随后加入165μl 交联剂戊二醛,搅拌12hrs。用氢氧化钠将颗粒悬浮液ph调节至7后,进行冷冻干燥,得叠氮化明胶颗粒粉末,炔烃化明胶颗粒粉末;
[0051]
3.使用分子量为6kda的聚乙烯醇(购买自中国西格玛-奥德里奇化学试剂公司) 将0.1g的6kda的聚乙烯醇和0.005g的2-羟基-4
′‑
(2-羟乙氧基)-2-甲基苯丙酮光引发剂溶解在1ml水性溶液中与0.2g明胶颗粒通过鲁尔转接头注射器反复吹打10次,得到预聚合胶体凝胶,其可注射和自修复性能如图1,2 所示,表明预聚合胶体凝胶具有优异的可注射性和自修复性能;
[0052][0053]
4.上述预聚合胶体凝胶在365nm,50mw/cm2紫外光下交联30s,得到双网络水凝胶;
[0054]
5.上述双网络水凝胶的储能模量和损耗模量(表4)使用旋转流变仪的时间扫描模式得到,其中频率为1hz,应变为0.5%。压缩力学应变和断裂强度通过力学测试机获得,其中压缩速率为0.0211/s。
[0055][0056]
实施例6
[0057]
1.明胶颗粒的制备使用实施例1方案1制备的明胶纳米颗粒;
[0058]
2.聚合基团的接枝使用分子量为6kda的聚乙烯醇二丙烯酸酯(购买自中国西格
玛-奥德里奇化学试剂公司)
[0059]
3.将0.1g的0.6,20kda的聚乙烯醇二丙烯酸酯和0.005g过硫酸铵,0.004g 四甲基亚胺溶解在1ml水性溶液中并与0.2g明胶颗粒通过鲁尔转接头注射器反复吹打10次,室温等待1hrs,过硫酸铵和四甲基亚胺诱导烯烃的自由基聚合使得聚乙烯醇网络的交联得到双网络水凝胶;
[0060]
4.上述双网络水凝胶的储能模量和损耗模量(表11)使用旋转流变仪的时间扫描模式得到,其中频率为1hz,应变为0.5%。压缩力学应变和断裂强度通过力学测试机获得,其中压缩速率为0.0211/s。
[0061][0062]
实施例7
[0063]
权利要求中共同混合的方式
[0064]
1.将5g上述不同接枝度的实例1中的改性明胶,重新溶于40℃100ml的去离子水中,并调节ph至2.5,在30min内加入300ml丙酮,并快速搅拌,使蛋白质分子缓慢脱水卷曲形成纳米级球体。随后加入165μl交联剂戊二醛,搅拌12hrs。用氢氧化钠将颗粒悬浮液ph调节至7后,进行冷冻干燥,得到改性明胶纳米颗粒粉末,称量不同质量分数的颗粒粉末,分别加入分子量为 6kda的聚乙烯醇(购买自中国西格玛-奥德里奇化学试剂公司),将0.2改性明胶纳米颗粒/聚乙烯醇和0.005g的2-羟基-4
′‑
(2-羟乙氧基)-2-甲基苯丙酮光引发剂溶解在1ml水性溶液中通过鲁尔转接头注射器反复吹打10次,得到可注射,自修复预聚合胶体凝胶,上述预聚合胶体凝胶在365nm, 50mw/cm2紫外光下交联30s,得到双网络水凝胶,双网络水凝胶的储能模量和损耗模量(表2)使用旋转流变仪的时间扫描模式得到,其中频率为1hz,应变为0.5%。压缩力学应变和断裂强度通过力学测试机获得,其中压缩速率为0.0211/s;
[0065]
2. 5ga型明胶溶解在100ml去离子水溶液中,并保持加热到40℃,得到澄清透明的明胶水溶液,滴加盐酸将溶液ph值调节至2.5,分别将240ml的丙酮溶液滴加至上述明胶水溶液中并保持加热40℃和持续搅拌(1000rpm),滴加总时间为20min,向上述纳米颗粒悬液中加入74μl的交联剂戊二醛(25wt%水溶液),交联时间12hrs,待反应结束后,向混合物中加入100mm浓度的甘氨酸,终止未反应完全的戊二醛的端基。将纳米颗粒悬浮液反复离心和在去离子水中重悬。将50ml的20mg/ml的明胶纳米颗粒悬浊液中分别加入分子量为0.6kda和20kda的聚乙二醇二丙烯酸酯(购买自中国西格玛-奥德里奇化学试剂公司)1g,搅拌24h后,在-60℃下冷冻干燥,得到明胶纳米颗粒/ 聚乙二醇二丙烯酸酯混合干粉。将0.2明胶纳米颗粒/聚乙二醇二丙烯酸酯混合干粉和0.005g的2-羟基-4
′‑
(2-羟乙氧基)-2-甲基苯丙酮光引发剂溶解在1ml水性溶液中通过鲁尔转接头注射器反复吹打10次,得到可注射,自修
复预聚合胶体凝胶,上述预聚合胶体凝胶在365nm,50mw/cm2紫外光下交联30s,得到双网络水凝胶,双网络水凝胶的储能模量和损耗模量(表2) 使用旋转流变仪的时间扫描模式得到,其中频率为1hz,应变为0.5%。压缩力学应变和断裂强度通过力学测试机获得,其中压缩速率为0.0211/s
[0066]
实施例8
[0067]
压缩回复过程
[0068]
用实施例1-6中制备的聚乙烯醇基分子量为6kda双网络水凝胶,通过在三维打印模具中成型得到圆柱形支架(直径12mm,高8mm)。使用万能力学测试机将双网络水凝胶压缩至自身的0.8倍形变时,快速抬起压缩探头(10mm/s)。,双网络水凝胶能快速跟随探头回复,并且结构完整,表明双网络水凝胶具有高弹性。
[0069]
实施例9
[0070]
拉伸性能
[0071]
用实施例1-6中制备的聚乙烯醇基分子量为6kda双网络水凝胶,通过三维打印模具中成胶得到标准单轴拉伸测试样条(根据iso527-2标准的5b型设计)。并使用配备有50n测力传感器的万能试验机以50mm/min的变形速度对水凝胶进行拉伸试验,可以看到双网络拉伸形变至自身2.5倍,结构保持完整。
[0072]
实施例10
[0073]
3d打印支架性能
[0074]
用实施例1-6中制备的聚乙烯醇基分子量为6kda双网络水凝胶通过鲁尔转接头注射器反复吹打10次,使用3d生物打印机将水凝胶打印成特定结构。并在365nm, 50mw/cm2紫外光下交联30s,得到双网络水凝胶支架(长,宽:15mm,高:2mm)。如图6所示,6kda聚乙二醇基高分子与明胶颗粒复合的双网络水凝胶展示了高弹性模量,打印支架可完整承受2kg的砝码;实施例1-6中制备的聚乙烯醇基分子量为6kda双网络水凝胶用1ml含有间充质干细胞的高糖培养基溶液中(500000 个/cm2接种)代替水性溶液,使用3d生物打印机将水凝胶打印成特定结构。并在365nm,50mw/cm2紫外光下交联30s,得到载细胞双网络水凝胶支架。双网络水凝胶支架在培养基中培养第7,21天,使用2mm钙黄绿素(绿色荧光标记活细胞)和4mm乙锭同型二聚体(红色荧光标记死细胞)对支架进行死活染色,并使用激光共聚焦显微镜观察细胞增殖情况。,第21天小鼠间充质干细胞的数量明显高于第七天在双网络水凝胶支架中的数量,表明细胞在双网络支架增殖,证实双网络水凝胶具有良好的生物相容性。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1