一种高效准确检测皮肤组织中NADH荧光的光纤探头的制作方法
一种高效准确检测皮肤组织中nadh荧光的光纤探头
技术领域
1.本发明涉及荧光探测领域,具体涉及一种高效准确检测皮肤组织中nadh荧光的光纤探头。
背景技术:
2.nadh(nicotinamide adenine dinucleotide)是一种化学物质,是烟酰胺腺嘌呤二核苷酸的还原态,还原型辅酶ⅰ。n指烟酰胺,a指腺嘌呤,d是二核苷酸。nadh在维持细胞生长、分化和能量代谢以及细胞保护方面起着重要作用。并且已经证明,检测皮肤组织中的nadh水平监测新陈代谢等方面的相关信息。因此,皮肤组织中nadh水平的实时动态检测具有重要意义。
3.非侵入式测量皮肤组织中nadh含量是实现人体线粒体功能及相关疾病检测的关键。目前非侵入式皮肤组织中nadh含量的检测主要采用荧光光谱方法,其中常规光纤探头采用单一的入射光纤及收集光纤结构,采集的nadh信号弱,且受漫反射光及皮肤组织中其他成分荧光的干扰较大。因而优化光纤探头结构从而高效准确的测量皮肤组织中nadh含量,对实现准确无创检测人体线粒体功能及相关疾病有重要意义。
技术实现要素:
4.为解决以上问题,本发明提供了一种高效准确检测皮肤组织中nadh荧光的光纤探头,包括套管、收集光纤、激发光纤、填充物,套管为圆形,收集光纤置于套管的中心,激发光纤为多个,激发光纤均匀分布于套管的内壁一侧,激发光纤不与收集光纤接触,填充物填充套管内除收集光纤和激发光纤外的区域。
5.更进一步地,激发光纤的半径为100微米。
6.更进一步地,收集光纤的半径为300微米。
7.更进一步地,激发光纤和收集光纤的中心距离为550微米。
8.更进一步地,激发光纤为12个。
9.更进一步地,激发光纤的端面为斜面,靠近收集光纤一侧激发光纤低;远离收集光纤一侧激发光纤高。
10.更进一步地,在收集光纤的端面附近,收集光纤只有纤芯。
11.更进一步地,在收集光纤的端面处,收集光纤纤芯的截面面积大。
12.本发明的有益效果:本发明提供了一种高效准确检测皮肤组织中nadh荧光的光纤探头,包括套管、收集光纤、激发光纤、填充物,套管为圆形,收集光纤置于套管的中心,激发光纤为多个,激发光纤均匀分布于套管的内壁一侧,激发光纤不与收集光纤接触,填充物填充套管内除收集光纤和激发光纤外的区域。应用时,光纤探头与皮肤接触。激发光纤发出紫外光,紫外光进入皮肤,皮肤中的nadh分子产生荧光,收集光纤收集荧光,从而实现nadh分子探测。在本发明中,激发光纤围绕在收集光纤的外侧,通过扩大面积的方式增加了针对nadh分子的激发光强度,不仅提供了nadh分子荧光的强度,而且减少了对皮肤的伤害,在皮
肤组织nadh含量监测中具有良好的应用前景。
13.以下将结合附图对本发明做进一步详细说明。
附图说明
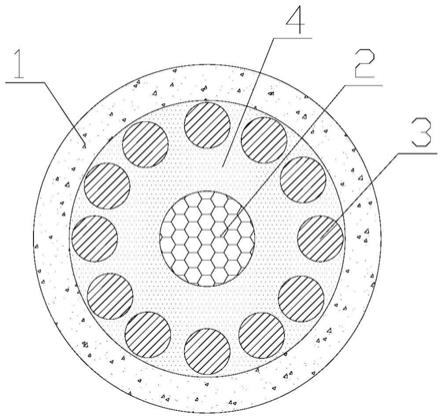
14.图1是一种高效准确检测皮肤组织中nadh荧光的光纤探头的示意图。
15.图2是蒙特卡罗模拟的nadh荧光和漫反射光强度与收集光纤半径之间的关系图。
16.图3是蒙特卡罗模拟的nadh荧光和漫反射光强度与激发光纤和收集光纤之间中心距离的关系图。
17.图4是蒙特卡罗模拟的nadh荧光和漫反射光强度与光纤探头和皮肤表面之间距离的关系图。
18.图中:1、套管;2、收集光纤;3、激发光纤;4、填充物。
具体实施方式
19.为使本技术的目的、技术方案及优点更加清楚明白,以下参照附图并举实施例,对本技术作进一步详细说明。
20.实施例1
21.本发明提供了一种高效准确检测皮肤组织中nadh荧光的光纤探头,如图1所示,该光纤探头包括套管1、收集光纤2、激发光纤3、填充物4。套管1为圆形,套管1的材料为不锈钢材料。收集光纤2置于套管1的中心,收集光纤2为多模光纤,收集光纤2包括纤芯、包层、涂覆层。收集光纤2为可见玻璃光纤,可以传播可见光。激发光纤3为多个,激发光纤3均匀分布于套管1内壁的内侧。激发光纤3也为多模光纤,激发光纤3包括纤芯、包层、涂覆层。激发光纤3为紫外石英光纤。激发光纤3不与收集光纤2接触,也就是说,激发光纤3和收集光纤2之间具有一定距离。填充物4填充套管1内除收集光纤2和激发光纤3外的区域。也就是说,填充物4用以固定收集光纤2和激发光纤3。优选地,填充物4具有一定的弹性。
22.应用时,激发光纤3的一端连接紫外光源,紫外光源的波长为340纳米。收集光纤2的一端连接ccd,用以探测荧光强度。nadh分子的吸收波段大概在320纳米-380纳米之间;在波长为340纳米紫外光的激发下,nadh发出荧光,荧光的波长大概在460纳米左右,通过探测nadh分子荧光强度实现皮肤中nadh含量监测。
23.在本发明中,激发光纤3围绕在收集光纤2的外侧,通过扩大面积的方式增加了针对nadh分子的激发光强度,不仅提高了nadh分子荧光的强度,而且减少了对皮肤的伤害,在皮肤组织nadh含量监测中具有良好的应用前景。另外,本发明将激发光纤3围绕在收集光纤2的周围,减少了探头的尺寸,便于应用或集成,对人体线粒体功能及相关疾病的无创检测有重要意义。
24.实施例2
25.在实施例1的基础上,应用蒙特卡罗方法模拟了光纤探头中各部件的最优尺寸。在这些模拟中,nadh分子设定在皮肤表面以下90微米处。激发光纤3的数量为12根。
26.图2是蒙特卡罗模拟的nadh荧光和漫反射光强度与收集光纤2半径之间的关系图。激发光纤3的半径被固定为100微米。图2表明当收集光纤2的半径rc为300微米时,即可实现高效的nadh荧光信号收集。
27.图3是蒙特卡罗模拟的nadh荧光和漫反射光强度与激发光纤3和收集光纤2之间中心距离的关系图。激发光纤3的半径被固定为100微米,收集光纤2的半径被固定为300微米。图3表明当激发光纤3和收集光纤2的中心距离d为550微米时,既可以高效地收集nadh荧光信号,又可以很好地降低漫反射光的干扰,并且可以有效地降低皮肤组织中其他成分荧光的干扰。也就是说,这样设置刚好可以收集到nadh分子所在皮肤层深度的荧光,而减少了其它深度荧光物质的干扰。例如,nadh主要在表皮层,而最大的干扰物质糖基化终产物(age)在真皮层,通过这种距离的设置,可以增加nadh分子荧光信号的收集,而减少age的干扰,实现深度分辨。
28.图4是蒙特卡罗模拟的nadh荧光和漫反射光强度与光纤探头和皮肤表面之间距离p的关系图。图4表明当收集nadh分子荧光时,探头表面应于皮肤紧密接触。
29.在以上蒙特卡罗模拟中,均设定激发光纤3和收集光纤2的端面为平面,激发光纤3和收集光纤2的端面平齐。
30.实施例3
31.在实施例1的基础上,激发光纤3的端面为斜面,靠近收集光纤2一侧激发光纤3低;远离收集光纤2一侧激发光纤3高。也就是说,每个激发光纤3的端面均为斜面,并且是向收集光纤2的一侧倾斜,并且每个激发光纤3端面倾斜的角度相同。这样一来,从激发光纤3端面出射的紫外光向收集光纤2一侧倾斜,在皮肤组织中,这些紫外光更多地聚集在收集光纤2的下侧,从而增强对收集光纤2下侧nadh分子的激发,nadh分子能够产生更强的荧光,从而提高nadh分子含量探测的准确度。
32.实施例4
33.在实施例3的基础上,在收集光纤2的端面附近,收集光纤2只有纤芯。也就是说,在收集光纤2的端面附近,收集光纤2纤芯外侧的包层和涂覆层被移除。收集光纤2的纤芯裸露在外,这样增加了收集光纤2纤芯与皮肤的接触面积,便于皮肤中的nadh分子荧光更多地进入收集光纤2,从而更精确地测量皮肤中nadh分子的含量。
34.实施例5
35.在实施例4的基础上,在收集光纤2的端面处,收集光纤2纤芯的截面面积大。也就是说,收集光纤2的纤芯粗细不同:在端面处,纤芯粗,在套管1内部,纤芯正常直径。当整个光纤探头与皮肤接触时,纤芯端面和侧面与皮肤具有更多的接触面积,从而使得皮肤中的更多nadh分子荧光耦合进入收集光纤2的纤芯,进而进入收集光纤2,从而实现更精确的皮肤中nadh分子含量探测。
36.更进一步地,填充物4低于激发光纤3和收集光纤2的端面。在应用时,本发明的光纤探头置于待测皮肤的下面,也就是说皮肤置于光纤探头上。皮肤自身的重力就压在光纤探头上。当填充物低于激发光纤3和收集光纤2的端面时,不仅激发光纤3的端面和收集光纤2的端面与皮肤紧密接触,而且收集光纤2纤芯的侧面也与皮肤紧密接触,增加了皮肤与收集光纤2纤芯的接触面积,皮肤中的nadh分子荧光也可以从收集光纤2纤芯的侧面耦合进入纤芯,提高了所检测到的荧光的强度,从而实现nadh分子含量的更精确监测。
37.更进一步地,在收集光纤2的端面处,收集光纤2的纤芯为球形。在制作时,可以应用激光烧灼的方式,使得收集光纤2的纤芯融化为球形。球形纤芯突出填充物4。球形纤芯与皮肤更容易接触。当皮肤与球形纤芯接触时,皮肤中的nadh荧光更倾向于垂直角度进入球
形纤芯,从而更多地耦合进入纤芯内,提高了所探测到的荧光强度,从而实现nadh分子含量更精确的探测。
38.以上所述仅为本技术的较佳实施例而已,并不用以限制本技术,凡在本技术的精神和原则之内,所做的任何修改、等同替换、改进等,均应包含在本技术保护的范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1