有机卤素化合物处理用铁粉的制造方法及土壤或地下水污染的净化方法与流程
本发明涉及有机卤素化合物处理用铁粉的制造方法及土壤或地下水污染的净化方法,该有机卤素化合物处理用铁粉分解土壤或地下水等中含有的有机卤素化合物。
背景技术:
作为电子部件的脱脂洗涤、干洗等的溶剂,使用以三氯乙烯(TCE)、四氯乙烯(PCE)等为代表的有机卤素化合物。并且,为了净化被该有机卤素化合物、这些有机卤素化合物由土壤中的微生物脱氯生成的顺式-1,2-二氯乙烯(cis-1,2-DCE)等污染了的土壤,正在进行各种技术的开发、实用化。例如专利文献1中提出有:向被三氯乙烯等有机卤素化合物污染了的土壤中混合比表面积为500cm2/g以上的、且含有C(碳)0.1质量%以上的铁粉,能够有效地分解土壤中的三氯乙烯等。专利文献2中提出有:高纯度铁粉(C含量小于0.1质量%、Si含量小于0.25质量%、Mn含量小于0.60质量%、P含量小于0.03质量%、S含量小于0.03质量%、O含量小于0.5质量%)对被顺式-1,2-二氯乙烯(cis-1,2-DCE)等难分解的有机卤素化合物污染的土壤、水的净化是有效的。在专利文献3、专利文献4和专利文献5中,本申请人公开了在铁粉颗粒的表面析出有金属铜的含铜铁粉。还公开了将该含铜铁粉添加至被有机卤素化合物污染的土壤、地下水等中进行混合时,能够效率良好地分解该有机卤素化合物。现有技术文献专利文献专利文献1:日本特开平11-235577号公报专利文献2:日本特开2002-316050号公报专利文献3:日本特开2000-005740号公报专利文献4:日本特开2002-069425号公报专利文献5:日本特开2003-339902号公报
技术实现要素:
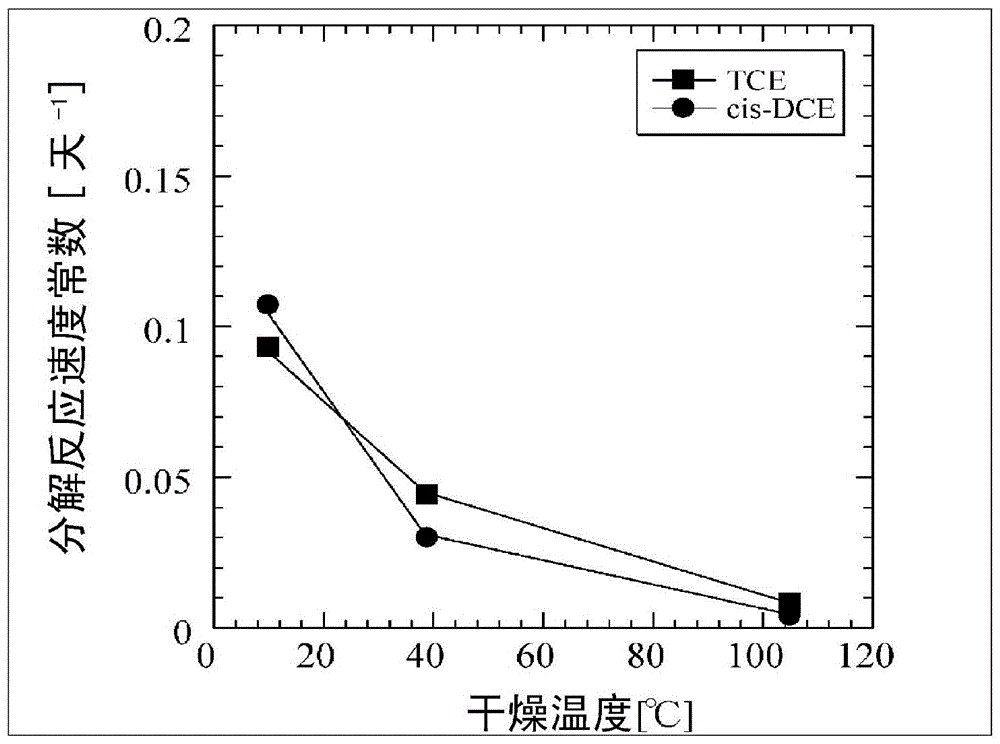
发明要解决的问题如上所述,本发明人致力于将有机卤素化合物脱氯分解而使污染浓度减少的技术开发。此时,作为该技术开发的技术要素,认为制造分解作为污染物质的有机卤素化合物的分解能力高的分解剂是重要目的之一。并且,作为该分解剂的代表例,认为有铁粉和以铁为主要成分的粉体。进一步,本发明人认为今后需要停止向上述有机卤素化合物分解用的铁粉中添加铜等环境负担物质,从而削减制造工序中的铜添加工序,简化整个工序;以及土壤净化工序后的土壤中不残留铜等的环境负担低的土壤净化处理剂。本发明针对上述状况而作出,其所要解决的课题是提供一种铁粉,其未含有铜等环境负担物质而具有与现有技术的有机卤素化合物处理用材料同等以上的有机卤素化合物处理性能。还提供使用了该铁粉的土壤或地下水污染的净化方法。用于解决问题的方案本发明人发现:将铁粉浸渍于选自水、和比水的蒸汽压更低并且含氧的有机溶剂的一种以上溶剂中,然后将浸渍于该溶剂中的铁粉进行固液分离,得到被该溶剂润湿了的铁粉,对得到的铁粉边保持温度小于40℃边进行干燥处理,由此,能够大幅度提高铁粉对有机卤素化合物的分解能力,至此完成本发明。即,为了解决上述课题,第一发明为一种有机卤素化合物处理用铁粉的制造方法,其特征在于,其具有:将铁粉浸渍于选自水、和比水的蒸汽压更低并且含氧的有机溶剂的一种以上溶剂中的工序;将浸渍于该溶剂中的铁粉进行固液分离,得到被该溶剂润湿了的铁粉的工序;以及对被该溶剂润湿了的铁粉边保持温度小于40℃边进行干燥处理的工序。第二发明为根据第一发明所述的有机卤素化合物处理用铁粉的制造方法,特征在于,边保持温度为0℃以上且10℃以下边进行所述干燥处理的工序。第三发明为根据第一或第二发明所述的有机卤素化合物处理用铁粉的制造方法,特征在于,将铁粉进行酸处理之后,进行所述将铁粉浸渍于选自水、和比水的蒸汽压更低并且含氧的有机溶剂的一种以上溶剂中的工序。第四发明为根据第一~第三发明的任一项所述的有机卤素化合物处理用铁粉的制造方法,特征在于,将所述干燥处理的工序进行0.1小时以上且72小时以下。第五发明为根据第一~第三发明的任一项所述的有机卤素化合物处理用铁粉的制造方法,特征在于,进行所述干燥处理的工序,直至溶剂重量为铁粉重量的0.5质量%以下。第六发明为根据第一~第五发明的任一项所述的有机卤素化合物处理用铁粉的制造方法,特征在于,作为所述铁粉,使用平均粒径为1μm以上且500μm以下的铁粉。第七发明为根据第一~第六发明的任一项所述的有机卤素化合物处理用铁粉的制造方法,特征在于,作为所述铁粉,使用具有板状比2以上的扁平形状的铁粉。第八发明为一种土壤或地下水污染的净化方法,其特征在于,其使用了通过第一~第七发明的任一项所述的有机卤素化合物处理用铁粉的制造方法而制造的铁粉。发明的效果根据本发明,能够低成本地得到不含有铜等添加物并且有机卤素化合物的分解能力高的有机卤素化合物处理用铁粉。附图说明图1为表示利用本发明的试样的有机卤素分解中有机卤素化合物的浓度经日变化的图表。图2为表示利用干燥温度不同的实施例的试样的有机卤素分解中有机卤素化合物的分解反应速度常数k的图表。图3为表示利用干燥温度不同的实施例的试样的有机卤素分解中有机卤素化合物的分解反应速度常数k的图表。图4为表示利用比较例的试样的有机卤素分解中有机卤素化合物的分解反应速度常数k和球磨机的旋转处理时间之间的关系的图表。具体实施方式(1)作为原料的铁粉本发明的有机卤素化合物处理用铁粉的制造中使用的铁粉为粒状。关于该铁粉的组成,只要是以铁为主要成分则没有特别的限制,总铁优选为80质量%以上、金属铁优选为75质量%以上。进一步,为了减少环境负担,优选不含有成为二次污染源的铬、铅等成分。具体而言,可以使用预先制造的铁粉,例如:由矿石还原而制造的还原铁粉、通过雾化等而制造的雾化铁粉等。并且,如果该铁粉的粒径达到预先希望的尺寸则不需要在制造工序中进行粒径调整,因此是优选的。具体而言,这些铁粉的平均粒径优选为1μm以上且500μm以下。作为该铁粉优选的一例,可列举出DOWAIPCREATIONCo.,Ltd.制的还原铁粉DKP-100。此处,将还原铁粉DKP-100的化学成分的分析结果示于表1中。将物性值示于后述的表2中。需要说明的是,表2的粒度分布是通过激光衍射法测得的评价结果。D10~D90是指粒径累积。将铁粉的重量百分率(%)作为纵轴、将粒径取对数作为刻度的横轴作图而得到的曲线称为粒径累积曲线,从该图表中将重量百分率50%时的粒径定义为D50(50%粒径)。D10、D90也按照同样的方法算出而求得。[表1]总铁金属铁FeOSCCuCrPb(质量%)(质量%)(质量%)(质量%)(质量%)(mg/kg)(mg/kg)(mg/kg)97.493.64.90.010.073306328由表1的化学成分组成可判断,本发明的铁粉中含有的铬、铅十分微量,不成为二次污染源。与铬、铅的含量相比,铜为大量含有,现有技术的有机卤素化合物处理用铁粉含有0.1质量%以上的铜,提高有机氯化物的分解效果,并且将农用地中的Cu含量基准值设定为125mg/kg,因而至少在日本国内达到符合法律制度的水平。进一步,本发明的铁粉的铜含量不足现有技术的有机卤素化合物处理用铁粉中铜含量的1/3,这可证实本发明的铁粉与现有技术的铁粉是基于不同机理而分解有机卤素化合物的。(2)铁粉的扁平化处理优选对作为原料的铁粉预先实施扁平化处理,从而制成板状比2以上的扁平形状铁粉的结构。该扁平化处理如下进行:使原料铁粉和水呈混合的状态,对原料铁粉和水的混合物施加冲击和/或压力,由此该铁粉的颗粒变形成扁平形状。为了对该原料铁粉和水的混合物施加冲击和/或压力,使用粉碎机实施塑性变形加工,从而进行。作为该粉碎机有“介质搅拌型粉碎机”:将加入容器中的冲击介质(即media)边搅拌边进行粉碎,具体而言,可以为磨碎机、球磨机。因为球磨机、磨碎机适合于细粉碎,容易控制冲击力、压力,因此容易得到所希望的粒度分布的扁平铁粉。需要说明的是,使用球磨机时,可以使用旋转驱动型、振动驱动型球磨机。在上述磨碎机、球磨机等中进行塑性变形加工时,与前述介质一起将原料铁粉和水(例如:离子交换水、工业用水、自来水等)装填至规定容器。并且,使该容器例如旋转,由此将原料铁粉变形、粉碎处理。例如,在使用旋转型球磨机进行处理的情况下,向处理用罐(可以使用磁制、不锈钢制等)中,投入介质、原料铁粉,进行旋转处理。尤其是向规定容器中加入水的目的是,为了提高铁粉的分散状态,使铁粉和介质均匀地高效地接触。因此,例如为了提高规定容器中铁粉的分散状态,出于铁颗粒的表面处理等目的,作为溶剂,也可以同时投入有机溶剂、油分、各种溶液等介质,而不仅是水。处理用罐内的气氛中,存在溶解于水或者残存于顶部空间的氧。可以处于保持存在氧的状态,也可以优选使用氮等非活性气体鼓泡等来去除该氧,防止铁粉剩余部分发生氧化。在扁平化处理中,通过提高(原料铁粉/介质)的填充比率,可使每一批次的处理量增加。另一方面,通过降低(原料铁粉/介质)的填充比率,使每单位时间的处理效率增加。因此,优选根据需要的铁粉的特性和处理量来调整(原料铁粉/介质)的填充比率。例如使用旋转球磨机进行旋转驱动型的扁平化处理时,通过确保适当的转速,铁粉和介质在罐内不会成为一个结块而运动,而是铁粉颗粒在介质间被赋予充分的冲击和/或压力。为了实现该状态,优选的是,控制上述转速,将旋转速度设为铁粉和介质保持分散状态、铁粉和介质沿着罐内壁重复上升和下落的程度。需要说明的是,旋转球磨机的适当的旋转速度取决于罐容量及铁粉和介质的填充条件,因此最好预先求出能够实现上述状态的转速。例如使用磨碎机进行扁平化处理时,提高铁粉和介质的填充量以及搅拌叶片的转速可使处理效率提高。因此,适合设为铁粉和介质不从容器中溢出的水准的填充量和转速。需要说明的是,由于铁粉的比重大,优选的方案是:调整转速以使铁粉不滞留在容器底部而是进行循环,或者使用泵等从下部将包含有铁粉的浆料抽出再返送到上部进行循环,由此提高处理效率。扁平化处理的处理时间可通过评价得到的铁粉的有机氯化物分解性能以及与该有机氯化物分解性能相关的物性等而设定适宜的条件。作为与该有机氯化物分解性能相关的物性评价项目,可列举出比表面积、粒度分布等。接着,将该扁平化处理后的铁粉扁平化、微粒化。在通过对原料铁粉施加冲击或压力而变形且各颗粒成为板状比2以上的扁平形状的铁粉的表面,容易露出变形前的铁颗粒内部的组织。将塑性变形加工后的铁粉、介质和水的混合物取出,使用筛等将介质与铁粉和水的混合浆料分离,得到铁粉。将得到的铁粉在小于40℃下进行干燥,得到具有扁平形状的铁粉。干燥工序优选进行0.1小时~72小时。(3)溶剂向铁粉的浸透/浸渍处理使选自水、和比水的蒸汽压更低并且含氧的有机溶剂的一种以上溶剂向上述(1)~(2)中说明的铁粉浸透。此处,比水的蒸汽压更低并且含氧的有机溶剂例如有甲醇、乙醇、丙醇、丙酮、甲苯等。其中,相比丙醇、丙酮、甲苯,优选甲醇、乙醇。为了使溶剂向本发明的铁粉中浸透,可以将铁粉浸渍于溶剂中,也可以向积聚的铁粉中注入或者散布溶剂。需要说明的是,上述(3)工序后得到的铁粉的表面被适度氧化,为了抑制过度的氧化,在上述(3)工序之前例如可进行稀盐酸处理而去除颗粒表面的氧化膜、或者可通过使上述(3)工序在非活性气氛(例如氮气等)中进行,从而防止因大气气氛下的处理导致的颗粒表面的氧化的推进。(4)铁粉的固液分离工序将浸渍于溶剂中的铁粉进行固液分离,得到被该溶剂润湿了的铁粉。具体而言,例如可以将浸透于溶剂中的铁粉置于滤纸上而进行固液分离。在该使用滤纸进行固液分离时,可优选通过组合使用抽滤而提高生产率的方案。该固液分离的结果是铁粉和溶剂被分离,得到的铁粉是固液分离成为被该溶剂润湿但不会滴下溶剂的程度。(5)铁粉的干燥工序对该固液分离后的铁粉实施边保持温度小于40℃(优选为30℃以下,最优选为0℃以上且10℃以下)边进行干燥的干燥工序。干燥工序优选进行0.1小时~72小时。另外,干燥工序优选在大气气氛或者比其氧化气体浓度低的气氛下进行。通过该干燥工序,使铁粉中的溶剂量为纯铁粉重量的0.5质量%以下。由于该干燥工序后的铁粉为轻微的聚集状态,因此进行不赋予大的冲击地破碎,得到本发明的有机卤素化合物处理用铁粉。破碎可以使用乳钵进行破碎、样品磨等。为了处理的容易度、颗粒分散性提高而进行破碎,在实验或者实施工序的条件下只要铁粉不是明显地聚集、粘附的程度,即便不实施也没有很大影响。可认为上述干燥工序后的铁粉由于处于构成该铁粉的铁颗粒的表面为适度氧化状态,因此发挥出优异的有机卤素化合物的分解能力。因此,本发明的铁粉的优选施工方法是,在施工现场实施上述干燥工序,将处于上述干燥状态的本发明的铁粉散布于土壤中。此外,只要能够对铁颗粒表面赋予所希望的氧化状态,则还可在与施工场所不同的另外场所完成至上述干燥工序为止,也可将得到的本发明的铁粉进行真空包装等,从而保持该铁粉的氧化状态而进行保管、运输。实施例以下,参照实施例,对本发明进行更具体地说明。(实施例1)向容量200mL的玻璃烧杯中投入100mL的蒸馏水和10g的铁粉(如表1、2所示,DOWAIPCREATIONCo.,Ltd.制的还原铁粉DKP-100),之后使用凯米搅拌器(Kemistirrer)搅拌5分钟。对得到的铁粉和水的混合物,使用吸滤器、过滤瓶、吸引器将滤纸上的铁粉进行吸滤。该吸滤中,滤纸使用ADVANTEC公司制的No.5C型。接着,该吸滤后停止吸引器,回收滤纸上的铁粉,作为铁粉A。该铁粉A的水分含有率为17%。需要说明的是,水分含量是指在大气压110℃的条件下从铁粉试样发生气化、脱离的水分量,定义为“水分含有率=含水重量/含有水分状态的铁粉重量”。此处,含水重量由含有该水分的状态的铁粉重量、与将含有该水分的状态的铁粉在设定为110℃的循环型干燥机中静置12小时以上的条件下进行绝对干燥后的铁粉重量之差而求出。采用与上述铁粉A同样的制备方法,进行吸滤后,暂时停止吸引器吸引。接着,使滤纸上的铁粉浸透于50mL的乙醇,静置1分钟,使铁粉中充分浸透乙醇。此时,再启动吸引器吸引,将乙醇从铁粉中吸引后停止吸引器,回收滤纸上的铁粉,作为铁粉B。该铁粉B的乙醇含有率为14%。将回收的铁粉A、B分别静置于大气气氛下温度设定为30℃的干燥机内,进行24小时干燥。接着,该干燥后,使用乳钵分别将得到的铁粉A、B的聚集而成的结块轻轻地破碎,得到本例的铁粉试样A、B。干燥后的铁粉试样A的水分含有率为0.2%,B的水分含有率为0.2%。A、B的板状比均为1.29。铁粉试样的板状比根据下式求出。需要说明的是,平均平面径如下求出:对50个颗粒测定扇平面方向中的长径和与其垂直的短径,求出平面径=(长径+短径)/2,取其平均而求出。平均厚度为测定50个颗粒的厚度并取其平均而求出。铁粉颗粒的平均径=(2×平均平面径+平均厚度)/3铁粉颗粒的板状比=平均平面径/平均厚度需要说明的是,如上所述,水分含量被定义为在大气压110℃的条件下从铁粉试样气化、脱离的水分量。水分含有率的测定使用卡尔-费休水分计(京都电子工业株式会社制的MKC-520卡尔-费休水分计)而进行。<评价试验>使用得到的铁粉试样A、B,进行cis-DCE分解试验。首先,将得到的实施例1的铁粉试样A、B各0.5g与离子交换水50mL一起,分别装入容量124mL的小瓶中,进行氮气气体的鼓泡,进行体系内氧的曝气、氮置换,然后用实施氟树脂(Teflon(注册商标))涂敷了的丁基橡胶的隔垫和铝盖进行密封。接着,使用微型注射器向各密封瓶内注入1μL的顺式-1,2-二氯乙烯(cis-1,2-DCE)。再同样使用微型注射器注入1μL的苯,作为用于DCE浓度变化评价的内标物。边进行150rpm的振动,边每日追踪DCE的浓度,至试验期间的15天为止,求出分解速度常数k。需要说明的是,将使用该铁粉试样的有机氯化物的分解反应假设为(式1)所示的一级反应,将其分解反应速度常数设为k。C/C0=e-k·t(式1)(C0:有机氯化物的初期浓度、C:时间t时的有机氯化物浓度、t:处理时间[天]、k:分解反应速度常数[天-1])其结果可知,铁粉试样A(蒸馏水浸渍)的cis-DCE的分解反应速度常数为0.064[天-1],铁粉试样B(乙醇浸渍)的cis-DCE的分解反应速度常数为0.082[天-1]。(实施例2)在容量200mL的玻璃烧杯中准备1mol%浓度的盐酸100mL,投入10g的铁粉(DOWAIPCREATIONCo.,Ltd.制的还原铁粉DKP-100),之后使用凯米搅拌器搅拌5分钟。对得到的铁粉和水的混合物,使用吸滤器、过滤瓶、吸引器将滤纸上的铁粉进行吸滤。该吸滤中,滤纸使用ADVANTEC公司制的No.5C型。接着,从铁粉将盐酸溶液吸滤后,保持持续吸引状态,使铁粉浸渍于200mL的离子交换水中,洗涤该铁粉。洗涤结束后,结束吸滤,得到本例的铁粉。将物性值示于表2中。[表2]该铁粉的水分含有率为17%。与实施例1同样地,在30℃下进行干燥处理后的该铁粉试样的水分含有率为0.2%。板状比为1.61。进行与实施例1同样的cis-DCE分解试验,其结果,本例的铁粉试样的cis-DCE的分解反应速度常数为0.038[天-1]。(比较例1)将实施例1、2中作为原料的铁粉(DOWAIPCREATIONCo.,Ltd.制的还原铁粉DKP-100)不进行浸渍、干燥而直接使用,进行实施例1、2中说明的cis-DCE分解试验。该铁粉的水分含有率为0.1%。板状比为1.42。cis-DCE分解试验的结果,本例的铁粉试样的cis-DCE的分解反应速度常数小于0.01[天-1],只见到几乎不能检测出来的程度的分解。(比较例2)将海绵状铁粉试样(表3中表示物性值、表4中表示化学成分的分析值)不进行浸渍、干燥而直接使用,进行实施例1、2中说明的cis-DCE分解试验。该铁粉的水分含有率为0.2%。板状比为1.07。cis-DCE分解试验的结果,本例的铁粉试样cis-DCE的分解反应速度常数小于0.01[天-1],只见到几乎不能检测程度的分解。[表3][表4](实施例3)向内容量2.3L的SUS304制的罐中,投入罐容量的80体积%左右(6580g)的直径10mm的氧化锆(ZrO2)滚珠。向其中投入100g的铁粉(上述还原铁粉DKP-100)后,再投入蒸馏水1L,用带有橡胶密封件的盖密闭,装入材料。将该装入材料的SUS罐置于球磨机旋转台上,转速120rpm下运转20小时,进行旋转处理。旋转处理时间结束后,取出SUS罐内容物,使用开口径5mm的筛,分离ZrO2滚珠与铁粉和水的混合浆料。对得到的铁粉和水的混合浆料,使用吸滤器、过滤瓶、吸引器将滤纸上的铁粉进行吸滤。滤纸使用ADVANTEC公司制的No.5C型。接着,该吸滤后停止吸引器,回收铁粉。将回收的铁粉试样在大气气氛下静置于设定为10℃的干燥机内,进行12小时干燥。接着,该干燥后,使用乳钵将得到的由铁粉的聚集等而成的结块轻轻地破碎,得到本例的铁粉试样。干燥后的该铁粉试样的水分含有率为0.3%、体积密度为1.43g/cm2、BET值为2.97m2/g。板状比为33.4。使用该铁粉试样0.5g,进行实施例1、2中说明的cis-DCE分解试验。再在同样的条件下进行TCE分解试验。该铁粉试样的cis-DCE的分解反应速度常数为0.107[天-1],TCE的分解反应速度常数为0.093[天-1]。(实施例4)除了将干燥温度设定为40℃以外,进行与实施例3同样的操作,得到本例的铁粉试样。表2中示出物性值。干燥后的该铁粉试样的水分含有率为0.2%、体积密度为0.92g/cm2、BET值为3.09m2/g。板状比为31.2。该铁粉试样的cis-DCE的分解反应速度常数为0.030[天-1],TCE的分解反应速度常数为0.044[天-1]。(比较例3)除了将干燥温度设定为105℃以外,进行与实施例3同样的操作,得到本例的铁粉试样。干燥后的该铁粉试样的水分含有率为0.2%、体积密度为0.71g/cm2、BET值为3.24m2/g。板状比为29.1。可知比较例3的铁粉试样的cis-DCE的分解反应速度常数为0.004[天-1],TCE的分解反应速度常数为0.008[天-1]。(实施例3、实施例4、比较例3的总结)将利用上述实施例4的试样的有机卤素分解中有机卤素化合物的浓度经日变化的图示于图1中。纵轴表示有机卤素化合物的浓度(将试验开始时的有机卤素化合物的浓度标准化为1,表示浓度降低相对于该标准值的比率),横轴表示天数。将三氯乙烯(TCE)的浓度用□,将顺式-1,2-二氯乙烯(cis-1,2-DCE)的浓度用○进行作图而得。由图1可知该铁粉将有机卤素化合物迅速地分解。另外,上述实施例3、实施例4、比较例3中,每日追踪DCE浓度,至试验期间的15天为止,求出分解速度常数k。将其结果在图2中用●作图。另外,除了使用TCE代替DCE以外,将相同条件下实施的试验结果在图2中用■作图。纵轴表示k值,横轴表示铁粉试样的干燥温度。如图2的结果可知,实施例3、实施例4、比较例3的铁粉试样中,干燥温度小于40℃时k值的上升程度升高。由该结果可知,实施例3、实施例4的铁粉试样通过扁平化和规定条件的干燥处理,对于有机卤素化合物的分解活性上升。(实施例5)使用与实施例3同样的罐、滚珠、铁粉,进行与实施例3同样的旋转处理,得到铁粉和水的混合浆料。对得到的铁粉和水的混合浆料,使用与实施例3同样的吸滤器、过滤瓶、吸引器、滤纸将滤纸上的铁粉进行吸滤。接着,边持续该吸引边在过滤水分的阶段使工业用乙醇100ml浸透于滤纸上残留的铁粉,将该铁粉上残留的水分用乙醇置换。将回收的铁粉在大气气氛下,静置于设定为10℃的恒温循环式干燥机内,进行12小时干燥。接着,该干燥后,使用乳钵将得到的由铁粉的聚集等而成的结块轻轻地破碎,得到本例的铁粉试样。干燥后的该铁粉试样的水分含有率为0.3%、体积密度为1.27g/cm2、BET值为3.03m2/g。板状比为35.1。可知该铁粉试样的cis-DCE的分解反应速度常数为0.185[天-1],TCE的分解反应速度常数为0.137[天-1]。(实施例6)除了将干燥温度设定为40℃以外,进行与实施例5同样的操作,得到本例的铁粉试样。干燥后的该铁粉试样的水分含有率为0.2%、体积密度为0.81g/cm2、BET值为3.09m2/g。板状比为33.6。该铁粉试样的cis-DCE的分解反应速度常数为0.019[天-1],TCE的分解反应速度常数为0.030[天-1]。(比较例4)除了将干燥温度设定为105℃以外,进行与实施例5同样的操作,得到本例的铁粉试样。干燥后的该铁粉试样的水分含有率为0.2%,体积密度为0.67g/cm2、BET值为3.32m2/g。板状比为31.8。该铁粉试样的cis-DCE的分解反应速度常数为0.008[天-1],TCE的分解反应速度常数为0.015[天-1]。(实施例5、实施例6,比较例4的总结)上述实施例5、实施例6、比较例4中,每日追踪DCE浓度,至试验期间的15天为止,求出分解速度常数k。将其结果在图3中用○作图。另外,除了使用TCE代替DCE以外,将相同条件下实施的试验结果在图3中用□作图。需要说明的是,图3中,纵轴表示k值,横轴表示铁粉试样的干燥温度。如图3的结果可知,实施例5、实施例6、比较例4的铁粉试样中,干燥温度小于40℃时k值的上升程度升高。由该结果可知,实施例5、实施例6的铁粉试样通过扁平化和规定条件的干燥处理,对于有机卤素化合物的分解活性上升。(比较例5)向内容量2.3L的SUS304制的罐中,投入罐容量的80体积%左右(6580g)的直径10mm的氧化锆(ZrO2)滚珠。向其中投入100g的铁粉(DOWAIPCREATIONCo.,Ltd.制的还原铁粉DKP-100)后,用带有橡胶密封件的盖密闭,装入材料。将该装入材料的SUS罐置于球磨机旋转台上,在转速120rpm下运转2、5、10、20小时的各条件下进行旋转处理。旋转处理时间结束后,取出SUS罐内容物,使用开口径5mm的筛,将ZrO2滚珠与铁粉分离,得到本例的铁粉试样。未进行干燥处理。得到的铁粉试样的板状比,对应于球磨机处理时间2/5/10/20小时分别为5.6/12.3/20.6/33.4。另外,实施与实施例3同样的TCE分解试验,将其结果在图4中用△作图。图4为表示该铁粉试样的TCE的分解反应速度常数k的经时变化的图表,横轴表示球磨机的旋转处理时间,纵轴表示TCE分解反应速度常数k。由图4的结果可知,本例的铁粉试样尽管使用了与实施例3~6的铁粉试样同样的球磨机而实施球磨处理,但TCE分解性能停留在低水平。(比较例6)将100g的比表面积大约20000cm2/g、含碳量0.2质量%的铁粉、并且具有50质量%以上通过150μm筛的粒度的铁粉(DOWAIPCREATIONCo.,Ltd.制的E-200)和1.27g(相当于0.8gCu)的氧化铜粉(日興ファインケミカルズ株式会社制的CuO粉)装填至容量300mL的样品混合器(具有锚状叶轮的混合器)中。装填二者后进行1分钟的搅拌,在此时,边继续搅拌边将1M的硫酸5mL添加至该混合器,继续搅拌20秒钟。之后,从混合器中取出内容物,在干燥炉中保持105℃将液体成分蒸发分离,得到本例的铁粉试样。将该铁粉试样实施与实施例3同样的DCE分解试验,其结果,第15天的cis-DCE的分解速度常数k值=0.104[天-1]。(比较例7)将100g的上述还原铁粉(DKP-100)和3.93g的硫酸铜五水合盐(CuSO4·5H2O:和光纯药株式会社制的试剂)装填至容量300mL的样品混合器(具有锚状叶轮的混合器)中。装填二者后进行1分钟搅拌,得到本例的铁粉试样。将该铁粉试样实施与实施例3同样的TCE、DCE分解试验,其结果,TCE分解反应速度常数和DCE分解反应速度常数如下。(TCE):k=0.12[天-1](cis-DCE):k=0.14[天-1](总结)可知实施例3的铁粉试样具有与现有技术中含有氧化铜的比较例6的铁粉试样同等以上的cis-DCE的分解速度常数。可知实施例5的铁粉试样具有与现有技术中含有氧化铜的比较例6的铁粉试样和现有技术中含有大量铜的比较例7的铁粉试样相比优异的TCE的分解速度常数、cis-DCE的分解速度常数。对于本发明的铁粉在土壤中能够有效地分解有机卤素化合物的详细原因还不明确,本发明人认为是如下理由。1.)通过调整氧化物的形态(FeO、Fe2O3、Fe3O4等)及其存在比率、氧化物层的厚度、由氧化造成的颗粒表面的微细结构的变化等颗粒表面的氧化状态,由此在与有机卤素的共存下铁颗粒表面上的活性位点和有机卤素分子的接触效率增加。2.)在上述1.的基础上,进一步将铁粉颗粒以塑性变形进行挤压、使之伸展,由此铁粉颗粒内部的铁母材在表面露出,并且由该伸展使铁粉颗粒的形状变形成为扁平形状,由此提高比表面积,使作为粉体的每单位重量的活性位点数提高。根据本发明,能够低成本地得到不含有铜等添加物并且有机卤素化合物的分解能力高的有机卤素化合物处理用铁粉。并且,通过使用该有机卤素化合物处理用铁粉,对被有机卤素化合物污染的土壤等的净化也做出很大贡献。另外,本发明的有机卤素化合物处理用铁粉的制造工序中,能够削减添加物的工序,由此能够简化制造工序,也能够降低制造工序和土壤净化时的环境负担。进一步,根据本发明,也能够使用通常市售的铁粉作为原料,因此能够从宽范围来选择原料供应商,对于工业利用也有效。产业上的可利用性在将本发明的铁粉用于土壤或地下水污染的处理时,可以考虑各种方法,关于代表性的方法进行说明。〈1〉在土壤中的使用例(原位处理法)为了覆盖通过事前调查判明的土壤污染区域,使用钵装置等将铁粉均匀地混合于土壤中。铁粉施工后,采样适宜的土壤监测污染物质浓度,由此确认净化倾向。在整个施工区域内使土壤环境基准值降低等到达设定基准时,视为净化完成。或者,将污染区域的土壤挖出来后,在地上将该铁粉均匀地混合,进行净化监测,确认到达设定基准后,填埋回原先的地方。〈2〉在地下水中的使用例在填充有该铁粉或者该铁粉和其他填充材的混合物的柱中,使从地下汲上来的污染地下水通水,在柱内地下水中的污染物质进行脱氯分解,由此在柱出口处流出满足低于环境基准值等设定基准的处理后的水。另外,也有透过性反应壁法的地下水净化方法:将该铁粉或者该铁粉和为了提高透水性的填充材料的混合物施工成壁状,以使含有污染物质(有机氯化物)的地下水通过,在该透过性反应壁内地下水中的污染物质进行分解处理,由此使通过后的地下水成为澄清的状态。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1