剥离的纳米碳材料的水性和有机悬浮液、其制备方法及其用途与流程
本申请要求分别于2014年6月12日、2015年2月13日和2015年5月13日提交的临时欧洲专利申请号EP 14172164、EP 15155087和EP151677536,以及于2014年7月25日提交的欧洲专利申请号EP 14306204的优先权,其各自的全部内容以引用方式结合于本文。
技术领域
本发明涉及用于制备完全剥离的(fully exfoliated),即,单独的(individualized)纳米碳材料,的水性和有机悬浮液的方法,以及其用途,包括复合材料、薄膜和沉积物的制造。
本发明更具体地涉及水性和有机纳米碳悬浮液(即,油墨组合物),尤其是完全剥离纳米碳的水性和有机悬浮液,以及这样的纳米碳悬浮液的用途。因此,本发明还涉及水性和有机油墨的制备、以及其用途。
从工业应用的角度来看,更尤其是关于加工这些悬浮液(对于给定的应用),能够获得形式为水性或有机悬浮液的纳米碳是非常感兴趣的。具体地,这样的悬浮液可以容易地用来在给定基底(substate)上沉积纳米碳,以形成纳米碳膜或制造含有纳米碳的复合材料。
在下面的描述中,在方括号([])之间的参考文献是指在实施例以后给出的参考文献清单。
背景技术:
碳已知为具有四种独特的晶体结构或结构家族:金刚石、石墨、富勒烯和碳纳米管。
碳纳米管的管状结构赋予它们独特的机械、电学或化学性能。因此,碳纳米管通常用于复合材料(Shaffer,M.S.P.,Windle,A.H.,“Fabrication and Characterization of Carbon Nanotube/poly(vinyl alcohol)Composites”,Adv.Mater.,11,pp 937-941(1999)[1])、氢燃料电池(Ye,Y.,Ahn,C.C.,Witham,C.,Fultz,B.,Liu,J.,Rinzler,A.G.,Colbert,D.,Smith,K.A.,Smalley,R.E.,“Hydrogen Absorption And Cohesive Energy Of Single-Walled Carbon Nanotubes”,App.Phys.Lett.,74,pp 307-2309(1999)[2];Liu,C.,Fan,Y.Y.,Liu,M.,Cong,H.T.,Cheng,H.M.,Dresselhaus.M.S.,“Hydrogen Storage In Single-Walled Carbon Nanotubes At Room Temperature”,Science,286,pp1127-1129(1999)[3];Kong,J.,Chapline,M.G.,Dai,H.,“Functionalized Carbon Nanotubes For Molecular Hydrogen Sensors”,Adv.Mater.13,1384-1386(2001)[4]、超级电容器(Aldissi,M.;Schmitz,B.;Lazaro,E.;Bhamidipati,M.;Dixon,B.,“Conducting Polymers in Ultracapacitor Applications”,56th Annu.Tech.Conf.--Soc.Plast.Eng.,(Vol.2),pp 1197-1201(1998)[5];An,K.H.;Kim,W.S.;Park,Y.S.;Moon,J.-M.;Bae,D.J.;Lim,S.C.;Lee,Y.S.;Lee,Y.H.“Electrochemical Properties of High-Power Supercapacitors Using Single-Walled Carbon Nanotube Electrodes”,Adv.Funct.Mater.11,pp 387-392(2001)[6]、催化(Yu,R.,Chen,L.,Liu,Q.,Lin,J.,Tan,K.-L.,Ng,S.C.,Chan,H.S.O.,Xu,G.-Q.,Hor,T.S.A.“Platinum Deposition On Carbon Nanotubes Via Chemical Modification”,Chem,Mater.10,pp 718-722(1998)[7];(Planeix,J.M.;Coustel,N.;Coq,B.;Brotons,V.;Kumbhar,P.S.;Dutartre,R.;Geneste,P.;Bernier,P.;Ajayan,P.M.,“Application Of Carbon Nanotubes As Supports_in Heterogeneous Catalysis”,J.Am,Chem,Soc.116,pp 7935-7936(1994)[8])以及纳米尺寸的电子部件或系统(Tans,S.J.,Verschueren,A.R.M.,Dekker,C.,“Room-Temperature Transitor Based On A Single Carbon Nanotube”,Nature 393,pp 49-52(1998)[9];Bachtold,A.;Hadley,P.;Nakanishi,T.;Dekker,C.,“Logic Circuits With Carbon Nanotube Transistors”.Science 294pp,1317-1320(2001)[10])。
科学界还对替代的碳纳米材料产生了兴趣,其具有可比性能如石墨烯,或其它有价值的性能如碳纳米角(nanohorn)、纳米金刚石和富勒烯。
一种挑战是将这些纳米碳材料加工成溶液或悬浮液以使得能够进行它们的操作和工业加工,特别是用于在基底上制备复合材料、薄膜或沉积物。对于制备纳米碳形式(即,碳纳米管和石墨烯)的溶液或悬浮液的绝大多数的研究努力导致具有以下主要缺点的方法:产生的碳纳米管和石墨烯平面(plane)最终(end up)被功能化和/或变性,其对于它们的电气性能是有害的,或不良剥离的。[Paton,K.R.et al.Scalable production of large quantities of defect free few-layer graphene by shear exfoliation in liquids.Nat.Mater.(2014)[23]]
Penicaud et al.(WO 2005/073127[11])报告了第一个成功的用于在有机溶剂中制备碳纳米管溶液的方法。Penicaud等还开发了用于在有机溶剂中溶解石墨烯和碳纳米角的方法:分别为WO 2009/056696[12]和WO2011/154894[13]。上述方法允许进入单独的(完全剥离的)碳纳米管、[单独的单壁碳纳米管的浓缩液,A.Pénicaud,F.Dragin,G.Pécastaings,M.He,E.Anglaret,Carbon(2014),67,360-367[24]]石墨烯平面、和碳纳米角(无缺陷),其可用于各种应用,包括在基底上沉积这些纳米碳形式以及将它们加入复合材料。然而,这些方法的一个缺点是:必须在惰性气氛下处理纳米碳有机溶液,对于工业规模应用而言,其可能是昂贵的。
因此,对于用于溶解纳米碳的方法存在真正的需要,上述方法纠正在本领域中已知的这些问题、缺陷和障碍,更具体地上述方法允许获得完全剥离的纳米碳的水性或有机悬浮液,其可以在环境大气中容易用于加工纳米碳材料(用于给定的应用),从而降低纳米碳组合物的制造成本,便于存储以及提高大量纳米碳的可达性。
具体实施方式
在第一方面,通过提供用于制备完全剥离的纳米碳材料的水性或有机悬浮液的方法,本发明具体地旨在满足这种需要,包括以下步骤:
a)在惰性气氛下,将纳米碳插层化合物(intercalation compound)溶解于非质子有机溶剂(A)或非质子有机溶剂的混合物(A’);从而导致还原纳米碳的有机溶液;
b)再氧化(去除电子)以将还原纳米碳材料复原到其中性状态,从而导致中性纳米碳材料在有机溶剂(A)或非质子有机溶剂的混合物(A’)中的有机悬浮液;以及
c)混合在步骤b)中得到的中性纳米碳的有机悬浮液和适量的脱气水、脱气离子水溶液、脱气有机溶剂(B)、有机溶剂的脱气混合物(B’)、或(B)或(B’)与水或离子水溶液的脱气混合物;
其中溶剂(A)或溶剂混合物(A’)是完全或部分水混溶性的或完全或部分地与溶剂(B)或溶剂混合物(B’)混溶;
从而导致纳米碳材料的空气亚稳的水性或有机悬浮液。
如在整个本文件中使用的,措辞“(B)或(B’)与水或离子水溶液的脱气混合物”是指,(B)或(B’)与水或离子水溶液的总体混合物(overall mixture)被脱气。
有利地,在可能涉及它们的任何变体中(例如在步骤a)中),在步骤a)中使用它以前,可以将溶剂A或溶剂A’的混合物脱气,以溶解纳米碳插层化合物(还称为“纳米碳化物盐”)。
在再氧化步骤b)以后,系统变得有点不稳定,并且步骤c)应该跟进步骤b)以稳定系统(由于吸附在纳米碳材料的表面上的离子,如下文进一步描述的)。
有利地,可以优选地立即在步骤b)以后进行步骤c)。
当纳米碳材料是碳纳米管时,可能有利的是不进行步骤b)并直接进行步骤c)。因此,提供了用于制备完全剥离的(单独的)碳纳米管的水性或有机分散体的方法,包括以下步骤:
a)在惰性气氛下,将碳纳米管碱性盐(alkali salt)溶解于非质子有机溶剂(A)或非质子有机溶剂的混合物(A’);从而导致还原碳纳米管的有机溶液(还称为“碳纳米管化物溶液(carbon nanotubide solution)”);以及
c)混合在步骤a)中得到的还原碳纳米管的有机溶液和适量的脱气水、脱气离子水溶液、脱气有机溶剂(B)、有机溶剂的脱气混合物(B’)、或(B)或(B’)与水或离子水溶液的脱气混合物;
其中溶剂(A)或溶剂混合物(A’)是完全或部分水混溶性的或完全或部分地与溶剂(B)或溶剂混合物(B’)混溶;
从而导致碳纳米管的空气亚稳的水性或有机分散体。
碳纳米管碱性盐可以具有通过在本领域中已知的方法可以实现的任何C:M比率,M表示任何碱金属,如Na、Li、K、Rb或Cs,优选Na、Li或K。可以通过各种已知的方法来还原碳纳米管,并且可以分离产生的MCx盐,具有范围广泛的x值(6至500以上)(x是整数)。例如,可以在任何碱金属的存在下直接还原碳纳米管,如Na、Li、K、Rb或Cs,优选Na、Li或K。因此,可以在碱金属的存在下直接进行还原,例如在液体或蒸汽相中或在氨中。在碱金属的存在下的还原方法是在本领域中众所周知的(见例如[18]、[25]),并导致具有如上所述的化学计量的广泛的可能范围的CNT碱性盐,通常具有最大化学计量MC6至MC8,其中M表示碱金属(最大化学计量KC6至KC8,当碱金属是钾金属时)。可替换地,可以通过在惰性气氛下使具有化学式A+B-的适宜的聚芳基碱性盐和碳纳米管反应来还原碳纳米管,其中A+表示碱金属阳离子以及B-表示有机基团的阴离子,如下文更详细描述的(见例如[11]、[18]、[49]、[50])。同样,用这种方法,还可以分离得到的ACx盐,具有范围广泛的x值(10至500)(例如A=K)。
例如,当碱金属是K时,碳纳米管碱性盐可以具有KC6、KC8、KC25、KC100或KC200化学计量。因为具有较高C含量(较低K含量)的碳纳米管碱性盐预期表现出更少缺陷,当经受混合步骤c)(例如,用脱气水、脱气离子水溶液等骤冷(quenching))时,具有较高C含量的碳纳米管碱性盐通常是优选的。有利地,碳纳米管碱性盐是KC25或C含量大于或等于KC25的纳米管钾盐,例如KC25、KC100、KC200、KC370、KC500,或C:K化学计量为KC25至KC500之间的任何位置的纳米管钾盐。
碳纳米管可以是单壁(SWCNT)、双壁(DWCNT)、少壁(FWCNT)或多壁(MWCNT)碳纳米管,优选单壁、双壁或少壁碳纳米管,最优选单壁碳纳米管。
有利地,在其中可能涉及步骤c)的任何变体中,当在步骤c)中使用脱气有机溶剂(B)或有机溶剂的脱气混合物(B’)时,(B)和混合物(B’)优选含有能够与纳米碳的碳表面相互作用的离子物质。优选地,离子物质能够吸附在纳米碳的碳表面上。因此,(B)和溶剂混合物(B’)优选允许盐物质的完全或部分解离。离子物质可以是能够吸附在纳米碳的碳表面上的任何离子。例如,离子物质可以是疏水性离子。例如,适宜的疏水性离子包括苯基取代的离子,例如,如四苯基鏻、四苯基硼酸盐或四苯基鉮。离子物质还可以包括其它离子如OH-、H3O+、铵(NH4+)或取代的铵离子、或易于与纳米碳π-π相互作用的离子物质,例如,但不限于,苯基取代的疏水性离子(例如,四苯基鏻、四苯基硼酸盐或四苯基鉮,仅举几例)。有利地,离子物质可以是携带π堆叠实体(πstacking entity)、能够促进吸附在纳米碳表面上的任何物质。这样的离子物质的实例是携带多芳族实体的那些,如萘基、蒽基、芘基、苝基等,(携带极性部分(“极性头部”)),以及它们的相应的家族。其中,来自环境友好盐的离子物质将是优选的。那些离子物质的实例是1-芘磺酸盐、2-萘氧基乙酸盐、或2-萘磺酸盐,优选1-芘磺酸盐或2-萘氧基乙酸盐。还可以使用尿酸盐离子。
同样,在其中可能涉及步骤c)的任何变体中,有利地,当在步骤c)中使用(B)或(B’)与水或离子水溶液的脱气混合物时,得到的脱气混合物优选含有能够与纳米碳的碳表面相互作用(例如,吸附于其上)的离子物质。离子物质可以是能够吸附在纳米碳的碳表面上的任何离子。例如,离子物质可以是疏水性离子或任何物质(其携带π堆叠实体,能够促进吸附在纳米碳表面上,如上述那些)。例如,得到的脱气混合物可以含有离子物质,其是OH-、H3O+、铵(NH4+)或取代的铵离子、或易于与纳米碳π-π相互作用的离子物质,例如,但不限于,苯基取代的疏水性离子(例如,四苯基鏻、四苯基硼酸盐或四苯基鉮,仅举几例)或多芳基取代的离子如萘基、蒽基、芘基、苝基等(其携带极性部分)(例如,1-芘基磺酸盐离子、2-萘氧基乙酸盐离子、2-萘基磺酸盐离子,优选1-芘基磺酸盐离子或2-萘氧基乙酸盐离子)。
认为,在纳米碳表面上的上述离子吸附有助于稳定在步骤c)中得到的纳米碳材料的悬浮液。
可以通过一种方法来制备(B)或(B’)与离子水溶液的脱气混合物,上述方法包括以下步骤:混合(B)或(B’)与水,然后添加一种或多种适宜的盐物质(其产生能够与纳米碳的碳表面相互作用(例如,吸附在其上)的一种或多种上述离子物质)。可替换地或另外地,可以通过一种方法来制备(B)或(B’)与离子水溶液的脱气混合物,上述方法包括以下步骤:混合(B)或(B’)与含有一种或多种上述离子物质的离子水溶液。可以随后将得到的混合物脱气。
在一种变体中,在进行步骤b)之前,步骤a)可以接着是将适宜的离子物质加入在步骤a)中得到的还原纳米碳的有机溶液。因此,提供了用于制备完全剥离的纳米碳材料的水性或有机分散体的方法,包括以下步骤:
a)在惰性气氛下,将纳米碳插层化合物溶解于非质子有机溶剂(A)或非质子有机溶剂的混合物(A’);从而导致还原纳米碳的有机溶液;
a’)在惰性气氛下,将适宜的离子物质加入在步骤a)中得到的还原纳米碳的有机溶液;
b)再氧化(去除电子)以将还原纳米碳材料复原到其中性状态,从而导致中性纳米碳材料在有机溶剂(A)或非质子有机溶剂的混合物(A’)中的有机分散体;以及
c)混合在步骤b)中得到的中性纳米碳的有机分散体和适量的脱气水、脱气离子水溶液、脱气有机溶剂(B)、有机溶剂的脱气混合物(B’)、或(B)或(B’)与水或离子水溶液的脱气混合物;
其中溶剂(A)或溶剂混合物(A’)是完全或部分水混溶性的或完全或部分地与溶剂(B)或溶剂混合物(B’)混溶;
从而导致纳米碳材料的空气亚稳的水性或有机分散体。
如在本文所使用的,措辞“惰性气氛”是指这样的气体或气体混合物,其并不利于将还原纳米碳材料再氧化成它的中性状态。例如,可以在无氧和无水气氛下进行步骤a)和/或步骤a’)。有利地,可以在氩气、氦气或氮气气氛下进行步骤a)和/或步骤a’)。
在步骤a’)中添加的离子盐物质可以是前面提到的离子物质的任何一种或多种,可以原样地(as such)、或以在适宜的有机溶剂中的溶液中添加。可以脱气有机溶剂。当以在有机溶剂中的溶液添加时,优选作为在步骤a)中使用的相同溶剂(A)或溶剂混合物(A’)中的溶液来添加离子物质。可以将溶剂(A)或溶剂混合物(A’)脱气。
在变体“a)+a’)”中,因为将离子物质添加到步骤a)和b)之间,步骤c)可以简单地包括混合在步骤b)中得到的中性纳米碳的有机分散体和适量的脱气水、脱气有机溶剂(B)、有机溶剂的脱气混合物(B’)、或(B)或(B’)与水的脱气混合物。可替换地,经由步骤c),通过混合在步骤b)中得到的中性纳米碳的有机分散体和适量的脱气离子水溶液、含有离子物质的脱气有机溶剂(B)、含有离子物质的有机溶剂的脱气混合物(B’)、或(B)或(B’)与离子水溶液的脱气混合物,可以添加更多离子物质。经由步骤c)添加的离子物质可以相同或不同于经由步骤a’)添加的那些。在示例性实施方式中,经由步骤a’)和c)来添加相同的离子物质。
关于“变体a)+a’)”,可以选择/调节单独(经由步骤a’)或经由步骤a’)和c))添加的离子物质的浓度,其取决于A(A’)和在溶液中纳米碳化物盐的浓度。确实,纳米碳化物是聚电解质盐,在盐添加高于一定阈值以后,由于静电排斥的屏蔽,它易于絮凝。因此,可以添加的离子盐的量优选是如此,以致它并不引发/引起纳米碳化物的絮凝。通常,在步骤a)以后添加的离子物质的量是如此,以致在还原纳米碳的有机溶液中的离子物质浓度优选可以不超过10mM。例如,当四苯基硼酸钠用作离子盐时,有利地,添加的量可以是如此,以致在还原纳米碳的有机溶液中四苯基硼酸盐离子的浓度是约1mM。
同样,如针对关于碳纳米管描述的早先变体所提及的,关于变体“a)+a’)”,当纳米碳材料是碳纳米管时,可能有利的是不进行步骤b)。因此,提供了用于制备完全剥离的(单独的)碳纳米管的水性或有机分散体的方法,包括以下步骤:
a)在惰性气氛下,将碳纳米管碱性盐溶解于非质子有机溶剂(A)或非质子有机溶剂的混合物(A’);从而导致还原碳纳米管的有机溶液(还称为“碳纳米管化物溶液”);
a’)在惰性气氛下,将适宜的离子物质加入在步骤a)中得到的还原碳纳米管的有机溶液;以及
c)混合在步骤a’)中得到的有机溶液和适量的脱气水、脱气离子水溶液、脱气有机溶剂(B)、有机溶剂的脱气混合物(B’)、或(B)或(B’)与水或离子水溶液的脱气混合物;
其中溶剂(A)或溶剂混合物(A’)是完全或部分水混溶性的或完全或部分地与溶剂(B)或溶剂混合物(B’)混溶;
从而导致碳纳米管的空气亚稳的水性或有机分散体。有利地,可以在自发引起碳纳米管化物(nanotubide)(即,碳纳米管碱性盐)的再氧化的条件下进行步骤c),以将它们复原到它们的中性状态(碳纳米管)。这样的条件包括:
-在步骤c)中使用脱气质子溶剂。当在步骤c)中使用脱气水、脱气离子水溶液、或(B)或(B’)与水或离子水溶液的脱气混合物(步骤b))时,可以满足此条件。当用脱气有机溶剂(B)或有机溶剂的脱气混合物(B’)来进行步骤c)时,也可以将其实现,其中有机溶剂(B)和混合物(B’)的有机溶剂选自醇如甲醇、乙醇、正丙醇、异丙醇、正丁醇、2-丁醇、正戊醇、2-戊醇、或正己醇
-进行步骤c),通过混合在步骤a)中得到的还原碳纳米管的有机溶液和适量的脱气有机溶剂(B)或有机溶剂的脱气混合物(B’),含有不同于氧的适宜的氧化剂,其中(B)和(B’)是非质子有机溶剂。适宜的氧化剂包括但不限于碘、FeCl3、NOPF6。
有利地,当在自发引起碳纳米管化物的再氧化的条件下进行步骤c)时,可以缓慢进行混合的步骤以以尽可能温和的方式骤冷碳纳米管化物。例如,可以将在步骤a)中得到的还原碳纳米管的有机溶液逐滴加入适量的脱气水、脱气离子水溶液、脱气有机溶剂(B)、有机溶剂的脱气混合物(B’)、或(B)或(B’)与水或离子水溶液的脱气混合物。
上文针对碳纳米管变体所描述的所有变体和实施方式,关于碳纳米管碱性盐C:M比率(在本文中在细节上已作必要的修改)适用于变体“a)+a’)”。例如,当碱金属是K时,碳纳米管碱性盐可以具有KC6、KC8、KC25、KC100或KC200化学计量。有利地,碳纳米管碱性盐是KC25或C含量大于或等于KC25的纳米管钾盐,例如KC25、KC100、KC200、KC370、KC500或C:K化学计量为KC25至KC500之间任何位置的纳米管钾盐。
对于在本文中描述的所有变体,可以通过温和离心来除去可能存在的任何聚集体,如在本文件的其它地方所描述的(参见步骤a1)。
有利地,在步骤c)以后获得的纳米碳分散体可能很长一段时间是稳定的(至少数天,但更经常数周或数月),从而允许处理而无需除去溶剂A或溶剂A’的混合物。
对于本文描述的所有变体,有利地,当进行步骤c)时,通过分散稳定性的简单的眼睛(或光学显微镜)观察,可以适当选择/调节/优化A或A’与(i)水(或(ii)与离子水溶液或(iii)与B或B’或(iv)与水与B或B’的混合物或(v)与离子水溶液与B或B’的混合物)的比率。
当混合步骤c)涉及脱气水、脱气离子水溶液、或(B)或(B’)与水或离子水溶液的脱气混合物时,产生的纳米碳材料的悬浮液将被称为“水性悬浮液”或“水性分散体”。
同样,当混合步骤c)涉及单脱气有机溶剂(B)或有机溶剂的脱气混合物(B’)时,产生的悬浮液将被称为“有机悬浮液”或“有机分散体”。
当将在步骤a)或在步骤a’)(当使用变体“a)+a’)”时)中得到的溶液暴露于空气(包括干燥空气)或水时,可以自发发生再氧化步骤b)。
再氧化步骤b)可以简单地包括允许在步骤a)中或在步骤a’)(当使用变体“a)+a’)”时)中得到的还原纳米碳的有机溶液在环境气氛下放置(即,在氧气和水分的存在下)。例如,可以让还原纳米碳的有机溶液在环境气氛下放置数秒到数天,例如15秒至2小时,例如15秒至1小时,优选30秒至1分钟。可替换地或另外地,再氧化步骤b)可以包括将在步骤中a)或在步骤a’)(当使用变体“a)+a’)”时)中得到的还原纳米碳的有机溶液暴露于氧源,如氧气。例如,可以使氧气或干燥空气的流股鼓泡通过在步骤a)中或在步骤a’)(当使用变体“a)+a’)”时)中得到的还原纳米碳的有机溶液持续适量的时间。
还可以通过在步骤a)中或在步骤a’)(当使用变体“a)+a’)”时)中得到的还原纳米碳的溶液中添加不同于氧的适宜的氧化剂(以固体、气体、液体或溶液(即溶解于溶剂中)形式)来进行再氧化步骤b)。在这种情况下,可以在惰性气氛下进行步骤b)。适宜的氧化剂包括但不限于碘、FeCl3、NOPF6,以及可以可选地在惰性气氛下进行步骤b)。
还可以通过电化学来进行再氧化步骤b)并且可以可选地在惰性气氛下进行。因此,可以通过电化学方式来氧化在步骤a)中或在步骤a’)(当使用变体“a)+a’)”时)中得到的还原纳米碳溶液;在这种情况下,可以可选地在惰性气氛下进行步骤b)。
还可以在进行步骤c)的同时进行再氧化步骤b),(通过混合在步骤a)中或在步骤a’)(当使用变体“a)+a’)”时)中得到的还原纳米碳的有机溶液和适量的脱气有机溶剂(B)或有机溶剂的脱气混合物(B’),含有不同于氧的适宜的氧化剂,条件是,(B)和(B’)是非质子有机溶剂)。适宜的氧化剂包括但不限于碘、FeCl3、NOPF6,以及可以可选地在惰性气氛下进行步骤b)。
有利地,以温和的方式,再氧化步骤b)会影响在步骤a)中或在步骤a’)(当使用变体“a)+a’)”时)中得到的还原纳米碳的溶液的骤冷,带负电荷的纳米碳化合物变为中性。
如在本文所使用的,当指根据本发明的完全剥离的纳米碳材料的悬浮液时,“亚稳”具有在胶态悬浮液领域中热力学亚稳定性的常规含义。一般来说,如果在给定条件下许多状态原则上可进入胶态悬浮液,则具有最低电位的情况被称为稳定态,而其它状态则被描述为亚稳的。同样,如在本文所使用的,“亚稳的悬浮液”是指,悬浮液处于对应于热力学势局部最小(thermodynamic potential local minium)的平衡状态。
如在本文所使用的,当指根据本发明的完全剥离的纳米碳材料的水性或有机悬浮液/分散体时,术语“空气亚稳的”是指“在空气中亚稳的”并且是指这样的悬浮液/分散体,其不是氧或水敏感的,例如对于环境空气。
有利地,在步骤a)中和/或在步骤a’)中可以使用单一非质子有机溶剂(即,非质子有机溶剂(A))。再次,可以将单溶剂(A)脱气。
当在步骤a)中和/或在步骤a’)中使用有机溶剂混合物(A’)时,它可以是二元、三元、或更高级溶剂混合物(即,两种、三种、或更多种非质子有机溶剂的混合物)。优选地,(A’)可以是二元或三元有机溶剂混合物,最优选二元有机溶剂混合物。
有利地,在步骤a)中和/或在步骤a’)中使用的非质子有机溶剂可以是极性的。如在本文所使用的,当指有机溶剂(包括步骤a)和/或步骤a’)的非质子有机溶剂)时,“极性的”是指具有介电常数□≥4的任何有机溶剂。
在整个本文件中,除非另有说明,参照25℃的温度来提供所有介电常数值(□)。换句话说,除非另有说明,措辞“介电常数□≥n”是指“在25℃下的介电常数□≥n”。
例如,非质子有机溶剂(A)和在有机溶剂混合物(A’)中的非质子有机溶剂可以具有在25℃下的介电常数□≥4、□≥5、≥6、≥7、≥8、≥9或≥10。在步骤a)中和/或在步骤a’)中可以使用的示例性极性非质子有机溶剂,作为单溶剂(A)或混合物(A’),包括但不限于四氢呋喃(THF)、甲基-THF(Me-THF)、二甲亚砜(DMSO)、N-甲基吡咯烷酮(NMP)、二甲基甲酰胺(DMF)、N-甲基甲酰胺(NMF)、环丁砜、丙酮、乙腈、硝基甲烷、二甲氧基乙烷(DME)、乙酸乙酯、2-丁酮、甲基叔丁基醚(MTBE)、二乙醚、环戊基甲基醚(CPME)、二氯甲烷、或它们的两种或更多种的混合物。优选地,在步骤a)中和/或在步骤a’)中可以使用的极性非质子有机溶剂,作为单溶剂(A)或混合物(A’),可以是THF、DMSO、NMP、DMF、NMF、CPME或环丁砜,优选THF或DMSO。优选地,选自THF或DMSO的单极性溶剂(A)可以用于步骤a)和/或步骤a’)。
如前面提到的,溶剂A或溶剂A’的混合物,在其中可能涉及它们的任何变体中,可能在步骤a)中使用它之前进行脱气,以溶解纳米碳插层化合物,而不管步骤a)可以接着是步骤a’)或直接接着是步骤b)。
有利地,有机溶剂(B)可以是与非质子有机溶剂(A)或非质子有机溶剂混合物(A’)可混溶的任何有机溶剂。同样,混合物(B’)的有机溶剂可以构成自与(A)或(A’)可混溶的任何两种或更多种有机溶剂。有利地,(B)和混合物(B’)的溶剂可以是允许盐物质部分或完全解离的任何有机溶剂,例如导致上文提到的离子物质的盐物质(例如,疏水性离子如苯基取代的离子,例如四苯基鏻、四苯基硼酸盐或四苯基鉮,仅举几例;尿酸盐离子;多芳基取代的离子如携带极性部分的萘基、蒽基、芘基、苝基等(例如,它们的1-芘磺酸盐、2-萘氧基乙酸盐、2-萘磺酸盐、或尿酸盐)。
一般来说,可支持盐物质的电离的任何有机溶剂可以用作溶剂(B)或混合物(B’)。可以用于步骤c)中的示例性有机溶剂,作为溶剂(B)或混合物(B’),包括但不限于:
-上面针对(A)和(A’)列出的极性非质子溶剂;
-醇,如甲醇、乙醇、正丙醇、异丙醇、正丁醇、2-丁醇、正戊醇、2-戊醇、正己醇;
-酯,如乙酸甲酯、乙酸乙酯、乙酸丙酯、乙酸丁酯、丙酸甲酯;
-酮,如丙酮、丁酮、2-戊酮、3-戊酮、环戊酮、环己酮;
-芳族溶剂,如苄腈、硝基苯、氯苯、二氯苯;
-卤化溶剂,如氯仿。
有利地,有机溶剂(B)和混合物(B’)的有机溶剂可以是水混溶性的。例如,有机溶剂(B)和混合物(B’)的有机溶剂可以选自醇如甲醇、乙醇、正丙醇、异丙醇、正丁醇、2-丁醇、正戊醇、2-戊醇、或正己醇。
在溶剂混合物(B’)的情况下,混合物的一种或多种组分可以是不会自己支持盐物质的电离的非极性有机溶剂,条件是,总体溶剂混合物(B’)支持充分的电离以稳定纳米碳材料的悬浮液。例如,溶剂混合物(B’)可以含有一种或多种非极性有机溶剂如苯、甲苯、甲基萘、二乙醚、环戊基甲基醚(CPME)、戊烷、己烷、庚烷、环己烷、1,4-二氧杂环己烷,与足够量的至少一种能够支持盐物质的电离的有机溶剂混合(如上详述的),以致总体混合物(B’)允许适宜的盐物质的解离(即,这样的盐物质,其生成能够吸附在纳米碳表面的表面上的离子物质,如上文描述的那些。例如,离子物质可以是疏水性离子,例如,但不限于苯基取代的疏水性离子(例如,四苯基鏻、四苯基硼酸盐或四苯基鉮)、多芳基取代的离子如携带极性部分的萘基、蒽基、芘基、苝基等(例如,它们的1-芘磺酸盐、2-萘氧基乙酸盐、2-萘磺酸盐、或尿酸盐,优选1-芘磺酸盐或2-萘氧基乙酸盐)。例如,(B’)可以是(i)水混溶性有机溶剂如醇(例如,甲醇、乙醇、正丙醇、异丙醇、正丁醇、2-丁醇、正戊醇、2-戊醇、或正己醇),和(ii)一种或多种非极性有机溶剂如苯、甲苯、甲基萘、二乙醚、环戊基甲基醚(CPME)、戊烷、己烷、庚烷、环己烷、1,4-二氧杂环己烷的混合物。例如,(B’)可以是甲醇和甲苯的混合物。
有利地,步骤c)可能涉及混合在步骤b)中得到的中性纳米碳的有机悬浮液和适量的(B)或(B’)与水或离子水溶液的脱气混合物。
例如,(B)与水或离子水溶液的脱气混合物可以用于步骤c),其中脱气混合物可以是水或离子水溶液和有机溶剂(B)的脱气混合物,其中比率为100%水或离子水溶液/0%(B)至0%水或离子水溶液/100%(B)中任何位置。同样,(B’)与水或离子水溶液的脱气混合物可以用于步骤c),其中脱气混合物可以是水或离子水溶液和水混溶性有机溶剂混合物(B’)的脱气混合物,其比率为100%水或离子水溶液/0%(B’)至0%水或离子水溶液/100%(B’)之间的任何位置。例如,可以使用脱气混合物50%水/50%(B)或(B’)(例如,50%水/50%甲醇或50%水/50%乙醇)。
有利地,可以调节在步骤c)中使用的水(单独或在与(B)或(B’)的混合物中)的pH以变化它的离子强度。例如,可以通过添加任何碱或酸,例如但不限于HCl、HNO3、乙酸、NaOH、KOH、NH4OH,来调节pH。在本领域中已知的任何碱或酸可以用来调节在步骤c)中使用的脱气水(单独或在与(B)或(B’)的混合物中)的离子强度。优选地,可以在脱气以前进行pH调节。
接下来的6个段落涉及在步骤c)中提到的离子水溶液(单独或在与(B)或(B’)的混合物中),优选地(但不必然地)当未进行步骤a’)时以及当步骤b)直接跟随步骤a)时,以及适用于本文描述的其中可能涉及步骤c)的任何变体。
可以调节离子水溶液的pH以变化它的离子强度,很像上文描述的水pH调节。可以通过添加任何碱或酸,如但不限于HCl、HNO3、乙酸、NaOH、KOH、NH4OH,来进行pH调节。在本领域中已知的任何碱或酸可以用来调节离子水溶液的离子强度。优选地,可以在脱气以前进行pH调节。
有利地,离子水溶液可以含有离子物质如OH-、H3O+、铵(NH4+)或取代的铵离子如四取代铵离子,例如烷基铵盐,如四烷基铵盐例如Bu4N+。
有利地,离子水溶液可以含有疏水性离子如但不限于苯基取代的离子、多芳基取代的离子、尿酸盐离子、BF4-、PF6-或AsF6-。
有利地,离子物质可以是离子,其是OH-或H3O+或易于与纳米碳π-π相互作用的疏水性离子,如但不限于含有苯基的离子如四苯基鏻、四苯基硼酸盐或四苯基鉮和/或多芳基取代的离子如携带极性部分的萘基、蒽基、芘基、苝基等(例如,1-芘基磺酸盐离子、2-萘氧基乙酸盐离子、2-萘基磺酸盐离子,优选1-芘基磺酸盐离子或2-萘氧基乙酸盐离子)。
有利地,离子水溶液可以是四苯基硼酸钠(B-Ph4Na+)的水溶液。四苯基硼酸钠的浓度可以是1毫摩尔/l。
有利地,离子水溶液可以是四苯基氯化鉮(As+Ph4Cl-)的水溶液。四苯基氯化鉮的浓度可以是1毫摩尔/l。
有利地,可以在-22至202℃的温度下,例如,在20至25℃下,进行步骤a)。
一般来说,可以在具有或没有搅拌的情况下,来实施根据本发明的方法,更具体地步骤a)。当使用搅拌系统时,它可以是机械或磁搅拌系统或温和的超声处理。有利地,可以借助于机械搅拌来进行上述方法。有利地,可以借助于磁力搅拌来进行上述方法。
应当指出的是,虽然可以借助于搅拌系统(包括超声处理)来实施本发明的方法,但后者不是必需的。事实上,本方法的显著优势在于,它基于开始于中性纳米碳材料的软溶解(soft dissolution)法,其精确地消除了超声处理的使用以及它的产生的有害的尺寸缩短。因此,本发明的方法允许获得较大尺寸的完全剥离的纳米碳材料。
在本发明的方法的一种变体中,步骤a)和/或步骤a’)可以进一步包括离心步骤a1),其允许,在将纳米碳插层化合物溶解于非质子有机溶剂(A)或非质子有机溶剂的混合物(A’)以及可选地添加适宜的盐(按照步骤a’))以后,从在步骤a)和/或步骤a’)中得到的还原纳米碳的有机溶液中分离任何非溶解的部分。本领域技术人员将知道如何确定适当的离心条件以获得不包括可检测的聚集体的还原纳米碳有机溶液。例如,可以在100至200 000g之间下进行离心0.1至24小时。在某些实施方式中,在2 800g下进行离心步骤1小时。
有利地,可以借助于肉眼来检查在离心期间在还原纳米碳的有机溶液中聚集体的存在。因此,可以在离心期间以各种间隔来取得还原纳米碳的有机溶液的样品以确定后者是否将允许获得没有肉眼可见的聚集体的溶液。肉眼检查允许检测最小尺寸为毫米的大十分之一(100微米)等级的可能的聚集体。
有利地,可以利用光学显微镜来检查在离心期间在还原纳米碳的有机溶液中聚集体的存在。因此,可以在离心步骤期间以各种间隔来取得还原纳米碳的有机溶液的样品以确定,何时后者将允许获得没有用光学显微镜可见的任何聚集体的溶液。光学显微镜检查允许检测最小尺寸为一微米等级的可能的聚集体。例如,可以借助于放大率为10至100的光学显微镜来分析溶液样品。
有利地,在步骤c)中使用的脱气水、离子水溶液、有机溶剂(B)、有机溶剂混合物(B’)或(B)或(B’)与水或离子水溶液的混合物,以及溶剂A和A’(当使用前加以脱气时),可以通过在本领域中已知的任何常规方法加以脱气,以除掉任何溶解的(主要是氮气和氧气)气体。例如,可以通过将待脱气的液体放置在减压下并搅拌(机械或磁力搅拌)来脱气A和A’,以及在步骤c)中使用的脱气水、离子水溶液、有机溶剂(B)、有机溶剂混合物(B’)或(B)或(B’)与水或离子水溶液的混合物。例如,可以通过在30分钟期间施加0.2毫巴的真空同时搅拌,来脱气150ml水。在另一个实施例中,可以通过冷冻泵解冻(freeze pump thaw),优选数个循环,例如3个循环,来脱气在步骤c)中使用的脱气水或脱气离子水溶液。
将在步骤c)中使用的水、离子水溶液、有机溶剂(B)、有机溶剂混合物(B’)或(B)或(B’)与水或离子水溶液的混合物脱气是重要的。
在步骤a)中和/或在步骤a’)中使用前,对A或A’进行脱气可能是有利的但不是必需的:可以在使用前在具有或没有脱气A/A’的情况下有效和成功地进行本发明的方法。
如大量文件证明的,纳米碳不溶于水或大多数有机溶剂。虽然可以将纳米碳悬浮在水中(借助于表面活性剂)或一些有机溶剂中,在这两种情况下,以强烈的剪切或超声处理为代价而获得纳米碳分散体,从而损坏纳米碳并减小其尺寸。此外,在过程结束时,纳米碳被不良剥离。如在[11-13]中描述的在极性非质子溶剂中溶解纳米碳盐会允许纳米碳的完全剥离(还见[24]),但以空气敏感性为代价(即,得到的混合物是空气敏感的)。
不希望受任何特定理论的束缚,一般建议,当混合在步骤b)中得到的中性纳米碳的有机悬浮液和脱气水、脱气离子水溶液、脱气有机溶剂(B)、脱气有机溶剂混合物(B’)、或(B)或(B’)与水或离子水溶液的脱气混合物时,在接触溶剂(水或有机溶剂(B)或(B’))的任何疏水性材料(纳米碳)的表面上普遍存在的气体层的不存在迫使离子吸附在疏水表面上,从而稳定纳米碳的悬浮液,并第一次提供完全剥离的纳米碳在水性或有机介质中的非空气敏感系统。
如在本文所使用的,在本发明的上下文中,当指纳米碳材料时,术语“溶解”是指完全剥离的纳米碳材料的溶液的形成(如本文所定义的)。
如在本文所使用的,术语“纳米碳的溶液”是指组合物,其中纳米碳材料是在溶剂中的真溶液中,如本领域中常规理解的。有利地,纳米碳溶液是均匀的。例如,纳米碳溶液,在离心以后,不含纳米碳材料的聚集体。可以借助于肉眼来检查在溶液中聚集体的不存在。因此,可以在离心以后取得溶液的样品以确定是否获得不包括肉眼可见的聚集体的溶液。借助于肉眼的检查可以检测最小尺寸为毫米的十分之一(100微米)等级的任何聚集体。优选地,可以通过光学显微镜来检查在溶液中聚集体的不存在。通过光学显微镜的检查允许检测最小尺寸为一微米的可能的聚集体。在示例性实施方式中,可以借助于放大率为10至100的光学显微镜来分析样品溶液。更基本地,术语“溶液”是指热力学稳定系统,其中溶质和溶剂仍然无限期地混合的并且在一定时间以后不会相分离。如果纳米颗粒(如同纳米管和石墨烯的情况一样)具有光波长的大小等级的至少一个维度(dimension),则由于胶粒的散射,溶液可以呈现丁铎尔效应。
如在本文所使用的,术语“悬浮液”可与术语“分散体”互换使用,并且是指如本领域中常规理解的“分散体”。
如在本文所使用的,术语“纳米碳的悬浮液”或“纳米碳的分散体”是指组合物,其中纳米碳材料是在悬浮液中或分散在溶剂中。换句话说,悬浮液含有悬浮/分散在溶剂中的纳米碳材料的固体颗粒。有利地,在本发明的上下文中,术语“纳米碳的悬浮液”或“纳米碳的分散体”是指完全剥离的纳米碳(即,单独的纳米碳)。例如,当纳米碳是碳纳米管时,“完全剥离”是指以下事实:起始碳纳米管,其通常具有聚集的纳米管的束的形式,被分离成单个碳纳米管。同样,当纳米碳是石墨烯时,“完全剥离”是指以下事实:起始石墨材料,其由聚集的/堆叠的石墨烯平面组成,被分离成单个石墨烯平面。溶剂可以是水、离子水溶液、或一种或多种有机溶剂与水或离子水溶液的混合物,它们均可以完全或部分脱气(如本文所描述的),在这种情况下,纳米碳的悬浮液被称为“纳米碳的水性悬浮液”或“纳米碳的水分散体”。溶剂可以是脱气有机溶剂或两种或更多种有机溶剂的脱气混合物(如本文所描述的),在这种情况下,纳米碳的悬浮液被称为“纳米碳的有机悬浮液”或“纳米碳的有机分散体”。在本发明的上下文中,悬浮液或分散体基本上被定义为亚稳系统,即在一定量的时间之后相将最终分离的系统。
在本领域中,纳米碳的悬浮液和溶液均可以常规地称为“油墨”。然而,在本发明的上下文中,术语“油墨”是指可以通过本发明的方法来获得的完全剥离的纳米碳的悬浮液,例如当纳米碳的水性或有机悬浮液用于制造纳米碳的薄膜或沉积物时。
如在本文所使用的,术语“纳米碳”或“纳米碳材料”是指纳米尺寸的有序碳基结构(carbon-based structure)。措辞“纳米尺寸的碳基结构”被理解为是指一种材料,其尺寸范围为约石墨烯平面的厚度至在至少一个空间维度上的数个纳米。例如,在至少一个空间维度上材料的尺寸是0.3至20nm,优选0.3至10nm,最优选0.3至2nm。纳米碳包括碳纳米管、纳米金刚石、碳纳米角、石墨烯和富勒烯类型材料(例如,C60和C60聚合物、C70和更高级富勒烯)、或它们的任何氢化或部分氢化形式,如氢化或任何部分氢化石墨烯(例如,石墨炔(graphyne)、石墨烷(graphane))。术语“纳米碳”还包括其它有序碳形式如杯堆叠(cup stacked)的纳米碳、碳纳米锥(nanocone)等、或它们的任何氢化或部分氢化形式。纳米碳包括i)纳米碳化合物,其具有单个可定义结构(例如,单个碳纳米管(单壁(SWCNT),双壁(DWCNT)、少壁(FWCNT)和多壁(MWCNT))、来自石墨的剥离石墨烯平面、或单个碳纳米角、纳米金刚石、富勒烯);或ii)纳米碳结构的聚集体(例如,原始(pristine)碳纳米管、堆叠的(stacked)石墨烯平面(即石墨或乱层(turbostratic)碳)、原始纳米金刚石、或原始碳纳米角。
如在本文所使用的,"纳米碳插层化合物"或"NIC"是指这样的化合物,其包含至少两个带负电或带正电的单个纳米碳并分别插入(intercalate)有正或负抗衡离子。纳米碳碱性盐是NIC的实例,其中单个纳米碳结构是带负电荷以及抗衡离子是碱性离子。当纳米碳结构是石墨烯平面时,NIC被称为GIC(“石墨插层化合物”)。
如在本文所使用的,"原始碳纳米管(pristine carbon nanotube)"是指束形式的碳纳米管的聚集体(如本领域中常规理解的)。在本申请中,措辞“还原碳纳米管”是指碳纳米管的束,其是带负电荷的并由正的碱性金属抗衡离子中和。措辞“单独碳纳米管(individualized carbon nanotube)”或“单个碳纳米管(individual carbon nanotube)”是指碳纳米管束,其已被剥离成单个纳米管,即彼此分离的纳米管。
如在本文所使用的,"原始碳纳米角(pristine carbon nanohorn)"是指碳纳米角的球形聚集体(如本领域中常规理解的)。在本发明中,"碳纳米角"通常旨在包括多个角状体的"大丽花状(dahlia-like)"聚集体,其具有它们的向外的封闭部分、以及各自由多个角状体组成的多个组的组装体。
为简便起见,如上所定义的碳纳米角还可以在本文中称为"CNHs"(作为复数)。
CNH通常具有管状结构如碳纳米管,由圆柱圆形石墨片所形成,以及以圆锥形形成碳纳米角的一端。通常,以一种形式来聚集CNH,以致锥形部分像角那样伸出,同时管状部分位于中心,通过范德华力和/或共价键保持在一起。在本发明中待使用的原始CNH可以是通过常规方法所获得的那些。
例如,原始碳纳米角包括以球形聚集体组装的碳纳米角,如那些碳纳米角,其通常通过在惰性气体气氛中用激光束来照射原材料的碳物质的常规激光烧蚀方法来获得(见例如,Iijima et al.,Chem.Phys.Lett.,309(1999)165-170[14];以及Azami et al.,J.Phys.Chem.,(2008),112,1330-1334[15])。如在本文所使用的,措辞“原始碳纳米角(pristine carbon nanohorn)”是指组装成球形聚集体的碳纳米角,一般来说,不论所使用的合成方法。例如,包括在美国专利7,501,024[16]中描述的碳纳米角。
可与“原始碳纳米角”互换使用的另一个术语是“碳纳米角聚集体”。这样的聚集体可以具有大丽花形状、芽形状、种子形状、或在这些形状之间的中间形状。
一般来说,在碳纳米角聚集体中的每个纳米角形成自至少一个管部分和一个覆盖管部分的一端的锥形部分。纳米角可以具有一个以上的管部分(即,它们可以是支化的)。例如,它们可以具有三个管部分(三脚(tripod))。这些已报告例如于Zhang et al.,J.Phys.Chem.C,113,11184-11186(2009)[17]。
如在本文所使用的,"石墨插层化合物"或"GIC"是指这样的化合物,其包含至少两个单独的带负电或带正电石墨烯平面并插入有正或负抗衡离子。石墨碱性盐是GIC的特定实例,其中石墨烯平面是带负电荷以及抗衡离子是碱性离子。GIC可以是具有化学式为MCx的二元化合物的形式,其中M表示碱金属(M+)的正抗衡离子,以及x表示6至200的整数。更具体地,碱金属可以是钾。例如,GIC可以是化学式为KC8的二元化合物。
在另一种实施方式中,GIC可以是具有化学式为M(Solv)yCx的三元化合物的形式,其中M是碱金属离子(M+),Solv是非质子溶剂分子,x表示6至200的整数以及y表示0至4的整数。溶剂分子可以是芳族溶剂分子(例如苯或甲苯)或亲核溶剂分子(例如,其结构含有至少一个氧原子的溶剂,如THF)。例如,GIC可以是化学式为K(THF)C24或K(THF)2C24的三元化合物。
如在本文所使用的,“还原石墨烯”是指一个或多个带负电荷的单个石墨烯平面。负电荷离域(delocalize)到碳原子上,从而形成每个单个石墨烯平面。
有利地,石墨插层化合物可以是具有化学式MCx的二元化合物的形式,其中M表示碱金属(M+)的正抗衡离子,以及x表示6至200的整数。更具体地,碱金属可以是钾。例如,石墨插层化合物可以是化学式KC8的二元化合物。
有利地,石墨插层化合物可以是具有结构为M(Solv)yCx的三元化合物的形式,其中M是碱金属离子,Solv是亲核溶剂,其结构含有至少一个氧原子,x表示6至200的整数以及y表示0至4的整数。例如,碱金属可以是钾,,溶剂可以是THF以及石墨插层化合物可以是结构为K(THF)yCx的三元化合物,其中x表示6至200的整数,以及y表示0至4的整数。在某些实施方式中,石墨插层化合物是结构为K(THF)C24或K(THF)2C24的三元化合物。
纳米碳插层化合物
有利地,纳米碳插层化合物(NIC)可以通过在本领域中已知的任何方法加以制备。例如,可以通过相应的纳米碳材料的还原来制备NIC。示例性方法包括借助于在汽相或液相中的碱金属来还原纳米碳材料,纳米碳材料的电化学还原,以及在化学式A+B-的碱金属盐的存在下纳米碳材料的还原,其中A+表示碱金属阳离子以及B-表示有机基团的阴离子。见Doped Carbon Nanotubes,A.Pénicaud,P.Petit,J.E.Fischer,in Carbon Meta-Nanotubes:Synthesis,Properties and Applications,1st Ed.Marc Monthioux Ed.,John Wiley&Sons(2012),41-111[18].。
在还原涉及碱金属或碱金属盐的情况下,碱金属可以是允许本发明的实施的任何碱金属。它可以例如选自锂、钠、钾、铷或铯。优选地,碱金属可以是锂、钠或钾。
例如,可以直接在碱金属的存在下通过纳米碳材料的还原来制备NIC,如Na、Li、K、Rb或Cs,优选Na、Li或K。因此,可以在碱金属的存在下直接进行还原,例如在液体或蒸汽相中或在氨中。在碱金属的存在下的还原方法是在本领域中众所周知的。本领域技术人员将知道如何确定用于在碱金属的存在下实施还原方法的适当的实验条件,例如在蒸汽相中或在氨中。例如,可以通过在氩气氛下并在100℃下(K是液体),使石墨和K反应来制备GICS。此外,本领域技术人员可以根据在例如“Synthesis of graphite intercalation compounds”,A.Herold in Chemical physics of intercalation,A.P.Legrand and S.Flandrois Eds,NATO ASI Series,series B,Vol.172,pp.3-45(1987)[19]中描述的方法。本文中描述的方法可以适用于其它类型的纳米碳材料的制备,如碳纳米管、纳米金刚石、碳纳米角、和富勒烯。本领域技术人员还可以参考以下出版物,以获得关于纳米碳的碱性还原的进一步教导:
碳纳米管的碱金属掺杂:Lee,R.S.,Kim,H.J.,Fischer,J.E.&Thess,A.letters to nature Conductivity enhancement in single-walled carbon nanotube bundles doped with K and Br.Nature 255–257(1997).[25]
碳纳米角的碱金属掺杂:WO 2011/154894[13]
富勒烯的碱金属掺杂:Hebard,A.F.;Rosseinsky,M.J.;Haddon,R.C.;Murphy,D.W.;Glarum,S.H.;Palstra,T.T.M.;Ramirez,A.P.;Kortan,A.R.Nature,1991,350,600.[26]
还可以在获自碱金属的碱金属盐的存在下进行纳米碳材料的还原。例如,可以在化学式为A+B-的聚芳基碱性盐的存在下进行还原,其中A+表示碱性离子的阳离子以及B-表示多芳族化合物的阴离子。例如,描述了这样的聚芳基碱性盐和用于制备它们的方法:
对于石墨插层化合物:WO 2009/056696[12];C.Stein,J.Poulenard,L.Bonnetain,J.Golé,C.R.Acad.Sci.Paris 260,4503(1965)[20];“Synthesis of graphite intercalation compounds”,A.Herold in Chemical physics of intercalation,A.P.Legrand and S.Flandrois,Eds,NATO ASI Series,series B,Vol.172,pp.3-45(1987)[21];F.Béguin and R.Setton New ternary lamellar compounds of graphite,Carbon 13,293-)295(1975)[22];
对于碳纳米管:WO 2005/073127[11]
对于碳纳米角:WO 2011/154894[13]
有利地,多芳族化合物可以是萘、二苯甲酮、芴酮、苯醌或蒽醌,优越萘。有利地,聚芳基碱性盐可以是多芳基钾盐(即,化学式A+B-的盐,其中A+表示K+)。有利地,化学式A+B-的聚芳基碱性盐可以是萘钾盐(Naph-K+)。
还可以通过电化学方式来进行纳米碳材料的还原。借助于在溶液中存在的抗衡阳离子的插入来发生纳米碳材料的电化学还原。[Hodge,S.A.,Fogden,S.,Howard,C.A.,Skipper,N.T.&Shaffer,M.S.P.Electrochemical Processing of Discrete Single-Walled Carbon Nanotube Anions.ACS Nano 7,1769–1778(2013).[27]
有利地,可以,在惰性气氛下,通过将具有化学式A+B-的聚芳基碱性盐加入纳米碳材料来制备纳米碳插层化合物,其中:
A+表示碱离子的阳离子,以及
B-表示多芳族化合物的阴离子。
有利地,多芳族化合物可以选自由萘、二苯甲酮、芴酮、苯醌和蒽醌组成的组。
有利地,当,在如上所述的化学式A+B-的碱金属盐的存在下,通过纳米碳材料的还原来制备本发明的方法的步骤a)的纳米碳插层化合物时,可以在纳米碳插层化合物的形成以后以及在步骤a)中将它溶解于非质子有机溶剂中以前,进行过滤步骤。例如,当纳米碳插层化合物的制备涉及在获自碱金属的碱金属盐的存在下(例如,在如上详述的具有化学式A+B-的聚芳基碱性盐的存在下)的还原时,过滤可以允许从包含纳米碳插层化合物的固相分离液相(例如K+Napht-在THF中的溶液)。可以用适当的溶剂冲洗得到的插入有碱金属的纳米碳一次或多次。然后可以在非质子有机溶剂(A)或非质子有机溶剂的混合物(A’)中溶解以前,干燥如此冲洗的纳米碳插层化合物。
在变体中,上述方法(在任何上文描述的实施方式/变体中)可以可选地进一步包括步骤d):从在步骤c)中得到的水性或有机混合物去除非质子有机溶剂(A)或非质子有机溶剂的混合物(A’)。因此,上述方法可以包括以下步骤:
a)在惰性气氛下,将纳米碳插层化合物溶解于非质子有机溶剂(A)或非质子有机溶剂的混合物(A’);从而导致还原纳米碳的有机溶液;
b)再氧化(去除电子)以将还原纳米碳材料复原到其中性状态,从而导致中性纳米碳材料在有机溶剂(A)或非质子有机溶剂的混合物(A’)中的有机悬浮液;
c)混合在步骤b)中得到的中性纳米碳的有机悬浮液和适量的脱气水、脱气离子水溶液、脱气有机溶剂(B)、有机溶剂的脱气混合物(B’)、或(B)或(B’)与水或离子水溶液的脱气混合物;
其中溶剂(A)或溶剂混合物(A’)是完全或部分水混溶性的或完全或部分地与溶剂(B)或溶剂混合物(B’)混溶;以及
d)从在步骤c)中得到的水性或有机混合物去除非质子有机溶剂(A)或非质子有机溶剂的混合物(A’);
从而导致纳米碳材料的空气亚稳的水性或有机悬浮液。
在示例性实施方式中,步骤a)可以接着是在进行步骤b)之前的步骤a’),和/或可以进一步包括离心步骤a1)(如先前描述的)。
在示例性实施方式中,当纳米碳材料是碳纳米管时,可能有利的是,不进行步骤b)。因此,当纳米碳材料是碳纳米管时,上述方法可以包括步骤a)、c)和d);或步骤a)、a’)、c)和d);如上文立即描述的,区别为步骤c)将指“混合在步骤a)中得到的还原碳纳米管的有机溶液和…”;和/或可以进一步包括离心步骤a1)(如先前描述的)。
步骤d)变体:
对于纳米碳材料的空气亚稳的水性悬浮液
有利地,非质子有机溶剂(A)或非质子有机溶剂的混合物(A’)可以是水混溶性的。
有利地,非质子有机溶剂(A)可以是极性的。类似地,有利地,混合物(A’)的非质子有机溶剂可以是极性的。因此,溶剂(A)和组成混合物(A’)的溶剂有利地可以具有介电常数□≥4。
有利地,非质子有机溶剂(A)可以具有低于水的沸点的沸点(即,在1大气压(1.01325.105Pa)下,溶剂沸点是<100℃)。类似地,有利地,混合物(A’)的非质子有机溶剂可以具有低于水的沸点的沸点。
有利地,在步骤a)中和/或在步骤a’)中,非质子有机溶剂(A)或混合物(A’)的非质子有机溶剂可以完全与水可混溶。这样的溶剂包括但不限于四氢呋喃(THF)、丙酮、乙腈、二甲氧基乙烷(DME)等。
在步骤a)和/或步骤a’)中的非质子有机溶剂(A)或混合物(A’)的非质子有机溶剂可以部分与水可混溶。这样的溶剂包括但不限于乙酸乙酯、2-丁酮、甲基叔丁基醚(MTBE)、二乙醚、二氯甲烷、环戊基甲基醚(CPME)等。
有利地,在步骤a)中和/或在步骤a’)中使用的水混溶性非质子有机溶剂(A)或混合物(A’)的非质子有机溶剂可以是沸点低于水以及介电常数□≥4的任何非质子有机溶剂。非质子有机溶剂可以完全与水可混溶,或部分与水可混溶。有利地,水混溶性非质子有机溶剂(A)或混合物(A’)的非质子有机溶剂可以是四氢呋喃(THF)、丙酮、乙腈、二甲氧基乙烷(DME)、乙酸乙酯、2-丁酮、甲基叔丁基醚(MTBE)、二乙醚、二氯甲烷、石油醚、环戊基甲基醚(CPME)等。有利地,水混溶性非质子有机溶剂(A)或混合物(A’)的非质子有机溶剂可以是四氢呋喃(THF)。
有利地,在步骤d)中,可以通过蒸发来去除非质子有机溶剂(A)或混合物(A’)的非质子有机溶剂。有利地,可以通过在本领域中已知的任何常规方法来进行蒸发。例如,可以使用旋转蒸发器或可以简单地静置蒸发溶剂混合物。有利地,在所有这些方法中,应注意不加热混合物。
在示例性实施方式中,可以使用单一非质子有机溶剂(A)以及上述方法包括以下步骤:
a)在惰性气氛下,将纳米碳插层化合物溶解于沸点低于水并且介电常数□≥4的水混溶性非质子有机溶剂;从而导致还原纳米碳的有机溶液;
b)再氧化(去除电子)以将还原纳米碳材料复原到其中性状态,从而导致中性纳米碳材料在有机溶剂(A)或非质子有机溶剂的混合物(A’)中的有机悬浮液;
c)混合在步骤b)中得到的中性纳米碳的有机悬浮液和适量的脱气水、脱气离子水溶液、或(B)或(B’)与水或离子水溶液的脱气混合物;以及
d)从步骤c)的水混合物去除水混溶性的有机非质子溶剂;从而导致完全剥离纳米碳的水性悬浮液。
同样,在示例性实施方式中,步骤a)可以接着是在进行步骤b)之前的步骤a’),和/或可以进一步包括离心步骤a1)(如先前描述的)。
同样,在示例性实施方式中,当纳米碳材料是碳纳米管时,可能有利的是,不进行步骤b)。因此,当纳米碳材料是碳纳米管时,上述方法可以包括步骤a)、c)和d);或步骤a)、a’)、c)和d);如上文立即描述的,区别在于步骤c)将指“混合在步骤a)中得到的还原碳纳米管的有机溶液和…”;和/或可以进一步包括离心步骤a1)(如先前描述的)。
对于纳米碳材料的空气亚稳的有机悬浮液
有利地,步骤c)可能涉及混合在步骤b)中得到的中性纳米碳的有机悬浮液和适量的脱气有机溶剂(B)或有机溶剂的脱气混合物(B’)。
有利地,有机溶剂(B)可以具有大于在步骤a)和/或步骤a’)中使用的非质子有机溶剂(A)或混合物(A’)的非质子有机溶剂的沸点的沸点。类似地,有利地,混合物(B’)的有机溶剂可以具有大于在步骤a)和/或步骤a’)中使用的非质子有机溶剂(A)或混合物(A’)的非质子有机溶剂的沸点的沸点。
例如,有机溶剂(B)或混合物(B’)的有机溶剂可以具有□≥4、≥6、≥8、或≥10的介电常数。在上述步骤c)中可以使用的示例性有机溶剂(B)或混合物(B’)的有机溶剂包括但不限于苄腈、硝基苯、氯苯、二氯苯,和醇如但不限于乙醇或异丙醇。
在示例性实施方式中,可以使用单一非质子有机溶剂(A)以及上述方法包括以下步骤:
a)在惰性气氛下,将纳米碳插层化合物溶解于介电常数□≥4的非质子有机溶剂(A);从而导致还原纳米碳的有机溶液;
b)再氧化(去除电子)以将还原纳米碳材料复原到其中性状态,从而导致中性纳米碳材料在有机溶剂(A)或非质子有机溶剂的混合物(A’)中的有机悬浮液;
c)混合在步骤b)中得到的中性纳米碳的有机悬浮液和适量的脱气有机溶剂(B)(其具有介电常数□≥2以及大于步骤a)和/或步骤a’)的非质子有机溶剂(A)的沸点的沸点);以及
d)从步骤c)的水性混合物去除非质子有机溶剂(A),从而导致完全剥离纳米碳在溶剂(B)中的有机悬浮液。
同样,在示例性实施方式中,步骤a)可以接着是在进行步骤b)之前的步骤a’),和/或可以进一步包括离心步骤a1)(如先前描述的)。
同样,在示例性实施方式中,当纳米碳材料是碳纳米管时,可能有利的是,不进行步骤b)。因此,当纳米碳材料是碳纳米管时,上述方法可以包括步骤a)、c)和d);或步骤a)、a’)、c)和d);如上文立即描述的,区别在于步骤c)将指“混合在步骤a)中得到的还原碳纳米管的有机溶液和…”;和/或可以进一步包括离心步骤a1)(如先前描述的)。
薄膜/沉积物
在变体中,上述方法可以进一步可选地包括步骤d1):在给定基底上沉积步骤c)或d)的完全剥离纳米碳的水性或有机悬浮液。可以在具有或没有步骤d)的情况下进行步骤d1)。
因此,在示例性实施方式中,上述方法可以包括以下步骤:
a)在惰性气氛下,将纳米碳插层化合物溶解于非质子有机溶剂(A)或非质子有机溶剂的混合物(A’);从而导致还原纳米碳的有机溶液;
b)再氧化(去除电子)以将还原纳米碳材料复原到其中性状态,从而导致中性纳米碳材料在有机溶剂(A)或非质子有机溶剂的混合物(A’)中的有机悬浮液;
c)混合在步骤b)中得到的中性纳米碳的有机悬浮液和适量的脱气水、脱气离子水溶液、脱气有机溶剂(B)、有机溶剂的脱气混合物(B’)、或(B)或(B’)与水或离子水溶液的脱气混合物;
其中溶剂(A)或溶剂混合物(A’)是完全或部分水混溶性的或完全或部分与溶剂(B)或溶剂混合物(B’)混溶;
从而导致纳米碳材料的空气亚稳的水性或有机悬浮液;以及
d1)在基底上沉积在步骤c)中得到的完全剥离纳米碳的水性或有机悬浮液。
在其它示例性实施方式中,上述方法可以包括以下步骤:
a)在惰性气氛下,将纳米碳插层化合物溶解于非质子有机溶剂(A)或非质子有机溶剂的混合物(A’);从而导致还原纳米碳的有机溶液;
b)再氧化(去除电子)以将还原纳米碳材料复原到其中性状态,从而导致中性纳米碳材料在有机溶剂(A)或非质子有机溶剂的混合物(A’)中的有机悬浮液;
c)混合在步骤b)中得到的中性纳米碳的有机悬浮液和适量的脱气水、脱气离子水溶液、脱气有机溶剂(B)、有机溶剂的脱气混合物(B’)、或(B)或(B’)与水或离子水溶液的脱气混合物;
其中溶剂(A)或溶剂混合物(A’)是完全或部分水混溶性的或完全或部分地与溶剂(B)或溶剂混合物(B’)混溶;
d)从在步骤c)中得到的水性或有机混合物去除非质子有机溶剂(A)或非质子有机溶剂的混合物(A’);
从而导致纳米碳材料的空气亚稳的水性或有机悬浮液;以及
d1)在基底上沉积在步骤d)中得到的完全剥离纳米碳的水性或有机悬浮液。
同样,在薄膜/沉积物变体的示例性实施方式中,步骤a)可以接着是在进行步骤b)之前的步骤a’),和/或可以进一步包括离心步骤a1)(如先前描述的)。
同样,在示例性实施方式中,当纳米碳材料是碳纳米管时,可能有利的是,不进行步骤b)。因此,当纳米碳材料是碳纳米管时,上述方法可以包括步骤a)、c)、d)和d1);或步骤a)、c)、或d1);或步骤a)、a’)、c)、d)和d1);或步骤a)、a’)、c)或d1);如上文立即描述的,区别在于步骤c)将指“混合在步骤a)中得到的还原碳纳米管的有机溶液和…”;和/或可以进一步包括离心步骤a1)(如先前描述的)。
在已进行沉积并已消除溶剂以后,然后纳米碳化合物与表面相互作用并保持稳定在表面上。
因此,还提供了根据本发明的方法可获得的完全剥离纳米碳的空气亚稳的水性或有机悬浮液的用途,用于在基底上沉积纳米碳材料。例如,根据本发明的方法可获得的完全剥离纳米碳的空气亚稳的水性或有机悬浮液可以用于透明导电膜的制备。
可以通过在基底上简单沉积(滴铸(drop-casting))一定量的纳米碳的水性悬浮液或有机悬浮液,接着蒸发水性和/或有机溶剂以分离纳米碳化合物,来进行沉积步骤。
还可以通过施加,例如利用刷或允许在基底上沉积纳米碳悬浮液膜的任何其它工具,来进行沉积步骤d1)。
还可以通过浸涂来进行纳米碳沉积。例如,可以将基底浸入纳米碳的水性或有机悬浮液一段时间以允许纳米碳材料在基底表面上的吸附。然后可以从水性或有机悬浮液除去基底,优选具有均匀速度以获得均匀涂层,以及然后可以从基底蒸发水和/或有机溶剂。
还可以通过旋涂来实施纳米碳沉积。例如,可选地在高温下,可以在旋转基底上沉积纳米碳的水性或有机悬浮液的小滴。优选地,在整个过程中保持旋转恒定以获得均匀涂层,然后蒸发水和/或溶剂。当在高温下进行旋涂时,温度可以是10至200℃。
可选地在加热基底上,可以通过喷涂来进行纳米碳沉积。
可以通过多种涂层方式,如辊-辊沉积(roll to roll deposition)、刮涂(Dr Blade coating)等,来进行纳米碳沉积。
这样的方法是本领域技术人员已知的,他们将知道如何适应实验条件,其取决于参数如基底的特性、在基底和纳米碳之间的相互作用、纳米碳水性悬浮液或有机悬浮液对基底的润湿性、以及本领域技术人员将明了的其它相关参数。
可以使用的基底以非限制性的方式包括陶瓷、金属、玻璃、硅石、硅、辉钼矿(MoS2)、云母、石墨和/或塑料。有利地,基底可以是用来和/或适应于沉积碳纳米管、纳米金刚石、碳纳米角、石墨烯和富勒烯类型材料的任何已知基底。例如,基底可以是HOPG(高度取向的热解石墨)、Si/SiO2晶片、云母、玻璃、MoS2和适合此目的的各式各样的塑料。
在示例性实施方式中,在沉积纳米碳材料以前,可以官能化或改性基底。一般来说,可以使用本领域技术人员已知的任何表面改性方法。改性类型的选择将取决于基底的特性、使用的水溶液(水或离子溶液)、使用的有机溶剂(A、A’、B、B’)以及为改善纳米碳沉积物的质量所期望的在基底表面上的物理化学相互作用。
上文关于以下各项所描述的所有变体和实施方式:
─使用的纳米碳的类型;
─碳纳米管的可选的管开口(tube opening)处理;
─纳米碳插层化合物和用于制备它们的方法;
─步骤a)和/或步骤a’)的非质子有机溶剂;
─在步骤a)中得到的还原纳米碳的有机溶液;
─再氧化步骤b);
─没有再氧化步骤b),有利地当碳纳米碳材料可能是碳纳米管时;
─可选的离心步骤a1);
─用于步骤c)的溶剂(包括水和离子水溶液)的脱气方式;
─步骤c)的有机溶剂(B)和(B’),包括离子物质含量和支持盐物质的电离的能力;
─在步骤c)中使用的水(单独或在与(B)或(B’)的混合物中)的pH调节;
─在步骤c)中提到的离子水溶液(单独或在与(B)或(B’)的混合物中)的pH调节;
─在步骤d)中用于去除非质子有机溶剂的方式;
─在步骤c)或d)中得到的纳米碳的悬浮液的用途/应用;
适用(在细节上已作必要的修改)于上文描述的“步骤d)变体”和“薄膜/沉积物”实施方式,包括下文描述的复合应用。
在另一方面,本发明还提供了通过根据本发明的方法可获得的完全剥离纳米碳的空气亚稳的水性悬浮液。
在又一个方面,本发明还提供了通过根据本发明的方法可获得的完全剥离纳米碳的空气亚稳的有机悬浮液。
在又一个方面,本发明还提供了完全剥离石墨烯的空气亚稳的水性或有机悬浮液,其特征在于水性或有机悬浮液的拉曼光谱呈现对称2D带(还称为“G’带”),其可以用洛伦兹函数拟合,具有调节的R平方(Adjusted R-Square)大于0.98,半峰全宽(full width at half maximum)(FWHM)为≤45cm-1,优选≤40cm-1,更优选≤35cm-1,最优选≤30cm-1。有利地,完全剥离石墨烯的空气亚稳的水性或有机悬浮液可以是无表面活性剂的。
还可以通过吸收光谱来表征完全剥离石墨烯的空气亚稳的水性或有机悬浮液。在示例性实施方式中,完全剥离石墨烯的空气亚稳的水性或有机悬浮液呈现在λmax=269nm处的UV-可见吸收峰。有利地,完全剥离石墨烯的空气亚稳的水性或有机悬浮液可以是无表面活性剂的。
还可以通过不含表面活性剂来表征完全剥离石墨烯的空气亚稳的水性或有机分散体。因此,本发明还提供了完全剥离石墨烯的无表面活性剂的空气亚稳的水性或有机分散体。
完全剥离石墨烯的水性悬浮液的溶剂可以是水或离子水溶液和脱气有机溶剂(B)的脱气混合物、有机溶剂的脱气混合物(B’)、或B或B’与非质子有机溶剂(A)的脱气混合物、或非质子有机溶剂的混合物(A’)。
完全剥离石墨烯的有机悬浮液的溶剂可以是脱气有机溶剂(B)、有机溶剂的脱气混合物(B’)、或B或B’与非质子有机溶剂(A)的脱气混合物、或非质子有机溶剂的混合物(A’)。
在示例性实施方式中,完全剥离石墨烯的空气亚稳的水性或有机悬浮液主要含有,如果不是唯一的话,单层石墨烯。
在示例性实施方式中,在完全剥离石墨烯的空气亚稳的水性或有机悬浮液中存在的单层石墨烯是至少50%的在悬浮液中的碳质材料(carbonaceous material),更优选至少75%,最优选至少90%。换句话说,在示例性实施方式中,在完全剥离石墨烯的空气亚稳的水性或有机悬浮液中存在的多层石墨烯是小于50%的在悬浮液中的碳质材料,更优选小于25%,最优选小于10%。
在示例性实施方式中,在完全剥离石墨烯的空气亚稳的水性或有机悬浮液中单层石墨烯的存在浓度为≥0.01g/L,优选≥0.05g/L,优选≥0.10g/L,优选≥0.16g/L。
在又一个方面,本发明还提供了单独碳纳米管的无表面活性剂的空气亚稳的水性或有机悬浮液。可以通过光致发光来表征在悬浮液中单独碳纳米管的存在。自从2002年已使用这种技术,作为单独碳纳米管的存在的证据(参见[38])。
如在本文所使用的,术语“表面活性剂”是指任何物质,在1mM或0.05%w/w的浓度(以最低者为准)下和在25℃下,其降低水-己烷界面张力大于2mN/m。
已报告了碳纳米管在有机溶剂或水溶剂中的悬浮液,其中的一些可以含有单独碳纳米管。然而,在每种情况下,在表面活性剂的存在下,通过超声处理来获得单独碳纳米管的悬浮液。这样的报告的一个实例是O’Connell et al.的工作[38]。
形成鲜明对比,根据本发明的单独碳纳米管的水性或有机悬浮液是无表面活性剂的。此外,不是通过超声处理(其损坏纳米管)来获得单独碳纳米管。相反,使用了温和溶解技术,相比于碳纳米管的已知的悬浮液,其导致更高质量的单独碳纳米管的水性或有机悬浮液(具有更少缺陷/损害的单独碳纳米管)。
因此,提供了完全单独碳纳米管的水性或有机悬浮液,其特征在于,在没有任何表面活性剂的情况下,不存在借助于肉眼或借助于光学显微镜可见的任何聚集体。在光学显微镜下,碳纳米管的有机或水性悬浮液的检查允许检测最小尺寸为一微米等级的可能的聚集体。例如,可以借助于放大率为10至100的光学显微镜来分析悬浮液样品,以确认碳纳米管聚集体的不存在。
碳纳米管具有强烈的聚集倾向,以及在没有表面活性剂的情况下,它们将聚集,除非根据本发明的方法将碳纳米管放置在悬浮液中。这就是为什么所有已知的用来制备碳纳米管的水性或有机悬浮液的方法诉诸使用表面活性剂来将碳纳米管保持在悬浮液中。首次,本发明人提供了用来制备没有任何表面活性剂的单独碳纳米管的空气亚稳的悬浮液的方法,以及单独碳纳米管的无表面活性剂的水性或有机悬浮液。
在示例性实施方式中,单独碳纳米管的水性悬浮液的溶剂可以是水或离子水溶液的脱气混合物、脱气有机溶剂(B)、有机溶剂的脱气混合物(B’)、或B或B’与非质子有机溶剂(A)的脱气混合物、或非质子有机溶剂的混合物(A’)。
单独碳纳米管的有机悬浮液的溶剂可以是脱气有机溶剂(B)、有机溶剂的脱气混合物(B’)、或B或B’与非质子有机溶剂(A)的脱气混合物、或非质子有机溶剂的混合物(A’)。
在示例性实施方式中,碳纳米管可以是单壁(SWCNT)、双壁(DWCNT)、少壁(FWCNT)或多壁(MWCNT)碳纳米管,优选单壁、双壁或少壁碳纳米管,最优选单壁碳纳米管。
在示例性实施方式中,在进行步骤a)之前,可以有利地对碳纳米管进行管开放预处理。本领域技术人员可以找到关于用来开放管的已知方法的信息的充足来源。见例如Doped Carbon Nanotubes,J.Sloan,M.Monthioux,in Carbon Meta-Nanotubes:Synthesis,Properties and Applications,1st Ed.Marc Monthioux Ed.,John Wiley&Sons(2012),225-271。[48]
例如,可以通过在空气下加热它们直到它们失去一定的重量来开放碳纳米管。要做到这一点,可以将样品放置在热重分析装置(TGA)中并可以在加热以后监测在空气下的重量损失。然后,可以,以和在TGA中相同的加热斜坡,在空气下加热置于烘箱中的真实样品并当达到对应于特定重量损失的特定温度时取出烘箱。以后可以通过称重得到的样品来证实实际重量损失。取决于纳米管源,可以通过平衡足够的纳米管开放与纳米管损害和材料损失来确定最佳重量损失(即,当获得在(i)足够的纳米管开放和(ii)纳米管损害和材料损失之间可接受的比率时)。
如读者将明了的,一些商业CNT已经被打开。可以,借助于轻度超声处理,通过将它们分散在水中,来确定是否CNT可以被打开。如果CNT下降到底部,则它们被打开。如果它们浮起,则它们被关闭。
可以用本发明的方法,精确地以和常规CNT相同的方式,来处理打开的CNT。有利地,相比于当用常规CNT(其还未经受管开放预处理)来进行上述方法时,在本发明的方法中打开的CNT的使用导致更浓和更稳定的分散体。
通过根据本发明的方法,利用本文描述的任何变体,可以获得完全剥离石墨烯和单独碳纳米管的水性或有机悬浮液。因此,上文描述的关于下述各项的所有变体和实施方式:
─使用的起始纳米碳(石墨或碳纳米管)的类型;
─非质子有机溶剂(A)或(A’);
─有机溶剂(B)和(B’),包括离子物质含量和支持盐物质的电离的能力;
─单独或在与(A)、(A’)、(B)和/或(B’)的混合物中使用的水的pH;
─单独或在与(A)、(A’)、(B)和/或(B’)的混合物中使用的离子水溶液的pH;
─完全剥离石墨烯或单独碳纳米管的有机或水性悬浮液的应用/用途,包括下文描述的复合应用;
适用(在细节上已作必要的修改)于上文描述的完全剥离石墨烯和单独碳纳米管的实施方式的水性或有机悬浮液。
复合材料(composite)
在另一方面,本发明还提供了通过本发明的方法可以获得的水性纳米碳悬浮液(水性油墨)用于制备复合材料的用途。
在又一个方面,本发明还提供了通过本发明的方法可以获得的有机纳米碳悬浮液(有机油墨)用于制备复合材料的用途。
在示例性实施方式中,本发明还提供了完全剥离石墨烯的空气亚稳的水性或有机悬浮液用于制备复合材料的用途,其中上述悬浮液的特征在于,悬浮液的拉曼光谱呈现对称2D带(还称为“G’带”),其可以用洛伦兹函数拟合,具有调节的R平方大于0.98,以及半峰全宽(FWHM)为≤45cm-1,优选≤40cm-1,更优选≤35cm-1,最优选≤30cm-1。
在示例性实施方式中,本发明还提供了单独碳纳米管的无表面活性剂的空气亚稳的水性或有机悬浮液用于制备复合材料的用途。
例如,可以通过一种方法来获得复合材料,上述方法包括以下步骤:混合水性或有机纳米碳油墨,优选根据本发明的有机纳米碳油墨,和聚合物溶液或聚合物混合物。上述聚合物可以是适合与根据本发明的水性或有机纳米碳油墨混合的任何聚合物。
有利地,通过本发明的方法可以获得的完全剥离纳米碳和/或水性或有机纳米碳油墨可以用于制备电子或微电子部件如电容器或晶体管。
有利地,除纳米碳颗粒之外,复合材料可以包含常规用于复合材料的其它材料,例如填料。
在所述复合材料的组合物中使用的填料可以具有纳米和/或微米尺寸。
如在本文所使用的,“纳米尺寸材料”是指这样的材料,其尺寸在至少一个空间尺寸上具有数个纳米。例如,在至少一个空间尺寸上材料的尺寸是0.3至20nm,优选0.3至2nm。
如在本文所使用的,"微米尺寸材料"是指这样的材料,其尺寸是1至100微米。
复合材料可以仅包含微米尺寸填料,或仅纳米尺寸填料,或微米和纳米尺寸填料的混合物(见例如FR 2 873 381[30],其中描述了在相同材料中包含纳米和微米填料的复合材料)。
在本文件中描述的方法解决了目前的在纳米碳结构的领域中阻碍研究开发的主要问题:缺少完全剥离纳米碳的空气稳定的或空气亚稳的液体制剂。因此它提供了可以在环境大气下处理的完全剥离纳米碳悬浮液。另外,这些油墨是不含表面活性剂的。
本发明的发明人是在水、离子水溶液、二元水-有机溶液或有机溶剂(含有完全剥离纳米碳)中开发一般纳米碳悬浮方法的最早的研究者。在科学文献中关于通过超声处理或搅拌所制备的含水性表面活性剂的配方有各种各样的报告。[Paton,K.R.et al.Scalable production of large quantities of defect free few-layer grephene by shear exfoliation in liquids.Nat.Mater.13,624-630(2014)][23]然而,如甚至在所述出版物的标题中显示的,获得的“石墨烯”不是完全剥离的并且厚度的分布是1至15层之间,其中最大宽度为约5层。因此,根据本发明的油墨(纳米碳水性悬浮液)在至少两个方面是远远优越的:(i)纳米碳是完全剥离的(见图6(AFM高度分布,在一层处达到高峰)和图11(薄膜厚度示出不大于2层均匀厚度),(ii)油墨是不含表面活性剂的。
同样,已报告纳米碳盐在极性非质子溶剂中的溶解(参见参考文献[11-13]和[24])。然而,得到的纳米碳混合物是空气敏感的并且不能在环境气氛下处理。在本发明的其中水或离子水溶液被有机溶剂(B)或有机溶剂混合物(B’)替换的变体中,可以获得完全剥离纳米碳的空气亚稳的有机悬浮液(到现在为止没有听说过的东西)。
从工业的角度来看,明确地,获得水性和/或有机纳米碳悬浮液/油墨的可能性是在纳米技术和复合材料工业中的重要因素,因为它是在此领域中推动技术进步的关键要素。
本发现违背本领域技术人员的先入为主的概念,根据其,认为不可能将纳米碳材料溶解于水或水溶液(即,二元水-有机溶剂溶液)或有机溶剂。
因此,本发明的方法非常有利地导致完全剥离纳米碳的第一种(就我们所知)水性悬浮液(水性油墨)。
另外,在另一方面,本发明的方法非常有利地导致完全剥离纳米碳的第一种(就我们所知)空气亚稳的有机悬浮液(有机油墨)。
在阅读随后的实施例以后,如由用于说明目的而给出的附图所说明的,本领域技术人员将容易看到其它优点。
附图说明
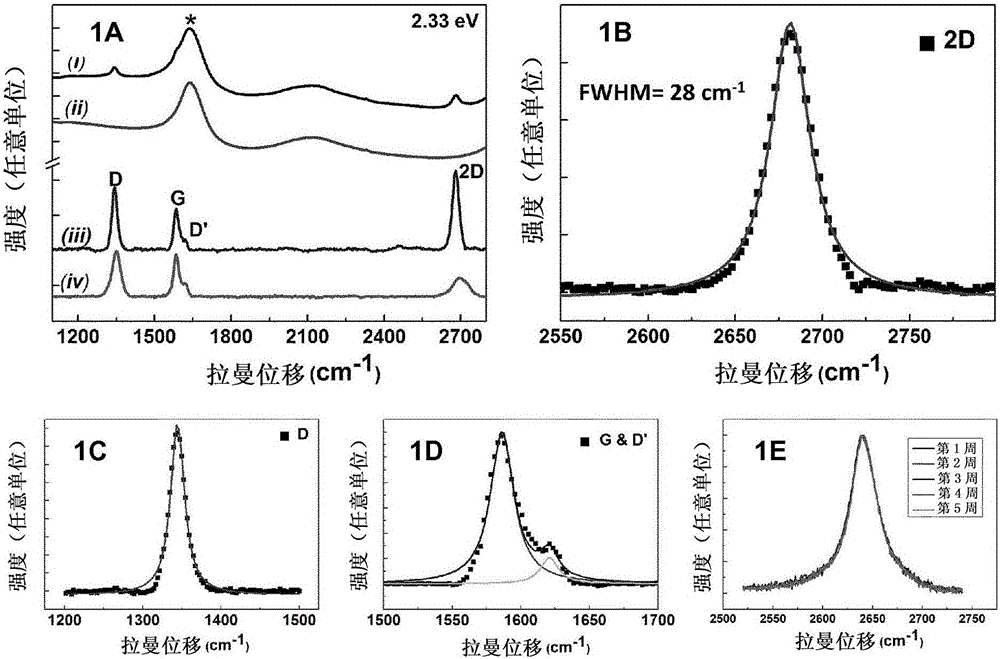
-图1A示出在2.33eV处石墨烯在水的悬浮液(i)、水(ii)的拉曼光谱以及在水减去以后获得的石墨烯谱(iii)。另外,示出含有按照参考文献32的实验细节所制备的胆汁盐的石墨烯悬浮液的光谱(iv)。按照实施例1b来制备具有光谱(i)的石墨烯悬浮液。依据在光谱(iii)相对于光谱(iv)中的2D带的形状和高度,脱气分散体的优越剥离是显而易见的。通过在相同比色杯中,分别从分散体(iii)和(iv)的光谱减去纯水的光谱来获得光谱(iii)和(iv),对于水的弯曲峰(标记有“*”的峰)归一化。
-图1B-1D示出在水中在2.33eV处来自按照实施例1b制备的石墨烯悬浮液的单层石墨烯(“SLG”)的2D、D、G和D’峰的典型拟合(fit)。在2D线的拟合中的轻微不对称是起因于在水背景减去中的缺陷。示于图1B的2D带具有调节的R平方为0.9895。
-图1E示出按照实施例1b制备的石墨烯悬浮液的拉曼2D带,作为时间的函数(在1.94eV处),显示优异的时间稳定性。
-图2示出,在不同能量下,实施例1b的在水中的石墨烯悬浮液的拉曼光谱。已通过从在相同比色杯中的石墨烯悬浮液的光谱减去纯水的光谱来获得所有石墨烯光谱,相对于水峰加以归一化。需要注意的是,相同程序应用于重水,其中水信号是远离G带并且得到相同的结果。在所有能量下,G带位于1587+/-2cm-1处。在约1300cm-1处的D带和在约2600cm-1处的2D带是分散的以及它们的位置随着能量而演变(如预期的)。强对称(一个洛仑兹线形)和窄(半峰全宽(FWHM)=28cm-1)的2D带是单石墨烯层的特征。
-图3示出来自实施例1b的石墨烯悬浮液的石墨烯沉积物的拉曼光谱。
-图4示出实施例1a的在水中的石墨烯悬浮液的吸收光谱。
-图5示出来自实施例1a的石墨烯悬浮液的石墨烯薄片的透射电子显微术(TEM)图像。
-图6示出来自实施例1a的石墨烯悬浮液的石墨烯薄片的原子力显微术高度图像(6B)和相关高度统计(6A)。如果设置阈值为0.51nm(即在单(0.34nm)和双(0.68nm)层的预期相应的厚度之间的一半(halfway)),示出的图像具有92%单层和7%双层石墨烯薄片。
-图7示出闪耀通过水(左小瓶)和实施例1b的在水中的石墨烯悬浮液(右小瓶)的激光束。激光未散射地通过水(左),而石墨烯分散体(右)则显示丁达尔效应,其起因于较大(胶体尺寸)石墨烯薄片的光散射。
-图8示出在90°下测得的动态光散射(DLS)数据,其说明,制备后两周,实施例1a的在水中的石墨烯分散体的散射性能没有显著变化。
-图9示出在90°下测得的动态光散射(DLS)数据,其说明,制备后两周,通过带负电荷盐稳定的实施例1a的在水中的石墨烯分散体的散射性能没有显著变化。
-图10示出在90°下测得的动态光散射(DLS)数据,其说明,制备后两周,通过带正电荷盐稳定的实施例1a的在水中的石墨烯分散体的散射性能没有显著变化。
-图11示出通过真空过滤制备自实施例1a的在水中的石墨烯分散体的石墨烯薄膜的透射光谱。
-图12A说明用于制备根据本发明的水性石墨烯分散体的示例性方法。具体地,在惰性气氛下,以单层石墨烯化物聚离子(graphenide polyion)的形式,将KC8,一种石墨插层化合物(GIC),溶解于THF。然后通过空气暴露将石墨烯化物离子氧化回到石墨烯(在THF中)并立即转移到脱气水。通过在单个石墨烯板之间的相互作用来确定水性石墨烯悬浮液的稳定性。在常规实验室条件下,溶解在水中的气体(约1mM)吸附在石墨烯表面上,包括在分散对象和促进聚集之间的长程吸引相互作用(图1A左下方)。相反,如果对水进行脱气(去除溶解的气体),则水-离子容易吸附在石墨烯表面上,从而将一定电荷赋予分散对象。排斥静电相互作用有利于分散材料的稳定性(图1A右下方)。
-图12B示出按照实施例1b获得的在0.16g/L下的空气稳定的水性SLG分散体的多个小瓶。
-图12C示出实施例1b的在水中的石墨烯分散体的UV-可见吸收光谱,其表明吸收峰是在针对在基底上单层石墨烯的吸收所报告的精确波长处[39]。
-表1:对应于图1A的数据:位置(cm-1),半峰全宽(FWHM,cm-1)和在2.33eV处的相关强度比率。
-表2:对应于图2的数据:位置ω(cm-1),线宽Г(cm-1),以及作为激发能的函数的相关强度比率。在1.17eV下无法适当测量*I2D/IG,因为在近红外中水的强吸收带。
等效物
以下代表性的实施例旨在帮助说明本发明,而不旨在也不应被解释为限制本发明的范围。确实,除本文说明和描述的那些之外,依据本文件的全部内容,包括随后的实施例以及本文引用的科学和专利文献的参考文献,对于本领域技术人员而言,本发明的各种修改以及其许多进一步的实施方式将变得显而易见的。应进一步理解的是,那些引用的参考文献的内容以引用方式结合于本文以帮助说明现有技术的状态。
以下实施例含有重要的附加信息、示例和指导,在其各种实施方式和等效物中,其可以适应于本发明的实践。
示例
通过实施例,其说明借此可以将本发明的方法降低到实践的一些实施方式,可以进一步理解本发明的方法及其应用。然而,应当理解的是,这些实施例并不限制本发明。本发明的变化(现在已知或进一步发展的)被认为属于如本文所描述的以及如下文所要求保护的本发明的范围内。
现将利用某些纳米碳材料来举例说明本发明,但是应当理解的是,这并不意味着将本发明限制于那些具体的纳米碳材料。
实施例
实施例1:石墨烯在水中的悬浮液的制备
实施例1a:
在惰性气氛下,将200mg的KC8(STREM Chemicals)分散在100mL的THF中,然后密封此混合物并在磁力搅拌器(800rpm)上混合4天。在搅拌以后,放置分散体过夜以允许形成较大石墨聚集体并沉降在底部。在3000 2000rpm下,离心在10mL玻璃小瓶中的混合物20分钟。通过移液管来提取顶部三分之二的溶液并保留供使用。对此样品进行光吸收测量和光散射测量。
脱气蒸馏水三十分钟,然后在75℃的水浴中加热30分钟。在环境条件下氧化石墨烯化物溶液一分钟。利用注射泵,逐滴同时轻轻搅拌,将4ml(2份)的在THF中的石墨烯化物溶液加入6ml(3份)的脱气水,以制备标记为WGrTHF3:2的样品(图8)。在室温下蒸发THF,时间为72小时,同时每两个小时轻轻搅拌,以产生石墨烯在水中的清澈的分散体,其中石墨烯浓度为0.35mg/mL。还通过将等体积的在THF中的还原石墨烯溶液(6mL)加入等体积的水(6mL)来制备在水中的不同浓度(0.53mg/mL)的石墨烯分散体(在实施例2和3中重复此过程)。
实施例1b:
石墨烯化物溶液
在惰性气氛下将108mg的KC8分散在18mL的蒸馏THF中,然后密封此混合物并在磁力搅拌器(900rpm)上混合6天。在搅拌以后,放置分散体过夜以允许形成较大石墨聚集体并沉降在底部。在3000rpm下离心在10mL玻璃小瓶中的混合物20分钟。通过移液管来提取顶部三分之二的溶液并保留供使用。
将石墨烯从THF转移到水
在环境条件下氧化石墨烯化物溶液一分钟。通过将在THF中的石墨烯化物溶液加入脱气水,接着THF蒸发,来将石墨烯转移到水。简单来说,将小心清洁的磁性特氟龙棒搅拌器引入待脱气的水(200mL)中以诱导气泡的成核作用。在0.2毫巴的压力下,对水进行温和搅拌,以进行30分钟的脱气。然后,在烧瓶上的空气压力柔和地上升回到大气压。将4ml脱气水转移到以前冲洗的20mL玻璃小瓶,随后是利用移液管并借助于使用不锈钢针的温和搅拌,滴加石墨烯化物溶液(在它的空气氧化一分钟以后)。在无尘环境中打开小瓶从而允许在室温下蒸发THF,同时,对于前十小时的每个小时和之后偶尔地,借助于不锈钢针轻轻搅拌,以产生石墨烯在水中的微暗分散体。通过混合不同体积的THF石墨烯化物溶液与脱气水体积比,来制备在水中的不同石墨烯浓度。在蒸发THF以后,将石墨烯保持在密封小瓶中。利用吸收光谱、拉曼光谱、动态光散射来表征分散体。
透射电子显微术:在多孔碳网格(holey carbon grid)上滴铸石墨烯分散体,供TEM表征。已用FEI Tecnai F20ST透射电子显微镜(TEM)来进行材料的结构和形态表征,在120kV的加速电压下操作以降低对石墨烯的束损伤,同时保存图像(0,0,2)石墨条纹(fringe)的分辨率,用于在折叠边缘上局部厚度的测量。已在TEM中利用EDAX能量分散X射线光谱仪(EDX)原位进行局部元素分析。不同的石墨烯分散体用来产生用于AFM表征的沉积物。利用类似于上文描述的条件和方案来制作用来在云母上产生AFM沉积物的石墨烯分散体,区别在于,用AsPh4Cl的脱气1mM水溶液来替代脱气水。在新切割的云母表面上,滴铸获得的石墨烯分散体,供AFM分析。
图12A图形化实施例1b的总体结果。在常规实验室条件下,溶解在水中的气体(约1mM)吸附在石墨烯表面上,其诱导在分散对象和促进聚集之间的长程吸引相互作用。相反,如果将水脱气(去除溶解的气体),则水-离子容易吸附在石墨烯表面上,从而将一定电荷赋予分散对象。排斥静电相互作用有利于分散材料的稳定性。电泳测量表明,分散石墨烯在水中变成带负电荷,这表明,正在发生OH-的优先吸附。
通过拉曼光谱,其是特别是用来确定层数、堆叠序列(在多层的情况下)、掺杂、缺陷的量和特性等的强大工具,来表征石墨烯样品。分散体的拉曼光谱报告于图1A和2并且示出石墨烯的典型的光谱。
虽然许多文章和公司声称《石墨烯》或《单层石墨烯》分散体、悬浮液或溶液,但在本发明之前不存在这样的分散体。通过借助于机械能(其是通常用于制备“石墨烯分散体”的技术)的分散石墨,人们违背热力学,来分开石墨烯在石墨中的有效填充。因此,得到的分散体必须是厚度的统计分布,其中单层形成上述分布的尾部(tail)。这事实上是在例如[23]中看到的情况。
相反,如果开始于已完全剥离系统,如在参考文献[12]和[47]的有机溶剂中的石墨烯化物溶液,本发明人发现,所有需要的是用来规避石墨烯再聚集的能障。在本发明的方法中,将水、离子水溶液、有机溶剂(B)、有机溶剂的混合物(B’)、或(B)或(B’)与水或离子水溶液的混合物(步骤c)脱气会提供障碍,而不需要除自然存在的OH-离子以外的任何添加剂。最终,通过降低或升高pH或添加其它离子,可以获得较高的石墨烯浓度,上述其它离子是如铵(NH4+)或取代的铵离子如四取代铵离子,例如烷基铵盐,如四烷基铵盐,例如Bu4N+;疏水性离子如但不限于BF4-、PF6-或AsF6-;尿酸盐离子;含有苯基的离子如四苯基鏻、四苯基硼酸盐(B-Ph4Na+)或四苯基鉮(As+Ph4Cl-);多芳基取代的离子如携带极性部分的萘基、蒽基、芘基、苝基等(例如,1-芘磺酸盐、2-萘氧基乙酸盐、2-萘磺酸盐、或它们的尿酸盐,优选1-芘磺酸盐或2-萘氧基乙酸盐)。
单层(singlelayeredness):
根据本发明的完全剥离石墨烯的水分散体的拉曼光谱报告于图1(例如,在图1A中的光谱(iii))。它显示了SLG的典型特点如半峰全宽(FWHM)低于30cm-1的窄的、对称2D(还被称为G’)带。利用单洛伦兹线,获得2D、D、G和D’峰的良好拟合(图1B-D)。有趣的是,比较根据本发明的石墨烯的脱气水分散体的拉曼光谱与其它水分散体的拉曼光谱,如按照参考文献[32]制备的超声处理辅助的胆酸钠(SC)悬浮液(在图1A中的光谱(iv))。依据根据本发明的脱气分散体的更尖锐和更强烈的2D带(光谱(iii)),而相比于超声处理辅助的分散体,D带只略有增强(光谱iv),剥离质量是显而易见的。最后,根据本发明的完全剥离石墨烯的这些水分散体的稳定性示于图1E,其中呈现拉曼2D带的时间演变。在至少五周的储存以后,可以看到没有明显的变化。同样,光散射实验表明,在5周期间,没有变化。单层石墨烯(SLG)的关键拉曼特征是2D(G’)带的形状和宽度。多层,AB堆叠的(Bernal)少层石墨烯显示具有通过多个洛伦兹线拟合的复杂形状的2D带[40]。乱层石墨,即沿c轴具有不相关石墨烯层的石墨,显示FWHM为50cm-1的单洛伦兹2D带[40,41]。另一方面,在大多数基底上,对于在2.33eV处的激发线,通过FWHM为20至35cm-1的单洛伦兹,可以良好拟合SLG的2D带[35,42-44]。同样,悬浮石墨烯显示28+/-2cm-1的2D FWHM[45]。因此,在2681cm-1处(在2.33eV下)观测到的具有纯洛伦兹形状和28cm-1的FWHM(以及119cm-1/eV的分散体)的2D带表明,根据本发明的石墨烯的脱气水性分散体主要含有,如果不是唯一的话,单层石墨烯。此外,根据本发明的脱气石墨烯水性分散体的拉曼2D带的位置和宽度密切匹配在SiO2上的支持石墨烯的那些[46]。拉曼光谱的其它特性是与关于SLG的文献一致。
总之,我们已经制备了大部分单层石墨烯在没有表面活性剂或任何其它稳定剂的水中的分散体,其特征在于拉曼光谱,其中2D带具有洛伦兹形状,以及具有低于40cm-1的全宽。
最少缺陷 依据缺陷诱导带Dt D’的分析(相对于位置ω(cm-1)和线宽Г(cm-1)以及作为激发能的函数的相关强度比的数据),可以获得关于缺陷的量和特性的更多信息。
遵循Tuinstra&Koenig[37]和Ferrari&Robertson[33,34],等分析了具有受控量的缺陷的石墨烯的拉曼光谱[35]。尤其是,ID/IG比率通过最大值,作为缺陷浓度的函数。
本文描述的脱气水分散体涉及低缺陷范围(称为《阶段I》)[33],因为,相比于针对阶段II有缺陷的石墨烯在40至60cm-1(D带)和30至40cm-1(D带)的范围内的观测值,G带不是分散的以及D和G带均具有低线宽(在2.33eV下分别为27和21cm-1)[35]。
在2.33eV下,1.5的ID/IG值导致0.06%缺陷,其大部分是边缘。因此,引入的缺陷的量可以安全地被认为是最小的。此外,在450℃下的沉积物的热处理以后,可以基本消除那些缺陷,从而将ID/IG值降低至0.7(图3)。在图1A中,一起示出脱气水分散体和按照参考文献[32]制备的超声处理辅助的胆酸钠(NaC)的光谱。依据针对脱气分散体的更尖锐和更强烈的2D带,剥离质量是显而易见的。
一般讨论:
据我们所知,到目前为止没有分散在液体中的高产率SLG的拉曼光谱研究的报告。到目前为止实现的最高SLG产率是通过石墨的超声处理,接着在NMP中超离心:对于c≈1.8g/l,为21%SLG[31]以及对于c≈0.11g/l,为33%SLG[36]。另一方面,Lotya等报告了分散在水性悬浮液中的石墨烯薄片的一些拉曼特征,其中使用胆酸钠作为分散剂(c≈0.3g/l),但由1至10个堆叠的层构成的薄片具有约20%的SLG[32]。最近报告了少量石墨烯层的可扩展方法,其中用高剪切混合来替换超声处理。它显示中心为5层并最高达约15层的宽厚度分布[23]。因此,脱气水分散体是第一种液体制剂,其中所有石墨烯存在为单层(对于0.16mg/ml的合理浓度)。
实施例2:在AsPh4Cl的水溶液中的石墨烯悬浮液的制备
使用类似于实施例1的条件和方案,区别在于,用AsPh4Cl的脱气1mM水溶液来替代脱气水,以制备样品+WGrTHF3:2(图10)。
获得石墨烯在AsPh4Cl的水溶液中的清澈的悬浮液,其中石墨烯浓度为0.35mg/mL。
实施例3:在NaBPh4的水溶液中的石墨烯悬浮液的制备
使用类似于实施例1的条件和方案,区别在于,用NaBPh4的脱气1mM水溶液来替代脱气水,以制备样品-WGrTHF3:2(图9)。
获得石墨烯在NaBPh4的水溶液中的清澈的悬浮液,其中石墨烯浓度为0.35mg/mL。
实施例4:碳纳米管在水中的悬浮液的制备
利用气相反应来制备KC8化学计量的SWCNT的盐。在惰性气氛下,将11.5mg的SWCNT(Tubal,来自OCSiAl)和5.25mg钾分开地加入派热克斯管(Pyrex tube),然后将上述管抽空至10-4毫巴并密封。在250℃下,加热含有SWCNT和钾的管两天。用在900rpm下的磁力搅拌器,将0.5mg的SWCNT的产生的盐分散在10mL的THF中24小时。在4000rpm下离心混合物30分钟。通过移液管来提取顶部三分之二的溶液并保留供使用。对此样品进行光吸收测量和光散射测量。
将蒸馏水脱气三十分钟。利用注射泵,将2ml(1份)的在THF中的还原SWCNT溶液逐滴加入2ml(1份)的脱气水,同时轻轻搅拌,以制备样品W_SWCNT_THF。在室温下蒸发THF,时间为72小时,同时每两个小时轻轻搅拌,以产生SWCNT在水中的清澈的悬浮液。对此样品进行光吸收测量和光散射测量。此悬浮液用来在不同基底上制作沉积物(利用滴铸和模压(stamping))。
实施例5:碳纳米管在水和DMSO中的分散体的制备
在250℃下,在抽空管中,通过钾和SWCNT反应三天来制备碳纳米管的盐。在惰性气氛下,在搅拌下,将2mg的产生的盐暴露于20ml的DMSO,时间为三天。在3000rpm下离心得到的溶液20分钟,以产生还原SWNT在DMSO中的0.067mg/mL溶液。在手套箱内,在惰性气氛下,通过添加1份NaTPhB DMSO溶液(1mM)来稀释1份的还原SWNT在DMSO中的溶液,以产生NaTPhB-还原SWNT在DMSO中的溶液(0.5mM),其中NaTPhB是指四苯基硼酸钠。借助于聚丙烯移液管,将得到的溶液注入等体积的脱气NaTPhB水溶液(1mM)。通过将NaTPhB在蒸馏水中的溶液脱气三十分钟来获得脱气NaTPhB水溶液。注射技术允许混合两种液体并且不需要进一步搅拌。关闭和保存得到的分散体,用于利用拉曼光谱、吸收光谱和薄膜沉积的表征。
对于实施例1-5,在溶液中,通过光散射测量、吸收光谱测量和拉曼光谱,来表征在水中的纳米碳悬浮液。
通过在混合纤维素酯膜(Millipore,0.025μm孔径,47mm直径)上的真空过滤来制备薄膜。利用浸涂、滴铸和模压,将薄膜沉积在玻璃和硅基底上。
当阅读本申请和上述说明性实施例时,本领域技术人员将明了的,本发明方法具有一般范围并且一般适用于如在本文件中定义的纳米碳材料。
虽然我们已经描述了本发明的多个实施方式,但显然的是,可以改变我们的基本实施例,以提供利用本发明的方法的其它实施方式以及从其获得的完全剥离的纳米碳材料。因此,应当理解的是,本发明的范围是通过所附权利要求而不是通过已通过实例的方式表示的具体实施方式来限定。
参考文献列表
[1]Schaffer,M.S.P.,Windle,A.H.,″Fabrication and Characterization of Carbon Nanotube/poly(vinyl alcohol)Composites″,Adv.Mater.,11,pp 937-941(1999)
[2]Ye,Y.,Ahn,C.C.,Witham,C.,Fultz,B.,Liu,J.,Rinzler,A.G.,Colbert,D.,Smith,K.A.,Smalley,R.E.,″Hydrogen Absorption And Cohesive Energy Of Single-Walled Carbon Nanotubes″,App.Phys.Lett.,74,pp 3072309(1999)
[3]Liu,C.,Fan,Y.Y.,Liu,M.,Gong,H.T.,Cheng,H.M.,Dresselhaus,M.S.,″Hydrogen Storage In Single-Walled Carbon Nanotubes At Room Temperature″,Science,286,pp1127-1129(1999)
[4]Kong,J.,Chapline,M.G.,Dai,H.,″Functionalized Carbon Nanotubes For Molecular Hydrogen Sensors″,Adv.Mater.13,1384-1386(2001)
[5]Aldissi,M.;Schmitz,B.;Lazaro,E.;Bhamidipati,M.;Dixon,B.,″Conducting Polymers InUltracapacitor Applications″,56th Annu.Tech.Conf.--Soc.Plast.Eng.,(Vol.2),pp 1197-1201(1998)
[6]An,K.H.;Kim,W.S.;Park,Y.S.;Moon,J.-M.;Bae,D.J.;Lim,S.C.;Lee,Y.S.;Lee,Y.H.″Electrochemical Properties Of High-Power Supercapacitors Using Single-Walled Carbon Nanotube Electrodes″,Adv.Funct.Mater.11,pp 387-392(2001)
[7]Yu,R.,Chen,L.,Liu,Q.,Lin,J.,Tan,K.-L.,Ng,S.C.,Chan,H.S.O.,Xu,G.-Q.,Hor,T.S.A.″Platinum Deposition On Carbon Nanotubes Via Chemical Modification″,Chem.Mater.10,pp 718-722(1998)
[8]Planeix,J.M.;Coustel,N.;Coq,B.;Brotons,V.;Kumbhar,P.S.;Dutartre,R.;Geneste,P.;Bernier,P.;Ajayan,P.M.,″ApplicationOf Carbon Nanotubes As Supports_in Heterogeneous Catalysis″,J.Am.Chem.Soc.116,pp 7935-7936(1994)
[9]Tans,S.J.,Verschueren,A.R.M.,Dekker,C.,″Room-Temperature Transistor Based On A Single Carbon Nanotube″,Nature 393,pp 49-52(1998)
[10]Bechtold,A.;Hadley,P.;Nakanishi,T.;Dekker,C.,″Logic Circuits With Carbon Nanotube Transistors″.Science294 pp 1317-1320(2001)
[11]WO 2005/073127
[12]WO 2009/056696
[13]WO 2011/154894
[14]Ljima,S.″Helical Microtubules of Graphitic Carbon.″Nature,354,56-58(1991)
[15]Azami et al.,J.Phys.Chem.,112,1330-1334(2008)
[16]US patent7,501,024
[17]Zhang et al.,J.Phys.Chem.C,113,11184-11186(2009)
[18]Penicaud et al.,″Doped Carbon nanotubes″,Chapter 2,in Carbon Meta-Nanotubes:Synthesis,Properties and Applications,1st Ed.Marc Monthioux Ed.,John Wiley&Sons(2012),pp.41-111
[19]″Synthesis of graphite intercalation compounds″,A.Herold in Chemical physics of intercalation,A.P.Legrand and S.Flandrois Eds,NATO ASI Series,series B,Vol.172,pp.3-45(1987)
[20]C.Stein,J.Poulenard,L.Bonnetain,J.Golé,C.R.Acad.Sci.Paris 260,4503(1965)
[21]″Synthesis of graphite intercalation compounds″,A.Herold in Chemicalphysics of intercalation,A.P.Legrand and S.Flandrois,Eds,NATO ASI Series,series B,Vol.172,pp.3-45(1987)
[22]F.Béguin and R.Setton New ternary lamellar compounds of graphite,Carbon 13,293-295(1975)
[23]Paton,K.R.et al.《Scalable production of large quantities of defect free few-layer graphene by shear exfoliation in liquids″,Nat.Mater.,13,624-630(2014)
[24]A.Pénicaud,F.Dragin,G.Pécastaings,M.He,E.Anglaret,″Concentrated Solutions of Individualized Single Walled Carbon Nanotubes″Carbon,67,360-367(2014)
[25]Lee,R.S.,Kim,H.J.,Fischer,J.E.&Thess,A.letters to nature Conductivityenhancement in single-walledcarbon nanotube bundles doped with K and Br.Nature 255-257(1997)
[26]Hebard,A.F.;Rosseinsky,M.J.;Haddon,R.C.;Murphy,D.W.;Glarum,S.H.;Palstra,T.T.M.;Ramirez,A.P.;Kortan,A.R.Nature,350,600(1991)
[27]Hodge,S.A.,Fogden,S.,Howard,C.A.,Skipper,N.T.&Shaffer,M.S.P.Electrochemical Processing of Discrete Single-Walled Carbon Nanotube Anions.ACSNano 7,1769-1778(2013).
[28]Chakraborty et al.,Angew.Chem.Int.Ed.,46,4486-4488(2007)
[29]Stankovitch etal.,Nature,2006,442,282-286
[30]FR 2 873 381
[31]Khan,U.,O′Neill,A.,Lotya,M.,De,S.,&Coleman,J.N.High-Concentration Solvent Exfoliation of Graphene.Small,6(7),864-871(2010)
[32]Lotya,M.,King,P.J.,Khan,U.,De,S.,&Coleman,J.N.High-concentration,surfactant-stabilized graphene dispersions.ACS nano,4(6),3155-3162(2010)
[33]Ferrari,A.C.,&Robertson,J.Interpretation of Raman spectra of disordered and amorphous carbon.Physical review B,61(20),14095(2000)
[34]Ferrari,A.C.,&Basko,D.M.Raman spectroscopy as a versatile tool for studying the properties of graphene.Nature nanotechnology,8(4),235-246(2013)
[35]L.G.,Jorio,A.,Ferreira,E.M.,Stavale,F.,Achete,C.A.,Capaz,R.B.,...&Ferrari,A.C.Quantifying defects in graphene via Raman spectroscopy at different excitation energies.Nano letters,11(8),3190-3196(2011)
[36]Torrisi,F.,Hasan,T.,Wu,W.,Sun,Z.,Lombardo,A.,Kulmala,T.S.,...&Ferrari,A.C.Inkjet-printed graphene electronics.Acs Nano,6(4),2992-3006(2012)
[37]F.Tuinstra,J.L.Koenig,Raman Spectrum of Graphite.J.Chem.Phys.53,1126(1970)
[38]M.J.O′Connell et al.,Science,297,593-596(2002)
[39]V.G.Kravets et al.,Phys.Rev.B,81,1-6(2013)
[40]L.M.Malard etal.,Phys.Rep.,473,51-87(2009)
[41]P.Lespade et al.,Carbon N.Y.,22,375-385(1984)
[42]Y.Y.Wang et al.,J.Phys.Chem.C,112,10637-10640(2008)
[43]A.Eckmann et al.,Phys.Rev.B,88,035426-11(2013)
[44]E.M.Ferreira et al.,Phys.Rev.B,82,125429-9(2010)
[45]Z.H.Ni et al.,ACS Nano,3,569-574(2009)
[46]S.Berciaud et al.,Nano Lett.,9,346-52(2009)
[47]A.Catheline et al.,Soft Matter.8,7882(2012)
[48]J.Sloan,M.Monthioux,″Doped Carbon Nanotubes″,in Carbon Meta-Nanotubes:Synthesis,Properties and Applications,1st Ed.Marc Monthioux Ed.,John Wiley&Sons(2012),pp.225-271
[49]Damien Voiry,Olivier Roubeau and Alain Pénicaud,″Stoichiometric control of single walled carbon nanotubes functionalization″,J.Mater.Chem.,20,4385-4391(2010)
[50]P.Petit,C.Mathis,C.Journet,P.Bernier,Tuning and monitoring the electronic structure of carbon nanotubes.Chem.Phys.Lett.305,370-374(1999)
- 还没有人留言评论。精彩留言会获得点赞!