高镍三元正极材料及其制备方法与其在电池制备中的应用与流程
y,其中0《x《1,0《y《1,优选依次为0.8:0.1:0.1
14.步骤(2)中,所述ce盐具体可为ce(no3)3·
6h2o;
15.所述sm盐具体可为sm(no3)3·
6h2o;
16.所述ce盐的ce离子与所述sm盐中的sm离子的摩尔比可为8:2;
17.优选地,步骤(1)中,所述混合盐溶液中,镍、钴、锰三种金属离子的总摩尔浓度可为0.5-2.5mol/l,具体为2mol/l。
18.所述碱液具体可为氢氧化钠溶液,其中,氢氧化钠的摩尔浓度可为3-10mol/l,具体可为4mol/l;
19.所述氨水的摩尔浓度可为0.5-5mol/l,具体可为1mol/l;
20.所述氨水中还加入水合肼,用于控制反应体系的电位;水合肼的加入量为步骤3)反应釜内液体总体积的四万分一;
21.所述化学反应在惰性气体保护下进行,所述惰性气体具体可为高纯氮气、氩气等;
22.所述惰性气体的流量可为1.0-3.0m3/h,具体可为2.0m3/h;
23.所述反应在搅拌下进行,具体地,控制反应釜搅拌桨的搅拌强度为600-800r/min,优选700r/min;
24.反应过程中通过加入碱液和氨水调节反应体系的ph值至10-13,优选11-12,更优选11.5;
25.反应体系的温度可为40-70℃,优选50-60℃,更优选55℃;
26.优选地,步骤(3)中所述混合盐溶液、所述混合盐水溶液、所述碱液和所述氨水并流加入到所述反应釜时的流量比可为(0.5-4):(0.5-4):(0.5-4):1,具体可为2:2:2:1;
27.优选地,步骤(3)中所述混合盐水溶液(氧离子导体前体组分溶液)加入的总含量为所述混合盐溶液的1at%-4at%,优选3at%;
28.优选地,步骤(5)中,所述lioh过量(基于粉末状前驱体)1-3wt%,优选2wt%;
29.优选地,步骤(5)中,所述煅烧的条件如下:以2-5℃/min加热到400-700℃保温4-8h,再以2-5℃/min加热到600-800℃,再以1-3℃/min加热到700-900℃高温锻烧11-13h,最后以0.3-0.7℃/min降到500-700℃;
30.优先地,以4℃/min加热到560℃保温6h,再以3℃/min加热到700℃,再以2℃/min加热到800℃高温锻烧12h,最后以0.5℃/min降到600℃。
31.由上述方法制得的高镍三元正极材料也属于本发明的保护范围。
32.所述高镍三元正极材料为氧离子导体ce
0.8
sm
0.2o1.9
改性高镍三元正极材料。
33.上述高镍三元正极材料在电池正极材料制备中的应用也属于本发明的保护范围。
34.本发明还提供一种电池,所述电池包含所述高镍三元正极材料。
35.与现有技术相比,本发明的有益效果体现在以下几个方面:
36.1、本发明在高镍正极材料的一次颗粒表面原位引入萤石型氧离子导体ce
0.8
sm
0.2o1.9
,充分利用其稳定的氧空位所具有良好的吸附氧和储存氧的特性,借助特定化学环境稳定住氧离子失去电子后形成的高活性中间产物,抑制其进一步氧化生成氧气,有利于固相中的氧离子发生可逆氧化还原过程,进而提升电池的热稳定性。
37.2、ce
0.8
sm
0.2o1.9
其中ce
4+
具有强氧化性,可以将ni
2+
氧化为ni
3+
,降低li
+
/ni
2+
混排,提高首圈效率和材料的结构稳定性。
38.3、本发明制备的高镍正极三元材料的制备简单、原料丰富、能耗低、生产工艺安全可靠、生产成本低,易于规模化生产。
39.本发明通过利用萤石型氧离子导体富含稳定的氧空位具有良好的吸附氧和储存氧的特性,对高镍正极材料的一次颗粒的表面上引入氧空位的结构设计与优化,通过吸附/钳制正极材料表面的o-、o
22-等氧离子氧化中间态,因此可以从动力学上减缓其继续氧化或者与电解质反应等不可逆过程,从而促进表面氧离子发生可逆、无产气的氧化还原过程,进而提高电池的安全性。
附图说明
40.图1是本发明实施例1制备的高镍三元正极材料的sem图;
41.图2是对比例1和实施例3制备的高镍正极三元正极材料的扣电dsc图,扣电电压范围为2.8-4.35v。
具体实施方式
42.下面结合具体实施方式对本发明进行进一步的详细描述,给出的实施例仅为了阐明本发明,而不是为了限制本发明的范围。以下提供的实施例可作为本技术领域普通技术人员进行进一步改进的指南,并不以任何方式构成对本发明的限制。
43.下述实施例中的实验方法,如无特殊说明,均为常规方法,按照本领域内的文献所描述的技术或条件或者按照产品说明书进行。下述实施例中所用的材料、试剂等,如无特殊说明,均可从商业途径得到。
44.实施例1
45.采用niso4·
6h2o、coso4·
h2o和mnso4·
h2o配备镍、钴、锰总摩尔浓度2mol/l的镍钴锰混合盐溶液;将氧离子导体前体组分ce(no3)3·
6h2o和sm(no3)3·
6h2o按摩尔比8:2配成混合盐水溶液;在反应釜内加入纯水作为底液,通过流量泵连续并流加入混合盐溶液、碱液、氨水、混合盐水溶液,并使其发生化学反应,其中naoh的浓度为4mol/l,nh3.h2o的浓度为1mol/l,并加入适量的水合肼(水合肼的加入量为反应釜内液体总体积的四万分一),在反应釜中加入适量的去离子水并加热至55℃恒温,全程通n2作为保护气氛。然后在反应釜中滴加碱液及氨水至ph为11.5同时伴随700r/min的速度充分搅拌。以蠕动泵控制溶液的流速,通过ph计调控反应釜的ph。反应开始时,先将混合盐溶液和混合盐水溶液以一定的流速泵入反应釜中(混合盐水溶液加入的总含量为混合盐溶液的1at%),通过调节碱液的流速控制ph值。待进料结束后陈化12h,将物料从出料口取出,抽滤,将固体反复洗涤后在真空烘箱中于120℃干燥12h。最后,对干燥后的前驱体称重并计算lioh的量(其中lioh过量2wt%,基于粉末状前驱体,即lioh与粉末状前驱体的重量比为:1.02:1)。用丙酮做分散剂将前驱体与lioh
·
h2o充分研磨后转入管式炉中煅烧,烧结过程中通入流速为150ml/min的氧气,以4℃/min加热到560℃保温6h,再以3℃/min加热到700℃,再以2℃/min加热到800℃高温锻烧12h,最后以0.5℃/min降到600℃,随炉冷却,得到高镍三元正极材料即可得到活性材料1。
46.对所得产品的形貌进行表征(见附图1)。
47.实施例2、实施例3和实施例4除了氧离子导体的成分加入量不同之外ce(no3)3·
6h2o和sm(no3)3·
6h2o的总含量为2at%,3at%和4at%外(实施例1为1at%),其他合成条件都相同。得到高镍三元正极材料即可得到活性材料2、3和4。
48.对比例1、未改性的高镍三元正极材料的制备
49.采用niso4·
6h2o、coso4·
h2o和mnso4·
h2o配备镍、钴、锰总摩尔浓度2mol/l的镍钴锰混合盐溶液;在反应釜内加入纯水作为底液,通过流量泵连续并流加入混合盐溶液、碱液、氨水,并使其发生化学反应,其中naoh的浓度为4mol/l,nh3.h2o的浓度为1mol/l,并加入适量的水合肼(水合肼的加入量为反应釜内液体总体积的四万分一),在反应釜中加入适量的去离子水并加热至55℃恒温,全程通n2作为保护气氛。然后在反应釜中滴加碱液和氨水至ph为11.5同时伴随700r/min的速度充分搅拌。以蠕动泵控制溶液的流速,通过ph计调控反应釜的ph。反应开始时,先将混合盐溶液以一定的流速泵入反应釜中,通过调节碱液的流速控制ph值。待进料结束后陈化12h,将物料从出料口取出,抽滤,将固体反复洗涤后在真空烘箱中于120℃干燥12h。最后,对干燥后的前驱体称重并计算lioh的量,(其中lioh过量2wt%)。用丙酮做分散剂将前驱体与lioh
·
h2o充分研磨后转入管式炉中煅烧,烧结过程中通入流速为150ml/min的氧气,以4℃/min加热到560℃保温6h,再以3℃/min加热到700℃,再以2℃/min加热到800℃高温锻烧12h,最后以0.5℃/min降到600℃,随炉冷却,得到未改性高镍三元正极材料。
50.电化学性能表征
51.将实施例1-4制备的高镍三元正极材料及对比例1制备的未改性高镍三元正极材料分别制作成扣式电池(cr2032),其中活性物质∶导电剂∶粘结剂=90∶5∶5(质量比),导电剂是super p,粘结剂是pvdf,电解液是溶解在ec、dec和dmc的混合溶剂(体积比为1∶1∶1)中的1m lipf6,扣式半电池组装全部采用锂片作为对电极,泡沫镍片作为缓冲垫片,制作环境水氧含量分别为:水浓度《2ppm,氧浓度《2ppm并充满氩气的手套箱中制作。测试电压范围为2.8~4.35v。0.2c下测试首轮充放电曲线,循环曲线则是在1c充电、1c放电下放得到。结果如表1、表2所示:
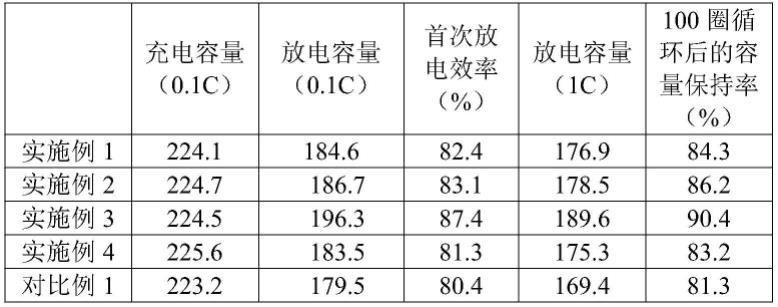
52.表1
[0053][0054]
表2
[0055] cac/ali
+
/ni
2+
实施例114.21932.86954.95750.28实施例214.15882.86874.96260.17实施例314.25992.86074.98470
实施例414.22362.86914.95760.33对比例114.15492.86804.91490.54
[0056]
从表1可以看出,实施例1-4制备的高镍三元正极材料与对比例1制备的未改性的高镍三元正极材料相比,不仅首次放电比容量有优势,而且100圈循环后的容量保持率好。氧离子导体改性量为3at%时高镍三元正极材料电化学性能得到明显改善,因此说明实施例3为最佳实施例,说明本发明提供的氧离子导体ce
0.8
sm
0.2o1.9
改性的高镍三元正极材料电化学性能更好。空白样在循环过程中容量的快速衰减归因于氧气的释放会引起结构的膨胀变形、阳离子失序、相变等,从而影响材料的结构稳定性。同时,在循环期间由于界面发生副反应会产生一层厚厚的csei膜进而阻碍li
+
的扩散,电化学极化阻抗和浓差极化阻抗的增加也将导致该现象的发生。氧离子导体ce
0.8
sm
0.2o1.9
改性的高镍三元正极材料电化学性能更好归因于在ce
0.8
sm
0.2o1.9
处理后,材料的比表面积增大,在充放电过程中材料提供了更多li
+
迁移位点使材料的活性更强。同时,传输路径变短以及通道变宽,从而提高了材料的倍率性能。
[0057]
c/a的比值常用来衡量形成的层状结构是否良好,该比值越大,材料的层状结构越好。从表2可得c/a的数值差别不大,都大于4.9,说明制备的材料层状结构良好,实施例3的c/a最大,说明层状结果最优;且li
+
/ni
2+
阳离子混排程度最低。这主要是由于ce
4+
具有强氧化性会诱导ni
2+
离子被氧化成ni
3+
,从而降低锂镍混排程度,充分表明氧离子导体ce
0.8
sm
0.2o1.9
改性的方法除了可以引入氧离子导体以外,还顺带实现了ce4
+
和sm
3+
的掺杂,有利于稳定层状结构。
[0058]
图1是实施例1制备的高镍三元材料的sem图,从图1可以看出,实施例1制备的三元单晶材料呈现良好的单晶形貌,颗粒分布均匀,表面较光滑。
[0059]
图2是对比例1和实施例3制备的高镍正极三元正极材料的扣电dsc图,扣电电压范围为2.8-4.35v。
[0060]
从图2中的测试结果可以看出,实施例3的峰值分解温度为224.14℃,对比例1的峰值分解温度为211.27℃,提高了12.87℃,逃逸的晶格氧可以被富含氧空位的ce
0.8
sm
0.2o1.9
修饰层捕获,能够有效抑制高活性氧从材料的本体结构中析出,从而改善电池的安全性能。
[0061]
以上对本发明进行了详述。对于本领域技术人员来说,在不脱离本发明的宗旨和范围,以及无需进行不必要的实验情况下,可在等同参数、浓度和条件下,在较宽范围内实施本发明。虽然本发明给出了特殊的实施例,应该理解为,可以对本发明作进一步的改进。总之,按本发明的原理,本技术欲包括任何变更、用途或对本发明的改进,包括脱离了本技术中已公开范围,而用本领域已知的常规技术进行的改变。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1