恩曲他滨水杨酸盐及其晶型、制备方法和用途与流程
本发明涉及化学药物领域,尤其涉及恩曲他滨水杨酸盐的晶型及其制备方法和用途。
背景技术:
恩曲他滨(emtricitabine),化学名为(2R,5S)-5-氟-1-[2-(羟甲基)-1,3-氧硫杂环戊烷-5-基]胞嘧啶,化学结构式如式1所示,为核苷类逆转录酶抑制剂。恩曲他滨临床上用于与其他抗逆转录酶药物合用治疗HIV-1感染(艾滋病)。此外,基于恩曲他滨和富马酸替诺福韦酯的固定剂量复方制剂在艾滋病的治疗和预防上具有举足轻重的地位。恩曲他滨可以与无机酸或者有机酸成盐。中国专利申请CN10167133报道,利用水杨酸官能团化的聚苯乙烯树脂从合成恩曲他滨的反应混合物中分离恩曲他滨。美国专利US6600044,PCT专利申请WO2009084033和WO2011107920,以及OrganicProcessResearch&Development,2006,10(3):670-672报道了恩曲他滨盐酸盐,并报道利用恩曲他滨盐酸盐实现恩曲他滨的分离纯化。US6600044还报道了恩曲他滨甲磺酸盐。WO2011083484报道了恩曲他滨琥珀酸盐一水合物,以及将其碱化游离制备恩曲他滨。WO2011095987报道,通过将恩曲他滨分别与2-氟苯甲酸、2-甲氧基苯甲酸、3-羟基-2-萘甲酸和L-焦谷氨酸等有机酸成盐,达到从反应混合物中分离纯化恩曲他滨的目的。中国专利申请CN101066971A报道了恩曲他滨水杨酸盐一水合物,但并未公开恩曲他滨水杨酸盐的晶型。在说明书第6页“4、恩曲他滨的水杨酸盐(VI)的制备”中披露的制备方法:以2摩尔当量硼氢化钾为还原剂,在氢氧化钠存在下,在四氢呋喃和水中,还原(2R,5S)-(5-氟胞嘧啶-1-基)-1,3-氧硫杂环戊烷-2-羧酸L-薄荷酯。反应完全后,用10%盐酸调pH至4-5,再用氢氧化钠水溶液调pH至中性。减压回收四氢呋喃后,残留水层用甲苯洗涤后,加入1.1摩尔当量的水杨酸成盐,过滤水洗干燥得恩曲他滨水杨酸盐,收率84%。除核磁共振氢谱外,未见其他表征数据;仅从公开的核磁数据无法得知该制备方法得到的究竟是恩曲他滨水杨酸盐无水物或是一水合物。另外,CN101066971A报道的上述还原方法中,采用硼氢化钾作为还原剂,并且根本没有用到缓冲盐。本发明人重复上述操作发现,加入水杨酸后并无固体析出,无法得到该实施例声称的恩曲他滨水杨酸盐一水合物。CN101066971A已于2009年11月4日被视为公开后撤回专利申请。恩曲他滨是一个光学纯化合物,具有构型为(2R,5S)的两个手性中心。其主流合成路线为基于手性辅基的立体选择性合成。通常,手性辅基L-薄荷醇需要通过还原反应(通常采用硼试剂,例如,硼氢化钠、硼氢化钾;也可以采用其他还原剂,例如,四氢铝锂、二氢双(2-甲氧基乙氧基)铝钠(商品名RED-Al)脱除。经淬灭反应后,加入足量水溶解生成的恩曲他滨,然后以与水不互溶的有机溶剂(例如,甲苯)提走反应混合物中的L-薄荷醇,最后必须从所得的含有无机盐、含硼杂质等复杂成分的水溶液中,经分离纯化得到恩曲他滨。由于恩曲他滨在水中具有较高溶解度,因此,如何将反应产物恩曲他滨从含水的复杂混合物中高效地实施分离纯化,成为实现工业化大生产必须解决的难题。因此,本领域迫切需要提供一种高效的分离纯化恩曲他滨的方法。
技术实现要素:
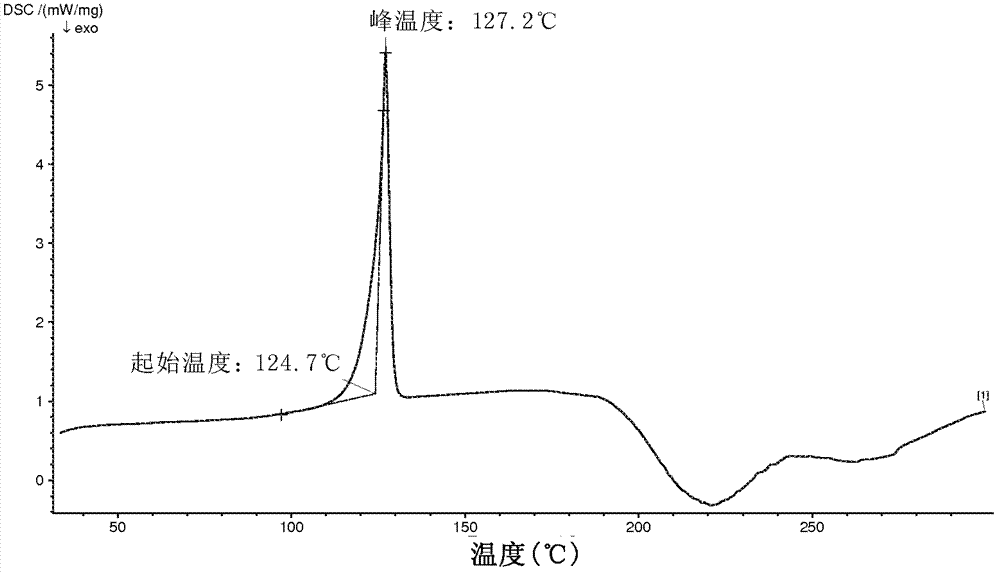
本发明旨在提供新的恩曲他滨水杨酸盐的晶型。本发明的另一个目的是提供上述恩曲他滨水杨酸盐的晶型的制备方法。本发明的再一个目的是提供上述恩曲他滨水杨酸盐的晶型的用途。在本发明的第一方面,提供了化学结构式如式2所示的恩曲他滨水杨酸盐的晶型,其中,式2中,n=0时代表恩曲他滨水杨酸盐无水物以及n=1时代表恩曲他滨水杨酸盐一水合物;在另一优选例中,提供了所述式2中,n=0的恩曲他滨水杨酸盐无水物晶型甲,其X-射线粉末衍射(XRPD)谱(CuKα辐射)中,在下述2θ角有特征峰:7.92±0.2°,9.51±0.2°,13.26±0.2°,14.37±0.2°,16.23±0.2°,19.94±0.2°,20.33±0.2°,22.26±0.2°,23.59±0.2°,26.69±0.2°,32.04±0.2°和38.81±0.2°。在另一优选例中,在所述晶型甲的差示扫描量热(DSC)谱中,有一个主要吸热峰,起始温度为123-127℃,峰温度为125-129℃。在另一优选例中,提供了所述式2中,n=0的恩曲他滨水杨酸盐无水物晶型乙的XRPD谱(CuKα辐射)中,在下述2θ角有特征峰:7.64±0.2°,10.07±0.2°,10.99±0.2°,12.36±0.2°,15.16±0.2°,15.44±0.2°,16.66±0.2°,17.21±0.2°,20.17±0.2°,23.77±0.2°,24.18±0.2°,25.23±0.2°,26.43±0.2°和28.72±0.2°。在另一优选例中,在所述晶型乙的DSC谱中,有一个主要吸热峰,起始温度为107-111℃,峰温度为111-115℃。在另一优选例中,提供了包含上述晶型甲和晶型乙的混合物,以重量计,所述晶型甲的含量为0-100%,所述晶型乙的含量为0-100%;较佳地,该混合物在其DSC谱中有下述两个吸热峰:其中,起始温度为105℃-116℃,更佳地为108℃-115℃;一个吸热峰的峰温度为112℃-120℃,更佳地为115℃-120℃;另一个吸热峰的峰温度为120℃-128℃,更佳地为120℃-127℃;较佳地,该混合物在其XRPD谱(CuKα辐射)中,在下述2θ角有特征峰:7.91±0.2°,10.12±0.2°,12.42±0.2°,14.37±0.2°,15.91±0.2°,16.24±0.2°,16.72±0.2°,20.25±0.2°,24.22±0.2°,25.70±0.2°,26.47±0.2°和28.92±0.2°。在另一优选例中,提供了包含上述晶型甲和晶型乙的混合物,该混合物在其XRPD谱(CuKα辐射)中,在下述2θ角有特征峰:7.91±0.2°,10.12±0.2°,12.42±0.2°,14.37±0.2°,24.22±0.2°和28.92±0.2°。在另一实施方式中,提供了所述式2中,n=1的恩曲他滨水杨酸盐一水合物晶型丙,在其X-射线粉末衍射谱(CuKα辐射)中,在下述2θ角有特征峰:7.22±0.2°,11.43±0.2°,13.76±0.2°,17.98±0.2°,18.65±0.2°,20.76±0.2°,21.44±0.2°,22.17±0.2°,23.67±0.2°,25.31±0.2°,26.77±0.2°和27.73±0.2°。在另一优选例中,所述晶型丙在其DSC谱有三个主要吸热峰,分别是:起始温度为68-72℃,峰温度为82-86℃;起始温度为107-111℃,峰温度为112-116℃以及峰温度为117-121℃。在本发明的第二方面,提供了一种如上所述的本发明提供的恩曲他滨水杨酸盐的晶型的制备方法,所述制备方法包括下述步骤:(a)将恩曲他滨和水杨酸在水中混合、加热溶解,得到混合物a;和(b)将混合物a冷却,得到如上所述的本发明提供的恩曲他滨水杨酸盐。在另一优选例中,在步骤(a)中加热至70-90℃或加热至恩曲他滨和水杨酸完全溶解。在另一优选例中,在步骤(b)中冷却至15-50℃,更佳地至室温-50℃。在本发明的第三方面,提供了一种如上所述的本发明提供的恩曲他滨水杨酸盐的晶型的制备方法,所述制备方法包括下述步骤:(i)将化学结构式如式3所示的化合物和还原剂反应,得到含有恩曲他滨的混合物i;所述还原剂为硼氢化钠;(ii)向混合物i中加入水杨酸成盐,得到含有恩曲他滨水杨酸盐的混合物ii;和(iii)从混合物ii中分离得到如上所述的本发明提供的恩曲他滨水杨酸盐。在另一优选例中,所述含有恩曲他滨的混合物i中的溶剂,以总重量计,其中水的含量为80-100%,更佳地为90-100%。在另一优选例中,所述制备方法包括下述步骤:(i)将化学结构式如式3所示的化合物和还原剂反应,淬灭反应后,将浓缩得到的残留物和水混合,用有机溶剂萃取,得到含有恩曲他滨的混合物i;所述还原剂为硼氢化钠;(ii)向混合物i中加入水杨酸成盐,得到含有恩曲他滨水杨酸盐的混合物ii;和(iii)从混合物ii中分离得到如上所述的本发明提供的恩曲他滨水杨酸盐。更佳地,所述淬灭反应是通过调节体系pH值进行。在另一优选例中,所述有机溶剂是与水不互溶的有机溶剂;更佳地,所述有机溶剂选自甲苯、环己烷。在另一优选例中,步骤(i)是将化学结构式如式3所示的化合物和还原剂反应,通过分液操作分取有机相,通过调节体系pH值淬灭反应,蒸馏溶剂进行浓缩,向所得残留物中加入足量水溶解生成的恩曲他滨,然后以与水不互溶的有机溶剂提走水相混合物中的L-薄荷醇,得到含有恩曲他滨的混合物i。在一优选例中,提供了上述恩曲他滨水杨酸盐的晶型的制备方法,包括以下步骤:(i)在磷酸氢二钾缓冲液和氢氧化钠存在下,在含水的极性溶剂中,将化学结构式如式3所示的化合物和硼氢化钠反应,经后处理,得到含有恩曲他滨的混合物i;所述极性溶剂选自甲醇、乙醇、异丙醇,极性溶剂与水的体积比为2∶1至3∶1;所述后处理包括:静置分层,分取富含产物的有机层,酸化并调节pH至4-4.5,碱化中和并调节pH至6.8-7.2,蒸馏溶剂;向所得残留物中加入足量水,溶解生成的恩曲他滨,然后用与甲苯提走水相混合物中的L-薄荷醇;(ii)向混合物i中加入水杨酸成盐,得到含有恩曲他滨水杨酸盐的混合物ii;其中,式3的化合物和水杨酸的摩尔比为1∶0.9至1∶1.1;(iii)从混合物ii中,经分离和干燥得到如权利要求1所述的恩曲他滨水杨酸盐的晶型;其水分含量为0-5%。在一优选例中,通过卡尔费歇尔滴定法测定水分含量控制所述步骤(iii)中的干燥程度:控制水分含量为0-1%,获得上述恩曲他滨水杨酸盐无水物的晶型甲和晶型乙的混合物;控制水分含量为4-5%,获得上述恩曲他滨水杨酸盐一水合物的晶型丙。在本发明的第四方面,提供了一种如上所述的本发明提供的恩曲他滨水杨酸盐的晶型的用途,所述晶型用于制备高纯度恩曲他滨,所述制备包括下述步骤:将式2化合物与碱化试剂混合,得到高纯度恩曲他滨;所述碱化试剂为叔胺,优选三乙胺。在本发明的第五方面,提供了一种高纯度恩曲他滨的制备方法,将如上所述的本发明提供的恩曲他滨水杨酸盐的晶型作为中间体,所述的制备方法包括步骤:(1)将化学结构式如式3所示的化合物和还原剂反应,得到混合物1;(2)将混合物1和水杨酸混合,加热溶解得到混合物2;(3)将混合物2冷却,得到如上所述的本发明提供的恩曲他滨水杨酸盐;和(4)将所得如上所述的本发明提供的恩曲他滨水杨酸盐与碱化试剂混合,得到恩曲他滨;所述还原剂为硼氢化钠;所述碱化试剂为叔胺,优选三乙胺。在另一优选例中,所述含有恩曲他滨的混合物1中的溶剂,以总重量计,其中水的含量为80-100%,更佳地为90-100%。在另一优选例中,所述的制备方法包括下述步骤:(1)将化学结构式如式3所示的化合物和还原剂反应,淬灭反应后,将浓缩得到的残留物和水混合,用有机溶剂萃取,得到含有恩曲他滨的混合物1;(2)将混合物1和水杨酸混合,加热溶解得到混合物2;(3)将混合物2冷却,得到如上所述的本发明提供的恩曲他滨水杨酸盐的晶型;和(4)将所得如上所述的本发明提供的恩曲他滨水杨酸盐的晶型与碱化试剂混合,得到恩曲他滨;所述还原剂为硼氢化钠;所述碱化试剂为叔胺,优选三乙胺。更佳地,所述淬灭反应是通过调节体系pH值进行。在另一优选例中,所述有机溶剂是与水不互溶的有机溶剂;更佳地,所述有机溶剂选自甲苯、环己烷。在另一优选例中,步骤(1)是将化学结构式如式3所示的化合物和还原剂反应,通过分液操作分取有机相,通过调节体系pH值淬灭反应,蒸馏溶剂进行浓缩,向所得残留物中加入足量水溶解生成的恩曲他滨,然后以与水不互溶的有机溶剂提走水相混合物中的L-薄荷醇,得到含有恩曲他滨的混合物1。在另一优选例中,在步骤(2)中加热至70-90℃或加热至混合物1和水杨酸溶解。在另一优选例中,在步骤(3)中冷却至15-50℃,更佳地室温-50℃。在一优选例中,提供了高纯度恩曲他滨的制备方法,包括以下步骤:(1)在磷酸氢二钾缓冲液和氢氧化钠存在下,在含水的极性溶剂中,将化学结构式如式3所示的化合物和硼氢化钠反应,经后处理,得到混合物1;其中所述极性溶剂选自甲醇、乙醇、异丙醇,极性溶剂与水的体积比为2∶1至3∶1;所述后处理包括:静置分层,分取富含产物的有机层,酸化并调节pH至4-4.5,碱化中和并调节pH至6.8-7.2,蒸馏溶剂;向所得残留物中加入足量水,溶解生成的恩曲他滨,然后用甲苯提走水相混合物中的L-薄荷醇;(2)将混合物1和水杨酸混合,加热溶解得到混合物2;式3化合物和水杨酸的摩尔比为1∶0.9至1∶1.1;(3)将混合物2冷却,分离析出的固体,经干燥,得到如权利要求1所述的恩曲他滨水杨酸盐的晶型;其水分含量为0-5%。(4)将所得如权利要求1所述的晶型与碱化试剂混合,得到恩曲他滨;所述碱化试剂为叔胺,优选三乙胺。在一优选例中,通过卡尔费歇尔滴定法测定水分含量控制所述步骤(3)中的干燥程度:控制水分含量为0-1%,获得上述恩曲他滨水杨酸盐无水物的晶型甲和晶型乙的混合物;控制水分含量为4-5%,获得上述恩曲他滨水杨酸盐一水合物的晶型丙。据此,本发明提供了一种高效的分离纯化恩曲他滨的方法。附图说明图1显示了实施例1所得恩曲他滨水杨酸盐无水物的晶型甲的XRPD谱。图2显示了实施例1所得恩曲他滨水杨酸盐无水物的晶型甲的DSC谱。图3显示了实施例2所得恩曲他滨水杨酸盐无水物的晶型乙的XRPD谱。图4显示了实施例2所得恩曲他滨水杨酸盐无水物的晶型乙的DSC谱。图5显示了实施例3所得恩曲他滨水杨酸盐无水物的甲乙混晶的DSC谱。图6显示了实施例4所得恩曲他滨水杨酸盐无水物的甲乙混晶的DSC谱。图7显示了实施例5所得恩曲他滨水杨酸盐无水物的甲乙混晶的XRPD谱。图8显示了实施例5所得恩曲他滨水杨酸盐无水物的甲乙混晶的DSC谱。图9显示了实施例6所得恩曲他滨水杨酸盐无水物的甲乙混晶的DSC谱。图10显示了实施例7所得恩曲他滨水杨酸盐一水合物的晶型丙的DSC谱。图11显示了实施例8所得恩曲他滨水杨酸盐一水合物的晶型丙的TGA谱。图12显示了实施例8所得恩曲他滨水杨酸盐一水合物的晶型丙的XRPD谱。图13显示了实施例8所得恩曲他滨水杨酸盐一水合物的晶型丙的DSC谱。图14显示了实施例9所得恩曲他滨水杨酸盐无水物的甲乙混晶的DSC谱。具体实施方式在探索有效分离纯化恩曲他滨的过程中,本发明发明人意外地发现了恩曲他滨水杨酸盐无水物的晶型甲、晶型乙、晶型甲和晶型乙任意比例的混合物(或称为甲乙混晶),以及恩曲他滨水杨酸盐一水合物的晶型丙。以所述恩曲他滨水杨酸盐的晶型作为中间体,经碱化游离可以有效获得高纯度(HPLC纯度)的药用级恩曲他滨。与此同时,发明人还发现,通过形成上述恩曲他滨水杨酸盐无水物的晶型甲、晶型乙、晶型甲及晶型乙任意比例的混合物(或称为甲乙混晶),以及恩曲他滨水杨酸盐一水合物的晶型丙,可以实现从还原式3的化合物制备高纯度的药用级恩曲他滨原料药的目的。在此基础上,完成了本发明。高纯度是指美国药典恩曲他滨专论草案征求意见稿(USPPendingMonographDraft1-ForPublicComment,Emtricitabine,2010,TheUnitedStatesPharmacopeia)所记载的三种方法,进行所得恩曲他滨的HPLC纯度检查,单一杂质含量不高于0.1%,总杂质含量不高于0.3%。恩曲他滨水杨酸盐本发明提供的恩曲他滨水杨酸盐的晶型,分子式为C15H16FN3O6S·nH2O(C8H10FN3O3S·C7H6O3·nH2O),化学结构式如式2所示。本发明提供的恩曲他滨水杨酸盐的晶型,不含结晶水(n=0)或为一水合物(n=0)。所述恩曲他滨水杨酸盐可以是单一晶型,例如晶型甲(n=0)、晶型乙(n=0)或晶型丙(n=1);也可以是不同晶型的混合物,例如晶型甲和晶型乙任意比例的混合物(简称:甲乙混晶)。当本发明提供的恩曲他滨水杨酸盐是晶型甲时,在晶型甲的X-射线粉末衍射(XRPD)谱(CuKα辐射)中,在下述2θ角有特征峰:7.92±0.2°,9.51±0.2°,13.26±0.2°,14.37±0.2°,16.23±0.2°,19.94±0.2°,20.33±0.2°,22.26±0.2°,23.59±0.2°,26.69±0.2°,32.04±0.2°和38.81±0.2°。所述晶型甲的典型XRPD谱如图1所示。在晶型甲的差示扫描量热(DSC)谱(温度范围30-300℃,升温速度10℃/分钟)中,有一个主要吸热峰,其起始温度(onsettemperature)为123-127℃,峰温度(peaktemperature)为125-129℃。所述晶型甲的典型DSC谱如图2所示。当本发明提供的恩曲他滨水杨酸盐是晶型乙时,在晶型乙的XRPD谱(CuKα辐射)中,在下述2θ角有特征峰:7.64±0.2°,10.07±0.2°,10.99±0.2°,12.36±0.2°,15.16±0.2°,15.44±0.2°,16.66±0.2°,17.21±0.2°,20.17±0.2°,23.77±0.2°,24.18±0.2°,25.23±0.2°,26.43±0.2°和28.72±0.2°。所述晶型乙的典型XRPD谱如图3所示。在晶型乙的DSC谱(温度范围30-300℃,升温速度10℃/分钟)中,有一个主要吸热峰(起始温度为107-111℃,峰温度为111-115℃)。所述晶型乙的典型DSC谱如图4所示。当本发明提供的恩曲他滨水杨酸盐是晶型甲和晶型乙的混合物时,在其DSC谱(温度范围30-300℃,升温速度10℃/分钟)中,有两个主要吸热峰,分别是:起始温度为105-116℃,峰温度为112-120℃以及峰温度为120-128℃。在本发明提供的一个实施例中,所得恩曲他滨水杨酸盐是晶型甲和晶型乙的混合物,其DSC谱(温度范围30-300℃,升温速度10℃/分钟)如图5所示,其中有两个吸热峰,分别是:起始温度为113.4℃,峰温度为117.9℃以及峰温度为125.4℃。在本发明提供的另一个实施例中,所得恩曲他滨水杨酸盐是晶型甲和晶型乙的混合物,其DSC谱(温度范围30-300℃,升温速度10℃/分钟)如图6所示,其中也有两个吸热峰,分别是:起始温度为111.6℃,峰温度为117.0℃以及峰温度为120.3℃。在本发明提供的又一个实施例中,所得恩曲他滨水杨酸盐是晶型甲和晶型乙的混合物,其XRPD谱如图7所示。在其XRPD谱(CuKα辐射)中,在下述2θ角有特征峰:7.91±0.2°,10.12±0.2°,12.42±0.2°,15.91±0.2°,16.24±0.2°,16.72±0.2°,20.25±0.2°,24.22±0.2°,25.70±0.2°,26.47±0.2°,28.46±0.2°和28.92±0.2°。其DSC谱(温度范围30-300℃,升温速度10℃/分钟)如图8所示,其中有两个吸热峰,分别是:起始温度为114.7℃,峰温度为119.0℃以及峰温度为123.6℃。在本发明提供的再一个实施例中,所得恩曲他滨水杨酸盐是晶型甲和晶型乙的混合物,其DSC谱(温度范围30-300℃,升温速度10℃/分钟)如图9所示,其中有两个吸热峰,分别是:起始温度为108.6℃,峰温度为116.4℃,以及峰温度为121.0℃。当本发明提供的是恩曲他滨水杨酸盐一水合物晶型丙时,在晶型丙的XRPD谱(CuKα辐射)中,在下述2θ角有特征峰:7.22±0.2°,11.43±0.2°,13.76±0.2°,17.98±0.2°,18.65±0.2°,20.76±0.2°,21.44±0.2°,22.17±0.2°,23.67±0.2°,25.31±0.2°,26.77±0.2°和27.73±0.2°。所述晶型甲的典型XRPD谱如图12所示。在晶型丙的DSC谱有三个主要吸热峰,分别是:起始温度为68-72℃,峰温度为82-86℃;起始温度为107-111℃,峰温度为112-116℃以及峰温度为117-121℃。本发明采用“X射线粉末衍射”(X-rayPowderDiffraction,XRPD)谱进行晶型表征。测定样品的XRPD谱的方法在本领域中是已知的。例如使用BrukerD8Advanced型号的X射线粉末衍射仪,采用铜Kα辐射获取样品的XRPD谱。本发明还采用“示差扫描量热”(DifferentialScanningCalorimetry,DSC)谱进行晶型表征。测定样品DSC的方法在本领域中是已知的。例如可使用NetzschDSC204F1热分析仪,以10℃每分钟的升温速率,从30℃升温至300℃,获取样品的DSC谱。本发明还采用“热重分析”(ThermogravimetricAnalysis,TGA)谱进行水合物表征。测定样品TG的方法在本领域中是已知的。例如可使用NetzschTG209F1热分析仪,以10℃每分钟的升温速率,从30℃升温至350℃,获取样品的TGA谱。恩曲他滨水杨酸盐(2)的制备方法本发明提供的恩曲他滨水杨酸盐(2)的制备方法,可以通过将恩曲他滨和水杨酸在溶剂中混合,加热溶解后,经冷却结晶来制备。所述的混合包括但不限于,向含有恩曲他滨的溶液中加入水杨酸,或向含有水杨酸的溶液中加入恩曲他滨。所述含有恩曲他滨的溶液中的恩曲他滨的来源没有限制,其HPLC(HighPerformanceLiquidChromatography,高效液相色谱)纯度可以为60%以上,较佳地为80%以上,更佳地为90%以上;所述的溶剂选自水、有机溶剂、或水和有机溶剂的混合,优选水。所述有机溶剂包括诸如醚类(例如,四氢呋喃、2-甲基四氢呋喃),以及醇类(例如,甲醇、乙醇)。恩曲他滨和水杨酸的摩尔比为1∶0.8至1∶1.5,优选1∶0.9至1∶1.1;最优选1∶1。可以通过本领域通常的技术手段(例如,离心、过滤),将析出的恩曲他滨水杨酸盐从成盐反应母液中分离出来。可以通过本领域通常的技术手段对所得恩曲他滨水杨酸盐进行干燥。干燥方法可以是常压干燥、真空(减压)干燥;干燥温度为0-100℃,优选20-90℃,更优选30-80℃。干燥程度,通常控制产品水分含量为0-5%。冷却结晶时可以加入晶种以利结晶。一般来说,要获得恩曲他滨水杨酸盐无水物的单一晶型,如晶型甲或晶型乙,需要更为严格地控制结晶条件。在获得恩曲他滨水杨酸盐无水物晶型甲的一种实施方式中,将恩曲他滨、水杨酸和水混合,加热溶解至澄清后,冷却、过滤、干燥得到晶型甲。恩曲他滨和水的重量比为1∶80至1∶120,优选为1∶90至1∶110,更优选为1∶95至1∶105;加热至70-90℃;静置冷却至室温充分析晶后,过滤、干燥得到晶型甲。从稀溶液中缓慢析晶趋向于得到恩曲他滨水杨酸盐(2)晶型甲。在获得恩曲他滨水杨酸盐无水物晶型乙的一种实施方式中,将水杨酸和水混合,加热溶解至澄清后加入恩曲他滨溶解,冷却、过滤、干燥得到晶型乙。恩曲他滨和水的重量比为1∶5至1∶15,优选为1∶8至1∶14,更优选为1∶10至1∶12;加热至70-90℃;搅拌冷却至40-60℃(优选45-55℃)时便进行过滤。从浓溶液中快速析晶趋向于得到恩曲他滨水杨酸盐无水物晶型乙。根据本发明记载的内容,本领域的熟练技术人员,可以通过调控结晶反应液的浓度、结晶反应液的温度、搅拌速度、降温速度、反溶剂等结晶工艺参数和工艺条件,来获得各种比例的恩曲他滨水杨酸盐无水物晶型甲和晶型乙的混合物。本发明提供的恩曲他滨水杨酸盐(2)的另一种制备方法的实施方式中,以(2R,5S)-(5-氟胞嘧啶-1-基)-1,3-氧硫杂环戊烷-2-羧酸L-薄荷酯(3)为起始原料,首先经还原反应脱去手性辅基L-薄荷醇,经后处理得到含有恩曲他滨的含水的混合物,然后通过与水杨酸成盐,使得生成的恩曲他滨形成水溶性差的恩曲他滨水杨酸盐(2),从含水的混合物中分离得到。还原反应所用的还原剂选自硼氢化钠、硼氢化钾、四氢铝锂、二氢双(2-甲氧基乙氧基)铝钠(商品名RED-Al),优选硼氢化钠、硼氢化钾;更加优选硼氢化钠。所述还原反应在磷酸盐缓冲液(例如磷酸氢二钾)和无机碱(例如氢氧化钠)存在下,在含水的极性溶剂(例如甲醇、乙醇、异丙醇)中进行。所述的后处理包括下述主要步骤,通过分液操作分取富含产物的有机相,通过调节体系pH值淬灭反应,蒸馏溶剂进行浓缩,向所得残留物中加入足量水溶解生成的恩曲他滨,然后以与水不互溶的有机溶剂(例如,甲苯)提走水相混合物中的L-薄荷醇。所述磷酸盐缓冲液选择磷酸氢二钾,磷酸氢二钾与式3化合物的摩尔比为2.5-3.5∶1,优选2.8-3.2∶1;所述无机碱选择氢氧化钠,氢氧化钠与式3化合物的摩尔比为0.03-0.06∶1,优选0.04-0.05∶1。所述含水的极性溶剂中,极性溶剂与水的体积比优选1.5-3.5∶1,更加优选2-3∶1。通常化合物3和水杨酸的摩尔比为1∶0.8至1∶1.5,优选1∶0.9至1∶1.1,更优选1∶1。恩曲他滨水杨酸盐(2)从中析出的含水的混合物中的溶剂,以总重量计,其中水的含量为80-100%,优选90-100%。恩曲他滨水杨酸盐(2)从含水的混合物中析晶时,接种与否并无特别要求,优选接种。可以通过本领域通常的技术手段(例如,离心、过滤),将析出的恩曲他滨水杨酸盐从成盐反应母液中分离出来。可以通过本领域通常的技术手段对所得恩曲他滨水杨酸盐进行干燥。干燥方法可以是常压干燥、真空干燥;干燥温度为0-100℃,优选20-90℃,更优选30-80℃。干燥程度,通常控制产品水分含量为0-5%。合成路线为:所述化合物3可以按照文献报道的方法制备。例如,欧洲专利申请EP0515157;中国医药工业杂志,2005,36(10):589-590;PCT专利申请WO2007077505。恩曲他滨水杨酸盐的晶型的用途本发明提供的恩曲他滨水杨酸盐的晶型可以作为制备恩曲他滨的中间体。所述恩曲他滨水杨酸盐(2)的晶型并没有特别限定,例如,可以是恩曲他滨水杨酸盐无水物晶型甲、晶型乙、或晶型甲和晶型乙任意比例的混合物,或者是恩曲他滨水杨酸盐一水合物晶型丙。所得中间体恩曲他滨水杨酸盐的晶型经碱化,即可游离得到恩曲他滨(1)。适宜的碱化试剂选自无机碱和有机碱,优选叔胺,更优选三乙胺、二异丙基乙基胺、三正丁胺,最优选三乙胺。适宜的碱化反应的溶剂选自甲醇、乙醇、异丙醇、正丁醇、异丁醇、丙酮、乙酸乙酯、乙酸异丙酯、四氢呋喃、2-甲基四氢呋喃、水,或者其混合物,优选甲醇、乙醇、异丙醇、乙酸乙酯、乙酸异丙酯或者其混合物,更加优选甲醇、乙醇或异丙醇与乙酸乙酯或乙酸异丙酯的混合物。例如,一条以恩曲他滨水杨酸盐(2)作为中间体制备恩曲他滨的合成路线为:在上述合成路线中,以(2R,5S)-(5-氟胞嘧啶-1-基)-1,3-氧硫杂环戊烷-2-羧酸L-薄荷酯(3)起始原料,首先经还原反应脱去手性辅基L-薄荷醇,经后处理得到含有恩曲他滨的含水的混合物,然后通过与水杨酸成盐,使得生成的恩曲他滨形成水溶性差的恩曲他滨水杨酸盐(2),从含水的混合物中分离出来。还原反应所用的还原剂选自硼氢化钠、硼氢化钾、四氢铝锂、二氢双(2-甲氧基乙氧基)铝钠(商品名RED-A1),优选硼氢化钠、硼氢化钾,更加优选硼氢化钠。采用硼氢化钠、硼氢化钾(优选硼氢化钠)作为还原剂时,通常添加磷酸盐或硼酸盐缓冲液以及无机碱,在含水的极性溶剂中进行反应。所述磷酸盐缓冲液,选择磷酸氢二钾,磷酸氢二钾与式3化合物的摩尔比为2.5∶1至3.5∶1,优选2.8∶1至3.2∶1;所述无机碱,选择氢氧化钠,氢氧化钠与式3化合物的摩尔比为0.03∶1至0.06∶1,优选0.04∶1至0.05∶1;所述极性溶剂选自甲醇、乙醇、异丙醇,极性溶剂与水的体积比优选1.5∶1至3.5∶1,更加优选2∶1至3∶1。所述的后处理包括下述主要步骤,通过分液操作分取富含产物的有机相,通过调节体系pH值至pH4-4.5淬灭反应,再进行碱化中和至pH6.8-7.2,蒸馏溶剂进行浓缩,向所得残留物中加入足量水溶解生成的恩曲他滨,然后以与水不互溶的有机溶剂(例如,甲苯)提走水相混合物中的L-薄荷醇。通常化合物3和水杨酸的摩尔比为1∶0.8至1∶1.5,优选1∶0.9至1∶1.1,更优选1∶1。恩曲他滨水杨酸盐(2)从中析出的含水的混合物中的溶剂,以总重量计,其中水的含量为80-100%,优选90-100%。恩曲他滨水杨酸盐(2)从含水的混合物中析晶时,接种与否并无特别要求,优选接种。可以通过本领域通常的技术手段(例如,离心、过滤),将析出的恩曲他滨水杨酸盐从成盐反应母液中分离出来。可以通过本领域通常的技术手段对所得恩曲他滨水杨酸盐进行干燥。干燥方法可以是常压干燥、真空干燥;干燥温度为0-100℃,优选20-90℃,更优选30-80℃。干燥程度,通常控制产品水分含量为0-5%。所述化合物3可以按照文献报道的方法制备。例如,欧洲专利申请EP0515157;中国医药工业杂志,2005,36(10):589-590;PCT专利申请WO2007077505。如本文所用,“HPLC纯度”是指将制备得到的恩曲他滨产品,经过HPLC检测,根据所得到的色谱图谱,进行面积归一法而得到的如式1所示化合物的峰面积在所有峰面积总和中所占有的百分数。采用的HPLC检查,参照美国药典恩曲他滨专论草案征求意见稿(USPPendingMonographDraft1-ForPublicComment,Emtricitabine,2010,TheUnitedStatesPharmacopeia)所记载的三种方法(Procedure1,Procedure2和Procedure3)进行。如本文所用,“室温”是指20-30℃。本发明提到的上述特征,或实施例提到的特征可以任意组合。本案说明书所揭示的所有特征可与任何组合物形式并用,说明书中所揭示的各个特征,可以任何可提供相同、均等或相似目的的替代性特征取代。因此除有特别说明,所揭示的特征仅为均等或相似特征的一般性例子。本发明的主要优点在于:1、本发明提供了新的恩曲他滨水杨酸盐无水物的晶型甲、晶型乙和甲乙混晶,以及恩曲他滨水杨酸盐一水合物的晶型丙。2、本发明提供了一种高纯度的药用级恩曲他滨的制备方法,包括将所述恩曲他滨水杨酸盐的晶型作为中间体,碱化后,将游离得到的恩曲他滨从含水的复杂混合物中高效地实施分离纯化,最终高效地获得高纯度的药用级恩曲他滨。3、本发明提供了一种适合工业化大生产的分离纯化恩曲他滨的方法,克服了现有技术的瓶颈,并具有产业化前景。下面结合具体实施例,进一步阐述本发明。应理解,这些实施例仅用于说明本发明而不用于限制本发明的范围。下列实施例中未注明具体条件的实验方法,通常按照常规条件或按照制造厂商所建议的条件。除非另外说明,否则所有的百分数、比率、比例、或份数按重量计。除非另行定义,文中所使用的所有专业与科学用语与本领域熟练人员所熟悉的意义相同。此外,任何与所记载内容相似或均等的方法及材料皆可应用于本发明方法中。文中所述的较佳实施方法与材料仅作示范之用。本发明通过卡尔费歇尔(KarlFischer)滴定法测定样品中的水分。X-射线衍射谱(XRPD)的测定仪器为BrukerD8AdvanceX-射线衍射仪,测定条件为:CuKα线,管电压40kV,管电流40mA。差示扫描量热(DSC)谱测定仪器为NetzschDSC204F1热分析仪,测定条件为:温度范围30℃至300℃,升温速度10℃/分钟。热重分析(TGA)谱测定仪器为NetzschTG209F1热分析仪,测定条件为:温度范围30℃至350℃,升温速度10℃/分钟。由于测定仪器的不同和测定条件的偏差,XRPD谱、DSC谱和TGA谱可能存在测定误差。在甄别和确定各种晶体结构时,应当将测定误差考虑在内。实施例1恩曲他滨水杨酸盐无水物晶型甲的制备将恩曲他滨(1)(0.5g,2mmol)、水杨酸(0.28g,2mmol)加入水(50ml)中,在搅拌下加热到80℃,溶清后停止搅拌,静置室温析晶两天。过滤,小心挑出几颗针状晶体弃去,真空干燥(80℃,6h),得棉花状白色晶体(0.1g,收率13%):水分(卡尔费歇尔滴定法)0.68%;元素分析(C15H16FN3O6S)C、H、N计算值(%)46.75,4.18,10.90,测定值(%)46.26,3.95,11.02;1HNMR(DMSO-d6)δ11.60(brs,exchangeable,1H),8.22(d,J=7.2Hz,1H),7.85(brs,exchangeable,1H),7.79(dd,J=1.6,8.0Hz,1H),7.61(brs,exchangeable,1H),7.51(m,1H),6.90-6.96(m,2H),6.13-6.16(m,1H),5.45(brs,exchangeable,1H),5.19(t,J=4.0Hz,1H),3.72-3.82(m,2H),3.43(dd,J=5.6,12.0Hz,1H),3.13(dd,J=4.4,12.0Hz,1H)。其XRPD谱见图1,其XRPD谱数据见表1。其DSC谱见图2:有一个吸热峰,起始温度为124.7℃,峰温度为127.2℃。表1实施例1所得晶型甲的XRPD谱数据峰2θ(°)d(A)峰面积相对强度(%)16.61313.354739002.0327.91511.161315321879.9439.5149.28864454523.24413.2626.6704140637.34514.3706.1585191678100.00616.2265.458218281195.37718.8474.7045114095.95819.9364.44992577213.45920.3304.36472933515.301022.2643.98963537918.461122.7613.9037139687.291223.5883.76873593518.751324.6943.602339512.061425.7993.4504119886.251526.6873.3375151217.891628.1283.169862483.261728.9363.083185744.471832.0362.7915158288.261932.8062.727766653.482035.2542.5437130736.822138.8052.31871986410.362240.4842.226399825.21实施例2恩曲他滨水杨酸盐无水物晶型乙的制备将水杨酸(2.79g,20mmol)加入水(55ml)中,油浴加热到88℃溶清后,加入恩曲他滨(5g,20mmol)搅拌溶解。撤去油浴,在搅拌下冷却到48℃后,过滤。真空干燥(65℃,4h),得白色固体(2.01g,收率26%):水分(卡尔费歇尔滴定法)0.72%;元素分析(C15H16FN3O6S)C、H、N计算值(%)46.75,4.18,10.90,测定值(%)46.35,4.14,11.06。其XRPD谱见图3,其XRPD谱数据见表2。其DSC谱见图4:有一个吸热峰,起始温度为108.6℃,峰温度为112.8℃。表2实施例2所得晶型乙的XRPD谱数据峰2θ(°)d(A)峰面积相对强度(%)17.63611.56772140016.16210.0668.78045194939.24310.9858.047313096998.93412.3577.15686030945.56513.5636.523418051.36615.1595.839812412993.76715.4365.7357132386100.00816.6595.31723725328.14917.2115.14786909252.191017.5235.056919181.451117.9834.92871725213.031218.8904.6940125559.481319.6224.52061420810.731420.1724.39842310717.451520.5704.314245423.431621.2594.17592071015.641723.7653.74093144623.751824.1803.67778815066.591925.2273.52736266047.332025.6813.4661130799.882126.4313.36932646819.992227.9913.185019541.482328.7203.10587798858.912429.9352.982528582.162530.6132.9179119419.022631.3632.849820981.582733.3972.68081947714.712836.4172.4651131239.912937.9572.3685108978.233039.8932.258038432.903140.7392.213051003.85实施例3恩曲他滨水杨酸盐无水物晶型甲和晶型乙混合物的制备将恩曲他滨(0.5g,2mmol)加入水(10ml)中,搅拌溶清,再加入水杨酸(0.28g,2mmol),加热溶清。搅拌过夜,任其冷至室温。过滤,用水(20ml)洗涤,真空干燥(80℃,4h),得白色固体(0.61g,收率78%):水分(卡尔费歇尔滴定法)0.35%;元素分析(C15H16FN3O6S)C、H、N计算值(%)46.75,4.18,10.90,测定值(%)46.66,4.24,11.18。其DSC谱见图5:有两个吸热峰,分别是:起始温度为113.4℃,峰温度为117.9℃以及峰温度为125.4℃。实施例4恩曲他滨水杨酸盐无水物晶型甲和晶型乙混合物的制备将水杨酸(0.56g,4mmol)和水(6ml)加热到80℃溶解,再加入恩曲他滨(1g,4mmol)搅拌溶解后,停止保温。在搅拌下冷却到35℃后,过滤。真空干燥,得白色固体(1.03g,收率66%)。其DSC谱见图6:有两个吸热峰,分别是:起始温度为111.6℃,峰温度为117.0℃以及峰温度为120.3℃。实施例5恩曲他滨水杨酸盐无水物晶型甲和晶型乙混合物的制备将磷酸氢二钾(26.91g,117.9mmol)加到水(43ml)中,搅拌溶清后,加入(2R,5S)-(5-氟胞嘧啶-1-基)-1,3-氧硫杂环戊烷-2-羧酸L-薄荷酯(15g,37.5mmol),再加入乙醇(106ml)。在室温滴加硼氢化钠(3g,79mmol)的0.12mol/L氢氧化钠水溶液(14.4ml)。滴加完毕后,再在室温搅拌至反应完全。静置分层。分取有机层,用6mol/L盐酸调节pH=4,再用2mol/L氢氧化钠水溶液调节pH=7。减压浓缩。向所得残留物中加水(200ml),用甲苯(3×110ml)洗涤后,加入水杨酸(5.19g,37.5mmol),加热到70-80℃溶清。接种,冷却到室温后过滤,真空干燥(80℃,4h),得恩曲他滨水杨酸盐(10.1g,收率70%):水分(卡尔费歇尔滴定法)0.35%。取上述所得恩曲他滨水杨酸盐(1g)加热至70℃溶于水(39ml),再加入活性炭(0.1g)同温搅拌脱色30min。趁热过滤,滤液静置过夜。过滤,真空干燥(80℃,4h),得恩曲他滨水杨酸盐精制品,为白色固体(0.27g,收率27%):元素分析(C15H16FN3O6S)C、H、N计算值(%)46.75,4.18,10.90,测定值(%)46.66,4.24,11.18。其XRPD谱见图7,其XRPD谱数据见表3。其DSC谱见图8:有两个吸热峰,分别是:起始温度为114.7℃,峰温度为119.0℃以及峰温度为123.6℃。表3实施例5所得恩曲他滨水杨酸盐的XRPD谱数据峰2θ(°)d(A)峰面积相对强度(%)16.69113.199434171.6227.91411.162812906261.1339.5149.2888155537.37410.1248.7298211143100.00512.4157.12352649512.55614.3686.15932164610.25715.0865.868011620.55815.3785.7570113205.36915.9105.56575109124.201016.2435.45244968023.531116.7195.29847852937.191218.0604.9077103584.911318.9094.689367323.191419.7594.4893121045.731520.2524.38132838713.441620.5714.3140113685.381721.2984.1684204379.681822.1874.0034103594.911922.7583.904142642.022023.5283.7781157877.482124.2193.671813405163.492225.7013.46348091138.322326.4703.36453820818.102426.7463.33042379911.272528.4643.13313070414.542628.9183.08498100438.362729.8462.9911118085.592832.1362.7831179078.482933.4372.6776162207.683036.3802.467571183.373138.4312.3404173698.233239.5342.277634991.663340.6602.217155302.623443.5822.0750112355.32实施例6以恩曲他滨水杨酸盐无水物晶型甲和晶型乙混合物为中间体制备恩曲他滨将磷酸氢二钾(71.76g,314mmol)加到水(115ml)中,搅拌溶清后,加入(2R,5S)-(5-氟胞嘧啶-1-基)-1,3-氧硫杂环戊烷-2-羧酸L-薄荷酯(3)(40g,100mmol),再加入乙醇(284ml)。在室温滴加硼氢化钠(8g,211mmol)的0.12mol/L氢氧化钠水溶液(38.4ml)。滴加完毕后,再在室温搅拌至反应完全。静止分层。分取有机层,加6mol/L盐酸调节pH=4,再加2mol/L氢氧化钠水溶液调节pH=7。减压浓缩。向所得残留物中加水(500g),用甲苯(3×300ml)洗涤后,加入水杨酸(13.83g,100mmol),加热到70-80℃溶清。加入少许实施例5所得恩曲他滨水杨酸盐作为晶种,冷却到室温后过滤。常压干燥,得恩曲他滨水杨酸盐(30.16g,收率78%)。其DSC谱见图9:有两个吸热峰,分别是:起始温度为108.6℃,峰温度为116.4℃以及峰温度为121.0℃。取上述所制备的恩曲他滨水杨酸盐(27g)加入乙醇(60ml)中,加热回流,滴加三乙胺(10.5ml),然后缓慢滴加乙酸乙酯(600ml),1h滴加完毕。然后冷却到室温,过滤,以乙酸乙酯洗涤滤饼,真空干燥(60℃,2h),得恩曲他滨粗品,为白色固体(13.71g,收率79%)。将所得恩曲他滨粗品在异丙醇中脱色重结晶,得药用级恩曲他滨(12.10g,收率88%),熔点154.5-155.7℃,[a]20D-143.51°(c=1,甲醇):参照美国药典恩曲他滨专论草案征求意见稿(USPPendingMonographDraft1-ForPublicComment,Emtricitabine,2010,TheUnitedStatesPharmacopeia)所记载的三种方法,进行所得恩曲他滨的HPLC纯度检查,Procedure1纯度为99.96%,其中最大单杂0.04%;Procedure2纯度为99.82%,其中最大单杂0.05%;Procedure3纯度为99.89%,其中最大单杂0.05%。实施例7恩曲他滨水杨酸盐一水合物晶型丙的制备将恩曲他滨(0.5g,2mmol)加入水(10ml)中,搅拌溶清,再加入水杨酸(0.28g,2mmol),加热溶清。搅拌过夜,任其冷至室温。过滤,用水(20ml)洗涤,常压干燥(50℃,48h),得恩曲他滨水杨酸盐一水合物,为近白色固体(0.60g,收率75%):水分(卡尔费歇尔滴定法)4.45%。其DSC谱见图10:有三个吸热峰,分别为:起始温度为70.0℃,峰温度为83.1℃;起始温度为109.0℃,峰温度为114.8℃以及峰温度为119.6℃。实施例8以恩曲他滨水杨酸盐一水合物晶型丙为中间体制备恩曲他滨将磷酸氢二钾(68.47g,300mmol)加到水(115ml)中,搅拌溶清后,加入(2R,5S)-(5-氟胞嘧啶-1-基)-1,3-氧硫杂环戊烷-2-羧酸L-薄荷酯(3)(40g,100mmol),再加入乙醇(365ml)。在室温滴加硼氢化钠(8g,211mmol)的0.12mol/L氢氧化钠水溶液(38.4ml)。滴加完毕后,再在室温搅拌至反应完全。静止分层。分取有机层,加6mol/L盐酸调节pH=4,再加2mol/L氢氧化钠水溶液调节pH=7。减压浓缩。向所得残留物中加水(500ml),用甲苯(3×300ml)洗涤后,加入水杨酸(13.83g,100mmol),加热到70-80℃溶清。加入少许实施例5所得恩曲他滨水杨酸盐作为晶种,冷却到室温后过滤。常压干燥(50℃,48h),得恩曲他滨水杨酸盐一水合物(32.30g,收率80%):水分(卡尔费歇尔滴定法)4.43%。1HNMR(DMSO-d6)δ8.18(d,J=7.2Hz,1H),7.79(dd,J=1.6,8.0Hz,1H),7.72(brs,exchangeable),7.58(brs,exchangeable),7.51(m,1H),6.90-6.95(m,2H),6.13-6.16(m,1H),5.41(brs,exchangeable),5.19(t,J=4.0Hz,1H),3.72-3.82(m,2H),3.43(dd,J=5.6,12.0Hz,1H),3.12(dd,J=4.4,12.0Hz,1H)。MS-ESI(电喷雾)m/z248.05[M(恩曲他滨)+H]+,495.08[2M(恩曲他滨)+H]+,137.06[M(水杨酸)-H]-。其TGA谱见图11:52.6-114.8℃减重4.12%。其XRPD谱见图12,其XRPD谱数据见表4。其DSC谱见图13:有三个吸热峰,分别为:起始温度为70.0℃,峰温度为85.0℃;起始温度为108.7℃,峰温度2为114.3℃以及峰温度为118.8℃。表4实施例8所得恩曲他滨水杨酸盐一水合物晶型丙的XRPD谱数据峰2θ(°)d(A)峰面积相对强度(%)17.22412.226654412100.028.29310.653513102.4310.9718.057546198.5411.4297.7360923117.0513.7596.43093325161.1614.4916.107637917.0716.7185.298721373.9817.2265.143348108.8917.9834.92861328624.41018.6534.7530825215.21119.6834.50667151.31220.2154.389113682.51320.7634.2745990618.21421.4354.14201756132.31521.8704.06072510446.11622.1674.00692948354.21723.6683.75611138820.91824.5183.627722794.21925.3103.5160735013.52026.7673.32782180440.12127.1433.282641937.72227.7343.21402097738.62328.7693.10067641.42429.3153.044149699.12530.3022.9471548810.12630.8472.896321904.02731.3832.848012332.32832.6702.738748568.92934.8212.574326975.03035.2932.541019183.53136.4782.461150309.23238.2912.348622714.23339.1622.298427385.03440.6652.216826664.9取上述所制备的恩曲他滨水杨酸盐一水合物(28.26g)加入乙醇(80ml)中,加热回流,滴加三乙胺(10.5ml),然后缓慢滴加乙酸乙酯(700ml),1h滴加完毕。然后冷却到室温,过滤,以乙酸乙酯洗涤滤饼,真空干燥(60℃,2h),得恩曲他滨粗品,为白色固体(13.69g,收率79%)。将所得恩曲他滨粗品在异丙醇中脱色重结晶,得药用级恩曲他滨(12.06g,收率88%),熔点154.6-156.8℃,[a]20D-143.59°(c=1,甲醇)。参照美国药典恩曲他滨专论草案征求意见稿(USPPendingMonographDraft1-ForPublicComment,Emtricitabine,2010,TheUnitedStatesPharmacopeia)所记载的三种方法,进行所得恩曲他滨的HPLC纯度检查,Procedure1纯度为99.95%,其中最大单杂0.05%;Procedure2纯度为99.78%,其中最大单杂0.08%;Procedure3纯度为99.88%,其中最大单杂0.05%。实施例9恩曲他滨水杨酸盐无水物晶型甲和晶型乙混合物的制备将实施例8所得恩曲他滨水杨酸盐一水合物(1.00g),真空干燥(50℃,8h;再55℃,8h),得恩曲他滨水杨酸盐无水物,为近白色固体:水分(卡尔费歇尔滴定法)0.51%。其DSC谱见图14:有两个吸热峰,分别为:起始温度为105.1℃,峰温度为114.6℃以及峰温度为120.1℃。比较实施例1恩曲他滨的制备,不采用恩曲他滨水杨酸盐向磷酸氢二钾(13.71g,60mmol)的水(33.5ml)溶液中加入(2R,5S)-(5-氟胞嘧啶-1-基)-1,3-氧硫杂环戊烷-2-羧酸L-薄荷酯(3)(10g,25mmol)和无水乙醇(90ml),冰水浴冷却至15℃。缓慢滴加含1%NaOH(2ml)的硼氢化钠(1.89g,50mmol)的水(16ml)溶液。滴毕,室温搅拌至反应完全。静止分层。分取有机层,加6mol/L盐酸调节pH为4,再用2mol/L氢氧化钠水溶液调节pH为7。减压浓缩,加水(60ml)稀释,用甲苯(3x50ml)洗涤。水层用活性炭常温脱色后,减压蒸馏至干。向所得残留物中加入无水乙醇(120ml),加热至回流,趁热过滤。滤液减压浓缩至大约30ml,室温搅拌析晶。过滤,真空干燥得恩曲他滨粗品白色固体(4.25g,69%),为白色固体:熔点145.8-148.5℃,[a]20D-137.10°(c=1,甲醇)。将所得恩曲他滨粗品(4.20g)在异丙醇中脱色重结晶,得恩曲他滨(3.40g,收率81%):熔点151.4-154.8℃,[a]20D-143.10°(c=1,甲醇)。参照美国药典恩曲他滨专论草案征求意见稿(USPPendingMonographDraft1-ForPublicComment,Emtricitabine,2010,TheUnitedStatesPharmacopeia)所记载的三种方法,进行所得恩曲他滨的HPLC纯度检查,Procedure1纯度为99.24%,其中最大单杂0.67%;Procedure2纯度为99.09%,其中最大单杂0.80%;Procedure3纯度为99.18%,其中最大单杂0.65%。本发明采用水杨酸盐无水物甲乙混晶和水杨酸盐一水合物晶型丙,恩曲他滨粗品收率高于采用琥珀酸盐一水合物的WO2011/083484,与采用2-氟苯甲酸盐的WO2011/095987和采用盐酸盐的WO2009/084033相当(表5)。水杨酸与2-氟苯甲酸相比,更为价廉易得;水杨酸与WO2009/084033采用的氯化氢的异丙醇溶液相比,更为操作简便,更为绿色环保。另方面,本发明采用水杨酸盐无水物甲乙混晶和水杨酸盐一水合物晶型丙分离纯化恩曲他滨,恩曲他滨总收率与采用盐酸盐的WO2011/107920相当;尤其,本发明所制备的恩曲他滨具有高纯度,参照美国药典恩曲他滨专论草案征求意见稿所记载的三种方法,进行其HPLC纯度检查,单一杂质均不高于0.1%,总杂质均不高于0.3%(表5)。水杨酸与WO2011/107920采用的氯化氢的异丙醇溶液相比,更为操作简便,更为绿色环保。此外,不通过成盐进行分离纯化的比较实施例1所制备的恩曲他滨,其HPLC纯度最低,虽经重结晶仍然无法达到药用标准(表5)。总之,根据收率、纯度、成本和操作简便性等多项指标综合评价,与现有技术相比,本发明采用所述水杨酸盐无水物或一水合物的晶型分离纯化恩曲他滨的技术效果最优。表5恩曲他滨分离纯化方法比较注1:为还原成盐和碱化游离两步的收率。注2:为还原成盐、碱化游离和重结晶三步的收率。注3:WO2011/107920测定方法不详。本发明采用美国药典恩曲他滨专论草案征求意见稿所记载的三种方法,进行HPLC纯度检查。以上所述仅为本发明的较佳实施例而已,并非用以限定本发明的实质技术内容范围,本发明的实质技术内容是广义地定义于申请的权利要求范围中,任何他人完成的技术实体或方法,若是与申请的权利要求范围所定义的完全相同,也或是一种等效的变更,均将被视为涵盖于该权利要求范围之中。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1