用于糖尿病慢性并发症的SOCS1衍生肽的制作方法
发明目的本发明涉及一种socs1衍生肽,所述socs1衍生肽可用于预防或治疗糖尿病慢性并发症,尤其是眼、肾、神经和血管并发症。所述糖尿病的眼部并发症包括糖尿病性视网膜病和黄斑水肿。基于socs1衍生肽的神经保护性,其除了对糖尿病性视网膜病(其神经变性起到基本作用)有效外,本发明(所述肽)被认为对视网膜的其它疾病(例如获得性或遗传性视网膜神经变性疾病)也具有潜在的有效性。
背景技术:
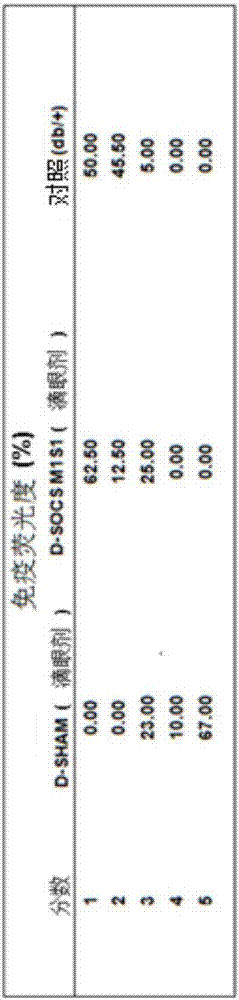
:糖尿病是一种多发的系统性疾病,经常导致一些器官病变,尤其是视网膜、肾脏、神经和血管系统。糖尿病并发症通常分为:a)急性并发症,如低血糖,酮酸中毒和高渗性昏迷;b)慢性或晚期并发症,又分为微血管并发症(肾病、视网膜病和神经病),大血管并发症(心血管疾病)和糖尿病足(大血管和微血管病)。糖尿病的巨大社会健康影响是由于糖尿病的这些慢性并发症,主要是眼部(视网膜病),肾(肾病)和血管(动脉粥样硬化)并发症。目前用于治疗糖尿病的方法,例如严格地控制葡萄糖和高血压,成功地阻止疾病的恶化,但是在许多情况下不能阻止慢性并发症的发作,尤其在视网膜病、心血管疾病,或者患者发展为肾衰竭,甚至参与透析和移植方案。糖尿病足是糖尿病最常见的糖尿病并发症之一,引起显著的发病率和高截肢风险,并且其治疗需要多学科方法。糖尿病性视网膜病是糖尿病最常见的并发症,也是全世界失明的主要原因之一。高血糖症和与其直接相关的代谢途径引起糖尿病性视网膜病的发病,并造成位于视网膜内的毛细血管床的损伤(微血管病变)。糖尿病性视网膜病变通常被认为是视网膜的微血管病变。然而,目前的证据表明,神经变性是参与微血管病变的发展的糖尿病性视网膜病发病的早期现象。目前对糖尿病性视网膜病的初始阶段没有特定疗法。此外,在疾病晚期阶段采取的特定疗法(激光凝固、玻璃体内注射试剂例如抗-vegf-“血管内皮生长因子”抗体、肾上腺皮质激素,或玻璃体切除术)效力有限,且具有很高的副作用。因此,非侵入性治疗方法对在初始阶段(神经变性)预防或治疗糖尿病性视网膜病是必要的。局部眼部给药(滴眼剂),因其非侵入性且能预防系统性副作用,将是最合适的给药途径。除了糖尿病性视网膜病之外,还存在伴随视网膜神经变性的其他疾病,例如老年性黄斑变性(amd)、青光眼和色素性视网膜炎。视网膜的神经变性疾病是指以渐进性神经元丢失为特征的视网膜病症。schmidt等对这些疾病、其关键部位,以及可能的保护途径和促使恢复的途径进行了深入分析。参见“neurodegenerativediseasesoftheretinaandpotentialfortheprotectionandrecovery”,currentneuropharmacology-2008,vol.no.6,pp.:164-178。在糖尿病性视网膜病中,神经变性(有效神经元的损失)发生在疾病的早期阶段,并导致眼睛功能异常,例如辨色力和对比敏感度的丧失。这些改变可通过在糖尿病患者体内,甚至是在患糖尿病低于两年的患者体内的电生理学研究来检测,即可在微血管损伤之前在眼科检查中进行检测。而且,延迟的多焦视网膜电图潜伏时间(mferg-it)来预测早期微血管异常的发展。另外,神经视网膜变性启动和/或激活的几种代谢和信号通路,参与微血管病变过程和血液-视网膜屏障(brb)的破坏。brb是一种眼睛的结构,它在视网膜的许多疾病中至关重要,特别地,它是糖尿病性视网膜病发病机理中的关键因素。brb由内部brb和外部brb组成。内部brb由紧密的内皮细胞连接而成。外部brb由视网膜色素上皮细胞(rpe)组成,细胞之间也紧密连接。糖尿病性黄斑水肿是由brb的破坏而引起。amd是由于brb的破坏而导致视网膜水肿的另一种常见的视网膜疾病。并且,brb的破坏也发生在许多眼部情况中,例如葡萄膜炎、创伤、眼内手术、血管视网膜病、遗传性营养不良等(cunha-vaz等,“theblood-retinalbarrierinretinaldisease”,europeanophthalmicreview-2009,vol.no.3,pp.:105-108)。近年来,研究者正在努力了解涉及糖尿病并发症发展的分子机制,以及研究它们对糖尿病并发症的治疗潜力。jak/stat(januskinase/signaltransducersandactivatorsoftranscription)信号通路是一种重要的细胞内机制,高血糖及其他因素通过它促成糖尿病及其并发症的发展。jak/stat途径控制许多细胞进程,例如增殖、迁移和分化,以及炎症介质的表达。据称,在粥样斑块中、在糖尿病患者的肾活检中以及在视网膜病和糖尿病性肾病的动物模型中中均有jak/stat途径成员的表达和活化的增加。socs(suppressorsofcytokinesignaling,细胞因子信号转导抑制物)蛋白家族是jak/stat途径负调控的主要内源性机制,并且其表达水平的改变与不同的免疫和炎性疾病相关。对socs蛋白家族成员遗传修饰的动物实验研究已经证明,socs蛋白家族在胰腺β-细胞中的保护作用,降低了糖尿病的发病率(等,diabetes2003;52:2696-700)和相关的肾损伤(等,jamsocnephrol2010;21:763-72)以及抗动脉粥样硬化效应(等,arteriosclerthrombvascbiol2009;29:525-531;wesoly等,actabiochimpol2010;57(3):251-260;liang等,intjmolmed.2013may;31(5):1066-74)。表明了这些内源性蛋白在糖尿病并发症中的治疗潜力。在之前的实验变态反应性脑脊髓炎(多发性硬化模型)(mujtaba等,jimmunol2005;175:5077-5086;jager等,jneuroimmunol2011;232:108-118)以及外周神经损伤模型(girolami等,expneurol2010;223:173-182)和痘病毒的病毒感染(ahmed等,jvirol2009;83:1402-1415)中已经描述了socs蛋白模拟肽的使用。socs多肽也被描述为细胞因子诱导信号传导的抑制剂,特别是在炎症和病毒或细菌感染中的抑制剂(us2009/0209458)。专利wo2010/151495描述了可用作抗病毒剂的socs-1或socs-3拮抗剂肽。专利文献us8,420,096描述了含有socs1/socs3序列和膜转位序列的可溶性肽及其在治疗免疫疾病中的潜在应用。专利us2009253618还描述了该类型肽在神经元分化中的应用。专利us2009030179使用这些肽socs-盒区域的几种合成肽作为抗菌剂。尽管在该领域中存在研究,事实上已假定jak/stat信号传导通路,socs蛋白和糖尿病之间存在关系,但是用于预防或治疗糖尿病的眼部、肾或血管并发症的肽自身的有效给药方式,迄今尚未被描述。socs模拟肽与眼部疾病也不相关。技术实现要素:已经发现,对应于socs1蛋白区域的多肽在治疗糖尿病动物模型体内的糖尿病慢性并发症中是有效的。另外,已经发现所述多肽能有效治疗视网膜神经变性疾病。因此,第一方面,本发明涉及一种用于预防或治疗糖尿病慢性并发症和/或视网膜神经变性疾病的分离多肽,所述多肽包括:a)序列seqidno2(dthfrtfrshadyrri);或b)a)的序列的变异体,其基于所述序列的所有氨基酸的同一性,与seqidno2的同一性至少为85%;所述糖尿病慢性并发症选自由糖尿病性视网膜病、黄斑水肿、糖尿病性肾病、糖尿病性血管病、糖尿病性微血管病、糖尿病性大血管病、糖尿病性动脉粥样硬化、糖尿病足和外周动脉疾病构成的组;所述视网膜神经变性疾病选自由糖尿病性视网膜病、青光眼和色素性视网膜炎构成的组。第二方面,本发明涉及一种包含有效治疗量的第一方面所述的多肽和至少一种药学上可接受的载体或赋形剂的组合物在预防或治疗糖尿病慢性并发症或视网膜的神经变性疾病中的应用;所述糖尿病慢性并发症选自由糖尿病性视网膜病、黄斑水肿、糖尿病性肾病、糖尿病性血管病、糖尿病性微血管病、糖尿病性大血管病、糖尿病性动脉粥样硬化、糖尿病足和外周动脉疾病构成的组;所述视网膜神经变性疾病选自由糖尿病性视网膜病、青光眼和色素性视网膜炎构成的组。第三方面,本发明涉及一种用于预防或治疗糖尿病慢性并发症和/或视网膜神经变性疾病的分离多核苷酸,所述多核苷酸编码:a)氨基酸序列seqidno2;或b)a)或b)的序列的变异体,其与序列seqidno2的同源性至少为85%;所述糖尿病慢性并发症选自由糖尿病性视网膜病、黄斑水肿、糖尿病性肾病、糖尿病性血管病、糖尿病性微血管病、糖尿病性大血管病、糖尿病性动脉粥样硬化、糖尿病足和外周动脉疾病构成的组;所述视网膜的神经变性疾病选自由糖尿病性视网膜病、青光眼和色素性视网膜炎。本发明另一方面是一种分离多肽在制备用于预防或治疗糖尿病慢性并发症和/或视网膜神经变性疾病的药物中的应用,所述多肽包含:a)序列seqidno2(dthfrtfrshadyrri);或b)a)的序列的变异体,其基于所述序列的所有氨基酸的同一性,与seqidno2的同一性至少为85%;所述糖尿病慢性并发症选自糖尿病性视网膜病、黄斑水肿、糖尿病性肾病、糖尿病性血管病、糖尿病性微血管病、糖尿病性大血管病、糖尿病性动脉粥样硬化、糖尿病足和外周动脉疾病构成的组;所述视网膜神经变性疾病选自由糖尿病性视网膜病、青光眼和色素性视网膜炎构成的组。本发明还涉及一种用于预防或治疗糖尿病慢性并发症和/或视网膜神经变性疾病的分离多核苷酸,所述多核苷酸编码:a)氨基酸序列seqidno2;或b)a)的序列的变异体,其与序列seqidno2的同源性至少为85%;所述糖尿病慢性并发症选自糖尿病性视网膜病变、黄斑水肿、糖尿病性肾病、糖尿病性血管病、糖尿病性微血管病、糖尿病性大血管病、糖尿病性动脉粥样硬化、糖尿病足和外周动脉疾病构成的组;所述视网膜的神经变性疾病选自糖尿病性视网膜病、青光眼和色素性视网膜炎构成的组。本发明也涉及一种分离多核苷酸在制备用于预防或治疗糖尿病慢性并发症和/或视网膜神经变性疾病的药物中的应用,所述多核苷酸编码:a)氨基酸序列seqidno2;或b)a)的序列的变异体,其与序列seqidno2的同源性至少为85%;所述糖尿病慢性并发症选自由糖尿病性视网膜病变、黄斑水肿、糖尿病性肾病、糖尿病性血管病、糖尿病性微血管病、糖尿病性大血管病、糖尿病性动脉粥样硬化、糖尿病足和外周动脉疾病构成的组;所述视网膜的神经变性疾病选自由糖尿病性视网膜病、青光眼和色素性视网膜炎构成的组。最后一方面,本发明涉及一种向患有糖尿病慢性并发症和/或患有视网膜神经变性疾病的患者施用有效治疗量的第一方面所述的多肽的治疗方法,所述糖尿病慢性并发症选自由糖尿病性视网膜病变、黄斑水肿、糖尿病性肾病、糖尿病性血管病、糖尿病性微血管病、糖尿病性大血管病、糖尿病性动脉粥样硬化、糖尿病足和外周动脉疾病构成的组;所述视网膜的神经变性疾病选自由糖尿病性视网膜病、青光眼和色素性视网膜炎构成的组。这些化合物可用作视网膜的局部神经保护剂。必须指出的是,本发明所使用的肽的局部给药方式,不仅能到达视网膜,而且还达到有效浓度,以预防糖尿病性视网膜病的发展。附图说明图1.糖尿病视网膜病变模型中血糖和体重的变化。(a)为整个研究中糖尿病视网膜病变模型的血糖水平示意图,(b)为整个研究中糖尿病视网膜病变模型的体重示意图。用抑制肽进行处理不影响这些参数(血糖和体重)。图2.socs1衍生肽的局部给药(滴眼剂)对神经胶质激活的影响;基于用载体[d-sham]处理的糖尿病小鼠,用含有socs1衍生肽[d-socsm1s1]的滴眼剂处理的糖尿病小鼠以及非糖尿病小鼠[对照(db/+)]中,代表性样品的视网膜中gfap(glialfibrillaracidicprotein,胶质纤维酸性蛋白质)染色的测量来进行神经胶质激活量化。图3.socs1衍生肽的局部给药(滴眼剂)对细胞凋亡的影响。通过tunel(terminaltransferasedutpnick-endlabeling,末端转移酶dutp缺口末端标记)技术测定用载体[d-sham]处理的糖尿病小鼠,非糖尿病小鼠[对照(db/+)]以及用socs1衍生肽[d-socsm1s1]处理的糖尿病小鼠中,每组代表性小鼠神经视网膜中阳性细胞的百分比。结果表示为平均值±sd。*:与其他组相比p<0.01。图4.用socs1衍生肽的治疗改善erg异常。(a)为实验组中a波振幅(上图)和a波潜伏期(下图)的示意图。(b)为实验组中b波振幅(上图)和b波潜伏期(下图)的示意图。图5.用socs1衍生肽的治疗阻止糖尿病引起的brb破坏。用载体[d-sham]处理的糖尿病小鼠和用socs1衍生肽[d-socsm1s1]处理的糖尿病小鼠中具有代表性的糖尿病小鼠,及非糖尿病小鼠[对照(db/+)]中评估的任意单位荧光(a.u.)中白蛋白外渗量。结果表示为平均值±sd。*:与其他组相比p<0.01。图6.用socs1衍生肽的治疗改善糖尿病小鼠中谷氨酸的代谢。(a)为任意单位荧光(a.u.)中glast免疫荧光值示意图。结果表示为平均值±sd。(b)为实验组中通过uplc测定的视网膜中谷氨酸的浓度示意图。结果表示为平均值±sd。*:与其他组相比p<0.001,**:与对照组相比p<0.01。图7.socs1衍生肽降低糖尿病性视网膜病中炎症基因的表达。采用rt-pcr测定用载体[d-sham]处理的糖尿病小鼠,非糖尿病小鼠(对照(db/+)以及用socs1衍生肽[d-socsm1s1]处理的糖尿病小鼠中il-1βmrna的表达量。结果表示为平均值±sd。*:与其他组相比p<0.05。rq:相对定量。图8.socs1衍生肽抑制糖尿病小鼠肾脏中stat的激活。对糖尿病小鼠肾切片中磷酸化的stat1和stat3进行免疫检测。图8显示了肾小球和肾小管间质区室的阳性染色量。结果表示为平均值±sd。*:与对照组相比p<0.02。图9.socs1衍生肽对糖尿病小鼠的肾保护作用。(a)为肾小球病变(hyper:细胞增生,mm:肾小球系膜,dil:毛细血管扩张),纤维化和肾小管变性(tub)及纤维化和间质炎症(int)的半定量评估示意图。(b)为肾小球面积的形态学分析示意图。(c)为pas+肾小球系膜面积的定量示意图。结果表示为平均值±sd。*:与其他组相比p<0.05。图10.socs1衍生肽阻止糖尿病性肾病的肾纤维化。(a)为糖尿病小鼠(对照和socs1)肾样品中肾小球和肾小管间质区室中胶原蛋白含量的定量分析示意图。(b)为肾皮质中细胞外基质蛋白(纤连蛋白和i型胶原蛋白),前纤维化因子(tgf-β)和肾小管病变标记(kim-1)mrna表达的rt-pcr分析示意图。结果表示为平均值±sd。*:与其他组相比p<0.05。图11.socs1衍生肽对糖尿病肾脏的抗炎作用。(a)为糖尿病小鼠肾样品中巨噬细胞(f4/80)和t-淋巴细胞(cd3)渗透的免疫过氧化物酶检测。图11a显示了肾小球和肾小管间质中的阳性细胞量。(b)为肾皮质中趋化因子(ccl2和ccl5)和tnfα细胞因子的mrna表达量的rt-pcr分析示意图。数据表示为平均值±sem。*:与对照组比较p<0.05。图12.mis1肽对实验性糖尿病的抗动脉粥样硬化作用。(a)为糖尿病小鼠横向主动脉切片中粥样斑块的大小随时间的变化示意图。(b)为糖尿病小鼠动脉粥样硬化病变中炎症内含物(moma2巨噬细胞染色)和斑块稳定性标记物(用天狼猩红染色胶原纤维和用α-肌动蛋白染色血管细胞)含量示意图。*:与对照组比较p<0.05。图13.socs1衍生肽及其无活性突变体对照的体外效果。(a)为在不同浓度的socs1衍生肽或突变肽存在下用细胞因子刺激的巨噬细胞中stat1和stat3的激活示意图。(b)为巨噬细胞和vsmc中产生的ccl2趋化蛋白示意图。c为巨噬细胞迁移分析示意图。*:相对基线条件p<0.05;#:与细胞因子刺激相比p<0.05。具体实施方式如上所述,本发明的第一方面涉及一种用于预防或治疗糖尿病慢性并发症和/或视网膜神经变性疾病的分离多肽,所述多肽包括:a)序列seqidno2(dthfrtfrshadyrri);或b)a)的序列的变异体,其基于所述序列的所有氨基酸的同一性,与seqidno2的同一性至少为85%;所述糖尿病慢性并发症选自由糖尿病性视网膜病、黄斑水肿、糖尿病性肾病、糖尿病性血管病、糖尿病性微血管病、糖尿病性大血管病、糖尿病性动脉粥样硬化、糖尿病足和外周动脉疾病构成的组;所述视网膜神经变性疾病选自由糖尿病性视网膜病、青光眼和色素性视网膜炎构成的组。本发明中提及的任何序列,尤其是seqidno1,seqidno2和seqidno3中的一个或多个氨基酸可以被修饰,例如它们可以被磷酸化。根据一些具体的实施方式,所述序列中仅一个氨基酸被修饰,优选为磷酸化。根据优选的实施方方式,磷酸化的氨基酸为酪氨酸(y)。本发明中,用语“%的同一性”或“至少%相同”是指氨基酸序列之间,通过以下方法测定的同一性的百分比:两个氨基酸序列的比对通过https://www.ebi.ac.uk/tools/msa/clustalw2/提供的服务,应用该服务的默认调整。因此,例如,seqidno1为本发明所定义的seqidno序列的变异体。本发明中,用语“糖尿病慢性并发症”应理解为包括但不限于眼,肾,神经和血管的并发症或病症,用语“血管”应理解为包括心血管和脑血管的并发症。具体地,其包括选自糖尿病性视网膜病、黄斑水肿、糖尿病性肾病和糖尿病性血管病(包括微血管病和大血管病,例如糖尿病性动脉粥样硬化,糖尿病足和外周动脉疾病)的并发症。因此,本发明所述肽用于预防或治疗选自糖尿病患者的眼,肾,神经和心血管并发症或病症的糖尿病慢性并发症。因此,在一些特定的实施方式中,糖尿病慢性并发症选自由糖尿病性视网膜病、黄斑水肿、糖尿病性肾病、糖尿病性血管病、糖尿病性微血管病、糖尿病性大血管病、糖尿病性动脉粥样硬化、糖尿病足和外周动脉疾病构成的组。根据优选的实施方式,糖尿病慢性并发症为眼部疾病,特别为糖尿病性视网膜病。本发明所述肽还可用于治疗视网膜神经变性疾病。本发明中,用语“视网膜神经变性疾病”应理解为包括由于神经胶质炎症(神经胶质激活或反应性神经胶质增生)而存在的眼部疾病。所述神经胶质炎症是由于视网膜神经元凋亡而导致的进行性神经元死亡,特别是光感受器,其可导致失明。所述疾病包括但不限于糖尿病性视网膜病、青光眼和色素性视网膜炎。根据本发明的一些具体实施方式,所述疾病选自由糖尿病性视网膜病,青光眼和色素性视网膜炎。根据优选的实施方式,视网膜的神经变性疾病为糖尿病性视网膜病构成的组。本发明中,用语“神经保护”应理解为包括但不限于可以使用的任何类型的预防性治疗或方法,使得形成神经视网膜的神经元保持在对应于健康受试者动物(包括人)的生理状态。“神经视网膜”是视网膜的神经感觉部分,并且负责视觉周期。特别地,本发明“用于局部治疗和/或预防”的肽,应理解为包括但不限于用于眼睛的局部治疗和/或预防,特别是视网膜神经变性疾病,选自糖尿病性视网膜病,青光眼和色素性视网膜炎。根据一个具体的实施方式,序列seqidno2的变异体与seqidno2的同一性至少为90%,甚至更优选约为94%;其位点相对应,例如序列seqidno2中一个氨基酸被另一个氨基酸取代,或者向序列seqidno2添加一个氨基酸。根据一个具体的实施方式,该变异体可以是seqidno1(dthfrtfrshsdyrri)。因为该序列在哺乳动物中高度保守,因此其它哺乳动物,如褐家鼠、大猩猩、家兔、黑猩猩、苏门答腊猩猩、荷兰猪或野猪,也均具有seqidno1或seqidno2。根据优选的实施方式,该序列seqidno2或其具有如上所述的百分比同一性的变异体,与细胞通透性区域结合。所述细胞通透性区域可以选自不同的通透性序列,通常是小的阳离子或疏水性肽,例如tat(seqidno4:ygrkkrrqrrr)、antp(seqidno5:rqikiwfqnrrmkw)、ptd-5(seqidno6:rrqrrtsklmkr)、seqidno7:8k(k=lys)和seqidno8:6r(r=arg)。更优选地,细胞通透性区域为赖氨酸-棕榈酸酯区域。甚至更优选地,细胞通透性区域结合在seqidno2或其同一性变异体的氨基末端。包含上述提到的序列或以如上定义的相同变异序列的任意多肽,均在本发明的保护范围内。然而,根据优选的实施方式,所述多肽主要由以下组成:a)序列seqidno2;或b)a)的序列的变异体,其基于所述序列的所有氨基酸的同一性,与seqidno2的同一性至少为85%。特别地,变异序列由序列seqidno1组成。本发明中,用语“主要由...组成”是指所定义的序列或其同源序列最多包含8个额外的氨基酸(换句话说,最多50%以上),在优选的实施方式中,最多7、6、5、4、3、2或1个额外的氨基酸,独立地与所述序列的氨基末端,羧基末端或序列的任何位点结合,成为序列的一部分。在之前的任何情况下,所述序列可能会也可能不会与如上定义的细胞通透性区域结合。根据一些具体的实施方式,所述多肽由序列seqidno2组成,其可能会也可能不会与如上定义的细胞通透性区域结合。在多肽用于糖尿病患者的眼部并发症或用于视网膜变性疾病例如糖尿病性视网膜病的情况下,根据一些具体的实施方式,含有seqidno2的序列或其如上定义的相同变异序列的多肽主要由以下组成或为:a)小鼠socs1蛋白[uniprot(universalprotein):o35716];b)人socs1蛋白(uniprot:o15524);或c)a)或b)的序列的变异体,其与小鼠socs1蛋白的氨基酸序列或人socs1蛋白的氨基酸序列的同源性至少为85%。与前述的任何具体实施方式一样,人或小鼠的socs1蛋白,或其相同变异体中的至少一个氨基酸可被修饰,优选为磷酸化。根据优选的实施方式,磷酸化的氨基酸或磷酸化氨基酸之一为酪氨酸(y)。同样,前述定义的socs1蛋白可以结合到细胞通透性区域,优选结合到棕榈酸酯-赖氨酸团体上。根据优选的实施方式,细胞通透性区域结合在多肽的n末端,细胞通透性区域更优选为棕榈酸酯-赖氨酸团体。所述至少85%同一性的变异体包括其他哺乳动物的socs1蛋白,例如褐家鼠、大猩猩、家兔、黑猩猩、苏门答腊猩猩、荷兰猪或野猪。根据具体的实施方式,人或小鼠socs1序列的变异序列与所述序列至少90%相同,甚至更优选约94%相同。本发明第一方面所指示的所有优选实施例也可应用于本发明的其余方面,下面将详细提供。本发明另一方面是一种分离多肽在制备用于预防或治疗糖尿病慢性并发症和/或视网膜神经变性疾病的药物中的应用,所述多肽包含:a)序列seqidno2(dthfrtfrshadyrri);或b)a)的序列的变异体,其基于所述序列的所有氨基酸的同一性,与seqidno2的同一性至少为85%;所述糖尿病慢性并发症选自由糖尿病性视网膜病、黄斑水肿、糖尿病性肾病、糖尿病性血管病、糖尿病性微血管病,糖尿病性大血管病、糖尿病性动脉粥样硬化、糖尿病足和外周动脉疾病构成的组;所述视网膜神经变性疾病选自由糖尿病性视网膜病、青光眼和色素性视网膜炎构成的组。根据本发明的另一方面,其涉及包含治疗有效量的根据上述任何一方面所述的多肽和至少一种药学上可接受的载体或赋形剂的组合物在预防或治疗糖尿病慢性并发症或视网膜的神经变性疾病中的应用;根据上述定义,其中,所述糖尿病慢性并发症选自由糖尿病性视网膜病变、黄斑水肿、糖尿病性肾病、糖尿病性血管病、糖尿病性微血管病、糖尿病性大血管病、糖尿病性动脉粥样硬化、糖尿病足和外周动脉疾病构成的组;其中,所述视网膜神经变性疾病选自由糖尿病性视网膜病变、青光眼和色素性视网膜炎构成的组。在本发明的优选实施方式中,所述组合物适用于或旨在用于预防或治疗糖尿病患者的眼部疾病和/或视网膜神经变性疾病,优选糖尿病性视网膜病。它还可以用于其他的视网膜神经变性疾病,例如,青光眼和色素性视网膜炎。因此,根据一些具体实施方式,所述载体或赋形剂是适于眼部给药的药学上可接受的载体或赋形剂。本发明所述组合物包含至少一种药学上可接受的载体或赋形剂。用语“药学上可接受的载体或赋形剂”是指与本发明所述肽一起施用的分子物质或实体。所述的载体或赋形剂将适合于所选的给药途径,并且根据给药途径所述载体或赋形剂对于本领域技术人员而言是显而易见的。所述载体可以是无菌液体,例如水或油,包括来自石油、动物、植物或合成来源的赋形剂、崩解剂、润湿剂或稀释剂。例如在e.w.martin的“remington'spharmaceuticalsciences”中记载了合适的载体和赋形剂,通过引用并入本文。本发明所述的组合物可以通过任何已知的途径给药,包括口服、胃肠道、非肠道、直肠,或通过呼吸途径和局部给药,特别是眼部给药。同样地,组合物可以含有对于本领域技术人员显而易见的其它合适的活性成分或佐剂。同样地,组合物可以仅含有本发明所述的单一多肽或本发明所述的两种或更多种多肽。在眼部给药的情况下,载体或赋形剂必须适合于这种给药途径。在这种情况下,所述组合物适宜以药学上可接受的眼用碱溶液或载体制备成溶液或水性悬浮液。在这种情况下,除了活性成分之外,本发明所述多肽可以含有其它佐剂,例如抗微生物剂、防腐剂、螯合剂、渗透压调节剂、ph调节剂、缓冲溶液、增稠剂等。当受试者在检测到功能异常(即,色差,对比敏感性和视网膜异常)时,在糖尿病性视网膜病的早期阶段接受有助于视网膜神经保护的化合物(例如本发明所述肽),则可以预防疾病。因此,如果能保护视网膜免受慢性高血糖的影响,则可以使其主要并发症最小化或甚至可以预防其发作,但是这需要实际改善糖尿病患者的生活质量。此外,所述肽防止brb的破坏。肽的局部眼部给药表现出真正的优势,可阻止更积极的治疗。糖尿病性视网膜病早期阶段治疗的真是优势是预防额外的并发症,即微动脉瘤、微出血、硬渗出物、黄斑水肿和新生血管。本发明组合物中,含有的肽浓度为1-12mg/ml。在眼部给药的特定情况下,组合物中至少含有5mg/ml的肽,在特定的实施方式中,其至少包含8mg/ml、9mg/ml或10mg/ml;在优选的实施方式,肽的浓度为10mg/ml±5%,即10mg/ml±0.5mg/ml。在腹膜内给药的特定情况下,组合物中含有1-5mg/ml的肽,在特定的实施方式中,其含有1-3mg/ml的肽;在优选的实施方式,肽的浓度为2mg/ml±10%或±5%,即2mg±0.2mg/ml或±0.1mg/ml。本发明的组合物适于每只眼睛每天施用10-200μg的肽。在具体的实施方式中,肽的日剂量为30-70μg/眼;在优选的实施方式中,肽的日剂量为40-60μg/眼,优选45-55μg/眼。在腹膜内或口服给药的情况下,所述组合物适于每天施用1-16mg肽/kg患者或受试者的重量,在具体的实施方式中,日剂量为2-10mg肽/kg患者或受试者的重量,优选2.5-3.5mg肽/kg患者或受试者的重量。本发明的另一方面涉及一种用于预防或治疗糖尿病慢性并发症和/或视网膜神经变性疾病的分离多核苷酸,所述多核苷酸编码:a)氨基酸序列seqidno2;或b)a)或b)的序列的变异体,其与序列seqidno2的同源性至少为85%;根据上述定义,所述糖尿病慢性并发症选自由糖尿病性视网膜病变、黄斑水肿、糖尿病性肾病、糖尿病性血管病、糖尿病性微血管病、糖尿病性大血管病、糖尿病性动脉粥样硬化、糖尿病足和外周动脉疾病构成的组;所述视网膜的神经变性疾病选自由糖尿病性视网膜病、青光眼和色素性视网膜炎构成的组。根据一个具体实施方式,用于预防或治疗糖尿病慢性并发症和/或视网膜神经变性疾病的分离多核苷酸编码:a)结合到赖氨酸基团的氨基酸序列seqidno2;或b)与赖氨酸基团结合的a)的序列的变异体,其与氨基酸序列seqidno2的同一性至少为85%;根据上述定义,所述糖尿病慢性并发症选自由糖尿病性视网膜病变、黄斑水肿、糖尿病性肾病、糖尿病性血管病、糖尿病性微血管病、糖尿病性大血管病、糖尿病性动脉粥样硬化、糖尿病足和外周动脉疾病构成的组;所述视网膜神经变性疾病选自由糖尿病性视网膜病、青光眼和色素性视网膜炎构成的组。上述多核苷酸适于局部用于或旨在局部用于预防或治疗前述疾病。优选地,上述多核苷酸适于用于或旨在用于预防或治疗糖尿病患者的眼部疾病和/或视网膜神经变性疾病,更优选用于预防或治疗糖尿病性视网膜病。本发明的一系列非限制性的、说明性的实施例如下。实施例材料和方法多肽:合成对应于小鼠socs1蛋白“激酶抑制区”序列的16个氨基酸的肽(seqidno1:dthfrtfrshsdyrri,aspthrhispheargthrpheargserhisserasptyrargargile),肽序列的n-末端(残基d,天冬氨酸)结合于细胞通透性区域(赖氨酸-棕榈酸酯),其中酪氨酸(y)被磷酸化。在实施例中,由seqidno1和棕榈酸酯-赖氨酸基团形成的衍生肽称为mis1或d-socsmis1。在一些情况下,后者与荧光标记物缀合使得能够在组织和细胞中进行随后的追踪。同样,还合成了用a(ala)取代f(phe)的非功能性突变肽(mut):seqidno3,dthartarshsdyrri,aspthrhisalaargthralaargserhisserasptyrargargile;非功能性突变肽同样结合到赖氨酸-棕榈酸酯细胞通透性区域,用作实验的对照。将上述合成的肽溶解(<1%dmso的盐水溶液)并过滤除菌。动物:使用两个实验模型,具体为2型糖尿病(db/db小鼠)实验模型和1型糖尿病实验模型(在apoe小鼠中注射链脲佐菌素)。将小鼠关在控制温度(20℃)和湿度(60%)条件的标准尺寸笼中,12小时的光照/黑暗循环,并且随意获得食物(标准饮食)和水。这些研究依据西班牙在实验动物使用、保护和护理方面的法律(皇家法令53/2013),遵循eec建议(86/609/eec)和arvo(associationforresearchinvisionandophthalmology)建议,并且之前已经由两个参与机构(iis-fundaciónjiménezdíaz/universidadautónomademadridandinstitutderecercahospitaluniversitarivalld'hebron)的伦理委员会批准。用socs1衍生肽的眼部局部治疗法来治疗由糖尿病引起的视网膜神经变性将mis1肽以滴眼剂的形式滴加于8周龄糖尿病小鼠(db/db)的眼中(每只眼滴5μl;10mg/ml;每天两次,持续15天;n=7只小鼠)。用非功能肽mut(n=7)、载体处理的糖尿病小鼠,及非糖尿病小鼠(db/+)作为对照。利用微量吸管将滴眼剂直接滴加在每只眼睛角膜的上表面。整个研究期间控制小鼠的体重和血糖(比色测定)。在第15天,小鼠解剖前约2小时滴加含mis1肽或载体的滴剂。利用颈脱位将小鼠安乐死后,立即将摘出的眼冷冻,并切下8mm的背腹部切片用于视网膜形态学分析和其他免疫组织化学分析。根据其它研究中所述的方法(bogdanov等人,plosone.2004;9:e97302),通过gfap(胶质纤维酸性蛋白质)免疫荧光评价神经胶质激活。将固定切片封闭(1%bsa和10%山羊血清的pbs溶液,室温下2小时),并与抗gfap抗体(稀释度1:500,4℃下16小时)一起温育,然后与第二抗体(alexa488山羊抗兔,稀释1:200)一起温育,然后将切片样品安装在共聚焦显微镜下分析并与hoesch对比。用相同的参数获取糖尿病和对照样品的图像,并且以0至5的等级分析gfap标记的形貌分布(anderson等人clinophthalmol2008;2(4):801-16)。得分1表示不存在神经胶质激活(gfap的阳性免疫荧光限于神经节细胞层),而得分5表示最大神经胶质激活(gfap的免疫荧光从神经节细胞层延伸到外核层的外边缘)。使用先前描述的方法(bogdanov等人,plosone.2004;9:e97302),通过tunel(terminaltransferasedutpnick-endlabeling;荧光试剂盒)免疫组织化学测定细胞凋亡,随后在荧光显微镜下量化。室温下,将视网膜切片在新鲜制备的20μg/ml蛋白酶k溶液中孵育5分钟使视网膜切片透化,然后使用绿色荧光[alexafluor594山羊-抗兔(invitrogen)(在pbs中稀释1:200)]鉴定凋亡细胞。采用荧光显微法在450-565nm(例如,488nm)的激发波长下评估视网膜切片的细胞凋亡,在515-565nm(绿色)的激发波长下检测视网膜切片的细胞凋亡。结果表示为使用imagej软件获得的tunel阳性细胞相对于hoestchst染色细胞的百分比。评估谷氨酸代谢以研究mis1肽产生神经保护的机制。通过超高效液相色谱(uplc)(acquity-uplc,waters)的masstrak氨基酸系统测定谷氨酸浓度。通过免疫荧光评价glast(glutamate/aspartatetransporter,谷氨酸酯/天冬氨酸转运体)。将石蜡切片在二甲苯中脱蜡并在一系列(浓度)递增的乙醇中再水化。然后将切片在酸性甲醇(-20℃)中固定1分钟,并用ph7.4的0.01m磷酸缓冲盐溶液(pbs)洗涤。之后,回收抗原,将切片浸没在抗原回收溶液(10mm柠檬酸钠,ph6.0)中,并在加压罐中150℃加热4分钟。室温下将切片在封闭溶液(0.5%bsa和10%山羊血清的pbs溶液)中孵育1小时。然后将切片与兔抗glast一抗(1:200,abcam)在4℃温育过夜;在pbs中洗涤一次后,室温下将切片与alexa488山羊抗兔二抗[1:200,molecularprobes(分子探针)]温育1小时。将切片在pbs中洗涤,用hoechst(1:500,sigma-aldrich)复染,并置于具有盖玻片的荧光封固介质(prolong,invitrogen)中。使用imagej软件通过激光共聚焦显微镜(olympusfluoviewtmfv1000共聚焦显微镜,hamburg,德国)定量测定glast免疫荧光。评价il-1β,tnf-α和il-6的表达。根据制造商的说明书,用dna酶消化的rneasyminikit(rneasy迷你试剂盒,qiagen,由izasa,巴塞罗那,西班牙分销)提取总rna。提取的rna(1μg)使用随机六核苷酸引物和appliedbiosystems试剂(appliedbiosystems,madrid,spain)进行反转录,反应体积为20μl。实时pcr在具有sybrgreensupermix的abiprism7000序列检测系统(perkin-elmerappliedbiosystems;madrid,spain)中进行。每个样品重复测定三次,且每次实验均设置阴性对照。人的s18作为内源基因表达的对照。采用δδct方法获得il-1β,tnf-α和il-6表达的相对定量(rq)。利用适应黑暗的麻醉小鼠(12小时过夜)进行视网膜电图(erg)记录。使用microniiifocalerg系统(phoenixresearchlabs,pleasanton,ca)测量焦视网膜电图(ferg)记录。使用安装在focalerg上的小鼠角膜晶状体中的电极,放置在头部眼睛之间的参考电极和放置在尾部中的接地电极来进行记录。此外,为了确保所有中心视网膜都被刺激,将光刺激投射在光盘上,并且使用最大可用光斑(直径为1.5mm)。在20ms白光刺激下记录两只眼的erg反应。白光刺激的强度为800、3200和12800cd·s·m-2,并且对每个强度进行平均6-10次连续闪光。放大erg信号,滤过的带在0.5和1000hz之间,并且用labscribe-2软件(bioseb,vitrolles,france)分析,来计算如iscev(internationalsocietyofclinicalelectrophysiologyofvision)所推荐的a波和b波振幅及a波和b波隐含期(marmor等人docophtalmol108:107a144)。从开始到安乐死前一天进行erg记录。用socs1衍生肽的眼部局部治疗法来治疗由糖尿病引起的brb的破坏8周龄糖尿病小鼠(db/db)接受滴眼剂形式的mis1肽(每只眼滴5μl;10mg/ml;每天两次,持续15天;n=7只小鼠)。用载剂(n=7)处理的糖尿病小鼠和非糖尿病小鼠(db/+)(n=7)作为对照。在整个研究期间控制小鼠的体重和血糖(比色测定),在第15天通过颈脱位法将小鼠安乐死。通过测定白蛋白的渗透性来评价brb的破坏。将石蜡切片在二甲苯中脱蜡并在一系列渐进的乙醇中再水化,然后将切片在酸性甲醇(-20℃)中固定1分钟,并用ph7.4的0.01m磷酸缓冲盐溶液(pbs)洗涤。室温下将切片在封闭溶液(2.5%干,脱脂乳)中温育30分钟,然后将切片与山羊抗人血清白蛋白的一抗(1:500,abcam)在4℃温育过夜;在pbs中洗涤一次后,室温下将切片与alexa594驴抗山羊二抗(1:200,molecularprobes)温育1小时;将切片在pbs中洗涤,用hoechst(1:500,sigma-aldrich)复染色,并置于具有盖玻片的荧光封固介质(prolong,invitrogen)中。通过激光共聚焦显微镜(olympusfluoviewtmfv1000共聚焦显微镜,hamburg,germany)分析白蛋白的免疫荧光。用socs1衍生肽的腹膜内治疗法来治疗由糖尿病引起的肾病和动脉粥样硬化通过链脲霉素注射(125mg/kg重量的10mm柠檬酸盐,ph4.5,连续两天)使8周龄的载脂蛋白e(apoe)缺陷的雄性小鼠患糖尿病。2周后,将血糖大于350mg/dl的小鼠随机分成两组(每组n=9只小鼠):处理组小鼠(mis1肽:65μg/天,200μl,腹膜内给药,每2天一次,连续8周)和对照组小鼠(载体)。在整个研究期间控制小鼠的体重和血糖(比色测定)。研究结束时,麻醉的小鼠用盐水灌注并处死,然后立即处理组织。在肾皮质(石蜡切片,5μm)中,通过pas和masson三色染色法研究肾小球和肾小管间质形态学,并且采用双盲和半定量方式以0-3的尺度(评分)评价病变。通过picro-sirius红染色测定肾纤维化和通过免疫组织化学测定渗透炎症细胞(f4/80+巨噬细胞和cd3+t淋巴细胞)。在主动脉中,根/弓区(从瓣膜8μm延伸至1000μm的系列冰冻切片)用油红o/苏木精染色,并且量化动脉粥样硬化病变的面积(metamorph程序)。通过使用picro-sirius红和α-肌动蛋白免疫荧光的胶原纤维染色来评估斑块稳定性。通过单核细胞/巨噬细胞(moma2)的免疫组织化学测定炎症组分。通过imagepro-plus程序定量阳性染色。通过常规商业试剂盒测定血清(糖化血红蛋白,胆固醇和肌酐)和尿液(白蛋白和肌酐)中的生化参数。体外研究使用含10%胎牛血清的培养基中培养raw264.7巨噬细胞和血管平滑肌细胞(vsmc)。将细胞同步化(无血清24小时),然后与不同浓度的肽(mis1或其对照,50-150μg/ml)预温育90分钟,并用细胞因子(ifnγ103u/ml;il-u/ml)刺激。通过磷酸化的stat1/stat3亚型的蛋白质印迹分析stat激活。通过elisa测定jak/stat途径依赖性趋化因子(ccl2)的表达。通过mtt比色法分析细胞活力,并通过趋化实验分析巨噬细胞迁移。统计分析结果表示为每组的全部小鼠和至少3种独立的细胞培养物的平均值±标准误差。使用graphpadprism(anova,tukey和studentt检验;p<0.05的显着性)程序进行统计分析。实施例1:本发明所述肽对视网膜神经变性的影响在2型糖尿病模型(db/db小鼠)中局部给予滴眼剂形式的mis1肽(50μg,5μl/眼,每天两次)15天。小鼠的体重和葡萄糖水平的变化如图1所示。用gfap标记物测量神经胶质激活(图2)。如所预期的,非糖尿病小鼠[(对照(db/+)]中gfap的表达主要限于视网膜的神经节细胞层(gcl)(图2)。用载体[d-sham]治疗的糖尿病小鼠比根据年龄匹配的非糖尿病小鼠显示出更显著的gfap表达。因此,100%的糖尿病小鼠显示gfap评分≥3。socs1衍生肽的两周给药导致反应性神经胶质增生显著减少,并且用socs1衍生肽[d-socsmis1]处理的小鼠的gfap评分均≤3(图2)。糖尿病小鼠[d-sham]视网膜层(onl,inl和gcl)中凋亡细胞的百分比与在相同年龄的非糖尿病小鼠[对照(db/+)]视网膜中观察到的相比显著更大(图3)。用socs1衍生肽[d-socsmis1]治疗的糖尿病小鼠显示出比用载体[d-sham]治疗的糖尿病小鼠显著更低的凋亡率。在用socs1衍生肽[d-socsmis1]治疗的糖尿病小鼠和非糖尿病小鼠之间,没有观察到凋亡细胞百分比的差异。socs1衍生肽的治疗降低了由糖尿病诱导的a波和b波振幅的减少,同时也降低了a波和b波潜伏期的增加(图4)。glast是由müller细胞表达的主要谷氨酸转运蛋白,它负责至少将50%的谷氨酸摄入哺乳动物的视网膜(图6a,上图)。用载体[d-sham]治疗的糖尿病小鼠的视网膜中glast含量降低,用socs1衍生肽[d-socsm1s1]治疗的糖尿病小鼠中glast含量没有降低(图6a,下图)。视网膜内谷氨酸水平降低,但没有达到统计学显着性(图6b)。因此,在mis1肽是视网膜神经保护剂的机制中,必须指出mis1肽阻止谷氨酸的增加和谷氨酸转运蛋白glast的减少。此外,mis1肽阻止由糖尿病诱导的il-1β的增加(图7)。必须指出,该细胞因子在糖尿病性视网膜病变的发病机理中起关键作用。总之,在糖尿病小鼠中以滴眼剂形式施用mis1肽阻止了视网膜神经变性,其通过与接受mut肽或载体的组相比,gfap胶质蛋白染色和凋亡的显著减少(约80%)来确定。socs1衍生肽的神经保护作用也通过视网膜(erg)的功能检查来证明。这些结果表明,本发明所述肽可用于治疗呈现视网膜神经变性的其它疾病,例如青光眼和色素性视网膜炎。像糖尿病诱导的视网膜神经变性,这些疾病的特征在于存在神经胶质炎症和由凋亡引起的进行性神经元死亡。实施例2:本发明所述肽对血液-视网膜屏障渗透性的影响在2型糖尿病模型(db/db小鼠)中以滴眼剂(50μg,5μl/眼,每天两次)的形式局部施用mis1肽15天。小鼠的体重和葡萄糖水平的变化如图1所示。通过测量白蛋白外渗来评价血管通透性。与对照小鼠[对照(db/+)]相比,用载体[d-sham]处理的db/db小鼠中观察到更大的白蛋白外渗。用socs1衍生肽mis1的处理阻止了db/db小鼠中白蛋白的外渗[d-socsm1s1](图5)。这些结果表明,本发明所述肽可用于治疗糖尿病性黄斑水肿,因为所述糖尿病性黄斑水肿的病理是由于血液-视网膜屏障的破坏使流体(水和溶液;最丰富的溶质是白蛋白)渗出到血管外中。本发明所述的socs1衍生肽能够阻止血液-视网膜屏障的破坏。实施例3:本发明所述肽对糖尿病小鼠肾病和动脉粥样硬化斑形成的影响在1型糖尿病模型(链脲佐菌素诱导的apoe小鼠)中用mis1肽(65μg/天,每2天一次)进行8周的系统治疗。表1显示了研究结束时糖尿病小鼠的临床和代谢参数。从表1可知,所有糖尿病小鼠显示出等效水平的高血糖(葡萄糖、糖化血红蛋白(hba1c)和胆固醇),表明所述肽的保护作用不是由于对糖尿病小鼠血糖的潜在控制。mis1肽的治疗也显著改善糖尿病小鼠的肾功能,观察到白蛋白水平降低28%。此外,采用mis1肽治疗组的小鼠中由慢性糖尿病引起的体重没有显著减轻。糖尿病小鼠肾切片的组织学分析显示,与接受载体治疗的糖尿病小鼠相比,采用mis1肽治疗组的糖尿病小鼠肾脏中stat1和stat3激活得到降低(图8),同时肾小球病变(hyper:细胞增生,mm:肾小球系膜,dil:毛细血管扩张)和肾小管间质病变(萎缩,退化和渗透)也得到改善(图9)。mis1肽显着减少肾小管间质纤维化(图10)和炎症淋巴细胞和巨噬细胞渗透(图11)。在另一系列实验中研究了采用mis1肽治疗的糖尿病小鼠的抗动脉粥样硬化性质。用油红o/苏木精染色的动脉粥样硬化斑块及其随后的量化,显示用mis1肽治疗的糖尿病小鼠中损伤的大小和延伸得到显著降低(与接受载体的对照组相比减少50%;图12a)。斑块组合物的分析显示,经治疗的小鼠中损伤部位的巨噬细胞数量减少,同时含有较高的胶原蛋白和血管细胞(图12b)。表明mis1肽的治疗减少了糖尿病小鼠体内的炎症并改善了糖尿病小鼠动脉粥样硬化的稳定性。表1:1型糖尿病小鼠的代谢和肾脏数据参数对照socs1体重(g)21.3±0.921.9±0.6血糖(mg/dl)528±12549±29糖化血红蛋白(ug/ml)470±74503±76总胆固醇(mg/dl)583±19611±59低密度脂蛋白胆固醇(mg/dl)557±19597±61高密度脂蛋白胆固醇(mg/dl)12±111±1甘油三脂(mg/dl)72±589±23天冬氨酸转氨酶(u/l)226±16176±20丙氨酸转氨酶(u/l)106±697±17肾脏体质量比(mg/g)20.5±1.116.4±1.3(p<0.05)血清肌酐(mg/dl)0.40±0.040.24±0.04(p<0.02)尿蛋白/肌酐比值(ug/umol)22.6±1.416.2±61.1(p<0.01)实施例4:体外研究小鼠巨噬细胞和小鼠血管平滑肌细胞的原代培养物(图13)用于体外研究。在两种细胞的原代培养物中,用促炎细胞因子ifnτ和il-6诱导刺激jak/stat途径的活化。巨噬细胞与浓度增加(50-150ug/ml)的抑制性肽mis1的预温育以剂量依赖性方式减少stat1和stat3的激活(通过蛋白质印迹测定两种蛋白质的磷酸化水平确定)。相反,相似剂量的mut肽(150ug/ml)不引起任何效果,因此证实了抑制性肽mis1的特异性。类似地,在免疫荧光图像中可以看到,mis1肽阻止了vsmc中stat1和stat3的激活。通过分析单核细胞趋化蛋白ccl2(其表达取决于jak/stat途径)的分泌,来测定mis1肽抑制的功能结果。与抑制性肽mis1预温育,但不与mut肽预温育,在vsmc和巨噬细胞中均显著降低(30-40%)细胞因子诱导的ccl2产生。最后,通过趋化实验证实抑制性肽mis1在巨噬细胞中的抗迁移效应。在任何研究的实验条件下,没有观察到vsmc和巨噬细胞的细胞活力的变化,这表明在所用浓度下肽的无毒性。实施例5:提供的数据可以外推到人类的理由用于本发明实施例的小鼠和细胞模型为医学和制药部门接受的允许将通过使用其获得的数据外推至人类疾病的模型。一方面,载脂蛋白e基因缺陷小鼠的特征在于胆固醇转运功能不足,导致在脂肪和外周组织中具有高脂质和胆固醇积聚的全身性高胆固醇血症。这种小鼠模型自发地发展(以加速的方式,如果它被喂养脂肪膳食)成动脉粥样硬化病变,具有类似于人类损伤的一些特征。因此,它是心血管研究中最广泛使用的模型之一。其次,apoe小鼠中1型糖尿病的诱导是结合高血糖和高脂血症(在这些病理学中的两个危险因素)的实验模型,并且具有由于糖尿病导致动脉粥样硬化和肾病的快速发展的特征。最后,db/db小鼠的特征在于瘦素受体缺陷,其为4-8周龄的2型糖尿病和肥胖小鼠的自发发展结果,随后的视网膜神经变性过程与糖尿病患者糖尿病性视网膜病变初始阶段非常相似。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1