烷烃脱氢成烯烃的制作方法
在工业过程中用于烷烃脱氢的现有技术是高温工艺,其通常在高于500℃下操作,并且在所有情况下都是低压工艺,其是鉴于以下事实:脱氢反应AH2=A+H2是吸热的,需要约120kJ/mole并涉及形成比反应物更多摩尔数的产物。因此,温度升高和低压均导致更高的转化率。A是不饱和化合物,并因此具有高反应性。烷烃的脱氢通常在没有稀释剂或在氢气作为稀释剂下进行。对于乙苯脱氢以生产苯乙烯,现有技术的工业工艺通过使用促进的氧化铁催化剂和水/蒸汽作为载气(稀释剂)以及碳抑制剂来进行。
脱氢中的寄生反应之一是碳形成,其导致催化剂的快速失活。因此,在某些应用中,催化剂的频繁再生可能是必要的。碳形成不仅是催化剂的问题。此外,必须仔细选择用于脱氢反应器和管道的材料(通常通过使用非常昂贵的合金),以避免导致称为金属粉尘的灾难性腐蚀形式的碳攻击。
金属硫化物用于烷烃脱氢的用途是本领域已知的。例如已知使用负载在二氧化硅上的硫化金属催化剂以用于异丁烷脱氢,其中金属是Zn、Cu或Mn、Mo、Fe、Co、Ni。然而,金属硫化物呈现低的稳定性,因为本应具有的高催化活性通常倾向于在脱氢期间快速下降。
美国专利3,787,517公开了链烷烃的氧化脱氢,其中链烷烃(烷烃)与作为氧化剂的硫化羰(COS)在负载的重金属催化剂(如负载在二氧化硅上的铁)的存在下反应。还公开了根据该方法的乙苯至苯乙烯的转化。
专利申请US 2004/0092784公开了通过使烷烃与含硫化合物在金属硫化物催化剂的存在下反应而使烷烃催化转化为烯烃的方法,但是该方法中生成了硫化氢,即形成了硫化氢作为反应产物。
美国专利3,787,517公开了使用混合的碱性金属氧化物/硫化物催化剂通过甲烷的氧化偶合来从甲苯生产苯乙烯,该方法避免了使用乙苯作为进料和使用过热蒸汽,而过热蒸汽的使用在工业生产苯乙烯中是正常的。
美国专利3,801,661公开了非芳香性烷烃通过金属硫化物催化剂脱氢成烯烃,其中存在H2S和蒸汽,尽管不是作为共反应物。
美国专利4,420,649公开了通过使用热解的羰基钌组分、铼组分和铂族组分使可脱氢的烃进行脱氢。因此,催化剂是昂贵的,另外,在脱氢中不使用硫化氢(H2S)。
专利申请US 2015/0018593公开了用于使C2-C4烷烃转化为烯烃的催化剂,其中催化剂是与选自AlPO4、膨润土、AlN和N4Si3的非布朗斯台德酸性粘合剂组合的金属碳化物、金属氮化物、金属硅化物、金属磷化物、金属硫化物或其混合物。在脱氢中不使用硫化氢(H2S)。
专利申请US 2014/0114107公开了用于在蒸汽存在下使乙苯脱氢的常规方法的变体,其中苯和甲苯被再循环。在脱氢中不使用硫化氢(H2S)。
金属硫化物催化剂对于精炼方法如氢化处理和所谓的酸变换水煤气变换方法是众所周知的。然而,这些方法通常在约300℃的区间下进行,而脱氢在约600℃下进行。因此,对这种催化剂的稳定性,特别是载体的热稳定性以及硫化物催化剂的稳定性,设定了更严格的要求。
因此,现有技术充满了这样的引文:其中烷烃或乙苯用金属硫化物催化剂在COS形式的含硫化合物或在脱氢过程中产生硫化氢的含硫化合物或在脱氢过程中产生SO2的含硫化合物的存在下进行脱氢,或者其中脱氢在硫化氢和蒸汽的存在下进行。
即使其在脱氢中不用作反应物,蒸汽在脱氢过程中的使用是不期望的,因为蒸汽需要通过能量密集的蒸发来产生并且必须在过程中被再次冷凝。蒸发热不能被完全回收。例如,在目前用于将乙苯转化为苯乙烯的方法中,向乙苯中加入大量蒸汽以抑制催化剂上的碳形成,稀释气体,从而降低乙苯分压以有利于平衡,并最终通过充当热载体来提供反应热。
因此,本发明的目的是提供一种用于使烷烃、烯烃或烷基苯脱氢成相应的不饱和化学产物的替代方法,其能够使催化剂保持高稳定性。
本发明的另一个目的是提供一种用于使烷烃、烷烃或烷基苯脱氢成相应的不饱和化学产物的替代方法,其更简单和更节能,并且同时能够使催化剂保持高稳定性。
本发明的另一个目的是提供一种用于使烷烃、烯烃或烷基苯脱氢的方法,其比现有技术的方法更便宜。
这些和其它目的通过本发明来解决。
我们惊奇地发现,当在少量H2S存在下且不使用蒸汽作为载气进行脱氢反应时,金属硫化物催化剂(硫钝化催化剂)可以以高效的方式使烷烃或烷基苯脱氢为各自的烯烃,例如丙烷至丙烯和乙苯至苯乙烯,并且具有高的稳定性和选择性。特别地,在脱氢过程中不需要COS、或SO2或元素硫形式的含硫化合物作为反应物。因此,结果是脱氢过程不形成H2S。
结果是,金属硫化物催化剂的稳定性随H2S/H2摩尔比而变化。由于我们处理的可能反应是MeS+H2=Me+H2S,其中Me通常是Fe、Co、Ni、Mo、W,所有这些都是烃流中的潜在的碳形成剂,而它们的硫化物和它们的混合物是氢化/脱氢催化剂。
现有的脱氢工艺和本发明解决的关键因素是向反应传递热。特别地,在常规的苯乙烯工艺中,这通过使用蒸汽作为载气来进行。该反应通常通过2-3个绝热催化床进行,在其间再加热至600-650℃。
根据本发明的基于硫化物的脱氢方法提供其它显著的优点。除了通过蒸汽重整避免不必要地形成CO2之外,由于在该方法中没有使用蒸汽,所以非常重要的优点是方法的灵活性和改善的能量效率,这是通过使用在使乙苯转化为苯乙烯的方法期间形成的芳香烃如苯或甲苯而不是蒸汽作为载气。它们具有非常高的热容,并且在热力学上非常稳定。更具体而言,苯-甲苯混合物的热容/热蒸发比率高于水-蒸汽,因此导致明显更低的对热应用的需求,该需求将必须通过在锅炉中燃烧额外的燃料来提供。虽然对冷应用的需求增加,但这种应用的成本要低得多。在该方法中产生的氢气可容易地通过使苯、甲苯、乙苯和苯乙烯冷凝出来而与其余物分离。将冷凝产物送至蒸馏,并使苯、甲苯和乙苯再循环。
因此,本发明最广义地涉及用于使烷烃、烯烃或烷基苯脱氢为相应的不饱和化学产物和氢气(H2)的方法,该方法包括使烷烃、烯烃或烷基苯与金属硫化物(MeS)催化剂接触,其中在一个或多个脱氢反应器中,在不使用蒸汽(H2O)作为烷烃、烯烃或烷基苯的载气并且在硫化氢(H2S)的存在下进行脱氢,并且不形成H2S作为反应产物。
因此,与现有技术相反的是,本发明避免在方法中使用产生H2S作为产物的化合物如COS。优选地,也不产生二氧化硫(SO2)。还与现有技术相反的是,不需要在使乙苯脱氢成苯乙烯的工艺中使用蒸汽作为载气。
金属硫化物(MeS)优选也通过预硫化步骤提供。
如本文所用,术语金属的硫化物(metallic sulfide)和金属硫化物(metal sulfide)可互换使用。
如本文所用,术语“载气”是指这样的气体,其显著有助于反应物的稀释以有利于脱氢反应的热力学平衡,抑制催化剂上的碳形成并且通过充当热载体来提供反应热。因此,载气是至少占待脱氢的进料(例如烷烃、烯烃或烷基苯或其混合物的进料)的20%(质量基准)的气体。几种载气可以组合以形成载气,因此载气可以占待脱氢的进料的至少90%(质量基准),优选至少100%,更优选大于200%,即载气的总量为待脱氢的进料的至少2倍。
术语“不使用蒸汽(H2O)作为载气”是指蒸汽占所使用的载气的10%(体积流量)以下,因为认识到任何工艺流可能携带或产生少量蒸汽。例如,蒸汽可以占载气的0.5-10%。更具体而言,蒸汽可以甚至占载气的5%以下,例如1-5%或0.5-5%。在任何情况下,对稀释反应物以有利于脱氢反应的热力学平衡、抑制催化剂上的碳形成以及通过充当热载体来提供反应热的主要贡献不是由蒸汽提供。在与上述和下述实施方案相关的具体实施方案中,载气中的蒸汽量为零或低于可检测的限度。
在与上述或下述实施方案相关的一个具体实施方案中,硫化氢(H2S)与烷烃、烯烃或烷基苯(在进料中)的摩尔比为0.01至0.2,优选0.01-0.1。因此,在该方法中使用少量的H2S,特别是在ppmv水平。在一个具体实施方案中,H2S与烷烃或烷基苯的摩尔比为0.02-0.05。例如,烷烃如丙烷的浓度可以为10%,而H2S以2000ppmv的量存在。
在与上述或下述实施方案之一相关的另一个实施方案中,硫化氢(H2S)与氢气(H2)的摩尔比为0.01至0.2,优选0.01至0.1,更优选其中脱氢过程的温度为600℃或更高。这是H2S与H2的初始摩尔比。已经发现,通过将H2S保持在这样的比例,从而导致该方法中H2S的量较少,现在可以保持高的催化剂稳定性,因为催化剂在脱氢过程中保持为金属硫化物。由此抑制了碳形成,其是催化剂失活和所伴随的不期望的效果例如金属粉尘的主要驱动力。
通过在连续操作模式下进行该方法来维持H2S在脱氢中的存在。以这种方式,催化剂作为MeS保持在硫化状态。例如,对于Me=Co,适用以下平衡反应:
9Co+8H2S=Co9S8+8H2
其中,可以从Kp=0.004907*exp(98105/T)估计平衡常数。
以烷烃、烯烃或烷基苯形式向该工艺的进料与除蒸汽之外的载气一起与连续的H2S流组合,该H2S流足够大以使金属(此处为钴)保持为硫化状态。本领域技术人员会理解,该H2S的量必须高于各自温度下的平衡常数Kp,该温度优选为脱氢反应器入口处的温度。因此,H2S与H2例如在脱氢反应器的入口处的初始摩尔比将在脱氢期间保持在约相同的低水平并且足够高以保持金属硫化物(MeS),尽管在脱氢期间产生氢。
在与上述或下述实施方案之一相关的具体实施方案中,硫化氢(H2S)与氢气(H2)的摩尔比为0.05-0.06,例如0.055。同样,这是H2S与H2的初始摩尔比。我们已惊奇地在该特定范围内发现高转化率和选择性,特别是由乙苯制备苯乙烯。优选地,温度为600℃或更高,例如高达650℃或700℃,并且硫化氢与乙苯的摩尔比为0.05-0.06,例如0.055。优选地,催化剂是负载在MgAl2O4载体上的CoMo氧化物,其中催化剂在使用前硫化,即预硫化。
在与上述或下述实施方案之一相关的另一个实施方案中,金属硫化物(MeS)的金属(Me)选自Fe、Co、Ni、Mn、Cu、Mo、W及其组合。优选地,金属是钴(Co)和钼(Mo)的组合。优选地,金属硫化物负载在氧化铝或尖晶石例如镁铝尖晶石(MgAl2O4)上。
在与上述或下述实施方案之一相关的另一个实施方案中,该方法在450-700℃,优选500-650℃的温度下进行。这些温度使得能够获得用于吸热脱氢反应的适当条件。
待脱氢的进料由烷烃、烯烃、乙苯及其组合组成。优选地,进料是烷烃、烯烃或乙苯中的一种。
在与上述或下述实施方案之一相关的另一个实施方案中,烷烃选自乙烷、丙烷、丁烷、戊烷及其组合。
在与上述或下述实施方案之一相关的另一个实施方案中,烯烃选自乙烯、丙烯、丁烯、戊烯及其组合。脱氢产生相应的不饱和化学产物,例如当进料中的烯烃是丙烯时其为丙二烯/丙炔。
在与上述或下述实施方案之一相关的另一个实施方案中,烷基苯是乙苯,且相应的不饱和化学产物是苯乙烯。
在与上述或下述实施方案之一相关的另一个实施方案中,未反应的烷烃、烯烃、烷基苯和副产物被再循环至一个或多个脱氢反应器。未反应的烷烃和副产物包括甲烷、乙烷、乙苯、苯、甲苯及其组合。
特别地,当该方法涉及乙苯脱氢成苯乙烯时,在副反应中产生苯和甲苯。因此,在与上述或下述实施方案之一相关的另一个实施方案中,苯、甲苯或两者的组合用作载气。由于苯和甲苯的非常高的热容以及它们的热稳定性,它们(而不是蒸汽)在工艺中用作载气在能量效率方面提供了巨大的好处,即在能量消耗方面出人意料地大幅降低对热应用的需求。
此外,产生苯的副反应也产生乙烯,并且产生甲苯的副反应也产生甲烷。乙烷也可以在该过程中作为副产物产生。因此,在与上述或下述实施方案之一有关的另一个具体实施方案中,使用甲烷、乙烷或两者的组合作为载气。这些也具有比蒸汽更高的热容与蒸发热的比率,并且在能量效率方面提供类似的益处。
特别是在通过乙苯脱氢生产苯乙烯期间,通过简单冷凝出苯、甲苯、乙苯和苯乙烯,所产生的氢气容易与其余产物(和副产物)分离。有价值的氢可以用作产物,而不是如目前常规脱氢方法中的稀释剂,而冷凝产物被送至蒸馏,并且苯、甲苯和乙苯被再循环到脱氢反应器中。
在与上述或下述实施方案之一相关的另一个具体实施方案中,脱氢在绝热反应器中进行,并且具有再加热步骤以及在反应器之间对该方法中产生的氢进行选择性氧化。该实施方案能够实现更高的能量效率。在第一反应器中产生的氢的选择性氧化优选在贵金属催化剂如基于Pt的催化剂上进行。
在与任何上述实施方案相关的另一个具体实施方案中,使用该方法中产生的含有H2和CH4的尾气作为载气,并在第一脱氢反应器的上游进行氢的选择性氧化。因此,可以在第一脱氢反应器上游和/或在第二脱氢反应器上游进行氢的选择性氧化。特别地,在由乙苯生产苯乙烯期间,苯-甲苯和在该方法中产生的含有H2和CH4的尾气作为载气的使用,以及在第一脱氢反应器上游和优选还在反应器之间(例如在第二脱氢反应器的上游)的氢气的选择性氧化的使用给出甚至更高的能量效率。不期望在第一脱氢反应器的上游使用这样的选择性氧化单元,因为这样没有氢气产生,相应地不需要这样的单元;但是通过这样做,获得了令人惊讶的更高的能量效率。本领域技术人员通常不鼓励在第一脱氢反应器的上游提供选择性氧化单元。使用蒸汽作为载气的典型方法会要求蒸汽与乙苯的摩尔比为5-6。这产生与用于氧化的空气结合的再循环尾气,这意味着再循环压缩机必须压缩到比本发明显著更高的压力。换句话说,看起来给出寄生的高能量消耗的方法在本发明中给出了能量效率方面的显著益处。
因此,以简单和简洁的方式提供了一种方法,其中不仅催化剂保持稳定,即没有由焦炭/碳形成而导致的失活,由此使得催化剂能够长时间地发挥作用而无需再生,但该方法特别是在由乙苯生产苯乙烯时在能量效率方面优于现有技术。
附图1-4用于说明本发明。图1对应于实施例3,并且显示了根据现有技术的用于将乙苯转化为苯乙烯的方法,其中使用蒸汽作为载气。图2对应于实施例4并且显示了根据本发明的方法,其中将乙苯转化为苯乙烯,其中载气是苯/甲苯的混合物,并且在该方法中还使用了H2S。图3对应于实施例5,并且显示了根据现有技术的用于将乙苯转化为苯乙烯的方法,其中蒸汽用作载气,并且其中对在第一反应器中产生的氢气进行选择性氧化。图4对应于实施例6并且显示了根据本发明的方法,其中将乙苯转化为苯乙烯,其中载气是苯/甲苯的混合物,在该方法中还使用了H2S,并且对在第一反应器中产生的氢气进行选择性氧化。图5对应于实施例7并且显示了根据本发明的方法,其中将乙苯转化为苯乙烯,其中载气是苯/甲苯和含有H2和CH4的废气再循环的混合物,在该方法中还使用了H2S,以及在第一和第二反应器之前进行选择性氧化。
实施例1-本发明
乙苯的脱氢
所用的催化剂由负载在MgAl2O4载体上的CoMo氧化物组成,催化剂在使用前硫化,即预硫化。装入反应器中的量是与也由MgAl2O4(尖晶石)载体组成的10.0g惰性材料混合的10.0g催化剂。
表1
反应器中的加载区为距离顶部凸缘635mm至244mm。在乙苯脱氢的整个测试期间,总流量约为48Nl/h。压力为3barg,这是使用本发明的装置可以进行该实验的最小压力。非选择性产物为苯、甲苯、甲烷、乙烷和乙烯。使用氮气作为载气。从硫化氢/氢气混合物添加硫化氢,由此加入氢气。除了限制相对接近于所计算的平衡值的转化率之外,多余的氢气可以引起增加的裂化。仅使用少量的通过摩尔(体积)比H2S/H2测量的H2S,并且不存在蒸汽。如表1所示,在催化剂上没有碳形成的情况下获得高的苯乙烯转化率(接近平衡)和高的苯乙烯选择性。在更高的温度下获得特别高的转化率和选择性,这是预期的,因为反应是吸热的,但在H2S/H2值特别是在0.05-0.06的范围内,具体而言在此处为0.054(表1的倒数第三行)时,获得了令人惊讶的高转化率和选择性。硫化氢(H2S)与氢气(H2)的摩尔比是初始摩尔比,而不是在进行反应之后的比率。
实施例2-本发明
丙烷的脱氢
丙烷的脱氢用与实施例1中乙苯的脱氢相同的催化剂进行。关于压力和作为稀释剂的氮气以及添加氢和硫化氢的混合物以保持催化剂硫化的条件是相同的。发现副产物是甲烷、乙烷和乙烯。没有发现硫醇。如表2所示,可以获得接近平衡的转化率和高选择性。未检测到催化剂上的碳形成。
表2
实施例3-现有技术
经典的苯乙烯工艺
苯乙烯在全世界范围内大量生产并且用于多种产品中。目前的主要工艺是基于使用铁基催化剂的乙苯的催化脱氢。
图1示出了典型的工艺布局。提供了本专利申请的附图,但没有提供详细的热交换网络,例如,待加热和冷却的流被分成方便的部分,其中进行加热和冷却至露点或泡点,以便为夹点分析提供输入。夹点分析提供了关于在热交换器网络中提供预定最小温度方法所需的最小热和冷应用的解答。在所有情况下都使用最低20℃的方法(实施例3-7)。
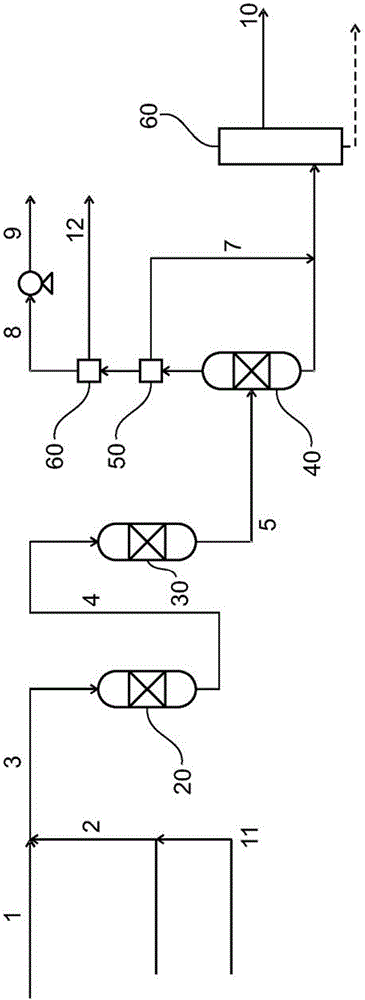
在图1中,将乙苯1与蒸汽2混合以形成混合进料流3,并在第一反应器20的入口处预热至645℃的入口温度。由于反应,温度在越过第一反应器后绝热下降至542℃。在进入第二反应器30之前,将来自反应器20的流出物流4再加热至645℃,其中流出物5在600℃下离开。在分离器40之前将其冷却至20℃,在其中倾析出水,并分离出粗的苯乙烯/苯/甲苯混合物6和未转化的乙苯。通过单元50中的沸石等来回收剩余痕量的芳香性化合物7,并将其加入到粗的苯乙烯流6中。将主要由氢气、甲烷、乙烯和二氧化碳组成的尾气8压缩至略高于环境压力并用作燃料9。
将粗的苯乙烯流送至蒸馏段60,在该处获得苯乙烯产物10。第一塔(未示出)将苯/甲苯与乙苯/苯乙烯分离,第二塔(未示出)将乙苯与苯乙烯分离。苯乙烯的最终纯化和苯/甲苯分离没有包括在该工艺比较中,因为假定它们在所有情况下都相同。
通过改变蒸汽含量,导致蒸汽与碳的比率为约1或蒸汽与油的重量比为约1.4(如通常在苯乙烯工业中所表示的),使乙苯至苯乙烯的转化率固定为70%。
通过2%的苯乙烯被转化为乙烯和苯,3%被转化为甲苯和甲烷来计算乙苯由于以下副反应的损失:其中乙苯分别转化为苯、乙烯和甲苯、甲烷。
所有的计算都是在每小时生产100MT苯乙烯(其离开第二蒸馏塔的乙苯/苯乙烯分离塔)的情况下得到的。
该工艺的夹点分析的结果示于表3中。热应用是307MW(相对热应用=100)。
实施例4-本发明
新的苯乙烯工艺
在该实施例中,通过使苯/甲苯混合物进行再循环,即使用苯/甲苯混合物作为载气,来实现蒸汽的其它两个功能,即稀释反应混合物和热载体。该物流可以通过从产物分离塔即第一蒸馏塔再循环而获得。
该方法由图2说明。
用再循环的苯/甲苯流2代替蒸汽,连同流11中的足够的H2S一起加入到新鲜和再循环的乙苯1中,以根据以下平衡在整个反应器中保持催化剂硫化物。
9Co+8H2S=Co9S8+8H2
其中,可以从Kp=0.004907*exp(98105/T)来估计平衡常数。
因此,进入第一反应器的进料包括乙苯、少量的H2S和作为载气的苯/甲苯。在苯/甲苯回收50之后,作为流12回收硫化氢。
表3中的夹点分析结果表明,对热应用的需求仅为278MW或比实施例4(现有技术)的工艺低约9%。
实施例5-现有技术
改进的经典苯乙烯工艺
在经典工艺(实施例3,图1)的改进方案中,通过在装置70中使用空气13在贵金属催化剂上对在第一反应器中产生的部分氢进行选择性氧化来提供两个反应器之间的再加热。图3示出了该构思。夹点分析(表3)的结果表明,该工艺配置将对热应用的需求降低到263MW,与实施例3的经典工艺相比,这是一个实质性的改进(14%的更好能量效率,根据相对热应用从100至86),尤其是因为用于在实施例3中的两个反应器之间再加热的介质是过热至非常高的温度(高达890℃)的蒸汽,然而,这也需要昂贵的用于构造的高合金钢。
实施例6-本发明
新型的具有选择性氢氧化的苯乙烯工艺
在该实施方案中,在脱氢反应器之间使用空气13进行的选择性氢氧化70与作为载气2的苯/甲苯的再循环以及根据本发明的在流11中的少量H2S的添加相组合。这在图4中示出。表3中的夹点分析结果显示出对能量效率的令人惊讶的更高影响,导致约23%的百分点改进(从278MW到214MW的热应用)。预期结果是如实施例5中所述的现有技术工艺一样的14%改进。
实施例7-本发明
在两个反应器之前具有选择性氢氧化的新苯乙烯方法
通过还将废气再循环引入返回至第一反应器,实现了甚至更好的能量效率。原理如图5所示。主要由H2、CH4和N2组成的废气再循环14也用作稀释剂和热载体,但也使用少量的苯/甲苯2。在第一反应器20的上游还添加有选择性氧化单元70。表3中的夹点分析的结果表明,对热应用的需求一直降低到186MW,比实施例5中改进的现有技术工艺(263MW的热应用)低29%。对压缩能量的需求从1MW增加到8.5MW,但是能量效率的益处仍然令人惊讶地高。
计算结果总结在表3中:
表3
根据本发明的使用硫钝化的脱氢催化剂的方法的益处是例如:
A)当避免使用蒸汽作为载气而是使用苯/甲苯混合物代替时,对于必须通过在锅炉中燃烧额外燃料来提供的热应用的需求显著降低。
B)在引入废气再循环和选择性氢氧化的情况下(实施例7),对热应用的需求甚至更显著地降低,并且比现有技术方法(实施例3和实施例5)分别低几乎40%(实施例3)或29%。
- 还没有人留言评论。精彩留言会获得点赞!