一种5‑羟基托特罗定凝胶制剂及其制备方法与流程
本发明是对托特罗定前体化合物5-羟基托特罗定药物剂型的改进,进一步讲是公开一种5-羟基托特罗定脂质体凝胶制剂,本发明还提供了所述制剂的制备方法,属于医学制药
技术领域:
。
背景技术:
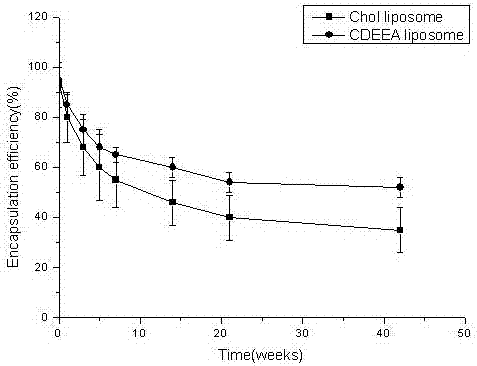
::临床研究表明,托特罗定经口服进入体内后在肝脏中经酶CYP2D6转化为不同代谢物,其中起主要药效作用的是5-羟基托特罗定。由于肝代谢酶的个体差异,口服托特罗定引起个体代谢产物含量不同,这不利于药品剂量控制,导致药效低,副作用增加,例如口干、便秘、消化不良、头痛、眩晕等。虽然可以通过普通注射方式给药,但对尿失禁患者长期治疗而言,每日一次或多次的注射方式将增加患者的痛苦和不适。本发明涉及的5-羟基托特罗定亦是毒蕈碱受体拮抗剂,对膀胱过度活动症具有治疗作用。当口服5-羟基托特罗定时生物利用度很低。因此为了克服临床应用中给药的缺陷,亟需通过改变药物的给药途径来提高药物的疗效、增加患者的顺应性。目前虽有研究针对本5-羟基托特罗定水凝胶制剂,但是并没有5-羟基托特罗定脂质体凝胶制剂的相关研究。与普通凝胶制剂相比,脂质体凝胶制剂因为脂质体特殊结构可以增加药物在皮肤局部部位的积累,有效延长药物释放时间,减少药物的全身吸收,从而降低药物的毒副作用。医药级有机硅弹性体,也称为硅凝胶,是由医药级乙烯基封端聚硅氧烷与含氢硅油经铂金催化体系加成聚合形成的新型高分子聚合物弹性体,具有优异的透过性能,能提高活性药物组分在皮肤上的渗透性,从而提高了药物的生物利用度,这种优点使其非常适合用于药物缓释、控释配方体系。在经皮给药系统中,骨架材料采用疏水性的有机硅弹性体。技术实现要素::本发明目的是提供一种胆固醇衍生物,一端为不带电荷的二乙胺基团,取代了胆固醇,与加入胆固醇的脂质体相比,具有胆固醇衍生物的脂质体长期稳定性更好,包封率更高。本发明还提供了一种5-羟基托特罗定凝胶制剂,将脂质体凝胶结合,外用涂抹经皮给药。本发明提供了胆固醇衍生物CDEEA的制备流程,用于该发明中脂质体的制备。本发明还提供了5-羟基托特罗定凝胶剂的制备方法。本发明涉及的一种胆固醇衍生物,命名为:4-cholesterocarbonyl-4'-(N,N-diethylamineethoxyethoxy)azobenzene,简称CDEEA,具有以下结构式:分子式为:C48H71N3O4;分子量为:754.10。本发明所述的胆固醇衍生物的制备方法,包括以下步骤:1)将对羟基偶氮苯甲酸、2,2'-二溴二乙醚、碱、催化剂按摩尔比为(5-8):(10-15):(0.5-2):(0.01-0.5)的混合比例在极性有机溶剂中于80-120℃回流反应12-48小时得到产物1;2)在室温条件下,将产物1、胆固醇、二环乙基碳二亚胺(DCC)和催化剂按摩尔比(1-2):(1-2):(1-1.5):(0.05-0.1)的混合比例反应12-36小时得产物2;3)将产物2和二乙胺按摩尔比1:(5-30)的混合比例于氯仿中回流反应24-72小时,氯仿洗涤,柱层析分离,得最终产物胆固醇衍生物;所述的碱选自:Na2CO3或K2CO3,;所述的催化剂选自:18-冠醚-6或KI;所述的催化剂选自:4-二甲氨基吡啶(DMAP)。本发明提供的一种5-羟基托特罗定脂质体凝胶制剂,其特征在于是由以下原料按重量%比制成的:5-羟基托特罗定1-3%、氢化大豆卵磷脂5-10%、胆固醇衍生物(CDEEA)5-10%、保湿剂5-15%、凝胶基质0.5-2%、成膜基质0.5-5%、有机硅弹性体0.5-5%、三乙醇胺0.5-3%、乙醇10-20%、余量为蒸馏水。所述的保湿剂为甘油;所述的凝胶基质为卡波姆934;所述的成膜基质为羟烷基纤维素类聚合物;所述有机硅弹性体为乙烯基封端聚硅氧烷与含氢硅油经铂金催化体系的聚合物。本发明所述的5-羟基托特罗定脂质体凝胶制剂的制备方法,包括以下步骤:1)氢化大豆卵磷脂和权利要求1所述的胆固醇衍生物溶于乙醇中,主药5-羟基托特罗定溶于1ml乙醇中,二者混合,将上述乙醇溶液迅速注入PBS中,漩涡混合均匀,进一步超声30s获得5-羟基托特罗定脂质体;2)取卡波姆934和羟丙甲纤维素缓慢撒入4ml蒸馏水中,过夜溶胀,加入甘油和有机硅弹性体,搅拌,先制成透明凝胶基质;3)将主药脂质体溶液加入凝胶基质中,搅拌均匀,加蒸馏水至指定质量,边搅拌边滴加三乙醇胺调节PH至7,即得乳白色凝胶。本发明的积极效果在于:提供一种新的胆固醇衍生物CDEEA,该衍生物的一端为不带电荷的二乙胺基团,取代了胆固醇,与加入胆固醇的脂质体相比,具有胆固醇衍生物的脂质体长期稳定性更好,包封率更高;与胆固醇脂质体相比,在长期贮存过程中,CDEEA脂质体更稳定,粒径变化小,包封率更高,对于脂质体的长期稳定性对无论是实验研究还是今后的临床应用都具有重大意义。本发明制备凝胶制剂可以经皮吸收,药物稳定性好,生物利用度高,可以避免口服给药产生的毒副作用以及注射给药带给患者的痛苦和不适。5-羟基托特罗定脂质体采用乙醇注入方法制得,现用现制,工艺简单,质量控制方便,成本低,环境污染小。将5-羟基托特罗定脂质体均匀分散在凝胶中,可以提高脂质体的稳定性。与普通凝胶制剂相比,脂质体凝胶制剂有效延长了药物释放时间,减少了药物的全身吸收,降低了药物的毒副作用,可以提高患者依从性,具有很好的临床应用前景。以卡波姆934为凝胶基质,对皮肤无刺激,具有良好的生物相容性,无粘滞感,易于被患者所接受。通过添加羟丙甲基纤维素使制备水凝胶制剂具备成膜性,干燥后能形成柔韧性膜,外用涂抹可避免了普通凝胶可被衣物带走的弊端,同时透气性好药物释放更平缓且使用更方便。凝胶基质中含有特殊辅料有机硅弹性体,它能显著改善凝胶体系的分散性、柔软度、湿润度、光泽度等性质,制备的凝胶光滑、晶莹、细腻,用后皮肤无异物感,药物持久缓慢释放,经皮吸收效果好,使用方便,提高患者顺应性。附图说明:图1是长期稳定性试验中,脂质体的粒径变化曲线;图2是长期稳定性试验中,脂质体的包封率变化曲线;图3是实施例4制备凝胶体外透皮累积释放率-时间曲线;图4是实施例5制备凝胶体外透皮累积释放率-时间曲线;图5是实施例6制备凝胶体外透皮累积释放率-时间曲线;图6是实施例7制备凝胶体外透皮累积释放率-时间曲线;图7是实施例8制备凝胶体外透皮累积释放率-时间曲线;图8是对照组制备凝胶体外透皮累积释放率-时间曲线;图9是对Wistar大鼠静脉注射托特罗定溶液及涂抹实施例4制备凝胶后的血药浓度-时间曲线。具体实施方式本发明的具体实施方法,由下列实施实例举例说明,但本发明的保护范围不局限于此。实施例1将对羟基偶氮苯甲酸、2,2'-二溴二乙醚、Na2CO3、18-冠醚-6在极性有机溶剂中以摩尔比5:10:2:0.3于80-120℃回流反应12小时,得产物1。在室温条件下,产物1、胆固醇、二环乙基碳二亚胺(DCC)和4-二甲氨基吡啶(DMAP)以摩尔比为1:1:1:0.1反应24小时。将化合物5和二乙胺以摩尔比1:10于氯仿中回流反应48小时,氯仿洗涤,柱层析分离,得最终产物胆固醇衍生物(CDEEA)。实施例2将对羟基偶氮苯甲酸、2,2'-二溴二乙醚、Na2CO3、18-冠醚-6在极性有机溶剂中以摩尔比8:15:1:0.5于80-120℃回流反应48小时,得产物1。在室温条件下,产物1、胆固醇、二环乙基碳二亚胺(DCC)和4-二甲氨基吡啶(DMAP)以摩尔比为2:2:1:0.05反应36小时。将化合物5和二乙胺以摩尔比1:20于氯仿中回流反应48小时,氯仿洗涤,柱层析分离,得最终产物胆固醇衍生物(CDEEA)。实施例3将对羟基偶氮苯甲酸、2,2'-二溴二乙醚、Na2CO3、18-冠醚-6在极性有机溶剂中以摩尔比5:15:0.5:0.01于80-120℃回流反应36小时,得产物1。在室温条件下,产物1、胆固醇、二环乙基碳二亚胺(DCC)和4-二甲氨基吡啶(DMAP)以摩尔比为1.5:1.5:1.5:0.1反应24小时。将化合物5和二乙胺以摩尔比1:30于氯仿中回流反应72小时,氯仿洗涤,柱层析分离,得最终产物胆固醇衍生物(CDEEA)。实施例45-羟基托特罗定凝胶制剂(按100g计):按以下处方制备凝胶(按100g计):5-羟甲基托特罗定3g,氢化大豆卵磷脂10g,实施例1制备的胆固醇衍生物10g,甘油5g,卡波姆9342g,羟丙甲纤维素2g,有机硅弹性体2g,三乙醇胺1g,乙醇15ml,余量为蒸馏水。将氢化大豆卵磷脂、胆固醇衍生物溶于乙醇中,另取5-羟基托特罗定溶于乙醇中,二者混合,迅速注入PBS中,漩涡混合均匀进一步超声得到5-羟基托特罗定脂质体;另取卡波姆934和羟丙甲纤维素撒入蒸馏水中,过夜溶胀,加入甘油和有机硅弹性体,搅拌制成透明凝胶基质;将主药脂质体溶液加入凝胶基质中,搅拌均匀,加蒸馏水至指定质量,滴加三乙醇胺调节PH至7,即得。实施例55-羟基托特罗定凝胶制剂(按100g计):按以下处方制备凝胶(按100g计):5-羟甲基托特罗定1g,氢化大豆卵磷脂10g,实施例2制备的胆固醇衍生物5g,甘油7g,卡波姆9340.5g,羟丙甲纤维素2g,有机硅弹性体1g,三乙醇胺1.2g,乙醇10ml,余量为蒸馏水。将氢化大豆卵磷脂、胆固醇衍生物溶于乙醇中,另取5-羟基托特罗定溶于乙醇中,二者混合,迅速注入PBS中,漩涡混合均匀进一步超声得到5-羟基托特罗定脂质体;另取卡波姆934和羟丙甲纤维素撒入蒸馏水中,过夜溶胀,加入甘油和有机硅弹性体,搅拌制成透明凝胶基质;将主药脂质体溶液加入凝胶基质中,搅拌均匀,加蒸馏水至指定质量,滴加三乙醇胺调节PH至7,即得。实施例65-羟基托特罗定凝胶制剂(按100g计):按以下处方制备凝胶(按100g计):5-羟甲基托特罗定2g,氢化大豆卵磷脂8g,实施例3制备的胆固醇衍生物10g,甘油8g,卡波姆9341g,羟丙甲纤维素4g,有机硅弹性体3g,三乙醇胺0.8g,乙醇15ml,余量为蒸馏水。将氢化大豆卵磷脂、胆固醇衍生物溶于乙醇中,另取5-羟基托特罗定溶于乙醇中,二者混合,迅速注入PBS中,漩涡混合均匀进一步超声得到5-羟基托特罗定脂质体;另取卡波姆934和羟丙甲纤维素撒入蒸馏水中,过夜溶胀,加入甘油和有机硅弹性体,搅拌制成透明凝胶基质;将主药脂质体溶液加入凝胶基质中,搅拌均匀,加蒸馏水至指定质量,滴加三乙醇胺调节PH至7,即得。实施例75-羟基托特罗定凝胶制剂(按100g计):按以下处方制备凝胶(按100g计):5-羟甲基托特罗定2.5g,氢化大豆卵磷脂8g,实施例1制备的胆固醇衍生物8g,甘油13g,卡波姆9342g,羟丙甲纤维素4g,有机硅弹性体4g,三乙醇胺1g,乙醇15ml,余量为蒸馏水。将氢化大豆卵磷脂、胆固醇衍生物溶于乙醇中,另取5-羟基托特罗定溶于乙醇中,二者混合,迅速注入PBS中,漩涡混合均匀进一步超声得到5-羟基托特罗定脂质体;另取卡波姆934和羟丙甲纤维素撒入蒸馏水中,过夜溶胀,加入甘油和有机硅弹性体,搅拌制成透明凝胶基质;将主药脂质体溶液加入凝胶基质中,搅拌均匀,加蒸馏水至指定质量,滴加三乙醇胺调节PH至7,即得。实施例85-羟基托特罗定凝胶制剂(按100g计):按以下处方制备凝胶(按100g计):5-羟甲基托特罗定2g,氢化大豆卵磷脂10g,实施例2制备的胆固醇衍生物10g,甘油15g,卡波姆9340.5g,羟丙甲纤维素0.5g,有机硅弹性体2g,三乙醇胺1.5g,乙醇10ml,余量为蒸馏水。将氢化大豆卵磷脂、胆固醇衍生物溶于乙醇中,另取5-羟基托特罗定溶于乙醇中,二者混合,迅速注入PBS中,漩涡混合均匀进一步超声得到5-羟基托特罗定脂质体;另取卡波姆934和羟丙甲纤维素撒入蒸馏水中,过夜溶胀,加入甘油和有机硅弹性体,搅拌制成透明凝胶基质;将主药脂质体溶液加入凝胶基质中,搅拌均匀,加蒸馏水至指定质量,滴加三乙醇胺调节PH至7,即得。本发明效果实验例1脂质体长期稳定性试验将制备好的含有胆固醇衍生物CDEEA的5-羟基托特罗定脂质体和传统胆固醇脂质体于4℃冰箱中贮存42周。与1w,3w,5w,7w。14w,21w,42w,通过检测粒径和包封率来观察胆固醇衍生物对脂质体长期稳定性的影响。每次取出100μl脂质体,加入900μlPBS进行稀释后加入ZetasizerNanoS90动态光散射仪样品池进行粒径测量。测脂质体包封率方法如下:取100μl脂质体,加入4.9mlPBS缓冲液后,加入TritonX-100,通过HPLC进行浓度测定,从而计算出不同时间点的包封率情况,并绘制曲线。从结果看出,在长期稳定性试验中,加入胆固醇衍生物的脂质体相比于传统脂质体,粒径变化和包封率变化都显著减小,稳定性更好。脂质体粒径变化见说明书附图1,脂质体包封率变化见说明书附图2。效果实验例2凝胶外观、成膜性、粘度实验考察实施例1-5制备凝胶的外观、成膜性、粘度、涂抹后感觉,结果如下表:结果表明,加入羟丙基纤维素卡波姆和有机硅弹性体值得的脂质体凝胶具有成膜性,减少涂抹后的异物感,粘度也适中,凝胶光滑细腻,涂抹后皮肤感觉舒适。效果实验例3凝胶体外透皮实验用Na2S脱去健康小鼠腹部鼠毛,清洗干净,断颈处死,立刻剪下其腹部皮肤,用刀片除去皮下脂肪组织和黏液组织,注意不要破坏角质层,用生理盐水洗净,置冰箱中保存备用。按照实施例4~8制备凝胶,并制备5-羟基托特罗定普通成膜凝胶作为对照组。从冰箱中取出鼠皮,恢复至室温,用生理盐水反复冲洗鼠皮,再用滤纸轻轻擦干。使用Franz扩散池,将皮肤固定在供给室和接收室之间,使角质层面向供给室,两室有效接触面积为0.636cm2。精密称取10mg凝胶剂,置供给室中涂匀,并与皮肤密切接触。于接收室中加入磷酸盐缓冲液(PBS)5ml(pH7.4,10mmol/L),水浴温度为(32±0.5)℃,恒速200r/min,分别于1h、2h、4h、6h、8h、10h、12h、18h和24h定时取样5ml(立即补回5ml新鲜介质),0.45μm微孔滤膜过滤,HPLC测定接收液中药物浓度。每批凝胶做6组平行实验。HPLC条件为:XDBC18柱5μm,4.5mm×250mm,柱温40℃,检测波长283nm,流动相为10mmol/L醋酸缓冲液(pH3.0)-甲醇(35:65),流速1ml/min。5批凝胶透皮释放结果如下,其中Jss为稳态药物透皮速率,Q为24小时药物透皮量:照下式计算透皮累积释放量Q(μg·cm-2):nQn=V·∑Ci/Si=1式中,Qn为第n次取样时的透皮累积释放量(μg·cm-2),V为接受液体积(ml),Ci为第i次取样时接收液中测得药物浓度(μg·cm-2·ml-1),S为有效渗透面积(cm2)。再按照下式计算透皮稳态渗透速率Jss(μg·cm-2·h-1):Jss=dQ/dt式中,t为透皮时间(h)。Jss(μg·cm-2·h-1)Q24h(μg·cm-2)实施例4240.24420.6±490.3实施例5185.43980.2±557.1实施例6234.433276.3±497.0实施例7296.133948.0±555.5实施例8277.923486.7±558.9对照组175.042690.3±268.5结果显示,五批凝胶透皮速率各不同,但都明显优于对照组其中,实施例7透皮速率最大。实施例4-8和对照组的制备凝胶的透皮累积释放量-时间曲线见说明书附图3~8。效果实验例4凝胶药代实验取健康成熟雄性家兔,重量为1.5~2.5kg,分为5-托特罗定溶液组、对照凝胶组和脂质体凝胶组,每组3只家兔。实验前一天,肌肉注射30mg/kg戊巴比妥钠麻醉凝胶组家兔,然后用剪刀将背部毛除去,皮肤不能有破损,除毛部位用记号笔标记(大小为4×4cm2),禁食12h。实验时,将实施例4和对照组制备的凝胶剂涂抹在除毛部位,注意涂抹均匀,给药3min后让动物自由活动。同时对另一组家兔i.v.5-托特罗定溶液。实验过程中,家兔自由进水。给药后,分别在0,15,30min,1,2,4,6,8,10,12,18,24,36,48h耳缘静脉取血,收集1ml血液,置含20μl肝素的EP管中,13,000rpm离心10min分离血浆,于-20℃冰箱保存待测。取100μl血浆,分别加入100μl内标溶液,100μl乙腈-水(80:20,v/v),溶液加入3ml提取试剂(乙醚:二氯甲烷=3:2,v/v),涡流混合30s,振荡10min,离心5min(3500rpm),取上清液于30℃下氮气吹干,残余物加150μl流动相溶解,取20μl进行LC/MS/MS分析。i.v.5-托特罗定溶液及涂抹对照组和实施例4制备凝胶后,家兔药代实验结果如下:结果表明,实施例4所制凝胶可平稳缓慢释放,生物利用度高于30%,具有临床使用意义。药后血药浓度-时间曲线见说明书附图9。当前第1页1 2 3
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1