自动化微生物分子检测设备的制作方法
本发明属于微生物的测定或检验方法技术领域,特别涉及一种自动化微生物分子检测设备。
背景技术:
微生物分子检测技术是基于微生物特异靶标分子进行的一种微生物检测技术。微生物,特别是有害微生物,在进行正常新陈代谢的同时,会合成一些独特的、能够表征自身特征的化合物,如黄曲霉毒素等。这些化合物的合成途径具有特异性,其中一些关键控制基因往往是独一无二的,其基因拷贝数能够直接反映微生物个体的数量,因此,利用微生物中特异的靶标基因进行微生物定量检测已成为国内外公认的有效方法之一。
荧光定量PCR法通过荧光染料或荧光标记的特异性的探针,对PCR产物进行标记跟踪,实时在线监控反应过程,结合相应的软件可以对产物进行分析,计算待测样品模板的初始浓度。利用其对各种食品中各类微生物的检测已获得我国各级政府和各类食品检测机构的认可,如2007年国家质量监督检验检疫总局发布的食品中致病菌检测方法-实时PCR法(SN/T 1870-2007)等。
虽然国内外研究人员在微生物靶标基因研究已获得重大成果,已完成了沙门氏菌、志贺氏菌、金黄色葡萄球菌、单核细胞增生李斯特氏菌、空肠弯曲菌、肠出血性大肠埃希氏菌、副溶血性弧菌、霍乱弧菌、创伤弧菌、溶澡弧菌等致病菌的靶标微生物筛选和检测方法的建立。但迄今为止,基于荧光定量PCR法的微生物分子检测并未在全国各检验检测机构获得广泛应用,主要原因如下:
1.检测流程复杂:对特定样本进行微生物分子检测,其流程主要包括样本处理、核酸提纯和靶基因定量检测。以固态食品为例,样本处理主要目标是将微生物富集和微生物细胞裂解;核酸提纯包括核酸结合、核酸盐洗、核酸洗脱等步骤;靶基因定量手工操作主要是荧光定量PCR体系配制,由于体系成分复杂,体系配制工作量较大。以上操作包括各种试剂的移加、加热、振摇、离心等,步骤多达50步以上,每个研究人员每天工作8小时,最多只能完成12个样品操作。
2.操作难度大:由于检测流程复杂,每一步骤的遗漏均会使得检测结果无效,且由于分子检测移液微量,精准度要求高,这加大了一线检测人员的操作难度。此外,手工操作往往存在人为误差,难以实现结果一致性,往往造成同样标准方法,不同检测人员做出的结果不同,使得操作人员在上岗前需进行大量的培训,大大增加检测结构的人力成本。
3.分析成本高:现今分子检测试剂大多来源于美国等国外试剂公司,每个样品分析试剂成本均在100元以上。国内一些分子检测试剂产家,其产品价格虽然低一些,但由于在实际使用中的复杂性,且现今还没有统一的质量标准,很难被市场所接受。
自动化微生物分子检测设备也是当前的研究热点。如申请号为201380018553.3的发明创造公开了一种用于自动分析生物试样的设备以及方法,步骤为:将生物试样溶解在水解酶和细胞裂解液中,并将核酸溶解在溶剂中,之后将核酸附着至磁性颗粒并洗涤附着有核酸的磁性颗粒;并且之后,使用有机溶剂来最终洗涤附着有核酸的磁性颗粒,并使用真空泵干燥磁性颗粒;并且之后,使附着至磁性颗粒的靶核酸溶解在溶剂中;并且之后,将所述溶解的靶核酸施加至包含核酸基扩增试剂的容器中并将其混合;并且之后,调节用于扩增的温度并且同时在反应器处照射激发光,并通过测量荧光来实时地探测扩增,在扩增之后通过使用红外灯使经扩增的产物失活,并且之后通过电泳获得图像。该设备实现了对某些特定试样的自动化检测,但其只能检测生物试样,且对生物试样的预处理仍需手工完成。
申请号为201410106397.2的发明创造公开了一种全自动两通道定量检测仪,其包括控制单元、核心单元和检测单元,采用全自动机械传动提高了工作效率及准确性。但其检测的目标试样仅仅为血液标本,也没有涉及对试样的预处理步骤,并且其需要孵育室进行孵育。
技术实现要素:
本发明的目的是克服现有技术的不足,提供一种自动化微生物分子检测设备,实现试样预处理、核酸提纯、检测整个过程的全程自动化,检测过程无人为误差,基本防止假阴性和假阳性。
本发明解决所述技术问题的方案是:一种自动化微生物分子检测设备,包括控制单元、移运单元、试样预处理单元、核酸提纯单元、检测单元;
控制单元用于人机互交、系统参数与数据的存储;
移运单元为机械臂,用于试样和试剂在各单元之间的移运或用于试样和试剂在各单元内的移运;
试样预处理单元包括预处理试剂存放区、分离模块;
核酸提纯单元将经过预处理后的试样中的核酸提纯;
检测单元对提纯后的试样进行检测,并得出结果。
作为改进,所述检测设备包括试样放置单元,试样放置单元包括多孔板和用于搁置多孔板的多孔板载架。
作为改进,所述分离模块为离心机。
作为改进,所述分离模块为抽滤装置。
作为进一步改进,所述抽滤装置包括围护结构、与围护结构分体式设置的抽滤多孔板、与围护结构分体式设置的多孔板,多孔板搁置在围护结构的内部,抽滤多孔板位于围护结构的顶部实现对围护结构内部空间的密闭,围护结构的内部空间与真空泵连通,多孔板用于承接从抽滤多孔板抽滤出来的液体得到核酸初提液。
本申请中所谓的抽滤多孔板与普通的多孔板之间的区别在于:抽滤多孔板的反应孔内开设有通孔,在通孔处覆盖有滤膜,反应孔内的试样在负压的作用下能透过滤膜流到反应孔之外。
作为再进一步改进,所述抽滤装置包括用于搁置所述多孔板的基座,基座与真空泵连通实现围护结构的内部空间与真空泵的连通,所述围护结构与基座分体式设置。
作为进一步改进,所述核酸提纯单元包括提纯试剂存放区、磁性粒子吸附洗脱模块。
作为改进,该检测设备还包括富集单元,富集单元位于核酸提纯单元之后,富集单元位于检测单元之前。富集单元用于对痕量靶标微生物进行富集。
作为进一步改进,所述富集单元包括多孔板、磁场产生装置,磁场产生装置用于在多孔板周围产生磁场,由移运单元将核酸粗提液或提纯后得到的高纯核酸试样加入多孔板的反应孔内或将被磁性粒子吸附后的核酸粗提液或高纯核酸试样从多孔板的反应孔内移除。
待测试样经细胞裂解液裂解后得到核酸裂解液,核酸裂解液经过过滤后得到核酸粗提液,核酸粗提液经过磁性粒子的吸附提纯后得到高纯核酸试样。本申请富集的对象既可以是核酸粗提液,也可以是纯化后得到的高纯核酸试样。
富集单元的结构与核酸提纯单元的磁性粒子吸附洗脱模块类似。它们之间的主要区别是:磁性粒子吸附洗脱模块只进行一次“加入试样--磁性粒子吸附—移除液体”的操作,而富集单元需进行多次“加入试样--磁性粒子吸附—移除液体”的操作。
作为进一步改进,所述检测单元包括PCR体系配制区、基因定量检测区。
本检测设备将现有技术中由手工完成的试样预处理单元整合进整套装置,不仅适合检测液态的试样,还适合土壤、食品、药品等固体试样的自动化检测。待分析的试样、试剂等放置在设备固定位置后,通过电脑一键式控制,由移运单元替代人手完成试样预处理、核酸提纯和靶基因荧光检测操作步骤,并按需自动调取设备中已有数据库中靶基因检测程序和定量标准曲线;最后自动计算获得待分析样品中靶标微生物的克隆数。而且检测前无需增菌处理,检测过程无人为误差,基本防止假阴性和假阳性。
需要着重说明的是:现有技术中,对试样的预处理均采用手工方式,预处理的固液分离均采用离心机。本方案创造性地采用在试样预处理单元中采用了抽滤装置,采用围护结构、抽滤多孔板、多孔板之间的配合,抽滤多孔板的孔底设置有滤膜,在负压作用下,试样溶液从抽滤多孔板内被吸至多孔板,实现多个试样的一次性高效分离。而且由于抽滤多孔板中滤膜的参与,使试样溶液的分离效果优于离心机的分离效果。
对于痕量试样,如果一个多孔板反应孔内的核酸粗提液所含的靶标核酸达不到被检出的含量,现有技术中的自动化检测设备尚未有解决的办法。这成为自动化微生物分子检测设备发展的瓶颈。本申请的富集模块可以对1个或多个试样的核酸进行富集,通过在装有磁性粒子的多孔板中多次进行“加入试样--磁性粒子吸附—移除液体”的操作,使靶标核酸达到可被检出的含量,从而实现痕量靶标微生物的原态检测。
附图说明
图1为本发明的布局示意图;
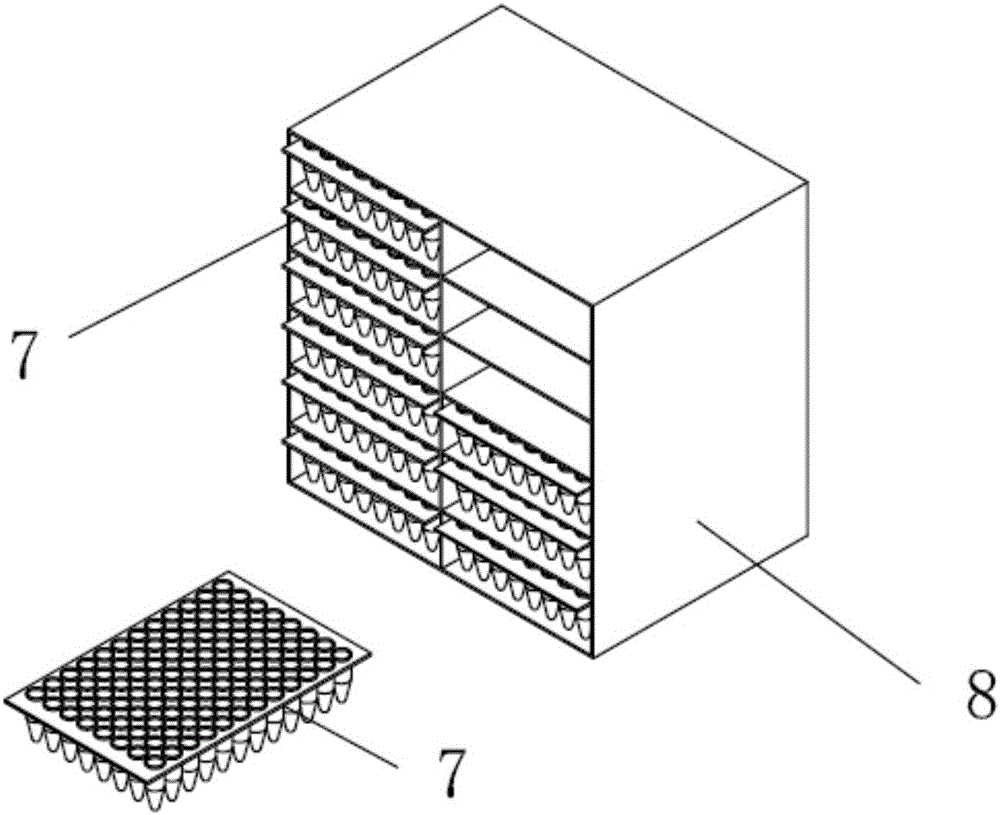
图2为本发明试样放置单元的结构示意图;
图3为本发明试样预处理单元的结构示意图;
图4为本发明分离模块的爆炸图;
图5为本发明抽滤多孔板的反应孔的结构示意图;
图6为本发明核酸提纯单元的结构示意图;
图7为本发明富集单元的结构示意图。
图中:1、控制单元;2、移运单元;21、移液机械臂;22、多孔板抓手机械臂;3、试样预处理单元;31、预处理试剂存放区;32、分离模块;321、围护结构;322、抽滤多孔板;323、基座;324、气管接头;325、通孔;33、振荡模块;4、核酸提纯单元;41、提纯试剂存放区;42、磁性粒子吸附洗脱模块;5、检测单元;51、PCR体系配制区;52、基因定量检测区;6、试样放置单元;7、多孔板;8、多孔板载架;9、富集单元;91、磁场产生装置。
实施例1
具体实施方式
实施例1
如图1所示,本发明涉及的一种自动化微生物分子检测设备,包括控制单元1、移运单元2、试样预处理单元3、核酸提纯单元4、检测单元5、试样放置单元6、富集单元9。控制单元1用于人机互交、系统参数与数据的存储。移运单元2为机械臂,移运单元2包括移液机械臂21和多孔板抓手机械臂22,其用于试样和试剂在各单元之间的移运或用于试样和试剂在各单元内的移运。移液机械臂21的头部有多通道移液枪,能够对试样和试剂的进行吸取和加液操作。
如图2所示,试样放置单元6包括多孔板7和用于搁置多孔板的多孔板载架8。检测前,将待测试样称量后分别置入多孔板7的反应孔内,装填完毕的多孔板7预先搁置在多孔板载架8上,测试开始后,多孔板抓手机械臂22能将多孔板载架8上的多孔板7移运至指定位置。
如图3所示,试样预处理单元3包括预处理试剂存放区31、分离模块32、带有温控装置的振荡模块33。预处理试剂存放区31放置细胞裂解液等预处理需要使用的试剂,可以将装有待测试样的多孔板7置于振荡模块33上,振荡模块33参照现有技术中的多孔板振荡器设置。移液机械臂21带着多通道移液枪将预处理需要使用的试剂注至多孔板7的反应孔内,每加入一种试剂后,根据需要进行加热和/或振荡处理;待裂解液完全透明,无肉眼可见的微小颗粒后,将核酸裂解液移取至分离模块32,进行真空抽滤,收集滤液得到核酸粗提液。
分离模块32的结构如图4所示,图中所示的为抽滤装置。该抽滤装置包括用于搁置所述多孔板的基座323、围护结构321、与围护结构321分体式设置的抽滤多孔板322、与围护结构321分体式设置的多孔板7。多孔板7搁置在围护结构321的内部,抽滤多孔板322位于围护结构321的顶部实现对围护结构321内部空间的密闭,围护结构321的内部空间与真空泵连通,抽滤多孔板322与多孔板7上、下对齐。基座323上设置有用于与真空泵相连的气管接头324,基座323与真空泵连通实现围护结构321的内部空间与真空泵连通,围护结构321与基座323分体式设置。基座323固定在仪器上,多孔板抓手机械臂22先将一多孔板7移至基座323,再将围护结构321移至基座323,最后将抽滤多孔板322移至围护结构321的顶部,将核酸裂解液移至抽滤多孔板322后开启真空抽滤操作,抽滤多孔板322出来的滤液由位于其下方的多孔板7收集。抽滤多孔板322的反应孔的结构如图5所示,反应孔的底部开设有通孔325,通孔325之上覆盖有滤膜。
作为显而易见的变形,分离模块32亦可为离心机。
如图6所示,核酸提纯单元4包括提纯试剂存放区41、磁性粒子吸附洗脱模块42。核酸提纯单元4用于将经过预处理后的试样中的核酸提纯。核酸提纯单元4可采用申请号为201380018553.3的发明创造所述的相关技术方案。
核酸提纯单元4主要完成的工作有:向装有核酸初提液的多孔板7中加入高盐溶液和可与核酸特异结合的磁性粒子,振摇混合一定时间后,使磁性粒子与核酸完全结合;在多孔板底部或各孔四周施加磁场,吸附磁性粒子,移除多孔板各孔中的全部液体;加入盐洗液,振摇混合一定时间后,充分洗脱去除磁性粒子结合的盐粒子;在多孔板7底部或各孔四周施加磁场,吸附磁性粒子,移除多孔板7各孔中的全部液体;加入乙醇,振摇混合一定时间后,充分洗脱去除磁性粒子结合的其它杂质;在多孔板底部或各孔四周施加磁场,吸附磁性粒子,移除多孔板各孔中的全部液体,室温干燥5-10分钟;加入核酸洗脱液,振摇混合一定时间后,充分洗脱吸附在磁性粒子上的核酸;在多孔板底部或各孔四周施加磁场,吸附磁性粒子,移取多孔板7各孔中的全部液体得到高纯核酸。
由于一个多孔板反应孔的体积有限,不能放置足够多的试样。如果一个反应孔内的试样产生的核酸不足以被检出,则提纯后的高纯核酸还需要进入富集单元9。
如图7所示,富集单元9包括多孔板7、磁场产生装置91,多孔板7在提纯核酸时位于磁场产生装置91之上,磁场产生装置91用于在多孔板7周围产生磁场,移液机械臂21带着多通道移液枪将核酸粗提液或提纯后得到的高纯核酸试样加入多孔板7的反应孔内或将磁性粒子吸附后的核酸粗提液或高纯核酸试样从多孔板7的反应孔移除。磁场产生装置91为电磁式磁场产生装置,通电后产生磁场,关闭电源后磁场消失。磁场产生装置91的顶部有用于容置多孔板7的凹陷。用于富集单元9的多孔板7数量可以大于2块,每块多孔板7的相同位置放置经过提纯的同种核酸粗提液或提纯后得到的高纯核酸试样。富集时,一块多孔板7位于磁场产生装置331的凹陷内,其他多孔板7位于操作台面上,所有多孔板7在相同位置的反应孔内放置的是同种核酸粗提液或提纯后得到的高纯核酸试样。
之后,经过富集单元9的高纯核酸试样进入检测单元5。检测单元5包括PCR体系配制区51和基因定量检测区52,检测单元5用于对提纯后的高纯核酸试样进行检测,并得出结果。检测单元5主要的工作有:取上述高纯核酸试样,加入靶标基因PCR扩增上下游引物、PCR扩增缓冲液、检测探针,于荧光定量PCR板中混合并封膜后,按照温度设定程序依次进行解链、退火、延伸进行靶基因的PCR扩增,于每延伸结束时进行荧光检测,通过荧光值计算靶标基因拷贝数,继而计算出待分析样品中靶标微生物的克隆数。
- 还没有人留言评论。精彩留言会获得点赞!