一种新型H2PO4ˉ离子荧光探针及制备方法与应用与流程
本发明涉及化合物合成领域,尤其是一种磷酸根荧光探针的制备方法及其应用。
背景技术:
磷酸根等阴离子在自然界、生物体系中存在非常的广泛,在生物学、医学、环境科学等领域都发挥着非常重要的作用。例如,人体骨格和牙齿的主要成分之一是PO43-,是人体保持健康所不可缺少的成分,但当血液中的H2PO4-含量过高时则会导致人体肾功能障碍,反而会危害人体健康;工业废水、生活废水中含有的过量PO43-会导致水体富营养化,从而造成水华现象;H2PO4-等阴离子是构成基因和遗传物质的重要元素之一,在信息传递和能量储存方面扮演了重要的角色。因此,对H2PO4-等阴离子如何快速有效的检测,是医学、生物学和环境科学等领域亟待解决的问题,受到了各界的广泛关注。
荧光分子探针是一种具有广泛应用价值的高灵敏度检测手段,其设计合成、应用及识别过程中所涉及的光物理和光化学问题受到了不同领域研究者的广泛关注。分子识别可看做为底物与给定受体选择性地键合,并可能具有专一性功能的过程。分子识别包括对所有阳离子、阴离子及中性有机、无机或生物分子的识别。阴离子在环境科学、生命科学和医学等领域扮演着重要的角色,相对于其他类型的分子识别,阴离子识别的研究相对滞后,直到上世纪八十年代中期,阴离子识别研究才引起了广泛的关注。可见,设计和选择识别阴离子所用受体,是识别研究阴离子的基础,是一项具有挑战性的课题。
基于以上原因,目前一些H2PO4-荧光分子探针已经被设计合成出(Inorg.Chem.Front.,2015,2,649-656;Org.Biomol.Chem.,2015,13,1979-1982;Sensors and Actuators B 213(2015)501-507)。但这些荧光探针大多只能在有机溶剂实现对H2PO4-的识别,或是荧光淬灭型荧光探针,使得在水溶液中对H2PO4-离子检测的应用受到限制。
技术实现要素:
有鉴于此,本发明提供一种新型的能在水溶液中选择性检测H2PO4-的荧光探针。本发明的新型荧光探针对H2PO4-离子有很好的选择性,其它离子对H2PO4-检测干扰较小,溶液的荧光强度与H2PO4-离子的浓度在检测范围内有一定的线性关系,表现出了优异的现实应用性;本发明的荧光探针分子体系结构简单,合成方法简单且效率高,易推广于实际水溶液对H2PO4-离子检测中。
本发明的第一目的在于提供一种新型H2PO4-离子荧光探针,具有以下结构式:
优选地,所述H2PO4-离子荧光探针的化学名称为:
(E)-4-(4-(bis(pyridin-2-ylmethyl)amino)styryl)-N,N-dipropylaniline。
优选地,所述H2PO4-离子荧光探针的化学式为:C32H36N4。
优选地,所述H2PO4-离子荧光探针优选与Cu2+络合使用。
优选地,所述H2PO4-离子荧光探针优选与Li+、K+、Na+、Ag+、Mg2+、Ca2+、Zn2+、Ba2+、Ni2+、Co2+、Hg2+、Pb2+、Mn2+、Fe3+、Cr3+、Al3+、Cd3+、Cu2+络合使用。
更优选地,所述H2PO4-离子荧光探针为与Cu2+络合使用。
最优选地,所述H2PO4-离子荧光探针与Cu2+络合使用的比例为等摩尔配比。
本发明的另一目的在于提供简单、便捷的上述H2PO4-离子荧光探针的制备方法,包括以下步骤:
1)将N,N-二己基苯甲醇溶于过量的亚磷酸三乙酯中获得混合溶液,将所述混合溶液滴加到单质碘中,控制N,N-二己基苯甲醇与单质碘的摩尔比为1∶1,室温反应,萃取、干燥、浓缩后,用柱色谱分离得到中间体N,N-二丙胺基苯甲基亚磷酸二乙酯(I);
2)将中间体N,N-二丙胺基苯甲基亚磷酸二乙酯与叔丁醇钾按摩尔比1∶4混合至研钵中,在红外灯下充分研磨30分钟,再加入与中间体等摩尔量的4-N,N-二-(2-吡啶亚甲基)胺基苯甲醛,继续研磨,加入适量的氯仿,萃取、浓缩,得到红色粘稠状物质,吸附后上色谱柱,用洗脱液淋洗,得到淡黄色固体产物,即为荧光化合物(L)。
优选地,本发明所述荧光化合物L的合成路线为:
优选地,本发明所述H2PO4-离子荧光探针的制备方法中,所述步骤1)中室温反应时间为12小时。
优选地,本发明所述H2PO4-离子荧光探针的制备方法中,所述步骤1)中萃取剂为二氯甲烷。
优选地,本发明所述H2PO4-离子荧光探针的制备方法中,所述步骤1)中洗脱液为二氯甲烷。
优选地,本发明所述H2PO4-离子荧光探针的制备方法中,所述步骤2)中使用TLC跟踪法控制反应进度。
优选地,本发明所述H2PO4-离子荧光探针的制备方法中,所述步骤2)洗脱液为石油醚与乙酸乙酯,体积比为15∶1(v/v)。
优选地,本发明所述H2PO4-离子荧光探针的制备方法中,所述步骤2)中吸附所述红色粘稠状物质为使用硅胶吸附。
本发明还提供了上述H2PO4-离子荧光探针在H2PO4-离子的高选择性检测中的应用。
由上及本发明的后续实施例可知,本发明的H2PO4-离子荧光探针及制备方法至少有以下优点:
1)荧光探针对H2PO4-离子有很好的选择性,其它离子对检测影响较小,溶液的荧光强度与H2PO4-离子的浓度在范围内有一定的线性关系,表现出了良好的实际应用性;该探针分子体系结构简单,合成方法简单且效率高,易推广于实际检测;
2)本发明所设计的H2PO4-离子荧光探针体系,合成路线较为简单,反应条件温和,后处理简单方面。溶液体系对H2PO4-离子识别操作也较为简单易行,识别结果便于监测,并且在紫外灯下肉眼就可以直观的看出其荧光颜色变化。本发明可以在水溶液中实现对H2PO4-离子的高选择性检测,具有广阔的应用前景。
附图说明
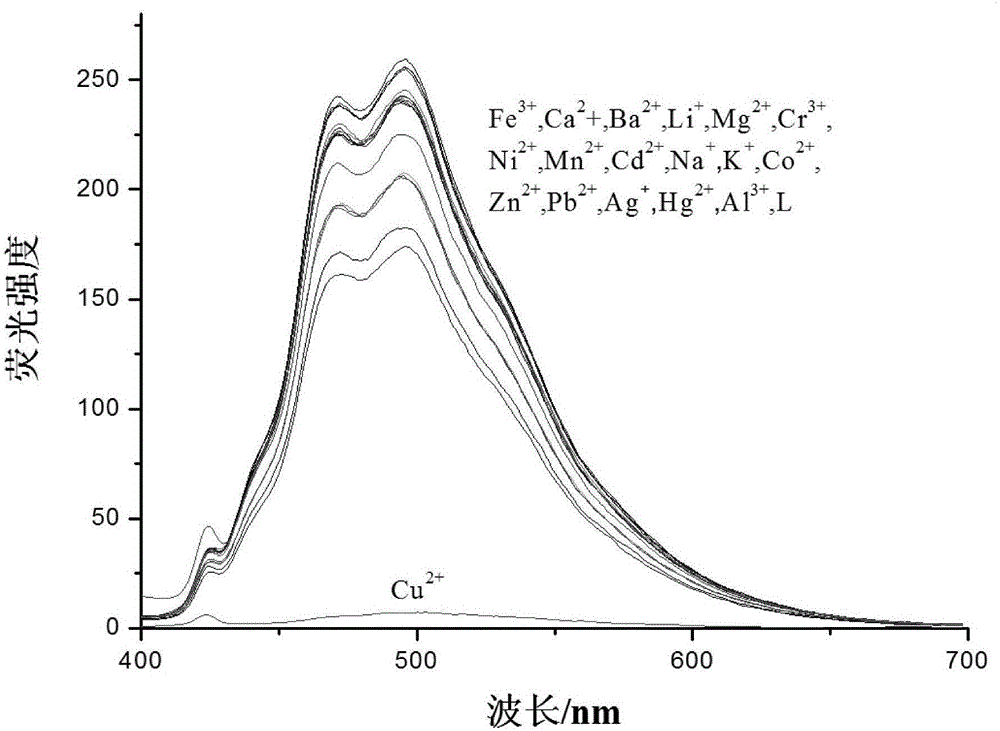
图1荧光化合物L在10mmol/L PH=7.4 HEPES缓冲溶液中与不同金属离子相互作用的荧光光谱;
图2紫外灯照射下荧光化合物L对Cu2+识别的颜色变化;
图3配合物L-Cu2+溶液体系中加入不同阴离子溶液的荧光光谱变化;
图4紫外灯照射下配合物L-Cu2+溶液体系对H2PO4-识别的颜色变化;
图5配合物L-Cu2+溶液体系中加入不同浓度的H2PO4-溶液荧光光谱变化;
图6配合物L-Cu2+溶液体系中在497nm处的荧光强度与H2PO4-溶液浓度的线性关系。
具体实施方式
以下通过具体实施例对本发明的技术方案进行进一步说明:
实施例1本发明荧光化合物L的合成
本发明的(E)-4-(4-(bis(pyridin-2-ylmethyl)amino)styryl)-N,N-dipropylaniline(L)按下述方法合成∶
1)中间体N,N-二丙胺基苯甲基亚磷酸二乙酯的合成
在50mL圆底烧瓶中,将0.291g(1mmol)的N,N-二己基苯甲醇溶于5mL的亚磷酸三乙酯中,然后将上述混合溶液滴加到0.258g(1mmol)的单质碘中,室温反应12h。二氯甲烷萃取,干燥,浓缩,以二氯甲烷为洗脱液用柱色谱分离。得产品0.32g,收率(Yield):77.8%。
核磁共振结果:1H NMR(CDCl3,400MHz,ppm):7.10(d,2H,J=6.8Hz);6.56(d,2H,J=8.4Hz);4.00(m,4H);3.21(t,4H,J=7.6Hz);3.25(d,2H,J=20.8Hz),1.55(s,4H);1.27(m,8H);0.88(t,6H,J=6.4Hz)。
2)本发明(E)-4-(4-(bis(pyridin-2-ylmethyl)amino)styryl)-N,N-dipropylaniline(荧光化合物L)的合成
称取2.24g(20mmol)叔丁醇钾和步骤1)获得中间体N,N-二丙胺基苯甲基亚磷酸二乙酯1.64g(5mmol),至研钵中,在红外灯下充分研磨几分钟,称取1.5g(5mmol)4-N,N-二-(2-吡啶亚甲基)胺基苯甲醛,加入反应体系中,继续研磨,使用TLC跟踪,加入适量的氯仿,萃取、浓缩,得到红色粘稠状物质,加硅胶吸附,上色谱柱,用(石油醚∶乙酸乙酯=15∶1(v/v))的洗脱液淋洗,得到(E)-4-(4-(bis(pyridin-2-ylmethyl)amino)styryl)-N,N-dipropylaniline的淡黄色固体1.3g,产率为54.6%。
核磁共振及质谱结果:1H NMR(400MHz,d6-CD3COCD3)δ:8.56(d,J=4.4Hz,2H),7.68-7.73(m,2H),7.34(d,J=8.8Hz,2H),7.22-7.31(m,6H),6.81(d,J=3.2Hz,2H),6.71(d,J=12.8Hz,2H),6.64(d,J=8.8Hz,2H),4.88(s,4H),3.29(t,J=7.6Hz,4H),1.56-1.65(m,4H),0.92(t,J=7.6Hz,6H).13C NMR(100MHz,d6-CD3COCD3):δ(ppm)164.53,154.69,152.60,152.53,141.67,132.48,132.30,131.99,130.61,130.07,128.70,127.14,126.22,117.92,116.98,62.58, 57.63,25.49,15.88.MALDI-TOF MS(M=477.30)。
实施例2本发明荧光化合物L的Cu2+络合物
将实施例1获得的荧光化合物L,用10mM pH=7.40HEPES缓冲溶液(HEPES∶DMSO=9∶1(v/v)),配制成4×10-5mol/L荧光化合物L溶液。将上述4×10-5mol/L荧光化合物L溶液中分别加入等摩尔量的0.01mol/L Li+、K+、Na+、Ag+、Mg2+、Ca2+、Zn2+、Ba2+、Ni2+、Co2+、Hg2+、Pb2+、Mn2+、Fe3+、Cr3+、Al3+、Cd3+、Cu2+各金属离子,如图1所示,各金属离子与荧光化合物L相互作用的荧光光谱图,仅仅Cu2+的加入形成配合物后使得溶液荧光基本淬灭。
如图2所示,在紫外灯下也能清楚观察到各金属离子与L相互作用的荧光颜色变化,仅有最左侧加入Cu2+的荧光化合物,由于Cu2+与荧光化合物L的相互作用,使得荧光显著消失(最左侧阴影)。
实施例3荧光化合物L的Cu2+配合溶液检测H2PO4-
在4×10-5mol/L荧光化合物L溶液10mM pH=7.40HEPES∶DMSO=9∶1,)加入等摩尔量的0.01mol/L Cu2+溶液,使得整个体系中荧光化合物L与Cu2+摩尔比为1∶1。在该混合溶液体系中,分别加入2倍当量的0.01mol/L CO32-、SO42-、NO3-、AcO-、F-、Cl-、Br-、I-、H2PO4-、PPi的钠盐溶液,监测溶液的荧光光谱变化(见图3),可以看出仅仅H2PO4-能使该溶液体系荧光显著增强;同样如图4,在紫外灯下肉眼就可以明显观察到荧光化合物L与Cu2+的混合溶液与各阴离子CO32-、SO42-、NO3-、AcO-、F-、Cl-、Br-、I-、H2PO4-、PPi相互作用的荧光颜色变化,其中仅有加入H2PO4-的混合溶液(最右侧)在紫外灯下能够观察到荧光。
总之,化合物L在10mM pH=7.40HEPES缓冲溶液中表现出较强的荧光,当Cu2+的加入使得荧光淬灭,再加入H2PO4-又使得荧光恢复,这个荧光“开-关-开”的过程显示了L-Cu2+溶液体系对H2PO4-的专一性识别。在L-Cu2+溶液体系中逐步加入H2PO4-的荧光滴定实验(见图5),可以看出随着H2PO4-浓度的增加,在λmax=497nm处的荧光强度也逐渐增加,荧光强度随H2PO4-浓度变 化的曲线表明,H2PO4-浓度在25μM-45μM的范围内有较好的线性关系(R2=0.9965),表现出了良好的实际应用性。
以上所述仅是本发明的优选实施方式,应当指出,对于本技术领域的普通技术人员来说,在不脱离本发明原理的前提下,还可以做出若干改进和润饰,这些改进和润饰也应视为本发明的保护范围。
- 还没有人留言评论。精彩留言会获得点赞!