一种氧调控性碱性成纤维细胞生长因子修饰细胞的方法与流程
本发明属于医学领域,涉及一种生长因子修饰细胞的方法,尤其涉及一种氧调控性碱性成纤维细胞生长因子修饰细胞的方法。
背景技术:
脊髓损伤(spinal cord injury,SCI)是中枢神经系统的严重创伤,呈高发生率、高致残率、高耗费的特点,会形成坏死囊腔、脊髓组织软化或形成胶质瘢痕,造成脊髓永久性功能丧失。严重影响人们的生活质量,给社会和家庭带来沉重的负担。
近年来,干细胞移植治疗脊髓损伤成为神经创伤康复研究的热点。干细胞可被诱导分化为神经细胞并融入患者的损伤组织,与正常的神经细胞形成神经元之间的突触样结构,使中枢神经系统的功能得到一定改善,使其成为了治疗脊髓损伤的新手段。目前可供选择的移植细胞类型有胚胎干细胞、神经干细胞、脐血干细胞、骨髓间充质干细胞等,其中神经干细胞被认为是治疗脊髓损伤最理想的移植细胞。
神经干细胞可以通过基因修饰用于神经系统疾病的基因治疗,表达外源性的神经递质,神经营养因子及代谢性酶。将这种多能干细胞移植入中枢神经系统损伤部位不仅可以存活和整合入宿主组织中,分化出神经元、星形胶质细胞和少突胶质细胞,填充因损伤造成的空洞,并且和宿主细胞之间可以形成突触样的结构,使神经组织损伤区域的组织结构得以修复,使中枢神经系统的功能得到一些恢复。但是目前对于神经干细胞移植后,其分化和增殖对于脊髓微环境中细胞自噬水平的影响,相关研究还十分匮乏。
碱性成纤维细胞生长因子(basic Fibroblast Growth Factor,bFGF),是由155个氨基酸组成的18kD多肽,主要分布于垂体、脑、脊髓及视网膜、肾上腺、胎盘等组织,具有广泛的生物学效应。bFGF在成年哺乳动物脊髓组织中呈低水平表达,但在脊髓组织损伤后bFGF表达显著上调。众多研究表明bFGF可促进血管生成、轴突再生、神经保护、组织修复、动员内源性神经干细胞,在中枢神经系统发育及损伤修复过程中具有重要作用。在大鼠急性脊髓损伤模型中,bFGF能够抑制神经细胞凋亡,增加脊髓缺血区血液供应,显著修复脊髓损伤面积,改善神经功能障碍。
但是作为一种干细胞分化中关键的营养因子,bFGF体内半衰期短,静脉给药后迅速降解,难以保持其生物活性;在脊髓损伤应用上,又是难以透过血脊髓屏障的生物大分子;同时,FGF受体在体内广泛分布于全身各组织器官,经静脉全身给药副作用大等也限制了它的应用。
技术实现要素:
本发明针对现有技术存在的缺陷,提供一种氧调控性bFGF表达的基因序列及使用该基因序列修饰细胞的方法。
本发明的第一个方面在于提供一种氧调控性bFGF表达的基因序列5HRE-CMVmp-bFGF(SEQ ID No.1)。
本发明的第二个方面在于提供一种基因序列5HRE-CMVmp(SEQ ID No.2)。
本发明的第三个方面在于提供一种采用基因序列SEQ ID No.1构建的质粒载体,所述质粒载体为重组腺相关病毒(AAV)、重组慢病毒和其他可用重组质粒载体中的任意一种或几种组合,优选为重组腺相关病毒。
作为本发明的一个优选实施例,所述重组腺相关病毒的制备方法包括:SEQ ID No.1的腺相关病毒载体与pHelper质粒一起,在含有细胞的培养基中进行转染,收集转染后的细胞,提取得到所述重组腺相关病毒。
作为本发明的一个优选实施例,所述重组腺相关病毒质粒的制备方法包括:
步骤1、以质粒pCMV-bFGF为模板,PCR扩增得到基因序列bFGF-polyA;
步骤2、设计引物,以质粒pShuttle-5HRE-CMVmp-Luc为模板,PCR扩增得到基因序列5HRE-CMVmp;
步骤3、将步骤2得到的基因序列bFGF-polyA与步骤3得到的基因序列5HRE-CMVmp配对,通过重叠PCR手段扩增基因序列5HRE-CMVmp-bFGF-polyA;
步骤4、以上游引物5’-ATAGTCGACCAATTCCTCGACGACTG-3’(SEQ ID No.4)和下游引物5’-GCCGTCGACTAAGATACATTGATGAG-3’(SEQ ID No.5)为引物,以质粒pShuttle-IRES-hrGFP-1为模板,PCR扩增得到IRES-hrGFP-polyA基因序列;将IRES-hrGFP-polyA基因序列与pENTR5’TOPO载体进行TOPO重组连接,将连接产物转化TOP10感受态细菌,提取质粒,并将该质粒进行SalI酶切,胶回收DNA片段IRES-hrGFP-polyA;
步骤5、制备5HRE-CMVmp-bFGF的重组穿梭质粒pShuttle/5HRE-CMVmp-bFGF,并予以SalI单酶切,并对经SalI单酶切后的pShuttle/5HRE-CMVmp-bFGF进行CIAP去磷酸化处理,将经CIAP去磷酸化处理后的pShuttle/5HRE-CMVmp-bFGF与胶回收DNA片段IRES-hrGFP-polyA于4℃连接16h,连接产物转化TOP10感受态细菌,提取质粒进行多重酶切鉴定筛选正确重组质粒pshuttle-5HRE-bFGF-IRES-hrGFP-polyA;
步骤6、以上游引物5’-CGCGTAATACTGGTACCGAG-3’(SEQ ID No.8)和下游引物5’-TCACTATTACACCCACTCGTGCAG-3’(SEQ ID No.7)为引物,以质粒pShuttle/5HRE-CMVmp-bFGF-IRES-hrGFP-polyA作为模板,PCR扩增5HRE-bFGF-IRES-hrGFP-polyA序列;
将PCR产物5HRE-bFGF-IRES-hrGFP-polyA与AAV-CAG-MCS-3FLAG载体进行无缝连接,将得到的连接产物转化TOP10感受态细菌,提取质粒进行多重酶切鉴定筛选正确重组腺相关病毒质粒AAV-5HRE-bFGF-IRES-hrGFP-polyA。
本发明的第四个方面在于提供bFGF修饰细胞的方法,所述方法包括如下步骤:
步骤1、提供基因序列SEQ ID No.1;
步骤2、将步骤1中得到的基因序列SEQ ID No.1构建为重组腺相关病毒载体;
步骤3、将所构建的重组腺相关病毒载体融合到干细胞中,得到氧调控性碱性成纤维细胞生长因子修饰的干细胞。
作为本发明的一个优选实施例,所述干细胞为全能干细胞、多能干细胞和单能干细胞的任意一种或几种组合,优选为全能干细胞和多能干细胞中的一种或几种,如骨髓间充质干细胞、神经干细胞、脐带干细胞、嗅鞘细胞和脂肪干细胞中的任意一种或几种组合,更优选为神经干细胞。
作为本发明的一个优选实施例,步骤2中,还包括包装构建得到的所述病毒颗粒。
作为本发明的一个优选实施例,将重组腺相关病毒质粒混合辅助质粒采用脂质体转染技术共转染293TN细胞,12h更换培养基,36h观察荧光强度大于90%,72h后收集培养基,在5*104rpm条件下离心,弃去上清,并向其中加入50uL PBS重悬所述重组腺相关病毒。
作为本发明的一个优选实施例,步骤3中将所构建的重组腺相关病毒载体融合到干细胞中的方法为:向含有干细胞的培养液加入包装后的质粒载体中,6ug/mL polybrene(聚凝胺)助转剂辅助感染,24h后更换培养基,得到经bFGF修饰的干细胞。
作为本发明的一个优选实施例,修饰干细胞低氧诱导bFGF表达,低氧诱导36h,荧光并WB检测确定筛选结果正确与否。
作为本发明的一个优选实施例,步骤3中所述干细胞的培养液包括:DMEM/F12基础培养基、表皮生长因子(EGF)、碱性成纤维细胞生长因子(bFGF)和B27。
作为本发明的一个优选实施例,步骤3中所述低氧环境为O2浓度小于1%。
作为本发明的一个优选实施例,步骤3中所述低氧处理的时间为6-72h,优选为12-60h,更优选为24-48h,如36h。
作为本发明的一个优选实施例,所述质粒载体为重组腺相关病毒、重组慢病毒和其他可用重组质粒载体中的任意一种或几种组合,优选为重组腺相关病毒。
作为本发明的一个优选实施例,所述重组腺相关病毒为AAV-5HRE-bFGF,所述重组腺相关病毒AAV-5HRE-bFGF的包装方法为:将所述重组病毒AAV-5HRE-bFGF与重组腺相关病毒包装质粒phelper共转染293TN细胞。
作为本发明的一个优选实施例,所述重组腺相关病毒为AAV-5HRE-bFGF。
本发明创造性的提出采用氧调控性bFGF修饰神经干细胞的方法治疗脊髓组织损伤,既保留了bFGF抑制神经细胞凋亡,增加脊髓缺血区血液供应,显著修复脊髓损伤面积,改善神经功能障碍的优点,又避免了因bFGF体内半衰期短,使用现有技术静脉注射而导致bFGF迅速分解的缺陷。
本发明首次通过构建氧调控性bFGF基因表达载体,实现治疗基因在特定病理条件下的可调控性表达。在缺血、缺氧环境中该载体可被有效诱导启动表达bFGF,在局部发挥促血管增生、神经保护和组织修复等作用。当机体缺血区新生血管形成,侧支循环建立,局部血液供应逐步恢复时,bFGF表达相应地逐渐下调,在常氧环境中,仅维持极低水平的bFGF表达,可避免传统基因治疗载体长期过量表达bFGF所产生的组织过度增生等诸多副作用及致瘤的风险。
低氧调控性bFGF基因治疗联合神经干细胞移植可以取长补短,相得益彰,为急性脊髓损伤治疗提供新的思路。通过基因水平调控促进神经干细胞增殖、迁移并分化为神经元;在提高其移植后存活率的同时,也能够影响炎症反应、氧化应激、血管新生等因子,改善脊髓损伤区域微环境,促进修复。
附图说明
图1为氧调控性重组腺相关病毒对hrGFP基因表达的影响;
图2-1为低氧环境下重组腺相关病毒的基因表达;
图2-2为低氧环境下重组腺相关病毒AAV-5HRE-bFGF在不同时间的基因表达;
图2-3为hrGFP基因在AAV-5HRE-hrGFP感染的PC12细胞中的表达;
图2-4为bFGF基因在AAV-5HRE-hrGFP感染的PC12细胞中的表达;
图3-1为重组腺相关病毒的PI染色图像;
图3-2为重组腺相关病毒的PI染色的细胞含量;
图3-3为重组腺相关病毒Hoechst染色图像;
图3-4为完整细胞核计数结果;
图4为重组腺相关病毒对原代神经干细胞分化的影响;
图5为制备的神经干细胞的荧光显微镜照片;
图6为不同条件下bFGF的蛋白表达水平;
图7为低氧条件下细胞液中的bFGF浓度;
图8为细胞培养液的荧光显微镜照片;
图9为bFGF基因蛋白对治疗脊髓损伤的影响;
图10为脊髓损伤组织的光镜照片。
具体实施方式
1重组腺相关病毒
1.1制备重组腺相关病毒质粒
步骤1、以重组质粒pCMV-bFGF为模板,PCR扩增得到基因序列bFGF-polyA;
步骤2、以上游引物CGCGTAATACTGGTACCGAG(SEQ ID No.8),和下游引物GATCTGACGGTTACTAAAC(SEQ ID No.9)为引物,以质粒pShuttle-5HRE-CMVmp-Luc为模板,PCR扩增得到基因序列5HRE-CMVmp;
步骤3、将步骤1得到的基因序列bFGF-polyA与步骤2得到的基因序列5HRE-CMVmp配对,通过重叠PCR手段扩增得到基因序列5HRE-CMVmp-Intron-bFGF-polyA;
步骤4、将步骤3得到的基因序列5HRE-CMVmp-Intron-bFGF-polyA酶切后,接入质粒AAV-MCS,得到重组腺相关病毒AAV-5HRE-bFGF。
采用类似制备方法制备重组腺相关病毒AAV-5HRE-hrGFP。
1.2包装重组腺相关病毒
1.2.1准备质粒把外源基因克隆进合适的载体。构建好的病毒载体和pHelper(携带腺相关病毒来源的基因)和pAAV-RC(携带AAV复制和衣壳基因)质粒进行大量抽提。
1.2.2AAV-293细胞培养
1.2.2.1AAV-293细胞复苏
1)预热培养基。
2)从液氮罐中取出细胞冻存管,迅速放入盛有37℃水的水浴中,并不时摇动,尽快解冻。用70%酒精擦拭消毒后,移至超净工作台。
3)吸出细胞悬液加入3ml培养基中,再加入5ml培养基稀释,轻柔吹散。
4)1000rpm,3min离心收集细胞。
5)适量培养基重悬细胞接种。
1.2.2.2AAV-293细胞传代(以10cm细胞皿为例)
1)弃去旧培养液,加入10ml灭菌PBS,轻轻晃动,洗涤细胞生长面,然后弃去PBS。
2)加入1mL胰酶消化液,消化1-2min直到细胞变圆开始脱落。
3)加入2mL完全培养基终止消化,并将细胞皿底细胞吹打成单细胞。
4)按需要离心重悬计数接种,或混匀细胞直接分到新的培养瓶中,继续培养。
1.2.2.3AAV-293细胞冻存
1)取培养2-3天生长旺盛的细胞,根据步骤1.2.2.2所述方法将细胞消化并吹打成单细胞。
2)以1000rpm的转速离心3min,收集细胞
3)加入适量PBS重悬细胞,计数。
4)1000rpm,3min离心收集细胞。
5)用冻存培养基再悬浮细胞至2×106~5×106个/ml,然后分装细胞悬液到2mL冷冻管,1mL冷冻管。
6)将小管置于程序降温盒,然后将程序降温盒放入-80℃冷冻过夜,第二天转移冻存细胞的小管到液氮中长期保存。
1.2.3细胞转染AAV-293细胞的接种
1)接种AAV-293细胞于10cm细胞皿中,备用。
2)转染前1h取出细胞培养板,去除原有细胞培养基,加入10mL Opti-MEM培养基。
3)制备转染试剂和质粒的复合物
a.将待转染的重组腺相关病毒载体质粒32μg(体积比pHelper:pAAV-RC:穿梭质粒=1:1:1)溶于Opti-MEM培养基中,总体积为500μL,轻轻混匀,静置5min。
b.将Obio转染试剂溶于Opti-MEM培养基,总体积为500μl,轻轻混匀,静置5min。
c.将Obio转染试剂稀释液滴加到质粒稀释液中,边加边轻轻混匀后在室温放置20min,使DNA和Obio转染试剂充分结合形成稳定的DNA-转染复合体。
4)取出细胞皿,将配好的DNA-转染试剂复合体加入到细胞培养板中,转染后换液。
5)6h后吸去培养基,PBS洗一次,加入10mL新鲜完全培养基培养。
1.2.4病毒收获及纯化
1)转染60h后,使用细胞刮将细胞刮下,并收集到离心管。
2)将收集到的细胞在4℃条件下离心5min,将细胞裂解液沉淀重悬在7mL的10mM Tris-HCl缓冲液中。
3)将细胞裂解液存储在干冰/乙醇浴中,37℃水浴中反复冻融8次。
4)使用10mM Tris-HCl将细胞裂解液定容到21mL。
5)超声仪超声7min。
6)向超声后的细胞裂解液中加入2ml DNase I(3mg/ml),并于37℃孵育30min。
7)再次超声7min。
8)加入2.5mL 10%脱氧胆酸钠,2.1mL 0.25%胰酶-EDTA,混合均匀后于37℃孵育30min,冰上放置20min。
9)加入16.9g CsCl,混合均匀后,37℃孵育20min。37℃孵育过程中不断摇动,直到CsCl完全溶解。
10)在4℃下,将3000g处理过的细胞裂解液离心30min,小心地将细胞裂解液转移到超速离心管(约5ml/tube)中。
11)于4℃下以53,000rpm的速度离心30h。
12)使用自制的针头收集病毒层。
13)4℃透析,12-16h换透析液,每次使用4L缓冲液。
1.2.5滴度测定
AAV的滴度是通过定量PCR检测基因组中AAV载体的基因组拷贝数来测定AAV的病毒颗粒数来测定的。
1)准备样品和标准品,梯度稀释标准品质粒和待测样品至原浓度的10-5、10-6、10-7和10-8;
2)根据反应数(X)计算反应总管体积(每个梯度做两个复孔,每10个反应多准备1个):
3)在每个反应孔中加入反应液15μl,然后加入5μl的模板;
4)上机,退火温度设为60℃,按照标准操作得到Ct值并计算AAV样品中的拷贝数。
2.提取神经干细胞及感染鉴定
材料和试剂
14~16d孕龄Sprague-Dawley大鼠胚胎、DMEM/F12培养基、表皮生长因子(epidermal growth factor,EGF)、碱性成纤维细胞生长因子(basic fibroblast growth factor,bFGF)、青链双抗、神经元特异性烯醇化酶(neuron specific enolase,NSE)抗体、胶质纤维酸性蛋白(gilial fibrillary acidic protein,GFAP)抗体、小鼠抗大鼠单克隆巢蛋白(nestin)、Hochest、Merge、B27、胎牛血清(fetal calf serum,FCS)、干细胞培养液;
其中,GFAP、Hochest、Merge和nestin均购自美国Sigma公司,B27和FCS均购自Gibco公司。
干细胞培养液的配制方法为在基础液体培养基中加入20μLEGF、10g/L或20g/L的bFGF、20mg/L的B27、1%青链双抗。
2.1提取神经干细胞
取孕龄14~16d的大鼠胚胎,于无菌条件下分离脑皮质组织,在显微镜下剥除脑膜及表面血管,机械消化后将其剪成糜状,加入DMEM/F12培养基,并通过200目不锈钢滤网。用基础培养基洗涤、离心后,用配制的干细胞培养液重新悬浮经离心后的大鼠神经细胞,使用改良牛鲍计数盘计数活体细胞至浓度为5×105个/ml,然后吸取2mL处理过的大鼠神经细胞,将其接种于50mL的玻璃细胞培养瓶,置于37℃、5%CO2、饱和湿度培养箱中连续培养2~3d,半量换液,培养至第7~10d时,根据细胞的生长状况和密度,吸除一半培养基,机械法吹散干细胞球,重新用干细胞培养液悬浮细胞,然后转入新的培养瓶中继续培养。
2.2鉴定神经干细胞
对培养的神经干细胞进行Nestin和Hochest免疫荧光染色。吸取适量的NSC球,以800r/min的转速离心5min,向其中加入含有5%FCS和NSC的培养液,接种于涂有多聚赖氨酸盖玻片的培养皿中。培养4d后使用PBS洗涤3次,每次洗涤5min,然后于室温下使用4%多聚甲醛固定15min,并使用PBS洗涤3次,每次5min。向其中加入浓度为0.2%的大鼠TritonX-100作用15min,PBS洗3次,5min/次,用山羊血清封闭液在37℃湿盒内封闭30min,加一抗Nestin(1∶50),4℃过夜,并使用PBS洗涤2次,每次5min,加入大鼠1∶100稀释的二抗(TRITC标记的羊抗鼠IgG),室温孵育4h,使用PBS洗涤3次,每次5min,洗涤结束后封片。在荧光显微镜下观察并照相记录结果,结果如图5所示。
2.3bFGF修饰细胞
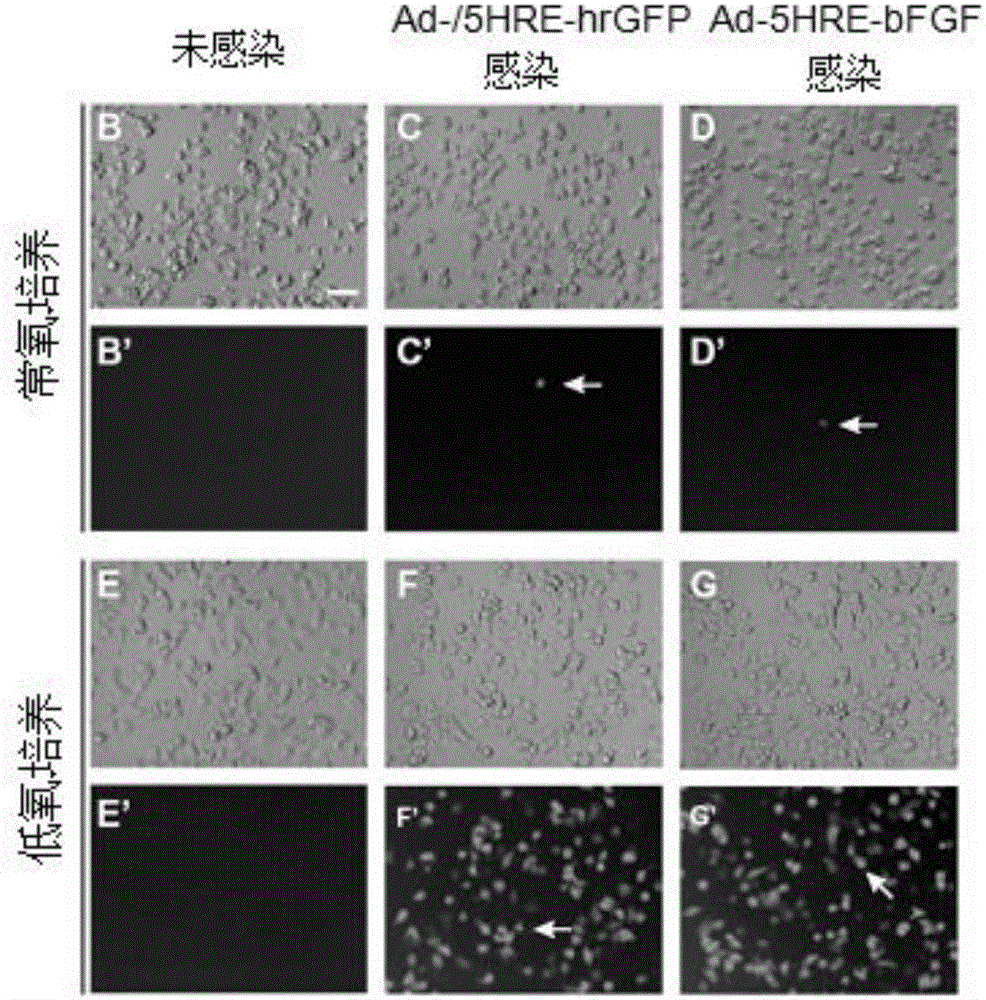
取经过包装的重组腺相关病毒AAV-5HRE-bFGF和AAV-/5HRE-hrGFP,取两个重组腺相关病毒的上清液以25MOI加入24孔板培养的大鼠原代神经干细胞中,培养18h后,将重组腺相关病毒AAV-5HRE-bFGF和AAV-/5HRE-hrGFP分别平均分为二组,其中一组在常氧(O2浓度为21%)培养箱中继续培养24h,另一组在低氧(O2浓度低于1%)培养箱中继续培养24h,培养结束后分别在荧光显微镜下观察,结果如图1所示。
由图1可知,在常氧环境下,培养的重组腺相关病毒AAV-5HRE-bFGF和AAV-5HRE-hrGFP,仅有极少数细胞表达hrGFP基因。而在O2浓度低于1%的低氧条件下培养的重组腺相关病毒AAV-5HRE-bFGF和AAV-5HRE-hrGFP,95%以上的细胞均可见hrGFP基因表达,且随着诱导时间的延长,hrGFP基因在AAV-5HRE-hrGFP感染的原代神经干细胞中的浓度逐渐增加,24h时达到峰值,hrGFP/GAPDH=1.1。随着诱导时间的延长,bFGF基因在AAV-5HRE-bFGF感染的原代神经干细胞中的浓度也逐渐增加,24h时达到峰值,bFGF/GAPDH=1.5。
在重组腺相关病毒AAV-5HRE-bFGF和AAV-5HRE-hrGFP感染原代神经干细胞18h后,分别在低氧条件下处理1-24h,并设置常氧对照组,采用免疫印迹法检测bFGF基因和hrGFP基因的表达情况,结果如下图2-1~2-4所示:
由图2-1~2-4可知,在低氧环境下,诱导3h即可检测到bFGF基因和hrGFP基因的表达,24h时达到高峰。而在常氧条件下,3h检测不到bFGF和hrGFP的基因表达,诱导24h时,也只检测到痕量的bFGF和hrGFP基因表达。
2.4重组腺相关病毒对抑制原代神经干细胞凋亡的影响
重组腺病毒载体AAV-5HRE-bFGF和AAV-5HRE-hrGFP分别感染PC12细胞18h后,在氧气体积浓度低于1%的低氧环境下处理6h,以诱导转基因表达,然后将含15%血清的常规培养液更换为无血清培养液,继续培养48h,通过碘化丙啶(PI)染色、Hoechst染色及完整细胞核计数等方法评价AAV-5HRE-bFGF的药理学活性。PI染色结果如图3-1,图3-2所示,AAV-5HRE-bFGF组细胞存活率达76.1%,而对照组(添加PC缓冲盐)与AAV-5HRE-hrGFP组细胞存活率分别为24.8%和25.3%。
Hoechst染色结果如图3-3所示,AAV-5HRE-hrGFP感染的PC12细胞血清剥夺后出现核固缩、核碎裂等凋亡特征,而AAV-5HRE-bFGF感染的细胞血清剥夺后细胞核形态仍保持正常。完整细胞核计数结果如图3、图4所示,与对照组(添加PBS)和AAV-5HRE-hrGFP组相比,AAV-5HRE-bFGF组完整细胞核数量明显增多,具有显著性差异(p<0.01)。
2.5重组腺相关病毒对原代神经干细胞分化的影响
重组腺相关病毒AAV-5HRE-bFGF和AAV-5HRE-hrGFP分别感染原代神经干细胞18h后,在氧气体积含量低于1%的低氧环境下处理6h,诱导bFGF和hrGFP转基因表达,然后将含15%血清的细胞培养液更换为含1%血清细胞培养液,继续培养6天后观察细胞的大体形态,并进行免疫荧光染色检测神经元特异性抗原NeuN。结果如图4所示,其中,AAV-5HRE-bFGF感染原代神经干细胞组多数细胞体呈梭形或三角形,长出数目、长短不等的突起,NeuN蛋白免疫荧光染色阳性。而对照组(添加PBS)组和AAV-5HRE-hrGFP感染原代神经干组中的原代神经干细胞仍保持圆形或椭圆形,无突起长出,NeuN染色阴性。
3氧调控性bFGF基因重组细胞对脊髓损伤的治疗
本测试分为对照组、模型组和实验组,均以10周龄、体重为280-320g的SD大鼠作为考察对象,每组32只,随机分配。空白组大鼠暴露T9-11脊髓。模型组大鼠暴露T9-11脊髓,并采用动脉血管夹(30g,2min)压迫脊髓法致SD大鼠急性脊髓损伤。实验组大鼠暴露T9-11脊髓,采用动脉血管夹(30g,2min)压迫脊髓法致SD大鼠急性脊髓损伤,并在皮下连续注射氧调控性bFGF基因重组细胞。
采用Basso-Beattie-Bresnahan(BBB)评分方法评价各组大鼠后肢的行走及肢体活动情况,于大鼠术后1天、3天和7天分别做脊髓功能评价,结果如图9所示。
由图9可知,术后1天,对照组后肢行动正常,模型组和实验组后肢行动均有不同程度的障碍。术后1天,模型组和实验组BBB评分无显著性差异。术后3天,实验组的BBB评分明显高于模型组(P<0.05)。术后7天,明显可见实验组大鼠可持续性前后肢协调行走,而模型组大鼠后肢仍旧不能负重走动(P<0.05)。
术后7天采用HE染色方法对各组脊髓损伤组织片进行苏木素-伊红染色,光镜下观察,结果如图10所示,对照组大鼠的组织切片脊髓组织结构致密清晰,未见明显的细胞凋亡和坏死。HE染色显示,术后7天,相比较模型组,实验组SD大鼠的脊髓组织结构更致密清晰,细胞丢失减少,白质中空泡形成数量明显减少。以上结果表明,氧调控性bFGF基因重组细胞能促进大鼠脊髓损伤的修复。
以上对本发明的具体实施例进行了详细描述,但其只是作为范例,本发明并不限制于以上描述的具体实施例。对于本领域技术人员而言,任何对本发明进行的等同修改和替代也都在本发明的范畴之中。因此,在不脱离本发明的精神和范围下所作的均等变换和修改,都应涵盖在本发明的范围内。
- 还没有人留言评论。精彩留言会获得点赞!