本发明涉及分子生物学检测,特别涉及一种用于评估叶酸代谢能力的核酸杂交膜条和一种用于扩增待检样品基因片段的聚合酶链式反应(PolymeraseChainReaction,PCR)引物;本发明还涉及一种用于评估叶酸代谢能力的试剂盒。
背景技术:
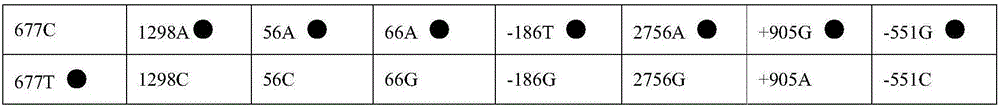
:叶酸代谢与许多重要的生化过程密切相关,一方面它可以影响核酸的合成,另一方面它参与了DNA、蛋白质的甲基化,此外还直接影响氨基酸的代谢,对细胞分裂、增殖和组织生长具有极其重要的作用。研究表明,叶酸代谢紊乱可影响DNA和氨基酸的合成及甲基化过程,并可导致高同型半胱氨酸血症,与先天性心脏病、神经管畸形等出生缺陷以及反复流产等有密切关系。叶酸代谢紊乱的因素十分复杂,包括饮食中叶酸及甲基供体等缺乏,叶酸代谢相关酶的遗传多态性,酒精和吸烟的影响等等。参与到叶酸代谢途径的酶有多种,包括二甲基四氢叶酸还原酶(MTHFR)、甲硫氨酸还原酶(MTR)、甲硫氨酸合成还原酶(MTRR)和胱硫脒β合酶(CBS)等,这些酶的某些核苷酸多态可导致叶酸代谢异常引起疾病或出生缺陷,其中母亲高同型半胱氨酸水平是先天性心脏病的高危因素。MTHFR是叶酸代谢的关键酶,催化5,10-亚甲基四氢叶酸还原为5-甲基四氢叶酸,后者与同型半胱氨酸共同被催化形成蛋氨酸,参与DNA甲基化等生物过程。人类MTHFR基因位于染色体1p36.3,其中有多个与MTHFR活性相关的SNP位点,例如G1965A、A1515C、C894T、以及C677T和A1298C等。MTHFR第677位碱基C>T变异(rs1801133),可导致MTHFR蛋白第222位的丙氨酸被缬氨酸取代,产生三种基因型:野生型(677CC),杂合变异型(677CT)和纯合变异型(677TT),在中国人群中的百分比分别为33%,44%和23%。与相比,杂合变异型(677CT)和纯合变异型(677TT)MTHFR酶活性与野生型(677CC)相比下降,为野生型的65%和30%,导致血清叶酸和维生素B12水平下降,同型半胱氨酸水平升高。MTHFR第1298位碱基A>C变异(rs1801131),可使MTHFR蛋白第433位的谷氨酰胺被丙氨酸取代,产生三种基因型:野生型(1298AA),杂合变异型(1298AC)和纯合变异型(1298CC),在中国人群中的百分比分别为66.8%,29.3%和3.9%。杂合变异型和纯合变异型MTHFR活性下降,可导致血浆中同型半胱氨酸水平升高。甲硫氨酸合成酶还原酶(MTRR)能够通过还原型甲基化作用重新生成具有功能活性的甲硫氨酸合酶,是叶酸代谢的关键酶之一。主要变异型有十余种,其中A66G是最主要和研究最多的突变。MTRR基因第66位碱基A>G变异(rs1801394),导致MTRR蛋白氨基酸链残基22位蛋氨酸被异亮氨酸替代,引起酶的活性降低,导致同型半胱氨酸血症,增加神经管畸形和先天性心脏病等出生缺陷性疾病的发病风险。其中野生型(66AA),杂合变异型(66AG)和纯合变异型(66GG)三种基因型在中国人群中百分比分别为58%,36%和6%。MTRR基因第一内含子c.56+781A>C多态(rs326119)的C等位基因可以降低MTRR基因的转录活性,导致MTRR的表达量下降,研究表明纯合变异型个体体内的同型半胱氨酸水平高于野生型个体,最终增加了先天性心脏病的易感性。甲硫氨酸还原酶(MTR)催化蛋氨酸合成的最终步骤,MTR基因位于1q43。MTR基因启动子区-186位碱基T>G多态(rs28372871)的G等位基因可以影响转录因子与基因启动子序列结合,降低MTR基因的转录活性,并且G等位基因可升高启动子区的甲基化水平,两方面相互作用最终引起MTR的表达量下降;大规模队列研究表明G等位基因是先天性心脏病的易感基因。MTR基因第2756位碱基A>G变异(rs1805087)可导致第919位氨基酸残基天冬氨酸被甘氨酸替代。大多数研究表明等位基因G可以导致个体的同型半胱氨酸水平下降,并且与多种肿瘤相关,但在中国人群中的研究并没有发现该变异与叶酸代谢异常及先天性心脏病相关。MTR基因下游+905位碱基G>A变异(rs1131450)位于基因的3’UTR位置,体外实验表明等位基因A可以通过影响miRNA的结合降低MTR的表达水平,导致同型半胱氨酸水平升高,从而增加了先天性心脏病的患病风险。胱硫醚β合酶(CBS)可以催化同型半胱氨酸形成胱硫醚,减轻同型半胱氨酸对机体的损害,是硫化反应的第一步。CBS基因位于21q22.3。CBS基因上游-551位碱基C>G变异(rs2850144)的G等位基因可以影响启动子与转录因子的结合,导致CBS的转录活性升高,表达量增加。虽然功能学研究并未发现G等位基因对同型半胱氨酸水平的影响,但在中国人群的病例对照研究和全基因组关联分析均表明,G等位基因对先天性心脏病的发生有保护作用。机体叶酸利用能力的先天性不足,引起叶酸缺乏时,需要对补充适当的叶酸,以维持机体机内正常的生物代谢。我国推荐孕期补充量为400微克/天,可以将显著降低患儿的出生缺陷,如能够降低NTDs(41%-85%),但是还有15%-59%却效果不明显,通过增加合适剂量的叶酸可以进一步降低NTDs。个性化补充叶酸,即让补充叶酸更具有针对性。专家建议:根据自己的遗传体质,在正确的时间补充合适剂量的叶酸。对MTHFR基因、MTRR基因及其相关位点的检测,可以直接发现被检测者叶酸代谢方面的遗传缺陷(即叶酸的利用能力),从而根据风险高低(相关代谢酶的活性程度)。如由发明人和中国疾病预防控制中心妇幼保健中心联合组织的孕期叶酸利用能力检测所提供的增补参考量:表1:孕期叶酸利用能力检测所提供的增补参考量表以上补充剂量指合成叶酸补充剂或强化剂的摄入量,不包括食物;对所有成年人包括孕妇和乳母,合成叶酸制剂的可耐受的最高摄入量(UL)设定为1000微克/天。因此800微克/天的叶酸制剂是安全的。对叶酸的增补剂量并非越多越好。大量研究发现,过量补充叶酸会导致以下不良后果:导致体内锌缺乏。锌是多种酶的活化剂,因此,孕母过量补充会导致胎儿生长缓慢,出生体重过低。叶酸作为合成核酸所必需的元素,是细胞生长和组织修复所必需的物质,更是胚胎发育过程中不可缺少的营养素,有“优生优育的营养素”美誉,对孕妇尤其重要。据我国婚前育龄女性血清抽样调查发现,我国城市和农村女性缺乏叶酸者分别有21%和38%。据卫生部及疾控中心相关报告,我国每年有90万新生儿缺陷性疾病诞生,患出生缺陷排在前5位的包括:先天性心脏病,神经管畸形,唇腭裂,唐氏综合征,多指(趾),这些都与孕妇叶酸缺乏有一定关系。1997年卫生部开始推荐孕期女性统一补充叶酸,剂量为400μg/d,该措施在出生缺陷预防中起了重要作用。但由于孕妇对叶酸的代谢能力不足,出生缺陷的发生率仍存在很大的地域差异。对于叶酸代谢能力正常的孕妇来说,每天补充400μg叶酸是足够的,但是对叶酸代谢能力存在障碍的孕妇来说,应该相应增加补充剂量,并加强孕期各项检测。近年来的研究表明,叶酸代谢能力在个体间的差异与部分基因位点的多态性有关,具体位点包括:亚甲基四氢叶酸还原酶(MTHFR)基因的c.677位点、c.1298位点;甲硫氨酸合成还原酶(MTRR)基因的c.56位点、c.66位点;甲硫氨酸合成酶(MTR)基因的-186位点、c.2756位点、+905位点;胱硫醚-β-合成酶(CBS)基因的-551位点。因此,利用现代基因分型技术检测孕母叶酸代谢相关基因,根据基因分型结果对受检者叶酸利用能力进行分级,进而针对性的调整叶酸补充剂量具有重大意义。目前,传统基因诊断方法包括酶切,限制性片段长度多态性分析(restrictionfragmentlengthpolymorphism,RFLP),直接测序等,这些方法或者不能定性,或者耗时费力、所需设备和耗材昂贵,更重要的是这些方法难以同时对不同基因的多个多态位点进行检测。而基因芯片法虽然能同时对不同基因位点进行检测,但它所需设备和耗材昂贵,不适用于在临床大规模推广,应用受到限制。技术实现要素:本发明所要解决的技术问题是:弥补上述现有技术的不足,提出一种用于叶酸代谢基因分型的核酸杂交膜条、一种用于扩增待检样品基因片段的PCR引物,以及一种用于叶酸代谢基因分型的试剂盒;本发明具有高通量、高效率、价格低廉、使用方便等优点。本发明提供一种用于叶酸代谢基因分型的核酸杂交膜条,其采用以下的技术方案:所述用于叶酸代谢基因分型的核酸杂交膜条,包括基底,以及在所述基底上固定有特异性的多态检测探针对,每一对多态检测探针包括一条突变探针和一条正常探针,每一对多态检测探针分别对应一个叶酸代谢相关基因多态位点,所述相关基因多态位点包括以下位点中的至少一个:亚甲基四氢叶酸还原酶(MTHFR)基因c.677位点、c.1298位点;甲硫氨酸合成还原酶(MTRR)基因c.56位点、c.66位点;甲硫氨酸合成酶(MTR)基因-186位点、c.2756位点、+905位点;胱硫醚-β-合成酶(CBS)基因-551位点;每一条所述突变探针和所述正常探针包含13-25个碱基的序列,在所述序列的中部位置包含其相对应的叶酸代谢相关基因的多态碱基。优选的,所述突变探针为SEQIDNO.1,SEQIDNO.3,SEQIDNO.5,SEQIDNO.7,SEQIDNO.9,SEQIDNO.11,SEQIDNO.13,SEQIDNO.15中的至少一个序列或其反向互补序列的DNA;所述正常探针为SEQIDNO.2,SEQIDNO.4,SEQIDNO.6,SEQIDNO.8,SEQIDNO.10,SEQIDNO.12,SEQIDNO.14,SEQIDNO.16中的至少一个序列或其反向互补序列的DNA。优选的,所述多态检测探针的3’或5’端带有氨基标记。本发明还提供一种用于扩增待检样品基因片段的PCR引物,其所述PCR引物的扩增产物含有如上所述的基因多态位点,所述PCR引物为以下8对中的至少一对:SEQIDNO.17和EQIDNO.18;SEQIDNO.19和SEQIDNO.20;SEQIDNO.21和SEQIDNO.22;SEQIDNO.23和SEQIDNO.24;SEQIDNO.25和SEQIDNO.26;SEQIDNO.27和SEQIDNO.28;SEQIDNO.29和SEQIDNO.30;SEQIDNO.31和SEQIDNO.32;其中SEQIDNO.17、SEQIDNO.19、SEQIDNO.21、SEQIDNO.23、SEQIDNO.25、SEQIDNO.27、SEQIDNO.29、SEQIDNO.31是上游引物;SEQIDNO.18、SEQIDNO.20、SEQIDNO.22、SEQIDNO.24、SEQIDNO.26、SEQIDNO.28、SEQIDNO.30、SEQIDNO.32是下游引物。优选的,所述的扩增产物分别包括如下位点:引物677F和引物677R的扩增产物包含MTHFR基因的c.677位点;引物1298F和引物1298R的扩增产物包含MTHFR基因的c.1298位点;引物56F和引物56R的扩增产物包含MTRR基因的c.56位点;引物66F和引物66R的扩增产物包含MTRR基因的c.66位点;引物-186F和引物-186R的扩增产物包含MTR基因的-186位点;引物2756F和引物2756R的扩增产物包含MTR基因的c.2756位点;引物+905F和引物+905R的扩增产物包含MTR基因的+905位点;引物-551F和引物-551R的扩增产物包含CBS基因的-551位点。优选的,所述上游引物和/或下游引物的5’端带有生物素或荧光标记。本发明还提供一种用于叶酸代谢基因分型的试剂盒,该试剂盒包含上述的用于叶酸代谢相关基因分型核酸杂交膜条,以及含有上述的用于扩增待检样品基因片段的PCR引物的PCR反应液。本发明与现有技术对比的有益效果是:公开了用于叶酸代谢基因分型的针对MTHFR基因c.677位点、c.1298位点,MTRR基因c.56位点、c.66位点,MTR基因-186位点、c.2756位点、+905位点,CBS基因-551位点的核酸杂交膜条、PCR引物及试剂盒。本发明是基于PCR-膜条杂交技术的基因检测方法,由于固定在基底上的多态检测探针对的大致中间位置包含有叶酸代谢能力相关基因多态位点,通过PCR-膜条杂交技术能直接对待检者的基因型进行确诊,对多态杂合子、多态纯合子等很容易判断,具有高通量、高效率、价格低廉、使用方便等优点。附图说明图1是本发明实施例叶酸代谢相关基因多态样品结果一示例。图2是本发明实施例叶酸代谢相关基因多态样品结果二示例。图3是本发明实施例叶酸代谢相关基因多态样品结果三示例。图4是本发明实施例叶酸代谢相关基因多态样品结果四示例。具体实施方式下面对照附图和结合优选具体实施方式对本发明进行详细的阐述。1、核酸杂交膜条的制备1.1、8对多态检测探针的制备按照表1中的序列合成16条探针,多态检测探针的3’或5’端带氨基标记,合成的方法为现有的常规的DNA合成法。表1:该表中,每一对多态检测探针包含一条突变探针和一条正常探针。其中突变探针为:677T,1298A,56A,66G,-186T,2756G,+905A,-551C;正常探针为:677C,1298C,56C,66A,-186G,2756A,+905G,-551G。每一条所述多态检测探针对分别对应包含一个叶酸代谢能力相关基因多态位点,所述叶酸代谢能力相关基因多态位点为以下位点中的至少一个:亚甲基四氢叶酸还原酶(MTHFR)基因的c.677位点、c.1298位点;甲硫氨酸合成还原酶(MTRR)基因的c.56位点、c.66位点;甲硫氨酸合成酶(MTR)基因的-186位点、c.2756位点、+905位点;胱硫醚-β-合成酶(CBS)基因的-551位点;每一条突变探针和所述正常探针包含13-25个碱基的序列,在所述序列的中部位置包含其相对应的叶酸代谢相关基因的多态碱基。1.2、核酸杂交膜条的制备a.用打印机在基底(本实施例中为尼龙膜)上打印位点阵列,并标明相应位点的探针名称,正常探针与突变探针固定在基底的不同位置上;b.用5%的EDAC溶液泡膜30分钟,以活化尼龙膜表面的羧基;c.分别用探针稀释液(10mmol/LTris,pH8.0)将16条探针稀释至5μmol/L;d.按尼龙膜条上打印的位点阵列,将16条探针按探针名称对应分别点加在尼龙膜相应位点上,探针上的氨基与尼龙膜表面的羧基发生交联反应;e.待尼龙膜条干燥后,用0.1mol/L的NaOH泡膜5分钟,以封闭尼龙膜表面未反应的羧基;f.用纯水洗涤尼龙膜,干燥后备用。表2:尼龙膜条上的探针阵列如下:677C1298A56A66A-186T2756A+905G-551C677T1298C56C66G-186G2756G+905A-551G2、PCR引物扩增根据本项目待检的8个多态位点的位置关系,设计了8对引物分别进行扩增,其中SEQIDNO.17、SEQIDNO.19、SEQIDNO.21、SEQIDNO.23、SEQIDNO.25、SEQIDNO.27、SEQIDNO.29、SEQIDNO.31是上游引物;SEQIDNO.18、SEQIDNO.20、SEQIDNO.22、SEQIDNO.24、SEQIDNO.26、SEQIDNO.28、SEQIDNO.30、SEQIDNO.32是下游引物,分别扩增相应的多态位点。上游引物和/或下游引物的5’端带有生物素或荧光素(如Cy3、Cy5等)标记。本发明实施例为对下游引物(677R、1298R、56R、66R、-186R、2756R、+905R、-551R)进行生物素标记,其PCR扩增后的产物可与本发明实施例中的探针杂交,PCR引物的DNA序列如表3所示。表3:2.1、提取模板DNA:使用其它商业化试剂盒从病人的血液中提取模板DNA。2.2、合成16条引物:合成的方法为现有的常规的DNA合成法。2.3、配制PCR反应液:配制成25μL/人份的PCR反应液,每人份的PCR反应液中各成份及浓度分别为:16条引物浓度分别为0.2μmol/L、Taq酶为0.1U/μL、1×PCRBuffer、MgCl2为1.5mmol/L、dNTP为0.2mmol/L、模板DNA1~10ng/μL。2.4、PCR扩增:PCR扩增的反应程序为:95℃预变性5分钟;95℃变性30秒,55℃复性30秒,72℃延伸30秒,循环35次;72℃再延伸5分钟。PCR扩增后的产物包含待测病人的DNA片段。3、杂交及显色3.1.杂交将PCR扩增后的产物与步骤1.2中的尼龙膜条加入到12mL的杂交液(2×SSC、0.1%SDS,pH7.4)中,在杂交箱中42℃杂交2~4小时以上。3.2.洗膜将尼龙膜条转移到预热至42℃的洗液(0.5×SSC、0.1%SDS,pH7.4)中,于42℃洗涤15分钟。3.3.过氧化物酶(Peroxidase,缩略词为POD)孵育将膜条放入新鲜配制的0.25U/mL的链霉亲合素-POD(streptin-POD)溶液中,37℃孵育15分钟,使链霉亲合素与PCR产物中的生物素结合,POD连接到PCR产物上,洗去多余的streptin-POD。3.4.显色现配显色液(0.1mol/L柠檬酸钠、0.1mg/mLTMB、0.0015%H2O2),将膜条放入显色液中避光显色15分钟,有杂交产物的膜条相应探针位置处会显蓝色斑点。4、结果判断如图1-4所示,膜条的显色结果,通过肉眼判断,以各位点显色信号的有无来判断待检样品的基因型,其中,图1的基因型为:677CC、1298AA、56AA、66AA、-186TT、2756AA、+905GG、-551CC纯合子;,图2的基因型为:677TT、1298AA、56AA、66AA、-186TT、2756AA、+905GG、-551CC纯合子;图3的基因型为:66AG杂合子;677CC、1298AA、56AA、-186TT、2756AA、+905GG、-551CC纯合子;图4的基因型为:677CT、1298AC杂合子;56AA、66AA、-186TT、2756AA、+905GG、-551CC纯合子。对于膜条上的8个待检位点来说,其中1种多态基因型显色,则判定为该基因型的纯合子;若1个位点的两种多态基因型都显色,则判定该位点为两种多态基因型的杂合子,以此对8个待检位点分别进行判定。针对中国人中较常见的8种与叶酸代谢相关的基因多态类型,通过将含有8对叶酸代谢相关基因多态位点的多态检测探针对固定在膜条上,与待检者相应DNA片段的PCR产物杂交,可同时检测与叶酸代谢相关的基因的4个基因8个多态位点。本发明是基于PCR-膜条杂交技术的基因检测方法,能直接对待检者的基因型进行确诊,具有准确性高、特异性强,能检出基因隐性携带者等优点。因此,应对孕妇或准备怀孕的女性进行基因检测,然后根据情况,指导对叶酸的补充。用本方法进行检测不需要贵重的专用仪器,只需要PCR实验室常规的设备即可,适用于在国内医院大范围推广使用。以上实施例中的核酸杂交膜条上的多态检测探针对同时包含MTHFR基因的c.677位点、c.1298位点,MTRR基因的c.56位点、c.66位点,MTR基因的-186位点、c.2756位点、+905位点和CBS基因的-551位点这4个基因的8个多态位点。在另一些实施例中,用于叶酸代谢基因分型的核酸杂交膜条对还可以包含对应一个或多个叶酸代谢相关基因多态位点的多态检测探针对,一个多态检测探针对包含针对该多态位点的一个突变探针和一个正常探针。以上内容是结合具体的优选实施方式对本发明所作的进一步详细说明,不能认定本发明的具体实施只局限于这些说明。对于本发明所属
技术领域:
的普通技术人员来说,在不脱离本发明构思的前提下,做出若干等同替代或明显变型,而且性能或用途相同,都应当视为属于本发明的保护范围。当前第1页1 2 3