他莫昔芬疗效相关基因基因多态性检测试剂盒及检测方法与流程
技术领域:
:本发明涉及生物技术及医学领域,特别是涉及药物他莫昔芬疗效相关基因他莫昔芬疗效相关基因(cyp2d6、cyp3a5和rras2)基因多态性检测试剂盒及检测方法。
背景技术:
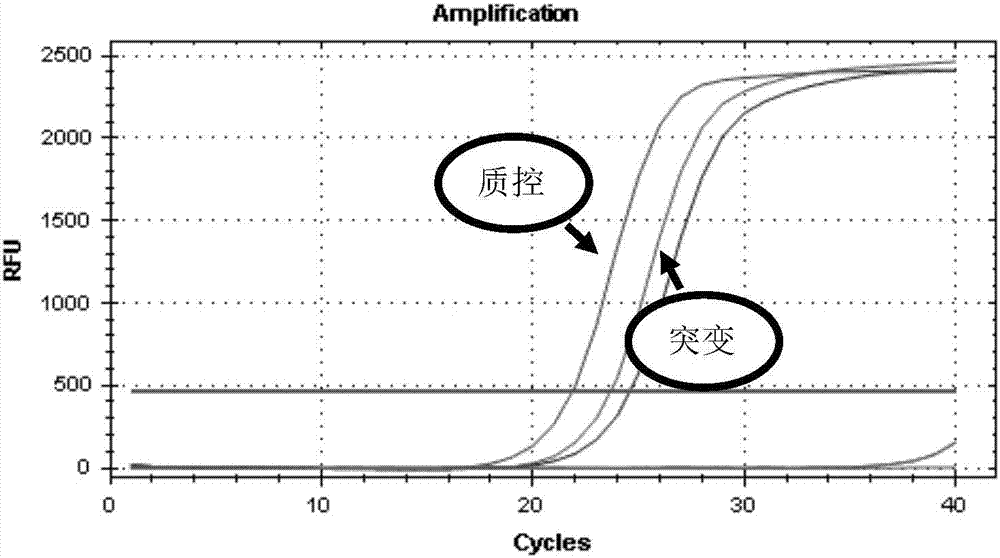
::辅助内分泌治疗是乳腺癌综合治疗中的重要方式,乳腺癌的化疗与体内激素水平密切相关。他莫昔芬(tamoxifen,tam)又名三苯氧胺,为人工合成的非胆固醇类抗雌激素药物,是内分泌辅助治疗乳腺癌的基础药物。tam与雌激素受体结合后,诱导改变受体的三维空间构型,阻止受体与dna上雌激素有关反应成分相结合,使转录等过程不能正常进行,阻止雌激素发挥作用,抑制激素依赖性乳腺肿瘤细胞的生长,达到治疗乳腺癌的作用。同时tam又是一种前体药物,在体内与雌激素受体(er)亲和力低,需经过p450代谢活化生成4-羟基-n-去甲基他莫昔芬(endoxifen)和n-去甲基他莫昔芬发挥作用,其中endoxifen治疗活性最强。tam被广泛的用于治疗乳腺癌患者,但同一药物剂量给不同病人服用,会造成药效和毒性出现个体化差异,少数病人会出现危险的不良反应。这种个体化差别不能完全以肝肾功能、年龄、生活方式或合并用药及病人依从性来解释,此时遗传因素起着重要决定因素。个体化用药,充分考虑每个病人的遗传因素、性别、年龄、体重、生理病理特征以及正在服用的其它药物等综合情况的基础上制定安全、合理、有效、经济的药物治疗方案。cyp2d6是催化tam生成endoxifen的关键酶。cyp2d6基因位于22号常染色体上为隐性遗传,有70多种变异等位基因,从而造成机体对药物疗效的显著个体差异。cyp2d6的常见基因型为cyp2d6*1(也可以认为是野生型cyp2d6wt)。cyp2d6有100多种等位基因变异,这些变异可以产生体内酶活性的差异变化,从而影响他莫昔芬的代谢,使携带不同基因型的乳腺癌病人对他莫昔芬的治疗反应不同。其中,cyp2d6最常见的等位基因是cyp2d6*10(100c>t)。基因突变引起酶活性降低,导致患者对他莫昔芬药物的耐受性增加,无病生存期也相应显著缩短。cyp3a5的基因多态性与tam服用中的众多不良反应有关,存在着较大的个体化差异。tam会引起的不良反应如发热、胸腔积液、中性粒细胞减少等方面,cyp3a5*1/*3等位基因患者比cyp3a5*3/*3基因型患者的不良反应存在显著性差异(p<0.05),提示cyp3a5*1/*3基因的患者会明显增加化疗引起的不良反应。tc21又被成为r-ras2,是ras蛋白家族的成员,主要负责控制细胞迁移,粘附,分化等信号通路,同时,tc21是唯一在人类癌细胞中存在突变的ras类蛋白。tc21的突变广泛存在于乳腺癌等癌细胞中,同时还发现在乳腺癌细胞中,tc21蛋白高过量表达。研究发现,ras基因中的tc21的突变,主要是rras2(582c>t),并有相关研究表明rras2蛋白控制着人体对tam药物的抗性,高表达rras2的乳腺癌患者,在接受治疗后,其复发率较高,并且突变中c/t或t/t基因型的患者,其对tam药物的抗性比其他患者强,其复发率也较高。关于基因突变检测方法有很多,各国学者对此都进行了大量研究。己经报道的方法包括直接测序法、dhplc、pcr-sscp/rflp、scorpionsarms、taqmanpcr、me-pcr等。这些方法各有优缺点,其中在临床和科研中较为常用的方法为直接测序法以及arms(amplificationrefractorymutationsystem,扩增阻滞突变系统)法。直接测序法检测能力有限,其检测灵敏度约20%左右,而且步骤复杂,整个检测过程涉及pcr-电泳-测序-测序结果的解读等一系列的步骤,费吋费力,但是该方法的优点是能够发现一些新的未知突变。arms方法是将分子信标(探针)与特异性的arms引物相结合创造出来的,arms引物3’端设计在突变位点,最后一个碱基与突变碱基配对,釆用无3’→5’外切酶活性的taqdna聚合酶,特异性的识别引物的3’末端,只有引物3’末端完全配对时,才能正常扩增,当引物3’末端发生错配时,不能有效的扩增。当引物与突变模板结合并延伸出相应的产物后,探针两端的荧光基团和淬灭基团分离而产生荧光。目前,市场上相关试剂盒包括qiagen公司和厦门艾德公司,价格昂贵。因此,本研究釆用arms技术与sybr染料相结合的方法,研发出一种拥有完全自主知识产权并且能够快速、敏感而且简便的检测他莫昔芬疗效相关基因(cyp2d6、cyp3a5和rras2)基因多态性的试剂盒。通过自己研发设计arms引物以及将scorpions探针换为sybr染料以使检测成本大大降低,这样更适合中国患者他莫昔芬疗效相关基因(cyp2d6、cyp3a5和rras2)基因多态性的检测。综上所述,该检测试剂盒及检测方法是一种灵敏度高,特异性强,方法简单,结果准确的他莫昔芬疗效相关基因(cyp2d6、cyp3a5和rras2)基因多态性检测方法。技术实现要素::本发明实施例的目的在于提供一种灵敏度高,特异性强,方法简单,结果准确的他莫昔芬疗效相关基因(cyp2d6、cyp3a5和rras2)基因多态性检测试剂盒及检测方法。本发明实施例是这样实现的,一种他莫昔芬疗效相关基因(cyp2d6、cyp3a5和rras2)基因多态性检测试剂盒,该试剂盒包括pcr缓冲液,特异性突变检测引物,质控引物。本发明还提供一种他莫昔芬疗效相关基因(cyp2d6、cyp3a5和rras2)基因多态性检测方法,包括以下步骤:(1)提供如权利要求1中所述的引物;(2)待测样品的处理和模板的提取;(3)配制荧光定量pcr反应体系;(4)利用arms引物区分野生型和突变型基因序列,通过sybrgreen染料和扩增产物的杂交,检测反应体系的sybr荧光强度来判定检测结果。sybr为检测信号,以sybr信号达到设定的阈值所需的的循环次数ct值作为判断标准,ct值小于32为阳性,ct值大于35为阴性,ct值介于32到35之间为弱阳性。本发明他莫昔芬疗效相关基因(cyp2d6、cyp3a5和rras2)基因多态性检测试剂盒采用sybr染料法,建立了针对人类cyp2d6、cyp3a5和rras2基因多态性(如表1)的多重实时pcr检测方法。本发明经过大量试验,研究和分析成功筛选出能够用于快速、灵敏、有效的检测他莫昔芬疗效相关基因(cyp2d6、cyp3a5和rras2)基因多态性的引物组合与探针组合,并利用这些引物和探针开发出具有这样的优点的用于检测他莫昔芬疗效相关基因(cyp2d6、cyp3a5和rras2)基因多态性的方法和试剂盒。本发明的检测试剂盒及检测方法具有灵敏度高,特异性强,方法简单,结果准确等特点,因此本发明具有实质性的技术效果,便与推广。表1:cyp2d6、cyp3a5和rras2基因多态性形式所述的特异性引物见下表2/3/4。表2:cyp2d6基因多态性的检测引物表3:cyp3a5基因多态性的检测引物表4:rras2基因多态性的检测引物本发明涉及的检测人类cyp2d6、cyp3a5和rras2基因多态性的荧光定量pcr方法不包括对待测样本的处理和模板提取的步骤,但对于来自甲醛固定石蜡包埋的样品和来自血浆的样品所获得的片段dna依然具有与新鲜组织样本dna相同的扩增和检测能力。本发明的检测试剂盒可在50ng野生型基因组dna背景下准确检出1%的突变dna,且针对性设计不同突变位点的特异性引物,使用荧光定量pcr进行检测,检测过程均为闭管反应,大大降低污染。附图说明:图1为本发明基因多态性检测试剂盒检测cyp2d6*10样品的扩增曲线图。图2为本发明基因多态性检测试剂盒检测cyp3a5*3样品的扩增曲线图。图3为本发明基因多态性检测试剂盒检测rras2(c582t)样品的扩增曲线图。具体实施方式:以下通过特定的具体实例说明本发明的实施方式,本领域技术人员可由本说明书所揭露的内容轻易地了解本发明的其他优点与功效。本发明还可以通过另外不同的具体实施方式加以实施或应用,本说明书中的各项细节也可以基于不同观点与应用,在没有背离本发明的精神下进行各种修饰或改变。在进一步描述本发明具体实施方式之前,应理解,本发明的保护范围不局限于下述特定的具体实施方案;还应当理解,本发明实施例中使用的术语是为了描述特定的具体实施方案,而不是为了限制本发明的保护范围;在本发明说明书和权利要求书中,除非文中另外明确指出,单数形式“一个”、“一”和“这个”包括复数形式。当实施例给出数值范围时,应理解,除非本发明另有说明,每个数值范围的两个端点以及两个端点之间任何一个数值均可选用。除非另外定义,本发明中使用的所有技术和科学术语与本
技术领域:
技术人员通常理解的意义相同。除实施例中使用的具体方法、设备、材料外,根据本
技术领域:
的技术人员对现有技术的掌握及本发明的记载,还可以使用与本发明实施例中所述的方法、设备、材料相似或等同的现有技术的任何方法、设备和材料来实现本发明。实施例11.样本处理和核酸提取利用商品化的dna提取试剂盒处理样本,具体操作参见试剂盒说明书,所提dna需用紫外分光光度计测定浓度和纯度,其dnaod260/od280的值应在1.8~2.0,浓度应在5~50ng/μl之间,样本dna质量不合格者不得用于检测,建议低于5ng/μl者重新取切片进行核酸提取,高于50ng/μl者予以适当稀释至规定的浓度范围,提取完的dna建议立即进行检测,否则请于-20℃以下保存,保存时间不要超过6个月。试剂盒质控品使用前室温融化,涡旋振荡10秒,2000rpm离心15秒待用。2.试剂配置2.1配置说明:检测反应设置阴性质控品和阳性质控品。2.2配置过程提前30分钟将试剂取出,室温融化,涡旋振荡10秒,2000rpm离心15秒待用。确定反应数n,n=待检样本数(n)+质控品数(2)+1。计算加到反应混合物中的各个试剂的量,计算如下表5:表5:pcr反应体系配置表。试剂pcr反应液p引物探针混合液纯化水反应液a(μl)12.5*n6.5*n4.0*n外控反应液b(μl)12.5*n6.5*n4.0*n取2个灭菌离心管配置上述2个反应体系,试剂全部加入后涡旋振荡10秒,2000rpm离心15秒。然后将上述混合液23μl/管分装至pcr反应管中(无菌和rnase-free)。3.加样表6:样品及质控品上样表。注:std代表阳性质控品;ntc代表阴性质控品。根据表5提示的上样比例,将已处理样本、阳性质控品p1和阴性质控品p2加入反应管中,盖紧管盖(避免气泡产生),2000rpm离心15秒将管壁上的液体全部甩至管底,然后立即进行pcr扩增反应。4.pcr扩增程序设置表7:pcr反应程序的设定。5.检验结果的解读利用arms引物区分野生型和突变型基因序列,通过sybrgreen染料和扩增产物的杂交,检测反应体系的sybr荧光强度来判定检测结果。sybr为检测信号,以sybr信号达到设定的阈值所需的的循环次数ct值作为判断标准,ct值小于32为阳性,ct值大于35为阴性,ct值介于32到35之间为弱阳性。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1