一种针对细胞的激光导向微流控芯片的制作方法
本实用新型涉及生物医学技术,具体是利用激光的光阱力侧向推动细胞来改变细胞的运动轨迹的微流控芯片。
背景技术:
早在20世纪初期,生物学、医学领域的科研人员已经开始进行细胞培养等工作。为了能更直观地观察细胞在生物体内的活动情况,人们开始在更开放的环境下模拟体内细胞所需的生活环境。微流控芯片的出现与发展促进了体外仿真的研究进程,由于微流控芯片具有高精度、高通量以及可塑造性强的特点,可以根据情况用不同工艺和材料制造出应用于不同领域的微流控芯片。
近年来,由于人们对循环肿瘤细胞的关注,对循环肿瘤细胞的分选的需求也在日益增加,在科研与临床应用中需要高通量和高分选率。虽然现有的几种方法分离效率高,但从制作工艺上来看比较复杂,或是需要对样品进行预处理,从而或多或少污染了样品。
近年来国内通过光压、光学镊子等手段来微观操作细胞成为研究热点。李银妹等人和张文静等人实现了用光学镊子捕获、操纵和分离细胞,并研究了不同液体中黏滞系数对其的影响;赵恩铭和刘志海已经实现了对聚苯乙烯颗粒和酵母细胞的捕获和弹射等作用,并探究了光阱力对不同尺寸微粒的力学作用。但利用精密微移平台通过光镊在垂直于芯片方向移动细胞效率不高,不适用于高通量的细胞筛选;用大功率激光捕获与弹射需要大功率激光器,还可能影响细胞活性。还未实现在微流控芯片中利用微小的侧向光阱力来改变细胞轨迹。
技术实现要素:
针对现有技术不足,本实用新型拟解决的技术问题是,提供一种可以使目标细胞运动轨迹发生偏转的微流控芯片,引入嵌入光纤可以降低对激光功率的要求,而且实际操作中简化操作步骤(不用现场建立光路),相对于之前发表在《微纳电子技术》上论文中所述芯片结构,此次使用兼容性更好的多模光纤,并且根据仿真与实际情况对通道进行了结构优化,加入了光纤嵌入位置,便于操作。该芯片具有通量高,无标记,适于实际应用等特点。
本实用新型的技术方案是,
一种针对细胞的激光导向微流控芯片,该芯片包括十字通道、上部废液通道、1号细胞收集通道、2号细胞收集通道、下部废液通道、上废液池、1号细胞收集器、2号细胞收集器、下废液池和光纤;
所述的十字通道的上通道和下通道连接,作为缓冲液通道;十字通道的前通道为细胞液通道,十字通道的后通道作为主通道,主通道的末端分离形成四个射线状连接的分支通道,其中,四个分支通道由上到下依次为上部废液通道、1号细胞收集通道、2号细胞收集通道、下部废液通道,每个通道之间夹角为30°,其中,2号细胞收集通道处于主通道的水平延长段;光纤垂直嵌入主通道末端之前的80um处下部;
上部废液通道的末端为上废液池、1号细胞收集通道的末端为1号细胞收集器、2号细胞收集通道的末端为2号细胞收集器、下部废液通道的末端为下废液池;
所述的十字通道、上部废液通道、1号细胞收集通道、2号细胞收集通道、下部废液通道材质均为聚二甲基硅氧烷。
所述的十字通道、上部废液通道、1号细胞收集通道、2号细胞收集通道、下部废液通道的内部通道宽度相等,通道厚度相等。
所述的十字通道、上部废液通道、1号细胞收集通道、2号细胞收集通道、下部废液通道的内部通道宽度均为100μm,通道厚度均为100μm。
与现有技术相比,本实用新型的微流控芯片结构设计巧妙,功能明确,便于加工,工作效率或筛选效率可达几个-几十个/秒,大幅提高,而且不需要采用任何试剂标注目标细胞,真正实现了无标记、高通量的细胞筛选现代医学要求。
附图说明
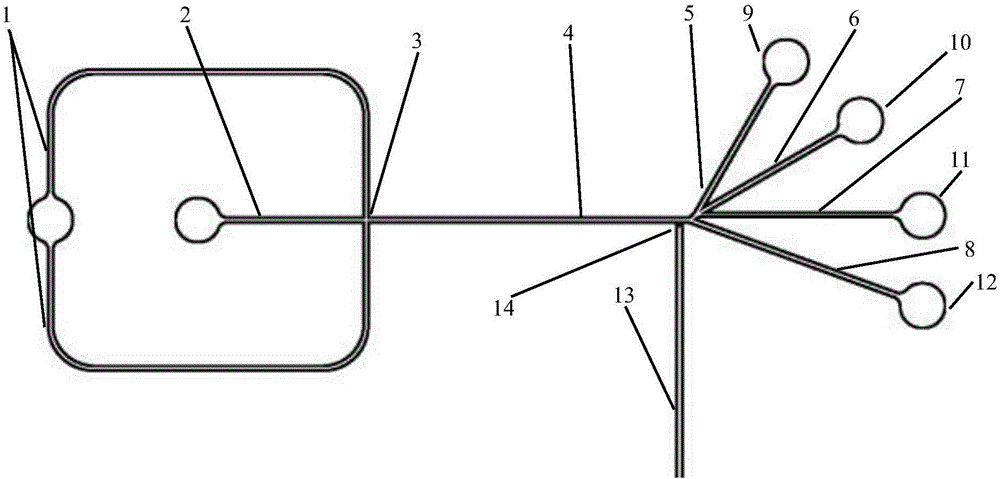
图1为本实用新型芯片结构示意图。
具体实施方式
下面结合实施例及其附图进一步描述本实用新型。
本实验所需微流控芯片结构设计为图1所示,其中包括了最常用的十字型通道作为鞘流结构,并且创新了独特的多分支通道结构,便于细胞的筛选和分类。该芯片包括:缓冲液通道(1)、细胞液通道(2)、十字通道(3)、主通道(4)、上部废液通道(5)、1号细胞收集通道(6)、2号细胞收集通道(7)、下部废液通道(8)、上废液池(9)、1号细胞收集器(10)、2号细胞收集器(11)、下废液池(12)和光纤(14);其十字通道(3)(包括主通道(4))上部废液通道(5)、1号细胞收集通道(6)、2号细胞收集通道(7)、下部废液通道(8)的设计宽度相等,制作时通道厚度也相等;
所述的十字通道(3)的上通道和下通道连接,作为缓冲液通道;十字通道(3)的前通道(2)为细胞液通道,十字通道的后通道(4)作为主通道,主通道的末端分离形成四个射线状连接的分支通道,共属同一节点,其中,四个分支通道由上到下依次为上部废液通道(5)、1号细胞收集通道(6)、2号细胞收集通道(7)、下部废液通道(8),每个通道之间夹角为30°,其中,2号细胞收集通道(7)处于主通道(4)的水平延长段;光纤垂直嵌入主通道末端之前的80um处;
上部废液通道(5)的末端为上废液池(9)、1号细胞收集通道(6)的末端为1号细胞收集器(10)、2号细胞收集通道(7)的末端为2号细胞收集器(11)、下部废液通道(8)的末端为下废液池(12)。
实施例1
本实用新型中,所述的十字通道(3)的上通道和下通道连接(呈方形),作为缓冲液通道;十字通道(3)的前通道(2)为细胞液通道,十字通道的后通道(4)作为主通道(主通道长24mm),主通道的末端分离形成四个射线状连接的分支通道,即1号细胞收集通道(6)、2号细胞收集通道(7)、上部废液通道(5)和下部废液通道(8)左端共同接入主通道(4)的尾端,其中2号细胞收集通道(7)处于主通道(4)的水平延长段,并且1号细胞收集通道(6)、2号细胞收集通道(7)、上部废液通道(5)和下部废液通道(8)的直径与主通道(4)直径相等,均为100μm,通道厚度也均为100μm,每个通道之间夹角为30°,以上四个通路的尾端分别对应1号细胞收集器(10)、2号细胞收集器(11)、上废液池(9)和下废液池(12)。为了能在微流控芯片中嵌入光纤,本实验采用聚二甲基硅氧烷(PDMS)作为芯片的主要制作材料,即十字通道(3)、上部废液通道(5)、1号细胞收集通道(6)、2号细胞收集通道(7)、下部废液通道(8)材质均为聚二甲基硅氧烷。在模板上对应位置(13)预留光纤(14)大小(光纤直径125um)的通道(光纤垂直嵌入主通道末端之前的80um处),使其端面垂直对准分岔路前端通道处。然后插入光纤后用PDMS注入光纤与通道之间的缝隙中,并用硅胶加固光纤与微流控芯片接口处使光纤与芯片形成整体。本实用新型芯片的工作原理及过程是:十字通道(3)更容易使从缓冲液通道(1)和细胞液通道(2)注入的缓冲液和被缓冲液包裹着的细胞液汇聚形成鞘流,并且通过控制进样器的流速来控制缓冲液通道(1)的流速和压力,保证细胞可以在主通道(4)里形成单细胞流,并且沿着流线的方向进入光纤嵌入位置(13)受到通过光纤的激光的照射,由于不同细胞不同的细胞膜和细胞质,所以对于不同波长、功率的激光照射下所受到的力也不同,从而实现对不同种类、大小的细胞进行筛选,通过调节功率使得轴向光阱力可以产生0-40μm的横向偏移量,足以将细胞分离到不同的通道中。经过细胞筛选的细胞进入最终的细胞1号收集通道(6)和2号细胞收集通道(7),完成具有高通量、无标记的细胞筛选过程。
本实用新型未述及之处适用于现有技术。
- 还没有人留言评论。精彩留言会获得点赞!