本发明属于配位化合物制备技术领域,具体涉及一种具有抗肿瘤活性的铁基配位化合物及其制备方法和应用。
背景技术:
配位化学是无机化学的一个重要分支学科,由瑞士化学家werner在1893年提出和建立。自werner于1913年获得诺贝尔化学奖以来,配位化学理论历经百余年的发展逐渐成熟,尤其是晶体场理论、配位场理论、分子轨道理论和价键理论的提出,对配位作用给予了合理的解释,使得配位化学一直是无机化学研究中的一个前沿领域,为配合物在新颖功能性材料上的发展提供了良好的理论基础。因其组成的多样性与结构的可调控性,使得配位化合物的合成、性质、结构和成键等研究内容十分丰富。有机-金属配合物不但结合了无机金属离子和有机配体两者的独有特性,而且表现出比纯无机材料和纯有机超分子材料更加优异多样的性能。近二三十年来,配合物在配位聚合物、金属有机骨架材料(mofs)、金属有机笼状物、配位超分子化学等领域得到快速发展,尤其在催化、吸附、识别、气敏、磁性、生物活性等方面的潜在应用价值引起了研究者的极大重视。
众所周知,癌症是目前危害人类健康的最严重的疾病之一,其致死率仅次于心血管病。据国际癌症研究署报道,到2020年全球癌症发病率将上升50%,发病人数将达到每年1500万,癌症的防治与研究已成为全世界医学家倍受关注的研究课题。无机药物化学是一类以研究无机离子药物在生物体内的分布、吸收、转化、排代及治病机理的一个新兴生物无机化学分支。1969年顺铂抗癌作用的发现毫无疑问推动了这一学科在金属配合物抗肿瘤活性研究的发展。近几年来,诸如cu、ru、sn等一些非铂类的过渡金属配合物也相继被发现具有一定的抗肿瘤活性。
基于目前抗肿瘤药物的合成、生产以及肿瘤化疗药物研究的现状来看,抗肿瘤新药的合成设计主要有以下三种途径:一是集中在各类已知靶标的有效药物中改造、合成,如拓扑异构酶抑制剂伊立替康(cpt-11)、信号转导抑制剂甲氨蝶呤的合成;二是对天然产物中的活性成份加以改造,如增加活性成份的水溶性,喜树碱的水溶性类似物托泊替康的合成;三是利用计算机辅助药物设计模拟出小分子先导化合物,然后与靶标蛋白组数据库进行匹配获得吻合度高的先导化合物。以顺铂为例的化疗药物存在着严重的不良反应,如肾毒性、神经毒性、骨髓抑制等,然而这类药物的使用仍然出现在50%以上的癌症患者的治疗方案中。因此,寻找高效、低毒、特异的抗肿瘤药物俨然成为癌症化学治疗研究工作者的当务之急。
技术实现要素:
本发明的目的在于提供一种具有抗肿瘤活性的铁基配位化合物及其制备方法与应用,其对k562、oe-19细胞均有明显抑制作用,有望用于制备相应的抗癌药物。
为实现上述目的,本发明采用如下技术方案:
一种具有抗肿瘤活性的铁基配位化合物,其化学式为[fe(c7h3no4)(c12h8n2)•h2o]•2h2o,分子量为455.21,为零维结构,单斜晶系,空间群为p2(1)/c,单胞参数为a=7.8226(16),b=27.730(6),c=9.2886(19),α=γ=90°,β=106.84(3)°,v=1928.5(7),z=4。
所述铁基配位化合物采用常温溶液挥发法制备而成,其具体步骤为:将2.05mmol2,6-吡啶二羧酸和1.2mmol1,10-邻菲啰啉放入烧杯中,加入15ml去离子水,搅拌混合15min后,加入1.2mmolfecl3•6h2o固体,室温下继续搅拌3h,得到红棕色澄清溶液,将溶液过滤,滤液于室温下静置挥发2周后析出红棕色块状晶体,再经过滤、干燥即得。
本发明的显著优点在于:
1)本发明合成方法简单、经济,为配位化合物的合成提供了有益参考,具有一定的推广意义。
2)本发明制备的铁基配位化合物对慢性粒细胞白血病细胞株k562和食管癌细胞株oe-19具有较好的体外抑制活性,有望制备成相应的抗癌药物。
附图说明
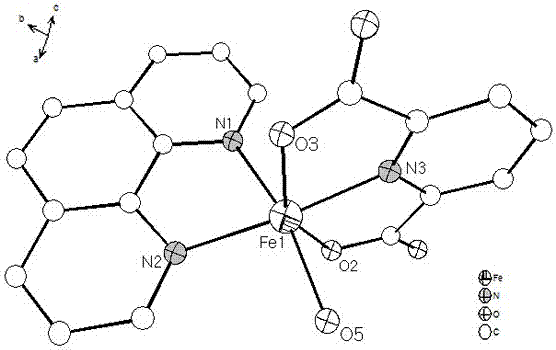
图1为本发明铁基配位化合物的分子结构图。
图2为本发明铁基配位化合物的配位环境图(图中的h原子及游离h2o分子均省略)。
图3为本发明铁基配位化合物通过1,10-邻菲啰啉配体上芳环的分子间π-π堆积形成的3-d结构图。
图4为本发明铁基配位化合物的x-射线粉末衍射谱图。
图5为本发明铁基配位化合物的红外光谱图。
图6为本发明铁基配位化合物对k562细胞和oe-19细胞的抑制情况图。
具体实施方式
为了使本发明所述的内容更加便于理解,下面结合具体实施方式对本发明所述的技术方案做进一步的说明,但是本发明不仅限于此。
将2.05mmol2,6-吡啶二羧酸和1.2mmol1,10-邻菲啰啉放入烧杯中,加入15ml去离子水,搅拌混合15min后,加入1.2mmolfecl3•6h2o固体,室温下继续搅拌3h,得到红棕色澄清溶液,将溶液过滤,滤液于室温下静置挥发2周后析出红棕色块状晶体,再经过滤、干燥即得铁基配位化合物[fe(c7h3no4)(c12h8n2)•h2o]•2h2o单晶,其产率为65%(以fe计算)。
1.[fe(c7h3no4)(c12h8n2)•h2o]•2h2o单晶的表征
a.采用日本理学rigakusaturn724ccdx-射线单晶衍射仪进行配位化合物单晶的x-射线单晶衍射实验。采用石墨单色化的mo靶kα射线(λ=0.71073)为辐射源。以ω扫描方式在一定角度范围内收集衍射数据,选取i>2σ(i)的独立衍射点用于单晶结构分析。
b.配位化合物的x-射线衍射收集数据采用crystalclear程序包还原,使用multi-scan或numberic方式进行吸收校正。结构解析使用shelx-97程序包,用直接法算出初结构,再根据傅里叶合成原理逐步推断出完整确定结构。非氢原子的坐标和各向异性温度因子采用全矩阵最小二乘法进行结构修正。化合物的氢原子坐标均采用理论加氢。所有或部分氢原子的坐标和各向同性温度因子参加结构计算,但不参与结构精修。
结构分析采用最小二乘函数、偏离因子、权重因子和权重偏离因子等数学表达式如下所示:
最小二乘函数:,
温度因子:,
偏离因子:,
权重因子:,
权重偏离因子:。
配位化合物的晶体学数据和衍射强度的收集条件见表1。
表1[fe(c7h3no4)(c12h8n2)•h2o]•2h2o单晶的晶体学数据表
经单晶结构分析可知,所得铁基配位化合物[fe(c7h3no4)(c12h8n2)•h2o]•2h2o是一个零维结构的化合物,属于单斜晶系,p2(1)/c空间群,z=4。
图1为该铁基配位化合物的分子结构图。由图1可见,该配位化合物的独立结构单元包括一个fe(ⅲ)离子,一个脱去两个质子的2,6-吡啶二羧酸,一个1,10-邻菲啰啉分子和一个配位水分子。所有原子均处于一般等效点上,其配位环境图如图2所示。从图2可以看出,该配位化合物中fe(ⅲ)为六配位,fe1分别与2,6-吡啶-二羧酸上的两个羧酸根上的o原子以及1,10-邻菲啰啉上的两个n原子和配位水分子配位,以fe(ⅲ)为中心形成一个四角双锥的配位构型,其中fe1–n1、fe1–n2、fe1–n3、fe1–o2、fe1–o3、fe1–o5键长为2.130(2)、2.100(2)、2.045(2)、2.159(2)、2.143(2)、2.099(2)。
图3为该铁基配位化合物通过1,10-邻菲啰啉配体上芳环的分子间π-π堆积形成的3-d结构图。由图3可知,每个邻菲啰啉配体上的芳环所成的几何平面基本相互平行,且相邻两个1,10-邻菲啰啉配体平面中心的距离在1.853左右。另外,层间的水分子也参与扩展通过弱作用力以稳定三维结构。
2.[fe(c7h3no4)(c12h8n2)•h2o]•2h2o的谱学表征
a.x-射线粉末衍射
采用日本理学x-rayminiflex2型号的粉末衍射仪进行配位化合物的x-射线粉末实验。在室温下,对样品进行测定,得到x-射线衍射图谱,测试条件为:cu靶kα辐射(λ=1.5403),20ma,40kv,扫描时间为0.02°/0.1s,扫描范围为:2θ=5~55°。
图4为该铁基配位化合物的x-射线粉末衍射谱图。如图4所示,与mercury模拟的粉末衍射数据图比较,实验图谱的主要峰位与模拟谱图的峰位基本一致,表明所测化合物均为纯相。
b.红外光谱(ir)分析
配位化合物的ir光谱均采用kbr压片,在室温下测定,所用仪器为perkin-elmerspectrum-2000ftir傅立叶变换红外光谱仪。扫描次数32次,扫描范围400~4000cm-1。
图5为该铁基配位化合物的红外光谱图,其中主要红外振动吸收峰的归属如表2所示:
表2[fe(c7h3no4)(c12h8n2)•h2o]•2h2o的主要红外振动吸收峰及其归属
3.[fe(c7h3no4)(c12h8n2)•h2o]•2h2o的体外抗肿瘤活性研究
将慢性粒细胞白血病细胞株k562和食管癌细胞株oe-19加入0.25%的胰蛋白中配制成细胞悬浮液,之后将细胞悬浮液(每毫升105~106个细胞)加入到96孔板中(每孔100μl),置于37℃环境中,在含有5%co2的条件下孵育24h。之后添加样品溶液(所述样品溶液是将[fe(c7h3no4)(c12h8n2)•h2o]•2h2o溶解在dmso中,经高压灭菌,并用rpmi1640培养液稀释至浓度依次为100、50、25、12.5、6.25、3.13、1.56、0.78μg·ml-1),72h后每孔加入20μl溶解在0.01mol·l-1pbs磷酸缓冲液中的mtt溶液(5mg·ml-1),继续培养4h。去上清液,加入150μldmso,置于摇床中,在室温下低速振荡10min,用比色分析法检测细胞的存活率,结果见图6及表3。
表3[fe(c7h3no4)(c12h8n2)•h2o]•2h2o的体外抗肿瘤活性
结果表明,铁基配位化合物具有较好体外抗肿瘤活性,而且对k562的抑制作用强于oe-19。
以上所述仅为本发明的较佳实施例,凡依本发明申请专利范围所做的均等变化与修饰,皆应属本发明的涵盖范围。