一种烟酸药物共晶及其制备方法与流程
本发明涉及药物共晶技术领域,具体地说是一种烟酸与2,6-二羟基苯甲酸或烟酸与4-氨基吡啶的药物共晶及其制备方法。
背景技术:
晶体工程是根据超分子化学的原理、方法以及控制分子间作用于晶体,用于设计和制造出奇特新颖、花样繁多、具有特定物理性质和化学性质的晶体。这些晶体通常是多维的、在空间上无限伸展的超分子聚集体,分子构筑单元在固态的排列状态决定了晶体材料的物理和化学性质。由此,通过选择合适的分子构筑基元,掌握这些分子间可采取的相互作用(例如配位键、氢键)的信息,使分子组分间的功能得到多方面配合,优化分子间不同强度的、定向的各种相互作用,就有可能得到具有特定构型和物理化学性质的材料,从而实现目标可控合成。
目前,药物共晶在修饰药物活性成分(activephaimaceuticalingredient,api)理化性质方面的应用近年来备受关注。药物活性分子(api)通常因含有各种官能团而具有不同的生物活性,这些官能团能够利用氢键或者其他非共价键作用而与其他有机分子通过分子间的识别作用生成超分子化合物,即药物共晶,而被引入的有机分子,被称为共晶试剂。共晶试剂的引入,可以改善药物本身的结晶性能、物化性质及药效,是药物固体试剂的一个新选择。常温下,药物活性成分(api)以多种固体形态存在,如多晶、溶剂化物、水合物、共晶、无定形以及盐等。一个药物的疗效很大程度上取决于api自身的理化性质及其选择的剂型,而api不同的固体形态对药物的溶解度、稳定性、溶出速率和生物利用度等均有影响。api固体形态的研究已成为新药开发中的一个重要方面,可为最佳药物固体形态的确定提供选择依据。
烟酸也称3-吡啶甲酸,又名尼可丁酸,是一种维生素,在众多维生素中结构最为简单,理化性质最稳定,对于人体和动物来说,均是不可或缺的营养成分,在食品,饲料,医疗等领域都被广泛应用。烟酸作为一种水溶性b族维生素,主要用于治疗血脂异常,这种血脂异常主要是由于低密度脂蛋白胆固醇增多和高密度脂蛋白胆固醇减少而导致的。同时,对于烟酸的研究发现其是冠心病治疗史上第一个显示可以减少该病死亡率的药物,2,6-二羟基苯甲酸和4-氨基吡啶是两个医药中的重要中间体。
现有技术的药物共晶,操作影响因素多,对于成本和技术的要求都较高,而且产物易受溶剂影响,得到高纯度的晶体不太容易。
技术实现要素:
本发明的目的是针对现有技术的不足而提供的一种烟酸药物共晶及其制备方法,采用甲醇与丙酮混合溶剂的室温挥发,将烟酸与2,6-二羟基苯甲酸或4-氨基吡啶通过氢键结合,得到空间群为单斜晶系cc或p21空间群的烟酸与2,6-二羟基苯甲酸药物共晶或烟酸与4-氨基吡啶药物共晶,合成选用的溶剂沸点较低,制备方法简便,不但保留了烟酸的药物特质外,而且溶解性有明显提高,该药物共晶中各组分可以是中性分子,因而药物共晶可涵盖所有的api,包括酸、碱和非离子化分子,并可用来配合api形成共晶的分子很多,这些物质可能包括食品添加剂、防腐剂、药用辅料、维生素、矿物质、氨基酸以及其他活性分子,甚至其他的api,因此,对于给定的药物,可以生成数以百计的药物共晶,延长原有药物的市场周期,具有广阔的应用前景。
实现本发明目的的具体技术方案是:一种烟酸药物共晶,其特点是以烟酸作为药物活性成分,2,6-二羟基苯甲酸或4-氨基吡啶为反应物,将药物活性成分与反应物研磨后在甲醇和丙酮的混合溶剂中,采用溶剂室温挥发,使烟酸与2,6-二羟基苯甲酸或4-氨基吡啶通过氢键结合,构成烟酸与2,6-二羟基苯甲酸或4-氨基吡啶的药物共晶基元,所述烟酸与2,6-二羟基苯甲酸的药物共晶为单斜晶系cc空间群,其轴长为:a=9.8810~10.6810;b=12.2014~12.6014;c=9.3629~9.8629;α=90°;β=94.6650~95.0650°;γ=90°;所述烟酸与4-氨基吡啶的药物共晶为单斜晶系p21空间群,其轴长为:a=11.7615~12.1615;b=8.1246~8.5246;c=11.1883~11.5883;α=90°;β=111.5310~111.7310°;γ=90°。
所述烟酸与2,6-二羟基苯甲酸通过氢键结合是以烟酸分子中的o(o2)原子和2,6-二羟基苯甲酸分子中的o(o6)原子作为氢键的给体,烟酸分子中的n(n1)原子和2,6-二羟基苯甲酸分子中的o(o4)原子作为氢键的受体,所形成的两个氢键为:[o2-h2b…o4(x+1/y,y-1/2,z+1),
一种烟酸药物共晶的制备方法,其特点是将烟酸与2,6-二羟基苯甲酸或4-氨基吡啶混合,研磨均匀后加入甲醇研磨至溶剂挥干,然后在甲醇/丙酮混合溶剂中超声至溶解完全,静置5~10天,析出的长条状或柱状白色透明晶体,为烟酸与2,6-二羟基苯甲酸或烟酸与4-氨基吡啶共晶,所述烟酸与2,6-二羟基苯甲酸或4-氨基吡啶、甲醇和甲醇/丙酮混合溶剂的重量体积比为:1mg:1~8mg:5~30μl:2~5ml,所述甲醇/丙酮混合溶剂中甲醇与丙酮的体积比为:0.5~2:1。
本发明与现有技术相比具有制备方法简单可控,合成周期短,重复性好,合成的烟酸药物共晶,保留了烟酸的药物特质外,溶解性有明显提高,延长原有药物的市场周期,具有广阔的应用前景。
附图说明
图1为烟酸与2,6-二羟基苯甲酸药物共晶结构单元示意图;
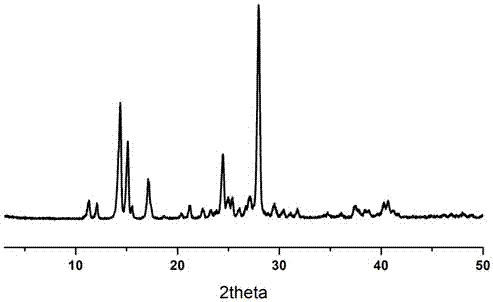
图2为烟酸与2,6-二羟基苯甲酸药物共晶的xrd图谱;
图3为烟酸与2,6-二羟基苯甲酸药物共晶热重图谱;
图4为烟酸与2,6-二羟基苯甲酸药物共晶在水溶液中的溶解曲线图;
图5为烟酸与2,6-二羟基苯甲酸药物共晶在乙醇溶液中的溶解曲线图;
图6为烟酸与4-氨基吡啶药物共晶结构单元示意图:
图7为烟酸与4-氨基吡啶药物共晶的xrd图谱;
图8为烟酸与4-氨基吡啶药物共晶热重图谱;
图9为烟酸与4-氨基吡啶药物共晶在水溶液中的溶解曲线图;
图10为烟酸与4-氨基吡啶药物共晶在乙醇溶液中的溶解曲线图。
具体实施方式
本发明以烟酸(c6h5o2n)为药物活性分子,2,6-二羟基苯甲酸(c7h6o4)为反应物,其烟酸与2,6-二羟基苯甲酸药物共晶的合成按如下结构反应式进行:
本发明以烟酸(c6h5o2n)为药物活性分子,4-氨基吡啶(c5h6n2)为反应物,其烟酸与4-氨基吡啶药物共晶的合成按如下结构反应式进行:
以下通过具体实施例对本发明作进一步的详细说明。
实施例1
称取30mg烟酸与37.6mg2,6-二羟基苯甲酸置于玛瑙研钵中,研磨均匀后加入20μl甲醇,迅速研磨至溶剂挥干,然后将混合物移至玻璃试管中,加入2ml丙酮与2ml甲醇的混合溶剂,超声至溶解完全,封住试管口并扎小孔静置挥发7天,试管底部开始析出白色透明长条状晶体,即为烟酸与2,6-二羟基苯甲酸药物共晶。
实施例2
称取30mg烟酸与26.4mg4-氨基吡啶置于玛瑙研钵中,研磨均匀后加入20μl甲醇,迅速研磨至溶剂挥干,然后将混合物移至玻璃试管中,加入2ml丙酮与2ml甲醇的混合溶剂,超声至溶解完全,封住试管口并扎小孔静置挥发9天,试管底部开始析出白色柱状透明晶体,即为烟酸与4-氨基吡啶药物共晶。
上述各实施例制备的药物共晶采用下述仪器对其进行共晶结构及其性能的检测:(1)、共晶结构由x-射线单晶衍射仪测定,全称为brukersmartapexⅱdiffractometer,mo-kα
(2)、pxrd衍射是由粉末衍射仪测定,型号为rigaku(d/max-ultimaⅳ)diffractometer,cu-kα
(3)、热重曲线是由tg-dsc分析仪测试的,型号是netzschsta449f3,氮气气氛下,升温速率10℃/min。
参阅附图1,实施例1制备的烟酸与2,6-二羟基苯甲酸药物共晶经检测,其共晶分子中的烟酸分子与2,6-二羟基苯甲酸分子通过氢键结合,构成烟酸药物共晶的基本单元。其中,烟酸分子中的o(o2)原子和2,6-二羟基苯甲酸分子中的o(o6)原子作为氢键的给体,烟酸分子中的n(n1)原子和2,6-二羟基苯甲酸分子中的o(o4)原子作为氢键的受体,所形成两个氢键的信息为:[o2-h2b…o4(x+1/y,y-1/2,z+1),
参阅附图2,实施例1制备的烟酸与2,6-二羟基苯甲酸药物共晶的x-射线衍射峰中可以看出,其特征峰值出现在:11.36。、12.12。、13.98~14.02°、14.24°、14.32°、14.4°、15.08°、17.12°、24.42°、24.56°和28.02°。
参阅附图3,实施例1制备的烟酸与2,6-二羟基苯甲酸药物共晶在氮气氛围测试条件下,其热重曲线在164~250℃开始分解,共失重59%。
对实施例1制备的烟酸与2,6-二羟基苯甲酸药物共晶进行如下溶解度测试:
(1)、称取67.6mg烟酸–2,6二羟基苯甲酸药物共晶(由单晶结构得到共晶中烟酸和2,6-二羟基苯甲酸的计量比为1:1,因此67.6mg共晶中烟酸的质量为30mg,已保证烟酸的量与空白组相同)作为实验组分别溶解于4ml水和4ml乙醇中,配得共晶溶液。
(2)、称取烟酸30mg分别溶解于4ml水和4ml乙醇中,烟酸溶液作为空白溶剂作对比。
(3)、用紫外分光光度计分别测定共晶水溶液,共晶乙醇溶液,烟酸水溶液,烟酸乙醇溶液的吸收情况,通过和空白溶剂的最大吸收峰对比,观察药物形成药物共晶后其溶解度的变化情况。
参阅附图4,图中a曲线为药物共晶的紫外吸收曲线,b曲线为空白溶液的紫外吸收曲线,从实验结果可以看出,药物共晶在水溶液中的溶解度相较于空白溶液明显红移。
参阅附图5,图中a曲线为药物共晶的紫外吸收曲线,b曲线为空白溶液的紫外吸收曲线,从实验结果可以看出,药物共晶在乙醇溶液中的溶解度相较于空白溶液明显红移,溶解度出现红移主要的原因分析可能是烟酸中的n原子上的孤对电子参与形成氢键,因此溶解度出现明显红移。
参阅附图6,实施例2制备的烟酸与4-氨基吡啶药物共晶经检测,其共晶分子中的烟酸分子与4-氨基吡啶分子通过氢键结合,构成烟酸药物共晶的基本单元。其中烟酸中的o(o1)原子和4-氨基吡啶中的n(n3)原子作为氢键给体,4-氨基吡啶中的n(n2)原子和烟酸中的o(o2)、n(n1)原子作为氢键受体,所形成三个氢键的信息为:[n3-h3b…n1,
参阅附图7,实施例2制备的烟酸与4-氨基吡啶药物共晶的x-射线衍射峰中可以看出,其特征峰值出现在:8.08°,15.68°,15.78°,18.42°,18.52°,20.26°,25.2°,25.34°,25.42°,25.6°,27.36°。
参阅附图8,实施例2制备的烟酸与4-氨基吡啶药物共晶在氮气氛围测试条件下,其热重曲线在145~294℃开始分解,共失重77%。
对实施例2制备的烟酸与4-氨基吡啶药物共晶进行如下溶解度测试:
(1)、称取56.4mg烟酸与4-氨基吡啶药物共晶(由单晶结构得到共晶中烟酸和4-氨基吡啶的计量比为1:1,因此56.4mg共晶中烟酸的质量为30mg,已保证烟酸的量与空白组相同)作为实验组分别溶解于4ml水和4ml乙醇中,配得共晶溶液。
(2)、称取烟酸30mg分别溶解于4ml水和4ml乙醇中,烟酸溶液作为空白溶剂作对比。
(3)、用紫外分光光度计分别测试共晶水溶液,共晶乙醇溶液,烟酸水溶液,烟酸乙醇溶液的吸收情况,通过和空白溶剂的对比得到药物共晶对于药物溶解度的改变状况。
参阅附图9,图中a曲线为药物共晶的紫外吸收曲线,b曲线为空白溶液的紫外吸收曲线,从实验结果可以看出,药物共晶在水溶液中的溶解度相较于空白溶剂变化不明显。
参阅附图10,图中a曲线为药物共晶的紫外吸收曲线,b曲线为空白溶液的紫外吸收曲线,从实验结果可以看出,药物共晶在乙醇溶液中的溶解度相较于空白溶剂变化不明显。
本发明制备的药物共晶不但具有烟酸药物特质外,而且溶解性有明显提高,延长原有药物的市场周期。以上各实施例只是对本发明做进一步说明,并非用以限制本发明专利,凡为本发明等效实施,均应包含于本发明专利的权利要求范围之内。
- 还没有人留言评论。精彩留言会获得点赞!