一种苯并噻唑衍生物、制备方法及其医药用途与流程
本发明涉及药物化学领域,具体涉及一种苯并噻唑衍生物,包括这些衍生物制备方法以及在抗炎领域的应用。
背景技术:
随着老龄化、城市化的不断扩张及生活环境的不断变化,很多与环境、年龄相关的疾病在世界范围内日益成为一个严重的健康问题。这些疾病包括癌症、炎症、老年痴呆症、组赛性肺病、心脏病、糖尿病及帕金森病等,而如何有效的预防与治疗这些疾病是全世界都在关注的课题。
氧化应激(oxidativestress)直接或者间接地损伤细胞内蛋白质、脂质等大分子物质的生理功能,被认为与肿瘤、炎症、帕金森病和老年痴呆症等。nrf2(核因子e2相关因子2)是细胞氧化应激反应中的关键因子,受keap1(keleh样环氧氯丙烷相关蛋白-1)蛋白的调控(freeradic.biol.med.2004,36,1208),通过抗氧化反应原件are(抗氧化反应元件)相互作用,调节抗氧化蛋白和ii相解毒酶的表达,如nad(p)h:醌氧化还原酶(nad(p)h:quinineoxidoreductase1,nqo1),血红素加氧1(hemoxygenase-1,ho-1)等。大量研究表明,在正常条件下nrf2与其抑制蛋白keap1结合,存在于细胞中。发生氧化应激时,keap1的半胱氨酸残基被修饰,构象改变后导致nrf2蛋白释放,进入细胞核中与are结合,促进靶基因的表达,从而发挥细胞保护作用。病理条件下,机体无法上keap1-nrf2解离。而nrf2蛋白可以经泛素化降解,不能入核诱导抗氧化基因的表达,导致疾病的发生(med.res.rev.2012,32,687)。
过去30多年中多个实验室开展了大量工作,从天然化合物或人工合成化合物库中筛选nrf2小分子激动剂,通过化学小分子模拟正常机体修饰keap1的半胱氨酸残基的生物过程,释放nrf2使其入核,发挥细胞保护作用。nrf2激活剂已经被用于治疗炎性相关疾病,如富马酸二甲酯已经被fda批准用于治疗多发性硬化症,cddo-me正在开张治疗肺动脉高压的二期临床。另外,一些具有抗炎活性的天然产物和类天然产物(姜黄素、白藜芦醇和查尔酮等)也已经被证实可激活nrf2(专利公布号:cn105566241a)。但令人遗憾的是,长时间使用共价结合修饰keap1蛋白,持续激活nrf2会引起较大的细胞毒性,易导致癌变发生。
近年来,设计直接抑制keap1-nrf2蛋白质相互作用的小分子成为了发现keap1-nrf2-are通路调节的一个新策略(curr.top.med.chem.2007,7,972)。目前,肽类keap1-nrf2相互作用抑制剂的细胞渗透能力限制其应用(org.biomol.chem.,2013,11,3553;bioorg.med.chem.lett.2013,23,3029);非肽类小分子keap1-nrf2结合抑制剂成为该领域研究热点。目前已有多个制药公司及高校都在开展此方面的研究,并报道了一系列keap1-nrf2相互作用的小分子直接抑制剂(medchemcomm.,2014,5,93;chemmedchem.,2014,9,699;j.med.chem.,2014,57,1121;j.med.chem.,2016,59,3991),在治疗肿瘤、炎症、抗帕金森病及抗老年痴呆症药物研发方面显示出极强的应用前景。
技术实现要素:
本发明公开一种如式i所示的苯并噻唑衍生物,其制备方法及其医疗用途。初步活性测试证明本发明化合物具有良好的keap1-nrf2蛋白蛋白相互作用抑制活性,可干扰keap1-nrf2的结合,从而激活nrf2,具有潜在的抗炎活性,可用于治疗众多与炎症相关的疾病,如肿瘤、帕金森病、老年痴呆症、慢性阻塞性肺疾病、动脉粥硬化、慢性肾病疾病、糖尿病或类风湿性关节炎。
本发明的化合物,(e)-烯丙基-(2-(2-(苯并[d]噻唑-2)-2-腈乙烯基)-5-(二乙基氨基)苯基)碳酸酯(式i),结构式如下:
本发明还公开了式i化合物的制备方法,如下:
1)式1化合物的合成步骤中,所采用的碱优选三乙胺、二乙胺、碳酸钠、碳酸氢钠、碳酸氢钾、碳酸钾、碳酸铯、二甲基氨基吡啶、吡啶或1,8-二氮杂二环十一碳-7-烯;溶剂优选甲醇、乙醇、n,n-二甲基甲酰胺、二甲亚砜、1,4-二氧六环和乙腈中的一种或几种;该反应温度为0℃~80℃,反应时间为1~24小时。
2)式1化合物到式i化合物的合成步骤中,碱优选三乙胺、二乙胺、二甲基氨基吡啶、吡啶或1,8-二氮杂二环十一碳-7-烯;溶剂优选二氯甲烷、丙酮、n,n-二甲基甲酰胺、1,4-二氧六环、二甲亚砜和乙腈中的一种或几种;该反应温度为-10℃~80℃,反应时间为1~24小时。
本发明基于nrf2-keap1蛋白蛋白相互作用,发现了一种具有良好药理活性的苯并噻唑衍生物。该化合物在基于荧光偏振的keap1-nrf2蛋白蛋白相互作用抑制实验中,表现出的活性优于阳性对照s47(j.med.chem.2014,57,1121)。在细胞实验中,该化合物可使大鼠心肌细胞nrf2入核,并使抗氧化因子ho-1、nqo1水平上调,同时抑制lps诱导的炎性因子tnf-α,il-1β,il-6水平的上调。因此,该化合物有望作为先导化合物,进一步开发为抗炎药物,在制备预防和/或治疗肿瘤、炎症、帕金森病及老年痴呆症的药物中具有潜在的应用前景。
附图说明
图1表面等离子共振实验测定化合物对keap1蛋白的亲和力图;
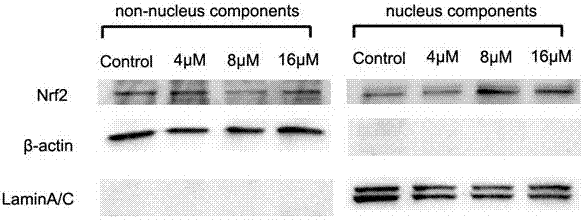
图2凝胶电泳图;
图3共聚焦显微镜下观察各组细胞中nrf2定位图;
图4化合物促进ho-1、nq01的mrna水平上调图;
图5化合物抑制脂多糖(lps)诱导的炎性因子tnf-a、il-1β、il-6mrna水平上调图。
具体实施方式
下面结合具体实施例对本发明做进一步的详细说明。
实施例1:式1化合物的制备
将3.5g苯并噻唑-2-乙腈和3.9g4-(二乙胺基)水杨醛溶于120ml甲醇溶液中,氮气保护,随后1ml三乙胺,室温搅拌12小时。之后将反应液浓缩,残余物经柱层析纯化后得到5.5g黄色固体化合物式1,产率79%。1hnmr(600mhz,cdcl3)δ8.01(1h,d,j=6hz),7.90(1h,d,j=6hz),7.47(1h,dd,j=6,6hz),7.35(1h,dd,j=6,6hz),7.29(1h,d,j=6hz),6.48(1h,d,j=6hz),6.40(1h,s),3.42(4h,t,j=6hz),1.22(6h,t,j=6hz).13cnmr(150mhz,cdcl3)δ156.1,151.6,142.2,137.2,130.9,130.2,126.2,124.8,122.6,122.4,121.7,121.4,111.0,108.2,97.1,96.9,45.3,12.7.esi-msm/z:350.1[m+h]+.
实施例2:式i化合物的制备
将700mg式1化合物溶于20ml二氯甲烷中,冰浴至0℃,加入424mg三光气和1ml三乙胺。待反应进行1小时,加入166mg烯丙醇,搅拌12小时。反应液减压浓缩,残余物经柱层析纯化后得到220mg黄色固体化合物式i,产率25%。1hnmr(400mhz,cdcl3)δ8.82(1h,s),8.02(1h,d,j=8hz),7.92(1h,d,j=8hz),7.51-7.35(3h,m),6.63(1h,d,j=12hz),6.14-6.07(1h,m),6.48(1h,s),5.48(1h,d,j=8hz),5.31(1h,d,j=8hz),4.86(2h,shz),3.45(4h,q,j=8.0hz),1.24(6h,t,j=7.0hz).13cnmr(100mhz,cdcl3)δ161.5,159.6,155.8,153.1,152.4,151.9,139.8,137.0,132.7,130.8,126.1,124.5,122.3,121.6,118.2,114.2,109.9,108.6,97.0,67.0,45.1,12.7.esi-msm/z:434.8[m+h]+.
实施例3:荧光偏振法测定化合物对keap1-nrf2蛋白结合抑制活性
荧光偏振法测定keap1-nrf2蛋白结合抑制活性将荧光探针(fitc–βala–deetgef–oh)溶解于缓冲液(10mmhepes,ph7.4,3.4mmedta,150mmnacl,0.005%tween-20)稀释至10nm,加入到梯度稀释的keap1蛋白中,室温避光孵育30分钟,荧光各向异性值用spectramaxm5e酶标仪读取(ex:485nm,em:535nm)。蛋白结合常数根据荧光各向异性值用mathematica7(wolframresearchinc.)拟合得到。具体公式如下:
实验对待测化合物进行单浓度(100μm),以化合物s47(j.med.chem.2014,57,1121)作为对照化合物,抑制率为
然后将化合物溶解于dmso用缓冲液(10mmhepes,ph7.4,3.4mmedta,150mmnacl,0.005%tween–20)稀释至需要浓度(1%dmso),20μl化合物加入到60μl含有10nm荧光探针(fitc–βala–deetgef–oh),400nm的keap1蛋白的溶液中,室温避光孵育1小时。荧光各向异性值用biotecksynergy2酶标仪读取(ex:485nm,em:535nm)。蛋白结合常数根据荧光各向异性值用mathematica7(wolframresearchinc.)拟合得到。具体公式如下:
其中a=kd1+kd2+lst+lt-rt;b=(lt-rt)kd1+(lst-rt)kd2+kd1kd2;c=-kd1kd2rt;
公式中,q值是荧光探针的与最高蛋白浓度下结合后的荧光强度和自由状态的荧光强度的比值,fsb为荧光探针结合部分,ab和af分别为结合和自由状态下的探针的各向异性值,kd1是探针的蛋白结合常数,lst为探针浓度,rt为蛋白浓度,kd2为化合物的蛋白结合抑制常数。
测试结果式i化合物在100μm浓度下对keap1-nrf2蛋白蛋白相互作用的抑制率为81.25%,其蛋白结合抑制常数kd2值为5.1μm,略优于阳性对照s47(kd2值为7.6μm)。
实施例4:表面等离子共振实验测定化合物对keap1蛋白的亲和力
计算配体偶联水平:1.5×rl=10440ru;预富集(phscouting),选择合适的偶联ph及配体浓度:将配体稀释于不同ph的10mmnaac中(配体终浓度约为25-50μg/ml),流经空白芯片表面,测试静电吸附的效果;偶联配体(immobilization):先用空白芯片静电吸附测试预富集能力,再用edc、nhs处理以活化芯片表面,然后进样配体,偶联600s,最终采用ethanolamine封闭芯片表面。
配制dmso浓度范围为4.5%-5.8%的系列校正溶液,分别在全部分析物之前、全部分析物之后、和每30个分析物之后进样校正溶液,用于校正分析物中dmso的浓度误差。
将分析物的储备液,用工作缓冲液逐级递减稀释成系列浓度(0、250、500、1000、2000、4000、8000、16000、32000、64000nm。采用kinetics/affinity程序进样,样品以流速30μl/min,进样120s,解离120s。
得到的数据用采用biacoret200evaluationsoftware进行分析。计算溶剂dmso浓度校正曲线,选择适当的浓度范围和结合曲线,扣除参比通道及零浓度,采用稳态模型进行拟合分析,获得亲和力数值及参数。实验结果如图1所示,化合物与keap1蛋白的亲和常数为48.1.μm。
report
parameters
实施例5:化合物促进nrf2向细胞核内转移
将大鼠心肌细胞h9c2细胞种植在小皿中,分别用4μm、8μm以及16μm化合物处理细胞6h,将处理好的对照组及实验组细胞吸弃培养液,用1×pbs清洗一次,加入1ml预冷1×pbs,用细胞刮子刮下细胞,用移液枪将细胞加入预冷的离心管中4℃、1000rpm离心5min,吸尽上清,留下细胞沉淀备用;利用试剂盒分别提取细胞核蛋白和非细胞核蛋白;取10μl提取的细胞浆蛋白样品及5μl细胞核蛋白样品到eppendorf管内,加ddh2o补足10μl,利用bca测蛋白浓度;制作分离胶12%,浓缩胶5%;100℃蛋白样品变性5min,每个样品上样12μg;60v进胶,120v恒压跑胶;用转移槽80v/160ma恒流转膜,2.5h;tbst配制的5%脱脂牛奶室温封闭1.5h;弃掉奶粉用tbst冲洗干净后,用tbst配制的5%的bsa溶液按1:1000的比例稀释一抗,pvdf膜4℃孵育过夜;tbst洗膜,3次,每次5min;用tbst配制的5%的脱脂牛奶溶液将二抗按1:5000的比例稀释,室温孵育1h;用tbst洗膜,3次,每次5min;使用化学发光仪用milipore底物显膜,用imagej分析凝胶电泳图并定量。结果显示8μm、16μm化合物使细胞核内nrf2水平显著上调(图2所示)。
另一方面,用8μm化合物处理h9c2细胞6h,吸弃培养液,pbs清洗一遍,细胞经固定,封闭后,加入nrf2一抗四度过夜,二抗孵育37度孵育1小时,dapi复染细胞核,共聚焦显微镜下观察各组细胞中nrf2定位在对照组中,nrf2主要位于细胞质中,8μm的化合物处理细胞6h,细胞核中的nrf2显著增多(图3所示)。
实施例6:化合物使ho-1、nq01mrna水平上调
nrf2入核能够激活下游抗氧化元件,因此,我们进一步利用rt-pcr分析了化合物是否能够激活下游抗氧化元件ho-1以及nq01。将h9c2细胞种植在小皿中,8μm化合物分别处理h9c2细胞2h、4h以及6h,trizol裂解细胞,提取细胞内rna,反转为dna,利用实时定量pcr仪分析,分析ho-1、nq01水平。结果如图4所示,化合物处理细胞2h、4h以及6h均显著上调ho-1以及nq01的mrna水平。
实施例7:化合物抑制脂多糖(lps)诱导的炎性因子tnf-a、il-1β、il-6mrna水平上调。
将h9c2细胞种植在小皿中,利用1μg/ml的lps刺激h9c2细胞建立炎症模型,8μm化合物与脂多糖共处理h9c2细胞6h,trizol裂解细胞,提取细胞内rna,反转为dna,利用实时定量pcr仪分析。结果如图5所示,8μm的化合物处理细胞6h能够显著抑制lps诱导的炎性因子tnf-a、il-1β、il-6mrna水平上调。
- 还没有人留言评论。精彩留言会获得点赞!