一种硼替佐米的杂质及其制备方法与流程
本发明属于药物化学及药物分析领域,具体涉及硼替佐米的杂质及其制备方法,以及其作为硼替佐米质量控制参照标准品的用途和硼替佐米及其杂质的测试方法。
背景技术:
硼替佐米(bortezomib),化学名称为[(1r)-3-甲基-1-[[(2s)-1-氧-3-苯基-2-[(吡嗪羰基)氨基]丙基]氨基]丁基]-硼酸,cas:179324-69-7,结构式如式i所示。
硼替佐米,商品名为万珂(velcade),是由美国千年制药公司(millenniumpharmaceuticals)研发的一种二肽硼酸类蛋白酶体抑制剂,也是第一个用于临床的蛋白酶体抑制剂,目前主要用于多发性骨髓瘤(mm)和套细胞淋巴瘤(mcl)的治疗。该药物于2003年5月获得美国食品药品管理局(fda)批准,用于治疗复发性和难治性多发性骨髓瘤。随后在欧洲、澳大利亚、马来西亚和中国等国家陆续上市,用于治疗复发性和难治性多发性骨髓瘤。
硼替佐米作为一种新型高效专一的蛋白酶体抑制剂,其可逆地与26s蛋白酶体结合,阻断蛋白的降解通道,从而防止肿瘤细胞的恶性增殖。26s蛋白酶体是一种大的蛋白质复合体,可降解被泛素化的蛋白质。泛素蛋白酶体通道对调节特异蛋白在细胞内的浓度中起到重要作用,以维持细胞内环境的稳定。蛋白水解会影响细胞内多级信号串联,这种对正常细胞内环境的破坏会导致细胞的死亡。而对26s蛋白酶体的抑制可防止特异蛋白的水解。体外试验证明,硼替佐米对多种类型的癌细胞具有细胞毒性,除对多发性骨髓瘤的治疗外,还对套细胞型淋巴瘤及其他b细胞类型淋巴瘤、霍奇金淋巴瘤等多种肿瘤有较强的抗肿瘤活性,同时还具有化疗耐药性,是第一个对血液系统和实体性恶性肿瘤都具有抗癌效应的蛋白酶体抑制剂,因此,硼替佐米作为肿瘤治疗的重要药物,具有广阔的应用前景和研究价值。
制备专利wo2005097809(同族专利cn1960996)公开了一种硼替佐米的制备方法,该方法以(1s,2s,3r,5s)-蒎烷二醇-l-苯丙氨酸-l-亮氨酸硼酸酯盐酸盐(式vii)为原料,在o-苯并三氮唑-n,n,n',n'-四甲基脲四氟硼酸(tbtu)作用下,与哌嗪甲酸(式viii)偶联得中间体(1s,2s,3r,5s)-蒎烷二醇-n-(2-吡嗪羰基)-l-苯丙氨酸-l-亮氨酸硼酸酯(式ix),再与异丁基硼酸(式x)在酸性条件下脱保护即得硼替佐米(式i),进一步通过重结晶等纯化手段即可制备高纯度硼替佐米,其合成路线如下:
本领域已知出于对人体给药安全考虑,在一种活性药物成分(api)产品商业化之前需要由国家和国际的管理机构建立毒理学上非特征性杂质的鉴定的极低下限。通常,每种杂质的限量少于约0.15%重量比。未鉴定的和/或非特征性杂质的限量明显更低,通常少于0.1%重量比。
本领域中也已知,硼替佐米或任何活性药物成分(api)中的杂质可能来自api本身的降解(这与纯api在储存过程中的稳定性相关)和制造过程,包括化学合成。工艺杂质包括未反应的原材料、原材料中所含的杂质的化学衍生物、合成副产物和降解产物。
除稳定性外,商业制造的api的纯度也明显是商业化的必要条件。在商业制造过程中引入的杂质必须限制在极小量,并且最好基本上不存在。例如,供api制造商使用的internationalconferenceonharmonizationoftechnicalrequirementsforhumanuse(“ich”)q7a指南要求通过规定原材料的质量、控制工艺参数,如温度、压力、时间和化学计量比和在制造法中加入提纯步骤,如结晶、蒸馏和萃取来使工艺杂质保持在设定限额以下。
化学反应的产物很少是具有符合药物标准的足够纯度的单一化合物。反应副产物以及该反应中所用的原材料多少也存在于产物混合物中。在api如硼替佐米制备过程中的某些阶段,通常必须通过hplc、tlc或gc分析法分析其纯度,以测定其是否适用于继续加工和最终用在药品中。api不需要绝对纯净,因为绝对纯净是通常不可实现的理论目标。相反,设定纯度标准以确保api尽可能不含杂质,并因此对临床应用而言尽可能安全。如上所述,在美国,foodanddrugadministration(食品和药品管理)指南推荐,一些杂质的量仅限于低于0.1%。
通常用光谱和/或其它物理方法鉴定杂质,然后得到一个峰位置,或tlc板中的斑点,之后鉴定杂质,例如通过它在色谱图中的相对位置来鉴定,色谱图中的相对位置成为“保留时间”。根据仪器使用条件以及很多其它因素,保留时间每天或甚至在一天之中都在变化。为了减少这些变化影响到杂质的准确识别,通常用“相对保留时间(rrt)”来鉴定杂质。杂质的rrt是用它的保留时间除以主峰的保留时间。
本领域已知,参照标准品可以用于未知混合物中参照标准化合物的定性和定量,当参照标准的已知浓度的溶液和未知混合物用相同技术分析时,参照标准是“外标”,可以通过比较检测器的响应强度来测定混合物中所述化合物的量。
如本领域技术人员已知的,通过了解其化学结构和合成途径,及通过鉴定终产品的杂质和确定终产品的杂质的量来大大加强工艺杂质的控制。
目前,已有多篇文献资料报道了硼替佐米的制备或纯化方法。硼替佐米制备专利wo2005097809描述了硼替佐米的制备及其纯化方法,该专利采用乙酸乙酯或甲基叔丁基醚重结晶进行纯化,纯化效果不明显。其它专利wo2009036281、wo2011098963、cn101812026、cn105601705、cn104822688、cn103897028等也存在同样的问题,且文献报道中也未公开关于硼替佐米杂质的控制方法。
因此,现有的硼替佐米制备技术中,存在产品纯度不高,缺乏对单个杂质的控制等不足之处。针对现有技术中的不足,本发明对硼替佐米产品中的杂质控制进行了研究,制备了两种以前未鉴定过的硼替佐米杂质即式v化合物和式vi化合物,这两个化合物均可能在硼替佐米的合成过程或储存期间形成,就申请人所知,这两个化合物从未被独立制备以及与硼替佐米分离,因此,我们发明了将这两个化合物作为杂质参照标准用于硼替佐米纯度分析定量的方法。。
技术实现要素:
本发明的目的在于提供一种式v化合物,其为硼替佐米的降解杂质,即(s,z)-n-[1-(3-甲基丁烯氨)-1-氧-3-苯基丙烷-2-基]吡嗪-2-甲酰胺。
上述式v化合物在一些实施方案中被分离为具有至少50%的纯度,或者至少60%的纯度,或者至少70%的纯度,或者至少80的纯度,或者至少90%的纯度,或者至95%的纯度,或者至少96%的纯度,或者至少97%的纯度,或者至少98%的纯度,或者至少99%的纯度。该纯度一般为hplc面积归一化法的纯度。
本发明还提供一种式v化合物和式vi化合物的制备方法,包括如下步骤:
(1)、在至少一种有机溶剂中,用至少一种乙酰化试剂和一种碱乙酰化式ii化合物,得到式iii化合物。
(2)、在至少一种有机溶剂中,用至少一种碱与式iii化合物进行消除反应,得到式iv化合物。
(3)、利用至少一种纯化手段将式iv化合物进行分离、纯化,分别得到式v化合物和式vi化合物。
其中,步骤(1)和(2)中所述有机溶剂选自二氯甲烷、四氢呋喃和二氧六环。
其中,步骤(1)中所述乙酰化试剂选自乙酸酐、乙酸和乙酰氯,优选为乙酸酐。
其中,步骤(1)中乙酰化试剂与式ii化合物的摩尔比为1~200:1,优选为1~10:1,更优选为3:1。
其中,步骤(1)和(2)中所述碱选自三乙胺、吡啶、吗啉、4-二甲氨基吡啶、1,8-二氮杂二环(5.4.0)十一碳-7-烯和1,5-二氮杂二环[4.3.0]壬-5-烯,优选为选自三乙胺和4-二甲氨基吡啶。
其中,步骤(1)和(2)中所述碱选自三乙胺和4-二甲氨基吡啶;步骤(1)中碱与式ii化合物的摩尔比为0.1~100:1,优选为1~10:1,更优选为3:1;步骤(2)中碱与式iii化合物的摩尔比为0.1~100:1,优选为1~10:1,更优选为2:1。
其中,步骤(3)所述纯化手段选自制备色谱和常规柱层析。
本发明还提供另一种式v化合物和式vi化合物的制备方法,包括如下步骤:
(1)、在至少一种有机溶剂中,用至少一种乙酰化试剂和一种碱同时乙酰化和消除式ii化合物,得到式iv化合物。
(2)、利用至少一种纯化手段将式iv化合物进行分离、纯化,分别得到式v化合物和式vi化合物。
其中,步骤(1)中所述有机溶剂选自二氯甲烷、四氢呋喃和二氧六环。
其中,步骤(1)中所述乙酰化试剂选自乙酸酐、乙酸和乙酰氯,优选为乙酸酐。
其中,步骤(1)中乙酰化试剂与式ii化合物的摩尔比为1~200:1,优选为1~10:1,更优选为5:1。
其中,步骤(1)中所述碱选自三乙胺、吡啶、吗啉、4-二甲氨基吡啶、1,8-二氮杂二环(5.4.0)十一碳-7-烯和1,5-二氮杂二环[4.3.0]壬-5-烯,优选为4-二甲氨基吡啶。
其中,步骤(1)中碱与式ii化合物的摩尔比为0.1~100:1,优选为1~10:1,更优选为5:1。
其中,步骤(2)所述纯化手段选自制备色谱和常规柱层析。
在一个具体的实施方案中,上述式v化合物和式vi化合物的分离纯化方法,进一步包括如下步骤:
(1)将上述式iv化合物用单一溶剂或混合溶剂溶解;
(2)可选地,利用常规柱层析将溶解的式iv化合物,通过单一溶剂或混合溶剂作洗脱液进行洗脱分离,分别得到纯化的式v化合物和式vi化合物。
(3)可选地,利用制备色谱柱将溶解的式iv化合物,通过单一溶剂或混合溶剂作流动相进行分离,分别得到纯化的式v化合物和式vi化合物。
在上述纯化步骤中,其中步骤(1)中所述溶剂包括二氯甲烷、三氯甲烷、四氢呋喃、乙酸乙酯、正己烷、正庚烷、石油醚或它们的混合液等;步骤(2)中所述洗脱液包括乙酸乙酯和正己烷混合液,或乙酸乙酯和正庚烷混合液,或乙酸乙酯和石油醚混合液,二氯甲烷和正己烷混合液,或二氯甲烷和正庚烷混合液,或二氯甲烷和石油醚混合液等;步骤(3)中所述流动相包括乙酸乙酯和正己烷混合液,或乙酸乙酯和正庚烷混合液,或乙酸乙酯和石油醚混合液,二氯甲烷和正己烷混合液,或二氯甲烷和正庚烷混合液,或二氯甲烷和石油醚混合液等。
本发明还提供了一种式v化合物和式vi化合物用于控制硼替佐米质量的用途。
本发明还提供了一种测定硼替佐米及其杂质的方法,该方法包括:
(1)提供一种硼替佐米样品;
(2)提供一种含有已知量和/或特性的式v化合物、或/和式vi化合物作参照样品;
(3)用色谱法测定硼替佐米样品中式v化合物、或/和式vi化合物的存在或/和量和/或硼替佐米的量。
上述测定方法中,所述色谱法优选高效液相色谱法(hplc)法。测定并确定硼替佐米样品中式v化合物、或/和式vi化合物的存在或/和量的高效液相色谱法(hplc)一般包括外标法、内标法、加校正因子的主成分自身对照法等,这些方法的具体操作过程都本领域常规的知识。所述的确定包括根据硼替佐米样品和参照样品的测试结果计算或对比式v化合物、或/和式vi化合物在硼替佐米样品中的存在和/或量。所述计算是本领域常规的知识和计算公式。在实际生产的硼替佐米样品中检测的式v化合物、或/和式vi化合物的含量在常规杂质限量以下,即不大于0.1%。
本发明还提供了一种测定硼替佐米及其杂质的方法,该方法包括:
(1)提供一种硼替佐米溶液作测试样品;
(2)提供一种含有已知量和/或特性的式v化合物、或/和式vi化合物的溶液作参照样品;
(3)用hplc测定(1)的测试样品和/或(2)的参照品,确定硼替佐米样品中式v化合物、或/和式vi化合物的存在或/和量。
上述方法中,所述的确定是指根据硼替佐米测试样品和参照样品的测试结果采用外标法、内标法或加校正因子的主成分自身对照法计算或判断式v化合物、或/和式vi化合物在硼替佐米样品中的存在和/或量。
上述方法中,hplc检测方法可采用:十八烷基硅烷键合硅胶为填充剂,检测波长为270nm,选择适宜流动相使测试满足常规要求,记录色谱图,用面积归一化法计算纯度。
总之,本发明提供了一种分离的硼替佐米降解杂质,即式v化合物,以及式v化合物和式vi化合物的制备方法及二者作为硼替佐米参照标准的用途。因此,本发明有效解决了现有技术中的缺乏对单个杂质的控制不足之处,为进一步控制硼替佐米的质量提供了保障。
附图说明
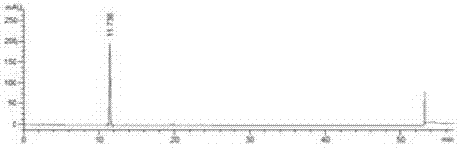
图1是实施例6的硼替佐米的标示物溶液的典型hplc色谱图。
图2是实施例6的式v化合物的标示物溶液的典型hplc色谱图。
图3是实施例6的式iii化合物的标示物溶液的典型hplc色谱图。
具体实施方式
下面的实施例用于进一步理解和说明本发明,但不限制本发明的范围。
一般操作
式ii化合物的制备,例如根据文献《synthesisandcharacterizationoforganicimpuritiesinbortezomibanhydrideproducedbyaconvergenttechnology》(scipharm.2012;80:67-75)中报道的方法制备,将其全文引入本发明用于参考,另外,也可通过商业途径购得。
质谱分析使用的仪器是agilent1200高效液相色谱系统、agilent公司g6410a串联三重四级杆质谱仪,离子源采用电喷雾离子源,正离子模式。分流的hplc洗脱液,允许大约为1μg/ml进入质谱仪的离子源。
核磁共振分析使用的仪器是brukeravance600核磁共振谱仪,使用氘代溶剂为dmso-d6。tms被用来作为一个质子的共振(δ1h0.00)和溶剂内部参考,dmso-d6作为碳共振内标(δ13c39.10-40.10)。
本发明使用下列缩词,并具有如下含义:
实施例1:硼替佐米的hplc分析方法
取硼替佐米适量,加0.1%磷酸溶液/乙腈(50:50)混合液适量溶解,用0.1%磷酸溶液/乙腈(50:50)混合液稀释制成每1ml中约含1mg的溶液,作为供试品溶液,按高效液相色谱法(中国药典2015年版二部附录ⅴd)测定。用十八烷基硅烷键合硅胶为填充剂,柱温为25℃,流速为1.0ml/min,检测波长为270nm,以0.1%磷酸溶液作为流动相a,乙腈作为流动相b,按下表比例做线性梯度洗脱(比例为其体积比),理论板数按硼替佐米计算应不低于3000。精密量取供试品溶液20μl,注入液相色谱仪,记录色谱图,用面积归一化法计算硼替佐米的纯度。必要时,可通过空白对照扣除系统峰面积或溶剂峰面积。
实施例2:式iv化合物的制备
1、式iii化合物的制备
将式ii化合物(10g,28.1mmol)和三乙胺(8.5g,84.0mmol)溶于200ml二氯甲烷中,氮气置换反应体系,控温0-5℃,缓慢加入乙酸酐(8.6g,84.2mmol),室温反应约10小时,tlc检测反应完全,停止反应。将反应液缓慢倒入冰水中,分液,水相用二氯甲烷提取一次,合并二氯甲烷层,再用盐水洗涤两次,无水硫酸镁干燥,过滤,减压浓缩至干得式iii化合物,类白色粉末,hplc:96.3%。
2、式iv化合物的制备
将式iii化合物(10g,25.1mmol)溶于200ml四氢呋喃中,氮气置换反应体系,室温搅拌下,缓慢加入dmap(6.1g,49.9mmol),室温反应约3小时,tlc检测反应完全,停止反应。将反应液缓慢倒入乙酸乙酯和水的混合液中,分液,水相用乙酸乙酯提取两次,合并乙酸乙酯层,用0.5n酸水洗涤两次,再用盐水洗涤一次,无水硫酸钠干燥,过滤,减压浓缩至干得式iv化合物,黄色粘稠物。
实施例3:式iv化合物的一锅法制备
1、式iv化合物的制备
将式ii化合物(10g,28.1mmol)和dmap(17.1g,140.0mmol)溶于200ml四氢呋喃中,氮气置换反应体系,控温0-5℃,缓慢加入乙酸酐(14.3g,140.1mmol),室温反应约6小时,tlc检测反应完全,停止反应。将反应液缓慢倒入乙酸乙酯和水的混合液中,分液,水相用乙酸乙酯提取两次,合并乙酸乙酯层,用0.5n酸水洗涤两次,再用盐水洗涤一次,无水硫酸钠干燥,过滤,减压浓缩至干得式iv化合物,黄色粘稠物。
2、式iv化合物的制备
将式ii化合物(10g,28.1mmol)和dbu(17.1g,112.4mmol)溶于200ml二氯甲烷中,氮气置换反应体系,控温0-5℃,缓慢加入乙酸酐(11.5g,112.6mmol),室温反应约8小时,tlc检测反应完全,停止反应。将反应液缓慢倒入冰水中,分液,水相用二氯甲烷提取一次,合并二氯甲烷层,再用盐水洗涤两次,无水硫酸镁干燥,过滤,减压浓缩至干得式iv化合物,黄色粘稠物。
实施例4:式v化合物的制备
1、式v化合物的制备
将实施例2步骤2中式iv化合物溶于乙酸乙酯中,采用乙酸乙酯与石油醚的混合体系作洗脱液,经200-300目硅胶填充的常规柱层析纯化分离得(s,z)-n-[1-(3-甲基丁烯氨)-1-氧-3-苯基丙烷-2-基]吡嗪-2-甲酰胺(式v化合物),hplc:97.7%。
质谱[esi-ms,m/z]中m+h+峰为339,m+na+峰为361。
13cnmr(600mhz,dmso)δ(ppm):169.2,162.8,148.3,144.4,143.9,143.8,137.5,129.6,128.5,126.9,120.2,119.2,54.1,38.2,25.1,23.4,23.3;
1hnmr(600mhz,dmso)δ(ppm):9.60-9.62(1h,d),9.13(1h,d),8.89(1h,d),
8.75-8.77(2h,m),7.16-7.27(5h,m),6.39-6.43(1h,m),5.02-5.06(1h,m),4.55-4.58(1h,m),3.07-3.14(2h,m),2.72-2.78(1h,m),0.92-0.97(6h,dd)。
2、式v化合物的制备
将实施例2步骤2中式iv化合物溶于适量乙酸乙酯中,采用制备色谱分离(色谱柱:santaisepaflash80g40-63µm),以正己烷作为流动相a,乙酸乙酯作为流动相b,按a/b=80:20进行洗脱,流速:10ml/min,收集目标成分,减压浓缩得(s,z)-n-[1-(3-甲基丁烯氨)-1-氧-3-苯基丙烷-2-基]吡嗪-2-甲酰胺(式ii化合物),hplc:99.6%。
实施例5:式vi化合物的制备
1、式vi化合物的制备
将实施例2步骤2中制备的式iv化合物溶于适量乙酸乙酯中,采用乙酸乙酯与石油醚的混合体系作洗脱液,经200-300目硅胶填充的常规柱层析纯化分离得(s,e)-n-[1-(3-甲基丁烯氨)-1-氧-3-苯基丙烷-2-基]吡嗪-2甲酰胺(式vi化合物),hplc:98.5%。
质谱[esi-ms,m/z]中m+h+峰为339,m+na+峰为361。
13cnmr(600mhz,dmso)δ(ppm):168.5,163.0,148.2,144.4,143.9,143.8,137.9,129.6,128.6,126.9,120.1,120.7,54.6,37.6,28.9,23.3,23.3;
1hnmr(600mhz,dmso)δ(ppm):9.95-9.96(1h,d),9.11(1h,d),8.88(1h,d),
8.80-8.81(1h,m),8.75(1h,m),7.15-7.26(5h,m),6.54-6.58(1h,m),5.25-5.28(1h,m),4.76-4.79(1h,m),3.08-3.16(2h,m),2.26-2.34(1h,m),0.97-0.98(6h,dd)。
2、式vi化合物的制备
将实施例2步骤2中制备的式iv化合物溶于适量乙酸乙酯中,采用制备色谱分离(色谱柱:santaisepaflash80g40-63µm),以正己烷作为流动相a,乙酸乙酯作为流动相b,按a/b=80:20进行洗脱,流速:10ml/min,收集目标成分,减压浓缩得(s,e)-n-[1-(3-甲基丁烯氨)-1-氧-3-苯基丙烷-2-基]吡嗪-2甲酰胺(式iii化合物),hplc:99.8%。
实施例6:硼替佐米、式v化合物、或/和式vi化合物的定性和定量分析
a.色谱条件
色谱柱&填充物:十八烷基硅烷键合硅胶为填充剂的色谱柱(waters
symmetryc18,5μm,4.6mm×250mm)
柱温:25℃
检测波长:270nm
进样量:20μl
流速:1.0ml/min
流动相:以0.1%磷酸溶液为流动相a,以乙腈流动相b,按下表比例做线性梯度洗脱(比例为其体积比)。
b.制备鉴别硼替佐米、式v化合物、或/和式vi化合物的标示物溶液
分别取硼替佐米、式v化合物、或/和式vi化合物适量,各自分别用0.1%磷酸溶液/乙腈(50:50)混合液适量溶解并稀释配制成浓度为约0.1mg/ml的溶液,即得各标示物溶液。将各标示物溶液分别注入色谱柱中测定,记录色谱图,即得各自的保留时间。在上述色谱条件下,硼替佐米的保留时间约为11.736min(色谱图见图1);式vi化合物的保留时间约为29.993min(色谱图见图2);式v化合物的保留时间约为31.286min(色谱图见图3)。依据本领域的知识,可以理解,硼替佐米、式v化合物、或/和式vi化合物各物质间均能达到有效分离,故该色谱条件能将硼替佐米、式v化合物、或/和式vi化合物准确鉴别。
c.制备试样溶液
用适量0.1%磷酸溶液/乙腈(50:50)混合液溶解硼替佐米,并稀释成浓度约1mg/ml的分析用的硼替佐米试样溶液。
d.制备1%试样溶液
取c中试样溶液用0.1%磷酸溶液/乙腈(50:50)混合液稀释成浓度约1%(10μg/ml)的试样溶液。
e.测定
将c的试样溶液和d的1%试样溶液注入色谱仪中,记录色谱图。
以外标法对杂质定位,按加校正因子的主成分自身对照法计算杂质的量。
ai为杂质i的峰面积,a1为1%试样溶液卡格列净的主峰面积,fi为杂质i的校正因子。
- 还没有人留言评论。精彩留言会获得点赞!