一种癌症诊断芯片及其试剂盒的制作方法
本发明涉及胃癌的诊断芯片及其试剂盒,属于医药生物
技术领域:
。
背景技术:
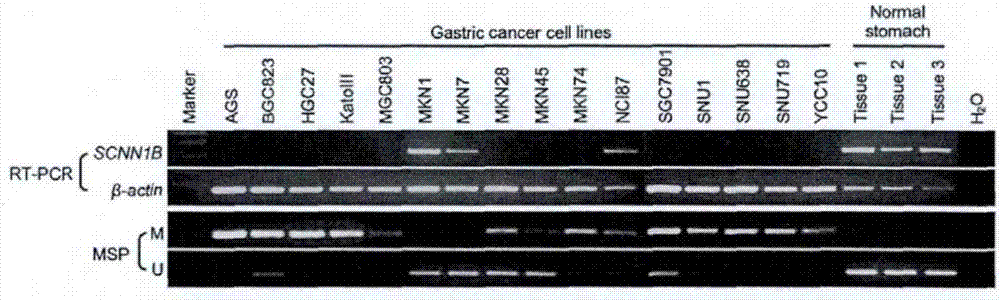
:胃癌是世界上最常见的恶性肿瘤之一。2012年全球新增胃癌病例数95万,死亡病例达到72.3万例,为世界第三大癌症死因,其中42.6%的胃癌发生在中国。2016年中国国家癌症中心发布的最新研究结果显示,在中国胃癌的发病率和死亡率均高居恶性肿瘤的第二位,目前仍是我国第二大最常见恶性肿瘤。胃癌的高发病率和患病率给全球带来了重大社会负担。尤其是尚处于发展中阶段的中国,目前正面临着极大的癌症压力。由于胃癌早期临床表现不典型,不易发现,患者就诊时往往已经是中晚期,加之缺乏有效的治疗手段,因此胃癌仍然是严重影响国人生命健康的重要疾病。因此积极探索胃癌的发病机制,寻找有效的早期诊断及预测临床预后的分子标志物,将为胃癌的诊断和治疗提供重要思路和理论依据,有利于缓解中国乃至全球的癌症负担。总的来说,胃癌男性多发,发病率约为女性的2倍。然而女性更年期后一旦失去雌激素水平保护,其胃癌发病率快速上升至与男性相同。大多数胃癌是腺癌,源自胃粘膜腺上皮,但其组织形态、发病机制和临床表现的差别确是多种多样的。1965年lauren根据胃癌的组织细胞学特点,将胃癌分成肠型胃癌和弥漫型胃癌。当肿瘤内两种类型成分相当时就称为混合型。流行病学研究发现50%的胃癌为肠型胃癌,而弥漫型胃癌和混合型胃癌分别占35%和15%。肠型腺癌的特征在于有不规则大小不等的腺样结构形成,常常与邻近豁膜的不规则肠化生相关。根据腺体结构,分化程度可分为高分化、中分化和低分化。肠型胃癌较常发生在老年男性患者,与慢性胃炎相关[6]01992年美国学者correa提出肠型胃癌常常经历一系列癌前病变改变,包括从慢性活动性非萎缩性胃炎一多灶性萎缩一肠化生一不典型增生/腺瘤,最后进展成胃癌。弥漫型胃癌分化程度较差,由散在于胃壁内、浸润性的癌细胞组成,其特征为未形成腺体结构,但能分泌粘液。弥漫型胃癌起源于胃固有钻膜,较常发生在年轻患者,男女比例接近。现代内镜技术日新月异,我们已经可以通过内镜检查识别早期胃癌而改善胃癌患者的总体生存。但在胃癌筛查中,传统方法如粪便隐血检验不够灵敏,导致大量假阴性结果。因此临床上对于无症状或症状不明显的患者进行早期筛查还是很困难。基于dna分子标记在肿瘤发生中发挥了关键作用,同时分子技术的dna标记物将对检测肿瘤样品更加敏感,此外,它还可以作为无创检测方法应用于血液检测。前期的研究结果发现,scnn1b基因在81.3%的胃癌细胞株(13/16)和胃癌组织(p<0.001)中表达沉默,而在人类正常胃组织中高表达。dna启动子区高甲基化水平与scnn1b的转录沉默相关。胃癌组织芯片检测结果显示scnn1b高表达是预测胃癌患者更长疾病特异生存时间的预后因子(p=0.004)。在胃癌细胞中过表达scnn1b能抑制细胞生长,诱导凋亡和go/g1期细胞周期阻滞,抑制细胞迁移与侵袭,体内实验抑制裸鼠皮下移植瘤生长。蛋白scnn1b与蛋白grp78直接相互作用,促进泛素化途径介导的蛋白grp78的降解。随后grp78蛋白水平的下降引发折叠蛋白应答(unfoldedproteinresponse,upr),顺序激活perk,atf4,chop和xbpis,导致caspase诱导的细胞凋亡以及对细胞迁移和侵袭的抑制。过表达scnn1b使胃癌细胞对未折叠蛋白应答(upr)诱导剂衣霉素((tunicamycin)细胞毒性的敏感性增强,说明scnn1b能通过未折叠蛋白应答(upr)介导肿瘤抑制。补救实验中过表达grp78抵消scnn1b对细胞生长和转移的抑制,而敲低grp78则加强了scnn1b对细胞生长的抑制。scnn1b能通过诱导细胞凋亡和细胞周期阻滞、抑制细胞迁移和侵袭以及促进细胞粘附,在胃癌行使抑癌基因的功能。我们还发现scnn1b能通过与grp78的直接相互作用、导致后者的降解及随后未折叠蛋白应答(upr)的激活。从而在胃癌中发挥肿瘤抑制作用。scnn1b的表达状态水平可以用来判断原发性胃癌的生存预后。因此我们还提出scnn1b可作为胃癌患者判断生存预后的新型肿瘤标志物。基于上述的研究发现,提供一种快速的胃癌检测的标志物以及相应的芯片显得尤为重要。技术实现要素:根据第一方面,本发明的目的是针对现有技术中的不足,提供微小核苷酸hsa-mir-092a-1在制备诊断胃癌的芯片中的应用。本发明的第二个目的是,提供微小核苷酸hsa-mir-092a-1在制备胃癌预后的疾病进展的芯片中的应用。本发明的第三个目的是,提供微小核苷酸hsa-mir-092a-1作为靶向提高scnn1b表达的靶点在制备治疗胃癌的药物中的应用。本发明提供了一种分离的寡核苷酸。根据本发明的实施例,所述寡核苷酸具有如seqidno:1所示的序列。根据本发明的实施例,发明人确定了生物样本存在胃癌的mirna生物标志物,该mirna生物标志物具有如seqidno:1所示的序列,并且确定了该mirna生物标志物与胃癌的诊断/预后以及治疗过程密切相关。其中,上述寡核苷酸的序列如seqidno:1所示:uauugcacuugucccggccugu。在本发明的最后一个方面,本发明提供了一种用于确定生物样本存在胃癌的芯片,以及相应的试剂盒。根据本发明的实施例,所述试剂盒包含探针,所述探针特异性识别具有如seqidno:1所示序列的所述的寡核苷酸。利用根据本发明的实施例的试剂盒,能够有效地确定生物样品是否存在胃癌。本发明可以直接将生物样本中提取分离出完整无降解的rna,经过荧光标记,利用生物芯片杂交技术进行芯片扫描和分析,从而确定生物体是否存在胃癌。本发明优点在于:本发明收集胃癌患者和正常人的血浆对全基因组mir表达谱进行研究。研究结果揭示了一系列mirs与胃癌相关,其中发现分子标记物hsa-mir-092a-1作为靶向提高scnn1b表达的靶点,在胃癌中具有显著低表达的现象;为有效控制治疗胃癌提供全新的治疗靶点。附图说明图1逆转录pcr检测scnn1b在胃癌细胞株及正常胃组织中的表达:在检测的16株胃癌细胞中,scnn1b在其中的13株胃癌细胞表达沉默。甲基化特异性pcr检测发现scnnlb的表达水平下调与其启动子区高甲基化相关。图2胃癌和正常细胞中scnn1b和hsa-mir-092a-1rna表达量变化图具体实施方式实施例1胃癌中差异mir分析1、样本的确定本实验选择来自香港威尔斯亲王医院的大样本胃癌临床队列研究((1998年-2002年,平均随访时间为40.8月,最长至157.9月),并保证每例病例都有5年以上的随访资料以及完整的临床信息。该队列研究纳入245例病例,均为未行新辅助治疗而直接手术切除并同时病理证实为原发性胃癌的患者。所有胃癌病例信息及组织样本收集前,均经过香港中文大学临床研究伦理委员会审议批准,并获得患者及其家属的知情同意。胃癌手术过程中收集胃癌组织及其配对的远端非肿瘤胃组织。标本收集后分为三份,一份进行临床病理验证,一份置入10%福尔马林固定24h(后续以石蜡包埋,制备组织芯片),一份迅速保存在液氮中备用(以待稍后提取组织rna和蛋白)。同时收集患者流行病学资料、影像学及其他临床资料,包括有效随访资料,供分子生物学研究。并进行有效随访.所有组织、临床资料和均纳入实验室组织库统一管理。我们将纳入本研究的大型临床队列研究的245例胃癌组织样本制作成组织芯片,通过下载tcga数据库中rna表达数据(rnaseq),比较胃癌组织与正常组织mir表达水平上的差异。通过研究发现,scnn1b蛋白在胃癌中低表达;同时通过图1的胃癌细胞和正常细胞的全基因组分析可以发现,scnn1b基本上在胃癌细胞中不表达。同时我们发现hsa-mir-092a-1能够靶向scnn1b,从图2的结果可以发现发现,hsa-mir-092a-1高表达时,相应的scnn1b也高表达。这一无法预料到的发现,显示出了惊人的医学价值。实施例2高表达hsa-mir-092a-1对癌细胞作用情况将胃癌细胞株ags,bgc823进行培养;所用培养基为含10%胎牛血清、100u/ml青霉素和100wg/ml链霉素的高搪dmem培养基(dulbecco'smodifiedeagle'smedium,gibco-invitrogen,carlsbad,ca,usa)。细胞置于37℃,5%co2和饱和湿度的无菌恒温箱内培养。正常生长情况下2-4天换一次培养液,通过0.25%胰酶(trypsin-edtasolution,gibco-invitrogen,carlsbad,ca,usa)将细胞1:3或1:4传代。构建过表达hsa-mir-092a-1载体:将mir-092a-1序列及其侧翼序列克隆至pmd19-t载体,由上海桑尼生物科技有限公司测序。结果显示mir-092a-1序列正确,将测序确认的mir-092a-1序列及其侧翼序列做亚克隆,插入pcdh-cmv-mcs-efl-gfp+puro载体的ecori/bamhi之间。载体命名为pcdh-cmv-mir-092a-1-efl-gfp+puro。将载体转染入293t细胞中,构建慢病毒载体。病毒感染及抗性筛选稳转细胞株:在六孔板中无抗完全培养基中接种2.0x106个细胞,37℃、5%co2过夜,稀释病毒:稀释液(靶细胞维持液培养基)1000ul+终浓度5μg/mlpolybrene,将慢病毒原液(100ul)加入到稀释液中(此时细胞个数按1x106计,即μ0ι=10);移去细胞培养液,加入step2稀释后的病毒液,同时建立对照(blank、negative),37℃、5%co2过夜(感染时细胞融合度为70-80%),移去细胞侵染后的病毒液,加入2ml完全培液,37℃、5%co2过夜;根据细胞状态,进行常规传代,传代同时(感染后72h),换用含嘌呤霉素(puro终浓度lμg/ml)的完全培养基以进行抗性筛选;以后每隔两天换用新的含puro的培养基,直至blank组细胞全部死亡;将存活下来的细胞换用含一半筛选浓度药物的培养基培养,进行为期一周的抗性维持。最后采用荧光定量pcr的实验方法筛选过表达细胞。通过pcr以及提取质粒鉴定,阳性细胞的mir表达量可以提高200%左右。为了鉴定靶向蛋白scnn1b的表达情况,采用荧光定量pcr进行检查,引物、条件、体系如下:1)real-timepcr反应体系(总体系15μl):2)real-timepcr反应程序:(3)引物对:通过实时定量荧光pcr法对上述转染胃癌中scnn1b基因的mrna表达水平进行再次验证,通过比较,同样也发现scnn1b在胃癌细胞ags,bgc823中的mrna表达水平提高185%和190%。另外,通过细胞生长曲线分析同样也发现过表达mir的胃癌细胞株ags,bgc823的生长速度明显低于只转染空载体的细胞株,生长速度分别下降89%和87%。这提示mir-092a-1可以靶向提高scnn1b的表达,进而抑制胃癌细胞的增殖。实施例3mir-092a-1检测胃癌中的应用将20例新的胃癌患者与20例正常患者的血清一起打乱进行盲测。提取mirna步骤按照本领域常规的方法进行。制备特异性结合mir-092a-1的检测芯片,其中芯片上面每一个孔均锚定有能够特异性集合mir-092a-1的检测探针,其序列与uauugcacuugucccggccugu反向互补配对。采用微珠捕获反应进行检测,所述芯片检测通过液相芯片检测仪对反应产物进行检测,通过检测发现,20例高mfi的样本均为胃癌患者,其平均结果如下,mirna胃癌患者(mfi)非胃癌人群(mfi)p值mir-092a-11.08990(0.5023-1.4568)8.9632(7.1375-9.9234)p<0.05通过这个检测发现,mir-092a-1可以高特异性的用于初步筛选胃癌患者,具有较好的应用前景。尽管本发明的具体实施方式已经得到详细的描述,本领域技术人员将会理解。根据已经公开的所有教导,可以对那些细节进行各种修改和替换,这些改变均在本发明的保护范围之内。本发明的全部范围由所附权利要求及其任何等同物给出。序列表〈110〉申永智〈120〉一种癌症诊断芯片及其试剂盒〈210〉1<212>rna<213>人工序列<400>mir-092a-1uauugcacuugucccggccugu〈210〉2<212>rna<213>人工序列<400>fagacaaccacaatggcttaaca〈210〉3<212>rna<213>人工序列<400>rtgaggctacatagtctcatggc当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1