本发明涉及生物技术领域,尤其涉及靶向药物分子领域,具体涉及一种具有双重靶向性和选择性的抗肿瘤多肽分子及其应用。
背景技术:
癌症是威胁全球人类生命的最大杀手之一,癌症治疗是当前医学研究所面临的一个重大挑战。化学治疗与手术治疗、放射治疗并列为癌症治疗的三大基本手段,在癌症治疗中占有重要地位。但是,传统的化疗药物由于其本身的诸多缺点和毒副作用,在杀死肿瘤细胞时,会给人体正常细胞也带来严重的损伤,导致不同副作用的产生,比如骨髓抑制、白细胞减少、患者疲乏无力、抵抗力下降、易感染、发热、出血等,大大降低了患者的生存质量,某些时候甚至由于出现严重的不良反应而被迫停止治疗。
因此,减少化疗药物的耐药,提高癌症治疗疗效,并克服化疗的毒副作用和提高患者的生活质量是化疗药物研发的重要目标。当代化疗药物研发已经进入“精准”靶向药物分子设计时代,针对已经明确的致癌位点,以“靶标-配体”的精准相互作用为基础来设计相应的治疗药物,药物进入体内会特异地选择致癌位点来相结合发生作用,使肿瘤细胞特异性死亡,而不影响正常细胞、组织或器官的功能。近些年,不断有小分子靶向抗肿瘤药物的新产品上市,如吉非替尼、克唑替尼、埃克替尼等,还有数百个产品正处于临床研发阶段。
小分子靶向药物的种类有多种,目前研究和利用能够靶向性杀伤肿瘤细胞而在正常细胞位置保持分子结构的完整性和细胞无毒性的小分子药物,相比于其他的靶向药物将更加具有广泛的应用价值。
技术实现要素:
本发明的目的在于提供一种具有双重靶向性和选择性的抗肿瘤多肽分子及其应用,其能够在正常细胞位置保持分子结构的完整性和细胞无毒性,而在肿瘤细胞位置释放出细胞杀伤性片段,从而实现对肿瘤细胞的选择性杀伤;同时其对肿瘤细胞具有双重靶向性。
本发明一方面提供了一种具有双重靶向性和选择性的抗肿瘤多肽分子,所述抗肿瘤多肽分子具有如下序列:ac-arg-gly-asp-gly-pro-leu-gly-leu-ala-gly-ile-ile-ile-gly-arg-arg-arg-arg-arg-arg-arg-arg-nh2(rr22),具体结构如下:
其中,arg为精氨酸,gly为甘氨酸,asp为天冬氨酸,pro为脯氨酸,ala为丙氨酸,ile为异亮氨酸;
所述抗肿瘤多肽分子能够被基质金属蛋白酶酶解,释放出具有肿瘤细胞杀伤性的lr15片段,所述lr15片段为
leu-ala-gly-ile-ile-ile-gly-arg-arg-arg-arg-arg-arg-arg-arg-nh2。
作为优选技术方案,所述抗肿瘤多肽分子含有:提高与癌细胞特异性结合能力的arg-gly-asp片段,具有基质金属蛋白酶响应性的gly-pro-leu-gly-leu-ala片段,赋予分子疏水性的ile-ile-ile片段,以及利于分子与细胞相互作用的arg-arg-arg-arg-arg-arg-arg-arg片段。
本发明另一方面提供了由上述具有双重靶向性和选择性的抗肿瘤多肽分子制备得到的肿瘤细胞选择性杀伤剂。由于上述技术方案所提供的抗肿瘤多肽分子具有arg-gly-asp片段,通过该片段可识别性结合肿瘤细胞表面的整合素,同时,所述抗肿瘤多肽分子能够被基质金属蛋白酶酶解,释放出具有肿瘤细胞杀伤性的lr15片段
leu-ala-gly-ile-ile-ile-gly-arg-arg-arg-arg-arg-arg-arg-arg-nh2,
因此,所述抗肿瘤多肽分子可制备成为肿瘤细胞选择性杀伤剂。
作为优选技术方案,所述肿瘤细胞选择性杀伤剂为将上述抗肿瘤多肽分子溶解于ph为7.0的tris缓冲液中。
本发明再一方面提供了由上述具有双重靶向性和选择性的抗肿瘤多肽分子在制备肿瘤细胞选择性杀伤剂中的应用。
作为优选技术方案,所述抗肿瘤多肽分子的浓度≤100μm时,对人体和动物正常细胞不具有毒性;所述抗肿瘤多肽分子的浓度为50-100μm时,对人体肿瘤细胞具有高毒性和杀伤性。
作为优选技术方案,所述人体正常细胞选自人胚肾细胞293e和猴肾成纤维细胞cos7中的至少一种,所述肿瘤细胞选自人宫颈癌细胞hela、人肺癌细胞a549、人肝癌细胞hepg2中的至少一种。
与现有技术相比,本发明的优点和积极效果在于:
1、本发明提供的抗肿瘤多肽分子结构中具有提高与癌细胞特异性结合能力的片段,具有基质金属蛋白酶响应性的片段,赋予分子疏水性的片段,以及利于分子与细胞相互作用的片段,含有ile-ile-ile片段的疏水性区域与arg-arg-arg-arg-arg-arg-arg-arg片段连接形成两亲性序列,具有细胞杀伤功能;不同的功能片段通过gly残基连接,能够保证这些片段的自由构象和功能发挥。
2、本发明提供的抗肿瘤多肽分子在正常细胞位置保持分子结构的完整性和细胞无毒性,而在肿瘤细胞位置释放出细胞杀伤性片段,从而实现对肿瘤细胞的选择性杀伤,具有“智能性”。
3、本发明提供的抗肿瘤多肽分子一方面通过rgd片段即arg-gly-asp片段识别性结合肿瘤细胞表面的整合素,另一方面能够被肿瘤细胞所过量表达的基质金属蛋白酶酶解从而释放出细胞杀伤性片段,而对正常细胞无响应,从而使得该多肽分子具有双重靶向性杀伤肿瘤细胞的功能。
4、本发明提供的抗肿瘤多肽分子可用于制备肿瘤细胞选择性杀伤剂,在多肽分子的浓度≤100μm时,对人体以及动物的正常细胞不具有毒性,但是浓度为50-100μm时,对人体肿瘤细胞具有高毒性和杀伤性。
附图说明
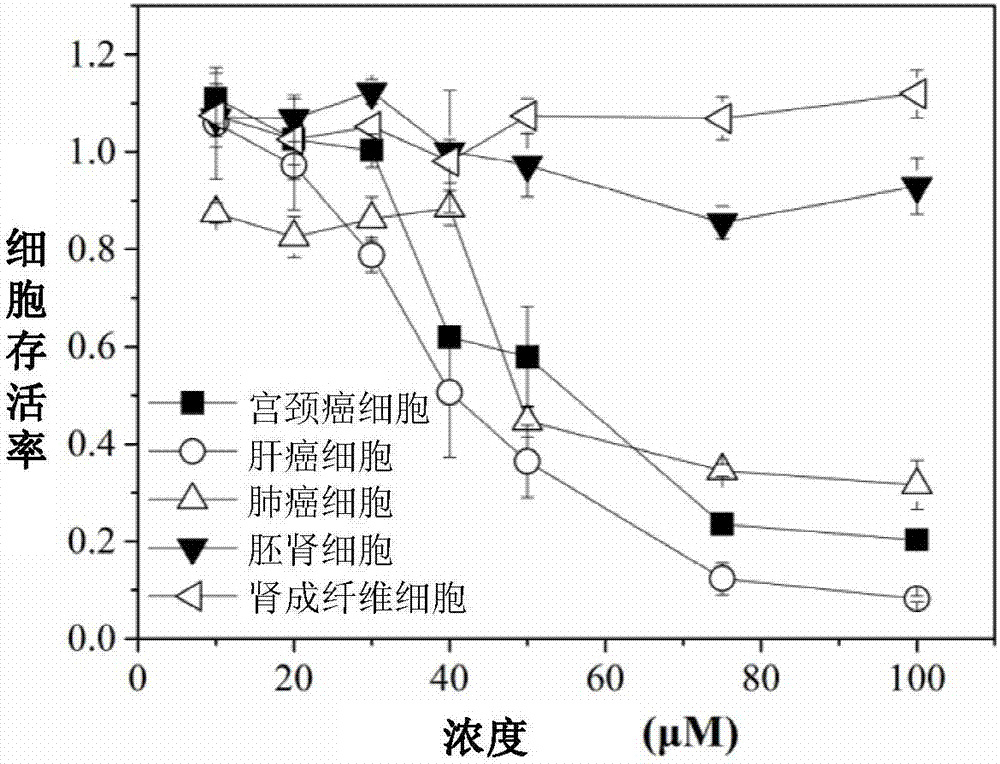
图1为本发明实施例所提供的不同种类的细胞在抗肿瘤多肽分子rr22存在下培养48h的存活率表征图;
图2(a)为本发明实施例所提供的多肽分子rr22在基质金属蛋白酶mmp7处理前(上图)和后(下图)的质谱结果图;
图2(b)为本发明实施例所提供的多肽分子rr22被基质金属蛋白酶mmp7酶解的理论片段释放图;
图3为本发明实施例所提供的正常细胞和癌细胞在不同多肽分子(a)gr19,(b)lr15存在下培养48h的存活率表征图。
具体实施方式
下面将对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
本发明实施例提供了一种具有双重靶向性和选择性的抗肿瘤多肽分子,还提供了上述具有双重靶向性和选择性的抗肿瘤多肽分子在制备肿瘤细胞选择性杀伤剂中的应用。
为了更清楚详细地介绍本发明实施例所提供的具有双重靶向性和选择性的抗肿瘤多肽分子,以下将结合具体实施例进行说明。
实施例1
具有双重靶向性和选择性的抗肿瘤多肽分子的合成(以合成0.25mmol肽分子为例)
1、材料
(1)称取负载量为0.318mmol/g的mbha树脂0.982g,dcm溶胀一夜;
(2)配制浓度为0.2mol/l的下列氨基酸的dmf(二甲基甲酰胺)溶液:
fmoc-ala-oh(n-芴甲氧羰酰基-丙氨酸):体积11ml,质量0.82g;
fmoc-gly-oh(n-芴甲氧羰酰基-甘氨酸):体积56ml,质量1.90g;
fmoc-pro-oh(n-芴甲氧羰酰基-脯氨酸):体积11ml,质量0.74g;
fmoc-ile-oh(n-芴甲氧羰酰基-异亮氨酸):体积32ml,质量2.26g;
fmoc-lys(boc)-oh(n-芴甲氧羰酰基-n’-叔丁氧羰酰基-赖氨酸):体积32ml,质量3.00g;
fmoc-arg(pbf)-oh(n-芴甲氧羰酰基-2,2,4,6,7-五甲基二氢苯并呋喃-5-磺酰-精氨酸):体积84ml,质量10.92g;
fmoc-leu-oh(n-芴甲氧羰酰基-亮氨酸):体积21ml,质量1.51g;
fmoc-d-asp-otbu(n-芴甲氧羰基-d-天冬氨酸-1-叔丁酯):体积1ml,质量0.96g;
配置上述溶液后,充分搅拌溶解,氨基酸用量均以2倍计算,保证充分反应。
(3)配制下列合成试剂:
a)活化剂(0.45mhbtu、0.45mhobt的dmf溶液):称取11.44ghbtu和4.07ghobt充分溶解于67mldmf溶液;
b)活化碱(2mdiea的dmf溶液):量取11.84ml二异丙基乙胺(diea)和22.17mldmf充分混合;
c)脱保护剂(20%(v/v)哌啶/0.1mhobt的dmf溶液):量取74.8ml哌啶,称取5.05ghobt充分溶解于300ml的dmf溶液;
d)盖帽剂(20%(v/v)乙酸酐、0.125mdiea、0.015mhobt的dmf溶液):量取2.2ml乙酸酐、0.24mldiea,称取0.0223ghobt,充分溶解于8.8mldmf溶液;
e)裂解剂(体积比tfa:tis:water=95:2.5:2.5):量取14.25mltfa,0.375mltis,0.375mlwater充分混合。
(4)利用cem公司的liberty微波多肽合成仪、应用fmoc固相合成法合成多肽,得到尚未裂解的连接有树脂的多肽粗产品。
(5)反应完成后将反应液转移到旋蒸瓶内,在35℃条件下真空旋转蒸发,除去dcm(二氯甲烷)、tfa等残余液体。用滴管将旋转蒸发后的液体逐滴加入7-8倍残液体积的冰乙醚内,静置产生沉淀后,用高速冷冻离心机在9000rpm、4℃条件下离心10min,反复乙醚沉淀,离心5-6次。除去上层清液,保留沉淀,通风橱内待乙醚挥发完之后,向沉淀中加超纯水,超声摇匀,放入冰箱中预冻1h,再使用冻干机-60℃冷冻干燥24h左右,得到纯化产品,即两亲性多肽,于-20℃密封保存。
实施例2
具有双重靶向性和选择性的抗肿瘤多肽分子的细胞毒性试验
首先在无菌的96孔板中接种100μl密度为1×105细胞/ml的细胞,置于37℃培养箱中24h,待其贴壁后将孔板中的培养液吸出,向每个孔中加入100μl新鲜培养液和100μl经过过滤的不同浓度的多肽溶液,每个浓度设立4个平行abspeptide,另外用只加tris(三羟甲基氨基甲烷)缓冲液、不加多肽的孔作为对照组abstris,之后将孔板重新置于37℃培养箱中48h,作用完成后,向每个孔中加入20μl浓度为5mg/ml的mtt(3-(4,5-二甲基噻唑-2)-2,5-二苯基四氮唑溴盐)溶液,培养箱中继续培养4h,之后将孔板中的液体吸出,在每个孔中加入150μl的二甲基亚砜,并向空白孔中加入等量的二甲基亚砜作为调零孔absblank,然后将孔板置于摇床上震荡10min使之充分混匀,最后用酶标仪测定570nm处的吸光值。细胞存活率的计算公式为:
细胞存活率=1-(abstris-abspeptide)/(abstris-absblank)
由图1可以看出,多肽分子的浓度在100μm以下与细胞共培养48小时,人胚肾细胞293e、猴肾成纤维细胞cos7的存活率都在90%以上,也就是说该多肽分子在浓度100μm以下时对所研究的人体和动物的正常细胞基本没有毒性;而50μm浓度以上细胞共培养48小时,对人宫颈癌细胞hela、人肺癌细胞a549、人肝癌细胞hepg2有明显杀伤,存活率降至50%以下,因此,由图1可知,该肽分子100μm浓度以下对人体癌细胞具有选择性杀伤能力。
实施例3
酶解试验
用ph7.0的tris缓冲液配制多肽分子:
ac-arg-gly-asp-gly-pro-leu-gly-leu-ala-gly-ile-ile-ile-gly-arg-arg-arg-arg-arg-arg-arg-arg-nh2(rr22)的溶液,其浓度为100μm,取出部分溶液加入基质金属蛋白酶mmp7作用,对样品进行质谱表征。
结果如图2所示,图2(a)的质谱图和图2(b)均表明基质金属蛋白酶mmp7可以成功酶解多肽分子,释放出两亲性的
leu-ala-gly-ile-ile-ile-gly-arg-arg-arg-arg-arg-arg-arg-arg-nh2(lr15)片段。
实施例4
不同多肽分子的细胞毒性试验
作为对比控制实验,合成如下分子:
(a)
ac-gly-pro-leu-gly-leu-ala-gly-ile-ile-ile-gly-arg-arg-arg-arg-arg-arg-arg-arg-nh2(gr19);
(b)实施例3的lr15;
测试上述三种多肽分子gr19和lr15的细胞毒性,具体实验方法与实施例2相同,与实施例2的多肽分子
ac-arg-gly-asp-gly-pro-leu-gly-leu-ala-gly-ile-ile-ile-gly-arg-arg-arg-arg-arg-arg-arg-arg-nh2(rr22)进行细胞毒性对比。
结果如图3所示。上述3个分子对正常细胞和肿瘤细胞都有明显毒性,而没有选择性。其中,gr19不具有细胞选择性杀伤能力与rr22的细胞选择性杀伤能力对比,说明rgd片段即arg-gly-asp片段对肿瘤细胞的特异性结合提高了分子的细胞选择性杀伤能力;lr15的细胞杀伤能力来源于其两亲性结构,与rr22在100μm浓度以下不具有对正常细胞的杀伤能力对比,说明只有在肿瘤细胞环境中,过量表达的mmp7酶酶解rr22分子释放出lr15片段之后,才激活了分子的细胞杀伤能力,因此,本发明的抗肿瘤多肽分子具有“智能性”和双重靶向性。