核酸样品制备方法与流程
本申请根据35u.s.c.§119(e)要求于2016年9月15日提交的美国临时专利申请no.62/395,339的优先权,其通过引用整体并入本文。
本文描述的技术涉及可用于制备用于分析的核酸分子的方法和组合物。
背景技术:
在下一代测序之前的靶标富集比全基因组、全外显子组和整个转录组测序更具成本效益,因此对于用于研究发现和临床应用的广泛实施更加实用。例如,由靶标富集方法提供的高覆盖深度使等位基因计数(在基因表达和拷贝数评估中)和低频突变的检测能够具有更宽的动态范围,这有利于评估癌症中的体细胞突变。用于下一代测序的当前富集方案的实例包括基于杂交的捕获测定(truseqcapture,illumina;sureselecthybridcapture,agilent)和基于聚合酶链式反应(pcr)的测定(haloplex,agilent;ampliseq,iontorrent;truseqamplicon,illumina;emulsion/digitalpcr,raindance)。基于杂交的方法不仅捕获由捕获探针覆盖的靶序列,而且捕获消耗测序能力的脱靶基因附近。另外,这些方法相对耗时、劳动强度大,并且具有相对低的特异性水平。
发明概述
本文公开的技术方面涉及制备和分析核酸的方法。在一些实施方案中,本文提供了可用于制备用于序列分析(例如,使用下一代测序)的核酸样品的方法和组合物。在一些实施方案中,本文描述的技术涉及确定核酸序列的方法。在一些实施方案中,本文所述的方法和组合物涉及在测序之前富集包含一种或更多种靶核苷酸序列的核酸。在一些方面,本公开内容提供了制备核酸(例如,用于测序分析)的方法,其涉及将一个或更多个以捕获部分修饰的核苷酸添加至核酸。在一些实施方案中,该方法还涉及将衔接子核酸与已添加以捕获部分修饰的核苷酸的核酸连接以产生连接产物。在一些实施方案中,该方法还涉及通过使连接产物与以捕获部分修饰的核苷酸的捕获部分的结合配偶体接触来捕获连接产物。在一些实施方案中,该方法还涉及扩增连接产物,例如通过聚合酶链式反应或另外的合适的扩增方法。在一些实施方案中,提供了用于制备核酸的方法,所述核酸涉及将一个或更多个核苷酸添加至包含靶核苷酸序列的核酸(例如,双链核酸)的3’端,其中一个或更多个核苷酸中的至少一个是以捕获部分修饰的核苷酸。在一些实施方案中,在核酸的3’端存在以捕获部分修饰的核苷酸有助于核酸的分离、纯化和/或洗涤,同时避免在整个核酸中并入经修饰的核苷酸(例如,随机地)。在一些实施方案中,提供了用于制备核酸的方法,其涉及将一个或更多个核苷酸并入包含靶核苷酸序列的核酸(例如,双链核酸)中,其中所述一个或更多个核苷酸中的至少一个是以捕获部分修饰的核苷酸。在一些实施方案中,使用引物(例如,逆转录引物)并入一个或更多个核苷酸。在一些实施方案中,在制备核酸的早起步骤期间并入一个或更多个核苷酸。例如,在一些实施方案中,在片段化、随机引发、第一链合成、第二链合成和/或末端修复期间并入一个或更多个核苷酸。
在一些方面,本公开内容提供了制备用于分析的核酸的方法,其中所述方法包括:(a)将一个或更多个核苷酸添加至包含靶核苷酸序列的双链核酸的3’端,其中一个或更多个核苷酸中的至少一个是以捕获部分修饰的核苷酸;(b)将衔接子核酸与已添加以捕获部分修饰的核苷酸的双链核酸连接以产生连接产物,其中位于衔接子核酸的3’端的一个或更多个核苷酸的序列与步骤(a)中添加至双链核酸的3’端的一个或更多个核苷酸互补;(c)通过使连接产物与以捕获部分修饰的核苷酸的捕获部分的结合配偶体接触来捕获连接产物;(d)通过聚合酶链式反应使用与靶核苷酸序列特异性退火的第一靶特异性引物和与衔接子核酸的互补序列特异性退火的第一衔接子引物来扩增连接产物。
在一些实施方案中,步骤(b)包括在连接酶连接衔接子核酸与双链核酸的条件下组合衔接子核酸、双链核酸和连接酶。在一些实施方案中,与双链核酸组合的衔接子核酸包含双链体部分和单链突出端(overhang)序列。在一些实施方案中,单链突出端序列包含位于衔接子核酸的3’端的一个或更多个核苷酸的序列,其与步骤(a)中添加至双链核酸的3’端的一个或更多个核苷酸互补。
在一些实施方案中,步骤(b)包括在连接酶连接衔接子核酸与双链核酸的条件下组合衔接子核酸、双链核酸和连接酶,其中与双链核酸组合的衔接子核酸是单链的。
在一些实施方案中,本文提供的方法还包括:(e)通过聚合酶链式反应使用第二衔接子引物和第二靶特异性引物扩增步骤(d)的扩增产物。在一些实施方案中,第二靶特异性引物相对于第一靶特异性引物嵌套(nested)。在一些实施方案中,第二靶特异性引物包含不与靶核苷酸序列退火的5’尾。在一些实施方案中,该方法还包括添加另外的引物,其包含与第二靶特异性引物的5’尾相同的3’部分。
在一些实施方案中,捕获部分是生物素部分。在一些实施方案中,生物素部分包含生物素-三甘醇、双-生物素、可光裂解生物素、脱硫生物素、脱硫生物素-三甘醇或生物素叠氮化物。
在一些实施方案中,以捕获部分修饰的核苷酸包含选自腺嘌呤、鸟嘌呤、胸腺嘧啶、尿嘧啶和胞嘧啶的核碱基,或其衍生物。在一些实施方案中,以捕获部分修饰的核苷酸包含腺嘌呤核碱基或其衍生物。在一些实施方案中,捕获部分与腺嘌呤核碱基或其衍生物的第5、6、7或8位处共价连接。在一些实施方案中,捕获部分与腺嘌呤核碱基的第7位处共价连接。在一些实施方案中,腺嘌呤核碱基中的第7位是碳原子。
在一些实施方案中,生物素部分通过任何合适长度的接头与核碱基共价连接。在一些实施方案中,生物素部分与核碱基共价连接,例如,通过长度为5至20个原子的接头(例如,长度为5个、6个、7个、8个、9个、10个、11个、12个、13个、14个、15个、16个、17个、18个、19个、20个原子)。在一些实施方案中,以捕获部分修饰的核苷酸是生物素-n-dntp,其中n是5至20的整数,其代表生物素部分的羰基与ntp核碱基上的附接位置之间的接头原子数。
在一些实施方案中,结合配偶体是链霉抗生物素蛋白。在一些实施方案中,链霉抗生物素蛋白与顺磁珠附接。
在一些实施方案中,在步骤(a)中,将一个核苷酸添加至包含靶核苷酸序列的双链核酸的3’端。
在一些实施方案中,方法还包括纯化非特异性核酸。在一些实施方案中,本文提供的方法还包括在步骤(b)之后和在步骤(c)之前的反应净化或洗涤步骤。在一些实施方案中,该方法还包括在步骤(c)之后和在步骤(d)之前:i)将包含以捕获部分修饰的核苷酸的双链核酸固定在顺磁性基底或表面上(例如,聚苯乙烯顺磁珠);和ii)洗涤经固定的双链核酸。在一些实施方案中,该方法在步骤(ii)之后还包括:iii)从顺磁性基底或表面释放经洗涤的经固定的双链核酸。在一些实施方案中,经洗涤的经固定的双链核酸通过与化学试剂接触和/或施加热量而从顺磁性基底或表面释放。在一些实施方案中,化学试剂是碱或碱性溶液。在一些实施方案中,化学试剂包含氢氧化钠(naoh)。应当理解,在一些实施方案中,接触可包括混合两种溶液(例如,一种溶液包含碱,另一种溶液包含经洗涤的经固定的核酸)、向溶液中添加固体,或向固体中添加溶液。在一些实施方案中,经洗涤的经固定的双链核酸通过与naoh接触并加热(例如,加热至室温以上,例如25至90℃、25至70℃、25至50℃、35至65℃、35至45℃、30至40℃、40至50℃的温度范围)从顺磁性基底或表面释放。在一些实施方案中,经洗涤的经固定的双链核酸保留在顺磁性基底或表面上,例如用于进一步制备用于分析。在一些实施方案中,在进一步制备用于分析之前,将经洗涤的经固定的双链核酸从顺磁性基底或表面释放。
在一些实施方案中,本文提供的方法还包括在步骤(a)之前对双链核酸进行5’磷酸化。
在一些实施方案中,本文提供的方法还包括,在步骤(a)之前:i)通过使用rna制备物作为模板进行随机引发的第一链合成反应和使用随机引发的第一链合成反应的产物作为模板进行第二链合成反应来制备cdna;以及ii)对cdna进行末端修复以产生平末端双链核酸。在一些实施方案中,该方法还包括在步骤ii)之后:iii)将包含以捕获部分修饰的核苷酸的双链核酸固定在顺磁性基底或表面上;iv)洗涤经固定的双链核酸;以及v)从顺磁性基底或表面释放经洗涤的经固定的双链核酸。在一些实施方案中,顺磁性基底或表面包含涂层(例如,聚苯乙烯涂层)。在一些实施方案中,通过进行基因特异性引发的第一链合成来制备cdna用于分析。在一些实施方案中,末端修复涉及使dna末端钝化和/或磷酸化。
在一些实施方案中,方法还包括,在步骤(e)之后:(f)将步骤(e)的扩增产物固定在顺磁性基底或表面上;(g)洗涤经固定的扩增产物;以及(h)从顺磁性基底或表面上释放经洗涤的经固定的扩增产物。在一些实施方案中,该方法还包括一个或更多个居间洗涤步骤(例如,在本文所述方法的任意步骤之间洗涤扩增产物)。例如,在一些实施方案中,该方法还包括在步骤(e)之后和在步骤(f)之前的洗涤步骤。
在一些实施方案中,在步骤(b)中,双链核酸在拥挤剂(crowdingagent)存在下与衔接子核酸连接。在一些实施方案中,拥挤剂是聚乙二醇,其量占连接混合物的5%至50%。在一些实施方案中,双链核酸是平末端的。在一些实施方案中,双链核酸包含单链突出端。
在一些方面,本公开内容提供了制备用于分析的核酸的方法,其中所述方法包括:(a)通过使用rna制备物作为模板进行随机引发的第一链合成反应和使用随机引发的第一链合成反应的产物作为模板进行第二链合成反应来制备cdna,其中rna制备物包含靶核苷酸序列;(b)对cdna进行末端修复以产生包含靶核苷酸序列的平末端双链核酸;(c)将平末端双链核酸固定在顺磁性基底或表面上;(d)洗涤经固定的平末端双链核酸;(e)从顺磁性基底或表面释放经洗涤的经固定的平末端双链核酸;(f)将一个或更多个核苷酸添加至释放的平末端双链核酸的3’端;(g)将包含可连接双链体部分和单链突出端序列的衔接子与步骤(f)所产生的核酸连接以产生连接产物,其中单链突出端序列与一个或更多个核苷酸互补;(h)通过聚合酶链式反应使用与靶核苷酸序列特异性退火的第一靶特异性引物和与衔接子核酸的互补序列特异性退火的第一衔接子引物来扩增连接产物;(i)通过聚合酶链式反应使用第二衔接子引物和第二靶特异性引物扩增步骤(h)的扩增产物,其中第二靶特异性引物相对于第一靶特异性引物嵌套;(j)将步骤(i)的扩增产物固定在顺磁性基底或表面上;(k)洗涤经固定的扩增产物;(1)从顺磁性基底或表面释放经洗涤的经固定的扩增产物。在一些实施方案中,在不洗涤连接产物的情况下进行步骤(h)。
在一些方面,本公开内容提供了制备用于分析的核酸的方法,其中所述方法包括:(a)通过使用核酸制备物作为模板进行随机引发的第一链合成反应和使用随机引发的第一链合成反应的产物作为模板进行第二链合成反应来制备cdna,其中核酸制备物包含靶核苷酸序列;(b)对cdna进行末端修复以产生包含靶核苷酸序列的平末端双链核酸;(c)洗涤平末端双链核酸;(d)将一个或更多个核苷酸添加至步骤(c)中经洗涤的核酸的3’端,任选地其中一个或更多个核苷酸中的至少一个是以捕获部分修饰的核苷酸;(e)洗涤步骤(d)所产生的核酸;(f)将包含可连接双链体部分和单链突出端序列的衔接子核酸与步骤(e)中经洗涤的核酸连接以产生连接产物,其中单链突出端序列与一个或更多个核苷酸互补;(g)通过聚合酶链式反应使用与靶核苷酸序列特异性退火的第一靶特异性引物和与衔接子核酸的互补序列特异性退火的第一衔接子引物来扩增连接产物;(h)通过聚合酶链式反应使用第二衔接子引物和第二靶特异性引物扩增步骤(g)的扩增产物,其中第二靶特异性引物相对于第一靶特异性引物嵌套;以及(j)洗涤步骤(h)的扩增产物。
在一些实施方案中,使用固相可逆固定技术进行洗涤步骤。
在一些实施方案中,一个或更多个核苷酸中的至少一个是以捕获部分修饰的核苷酸,并且所述方法还包括在步骤(f)之后和在步骤(g)之前使用以捕获部分修饰的核苷酸的捕获部分的经固定的结合配偶体来捕获连接产物;以及清洁捕获的连接产物。在一些实施方案中,捕获部分包含生物素部分,并且结合配偶体包含链霉抗生物素蛋白。
在一些实施方案中,第二衔接子引物相对于第一衔接子引物嵌套。在一些实施方案中,第二衔接子引物与衔接子核酸的互补序列特异性退火。
当结合附图考虑时,根据本发明的多种非限制性实施方案的以下详细描述,本公开内容的其他优点和新颖特征变得显而易见。在本说明书和通过引用并入的文件包含冲突和/或不一致的公开内容的情况下,以本说明书为准。
附图简述
将参考附图通过示例描述本发明的非限制性实施方案,附图是示意性的并且不旨在按比例绘制。在附图中,所示的每个相同或几乎相同的部件通常由单个数字表示。为了清楚起见,并非每个部件都标记在每个图中,在说明不是使本领域的普通技术人员理解本发明所必需的情况下,也没有在附图中展示本发明的每个实施方案的每个部件。在图中:
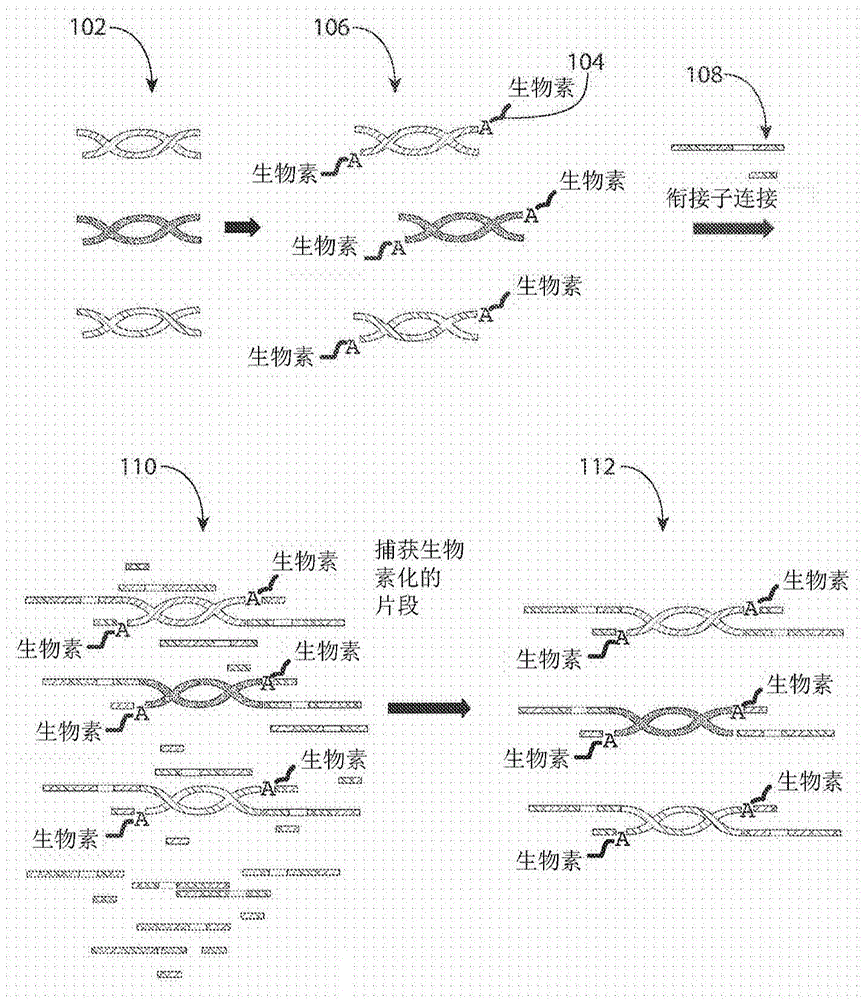
图1是允许捕获衔接子连接的核酸文库的方法的说明。
图2是制备用于分析的高保真核酸样品的方法的说明。
图3示出了使用模板rna链产生双链cdna样品的过程。
图4示出了使用模板rna链产生双链cdna样品的过程,其中在扩增之前从顺磁珠上洗脱捕获的连接产物。
图5是制备用于分析的高保真核酸样品的方法的工作流程的描述。
图6是凝胶的图像表示,其示出了在没有聚合酶失活的情况下已经进行末端修复的文库样品和在聚合酶热失活之后已经进行末端修复的文库样品。
图7是凝胶的图像表示,其示出了在不存在或存在拥挤剂的情况下连接的样品的衔接子连接效率。
图8a是说明可包含衔接子核酸的组分的图。
图8b是说明可包含第二靶特异性引物的组分的图。
发明详述
在另一些方面,本公开内容提供了与制备用于分析的核酸样品文库相关的改进技术。如本文所述,衔接子核酸可以与包含靶核苷酸序列的核酸连接。在文库准备和测序分析期间,例如,通过提供引物结合位点和分子条形码或索引序列,衔接子核酸的使用可以是有用的。在一些方面,本公开内容涉及与衔接子连接和衔接子连接的样品分离相关的过程的改进,其显著改善了分子条形码的保真度。
在一些方面,本公开内容涉及以下认识:在衔接子连接之后,将未连接的衔接子转移到随后的pcr反应中可导致分子条形码过量。该分子条形码的过量或膨胀可导致假阳性,因为一个分子应该只包含一个条形码。应当理解,在一些实施方案中,未连接的衔接子在一些情况下可以在pcr期间引发现有片段中的共有区域。在多个反应周期中,条形码或其他人工序列的另外的拷贝可以整合至单个分子内。因此,发明人已经认识和理解了需要与衔接子连接和衔接子连接的文库片段的分离相关的改进方法。
在一些方面,本公开内容提供了制备用于分析的核酸的方法,其包括:(a)将以捕获部分修饰的核苷酸添加至双链核酸(例如,cdna、grna)的3’端,连接衔接子核酸与具有以捕获部分修饰的核苷酸的双链核酸,并用以捕获部分修饰的核苷酸的结合配偶体捕获衔接子连接的核酸。
在一些实施方案中,以捕获部分修饰的核苷酸是生物素部分修饰的核苷酸。该方法的一般描述如图1所示,其提供了涉及生物素部分修饰的核苷酸的方法的非限制性实例。在该实施方案中,提供了平末端的5’磷酸化双链核酸文库102。将生物素标记的atp104添加至双链核酸的3’端以产生文库106,其包含位于片段的3’端的以捕获部分修饰的核苷酸。将文库片段与衔接子108连接以产生具有未连接的衔接子以及衔接子连接的文库片段的样品110。使用链霉抗生物素蛋白包被的表面相对于未连接的衔接子捕获或分离连接的文库片段,以产生使未连接的衔接子转移的发生最小化或消除的文库112。尽管该实施例利用生物素捕获部分,但是能够被特异性靶向用于分离(例如,通过与结合配偶体的相互作用)的任何部分可适用于本文所述的技术。
捕获部分
本文描述的技术方面涉及捕获部分用于分离目的分子(例如,核酸、连接产物等)的用途。如本文所用,“捕获部分”是指出于捕获(例如,分离/纯化)目的分子的目的而被配置成选择性地与结合配偶体相互作用的部分。
捕获部分和捕获部分的结合配偶体可包含任何合适的结合对。在一些实施方案中,结合对可通过共价或非共价结合选择性地相互作用。在一些实施方案中,结合对可通过杂交、离子键合、氢键、范德华相互作用或这些力的任何组合选择性地相互作用。在一些实施方案中,捕获部分和/或结合配偶体可包含,例如,生物素、抗生物素蛋白、链霉抗生物素蛋白、地高辛、肌苷、抗生物素蛋白、gst序列、经修饰的gst序列、生物素连接酶识别(bitag)序列、s标签、snap-标签、肠激酶位点、凝血酶位点、抗体或抗体结构域、抗体片段、抗原、受体、受体结构域、受体片段,或其组合。
在一些实施方案中,捕获部分包含生物素部分。在一些实施方案中,本文描述的技术可用于制备用于分析的核酸样品。因此,在一些实施方案中,核酸分子包含生物素化的捕获部分。在一些实施方案中,核酸分子包含至少一个包含生物素部分的以捕获部分修饰的核苷酸。在一些实施方案中,以捕获部分修饰的核苷酸包含式(i)的通式结构:
如式(i)中所示,以捕获部分修饰的核苷酸可包含与核苷酸的核碱基附接的生物素部分。例如,在一些实施方案中,生物素部分包含生物素-三甘醇、双-生物素、可光裂解生物素、脱硫生物素、脱硫生物素-三甘醇或生物素叠氮化物。以捕获部分修饰的核苷酸的非限制性实例显示在表1中。
表1.以捕获部分修饰的核苷酸的实例结构
在一些实施方案中,以捕获部分修饰的核苷酸包含捕获部分和核苷酸的核碱基之间的接头。在一些实施方案中,捕获部分通过任意合适长度的接头与核碱基共价连接。在一些实施方案中,捕获部分通过长度为5至20个原子的接头与核碱基共价连接。在一些实施方案中,接头包含脂族链。在一些实施方案中,接头包含-(ch2)n-,其中n是1至20的整数,包括端值。在一些实施方案中,n是1至10的整数,包括端值。在某些实施方案中,接头包含杂脂族链。在一些实施方案中,接头包含聚乙二醇部分。在一些实施方案中,接头包含聚丙二醇部分。在一些实施方案中,接头包含-(ch2ch2o)n-,其中n为1至20的整数,包括端值。在一些实施方案中,接头包含-(ch2ch2o)n-,其中n为1至10的整数,包括端值。在某些实施方案中,接头包含一个或更多个亚芳基。在一些实施方案中,接头包含一个或更多个亚苯基(例如,对位取代的亚苯基)。在某些实施方案中,接头包含手性中心。在某些实施方案中,接头包含一个或更多个磷酸酯、脂族链、杂脂族链和一个或更多个酰胺(例如-c(=o)nh-)。
在一些实施方案中,以捕获部分修饰的核苷酸是生物素-n-dntp,其中n是5至20的整数,其代表生物素部分的羰基与ntp核碱基上的附接位置之间的接头原子数。
在一些实施方案中,结合配偶体与不溶性支持物连接。因此,在一些实施方案中,可通过捕获部分与附接于不溶性支持物的捕获部分的结合配偶体之间形成的选择性结合相互作用将目的分子固定在不溶性支持物上。
在一些实施方案中,不溶性支持物包含珠或其他固体表面。例如,在一些实施方案中,珠是顺磁珠。珠用于分离的用途是本领域公知的,并且任何合适的珠分离方法可以与本文所述的技术一起使用。在一些实施方案中,珠可用于分离,因为感兴趣的分子可附接于珠,并且可以洗涤珠以除去未附接于珠上的溶液组分,从而允许纯化和分离。在一些实施方案中,可以基于诸如尺寸、密度或介电特性、离子特性和磁性特性将珠与溶液中的其他组分分离。
在一些实施方案中,不溶性支持物是顺磁珠。珠的使用允许通过离心或过滤,或者在顺磁珠的情况下通过施加磁场,将衍生的核酸捕获部分与反应混合物分离。在一些实施方案中,可使用磁场将顺磁珠引入、混合、取出并将其释放至溶液中。在一些实施方案中,利用顺磁珠的方法可以是自动化的。在一些实施方案中,可使用公知的化学方法使珠官能化,以提供具有合适的官能化的表面,用于连接捕获部分的结合配偶体。表面的衍生化以允许捕获部分的结合是本领域常规的。例如,用链霉抗生物素蛋白包被表面允许结合生物素化的捕获部分。用链霉抗生物素蛋白包被表面已描述于,例如,miller的美国专利no.5,374,524中。在一些实施方案中,可使用除珠之外的固体表面。在一些实施方案中,固体表面可以是平面表面,例如用于杂交微阵列的那些,或者固体表面可以是分离柱的填充物。
在一些实施方案中,捕获部分的结合配偶体可以在结合捕获部分之前,与其同时或在其之后与不溶性支持物附接。在一些实施方案中,优选使捕获部分与捕获部分的结合配偶体在二者都在溶液中时接触。在此类实施方案中,然后可通过使捕获部分:结合配偶体复合物与适当衍生的表面接触,将该复合物固定在不溶性支持物上。因此,在一些实施方案中,目的分子可通过在与目的分子附接的捕获部分和捕获部分的结合配偶体之间形成的复合物分离。
在一些实施方案中,可能需要将捕获部分与核苷酸的核碱基附接。以这种方式,3’端保持游离以任选与衔接子核酸连接,同时捕获部分可被结合配偶体捕获。在一些实施方案中,以捕获部分修饰的核苷酸包含选自腺嘌呤、鸟嘌呤、胸腺嘧啶、尿嘧啶和胞嘧啶的核碱基,或其衍生物。例如,在一些实施方案中,以捕获部分修饰的核苷酸包含腺嘌呤核碱基或其衍生物。在一些实施方案中,捕获部分与腺嘌呤核碱基或其衍生物的第5、6、7或8位处共价连接。在一些实施方案中,捕获部分与腺嘌呤核碱基的第7位处共价连接。腺嘌呤环如式(ii)所示:
在一些实施方案中,可能需要修饰与捕获部分附接的核碱基上的一个或更多个位置。例如,在一些实施方案中,腺嘌呤核碱基的7位是碳原子。然而,应当理解,任何能够形成另外的共价键的原子(例如,c、o、n、s等)可以被取代至适于附接捕获部分的核碱基上的位置。在一些实施方案中,在捕获衔接子连接的片段后,对文库进行扩增以富集靶核苷酸序列。用于分析的核酸的制备
本公开内容的方面提供了确定与已知靶核苷酸序列邻接的核苷酸序列的改进方法。传统的测序方法随机地(例如,“鸟枪”测序)或在用于设计引物的两个已知序列之间产生序列信息。相比之下,在一些实施方案中,本文所述的某些方法允许以高水平的特异性和灵敏度确定已知序列的单个区域的上游或下游的核苷酸序列(例如,测序)。
在一些实施方案中,本公开内容提供了使用下一代测序技术在确定核苷酸序列之前富集特定核苷酸序列的方法。在一些实施方案中,本文提供的方法可涉及富集包含脱氧核糖核酸(dna)的样品。在一些实施方案中,本文提供的方法包括:(a)将一个或更多个核苷酸添加至包含靶核苷酸序列的双链核酸的3’端,其中一个或更多个核苷酸中的至少一个(例如,1个、2个、3个、4个、5个或更多个)是以捕获部分修饰的核苷酸;(b)将衔接子核酸与已添加以捕获部分修饰的核苷酸的双链核酸连接以产生连接产物,其中位于衔接子核酸的3’端的一个或更多个核苷酸的序列与步骤(a)中添加至双链核酸的3’端的一个或更多个核苷酸互补;(c)通过使连接产物与以捕获部分修饰的核苷酸的捕获部分的结合配偶体接触来捕获连接产物;(d)通过聚合酶链式反应使用与靶核苷酸序列特异性退火的第一靶特异性引物和与衔接子核酸的互补序列特异性退火的第一衔接子引物来扩增连接产物。
在一些实施方案中,该方法还包括:(e)通过聚合酶链式反应使用第二衔接子引物和第二靶特异性引物扩增步骤(d)的扩增产物。例如,图2示出了可进行该实施方案的非限制性过程200。通过向3’端添加一个或更多个以捕获部分修饰的核苷酸204(例如,1个、2个、3个、4个、5个或更多个以捕获部分修饰的核苷酸),对包含靶核苷酸序列的双链核酸202进行加尾。将捕获部分标记的核酸与衔接子206连接以产生衔接子连接的文库片段208。通过引入捕获部分的结合配偶体来分离衔接子连接的片段,后者附接于磁性支持物210。施加磁场212,相对于未连接的衔接子分离衔接子连接的核酸。使用与靶核苷酸序列特异性退火的第一靶特异性引物214和与衔接子核酸的互补序列特异性退火的第一衔接子引物216对捕获的连接产物进行第一轮pcr。以这种方式,第一衔接子引物216引发由第一靶特异性引物214产生的链。使用第二靶特异性引物218和第二衔接子引物220进行第二轮pcr。如所示出的,第二靶特异性引物218相对于第一靶特异性引物214嵌套。同样如所示出的,第二靶特异性引物加尾有不与靶核苷酸序列杂交的5’区域。以与第一轮pcr相似的方式,第二衔接子引物220引发由第二靶特异性引物218产生的链。在该第二轮pcr中,另外的引物222包含在内,其包含(i)与第二靶特异性引物218的加尾5’区的至少一部分相同的3’区,和(ii)其可包含用于测序的其他元件(例如索引或条形码序列和引物结合位点)的5’区。在第二衔接子引物220从由第二靶特异性引物218产生的互补链产生有义链之后,然后另外的引物222引发现在的加尾区域的互补序列,以产生可用于测序的产物224。
在一些实施方案中,本文描述的技术允许从核酸样品中富集靶核苷酸序列。在一些实施方案中,核酸样品包含基因组dna。在一些实施方案中,核酸样品包含cdna。在一些实施方案中,可通过使用随机引发的第一链合成反应的产物作为模板进行随机引发的第一链合成反应来制备cdna,其中rna制备物包含靶核苷酸序列。在一些实施方案中,核酸测序文库由rna制备物制备。例如,图3一般性地示出了过程300,通过该过程300由rna模板制备双链核酸文库片段。
如所示出的,rna模板302在适于杂交的条件下与随机引物304(例如,随机六聚体)退火。在随机引发后,使用逆转录酶通过模板依赖性延伸实现第一链cdna合成以产生dna/rna杂合体306。dna/rna杂合体的rna链被酶促或化学切割。所得的保持与dna链310杂交的rna308片段通过聚合酶的作用用作第二链cdna合成的引物。在一些实施方案中,可能需要在第二链cdna合成后使聚合酶失活,例如,以在末端修复期间防止5’→3’和/或3’→5’核酸外切酶活性。在第二链cdna合成后,对双链cdna312进行末端修复以产生平末端的5’磷酸化cdna314。在一些实施方案中,在末端修复后进行spri净化(例如,ampure)。由于该过程中的后续步骤可能涉及将以捕获部分修饰的核苷酸添加至核酸的3’端,因此优选去除样品中的任何残留的dntp。因此,任何能够从溶液中除去dntp的净化方法都被认为适合于该技术。在一些实施方案中,以捕获部分修饰的核苷酸可以在制备核酸的较早步骤(例如,片段化、随机或特异性引发、第一链合成、第二链合成和/或末端修复)中添加至和/或并入核酸中。在这样的实施方案中,因此可能需要在添加和/或并入以捕获部分修饰的核苷酸的步骤之前进行净化步骤。
平末端的5’磷酸化cdna314加尾有在其3’端包含硫代酯键(thioatebond)(例如硫代磷酸酯键)的生物素标记的datp316(生物素-11-atp),并在与衔接子核酸连接之前进行spri净化以产生衔接子连接的文库片段318。显示包含拥挤剂(20%)可提高衔接子连接效率。通过引入链霉抗生物素蛋白包被的顺磁珠320捕获衔接子连接的片段318。一旦形成非共价的生物素-链霉抗生物素蛋白复合物,施加磁场322捕获衔接子连接的核酸,以将未连接的衔接子与所需产物分离。
如图3所示,在一些实施方案中,捕获的衔接子连接的核酸以珠固定的产物的形式进行第一轮pcr324。在另一些实施方案中,如图4所示,捕获的衔接子连接的核酸在第一轮pcr324之前从顺磁珠320洗脱。作为示例而非限制,可使用化学试剂和/或加热从珠中洗脱捕获的衔接子连接的核酸。在一些实施方案中,化学试剂是碱(例如,naoh)。在一些实施方案中,捕获的衔接子连接的核酸用低浓度(例如,小于1m、小于0.5m、小于0.1m、小于0.05m、小于0.01m、小于0.001m、小于0.0001m)的naoh洗脱。在一些实施方案中,捕获的衔接子连接的核酸用低浓度的naoh和加热洗脱。
使用与靶核苷酸序列特异性退火的第一基因特异性引物(“gsp1”)和与衔接子核酸的互补序列特异性退火的第一衔接子引物(“p5_1”),对经固定的的(例如,如在图3中)或洗脱的(例如,如在图4中)衔接子连接的核酸进行第一轮pcr324。通过这种方式,p5_1引发由gsp1产生的链。如所示出的,在一些实施方案中,gsp1(例如,第一靶特异性引物)加尾有不与靶核苷酸序列杂交的5’区域。在一些实施方案中,5’尾部区域可以防止引物二聚体,例如通过具有使引物二聚体的出现最小化的序列含量。在一些实施方案中,gsp1不加尾有5’加尾区域。如图3中进一步所示,使用第二基因特异性引物(“gsp2”)和第二衔接子引物(“p5_2”)进行第二轮pcr326。如所示出的,gsp2相对于gsp1嵌套。同样如所示出的,gsp2加尾有不与靶核苷酸序列杂交的5’区域。以与第一轮pcr相似的方式,p5_2引发gsp2产生的链。在该第二轮pcr中,另外的引物(“单引物”)包括在内,其包含(i)与gsp2的加尾5’区域的至少一部分相同的3’区域和(ii)包含可用于测序的其他元件(例如测序引物结合位点和样品索引)的5’区域。在p5_2从gsp2产生的互补链产生有义链之后,然后另外的引物引发gsp2加尾区域的现在互补的序列中引出,以产生可用于测序的产物328。
样品纯化
在一些实施方案中,可以在方法的任何适当步骤之前和/或之后从酶、引物或缓冲组分中分离靶核酸和/或其扩增产物。可使用任何合适的分离核酸的方法。在一些实施方案中,分离可包括固相可逆固定(solidphasereversibleimmobilization,spri)净化。用于spri净化的方法是本领域公知的,例如agencourtampurexp-pcrpurification(目录号a63880,beckmancoulter;brea,ca)。在一些实施方案中,酶可通过热处理失活。在一些实施方案中,通过酶处理除去未标记的dntp。
在一些实施方案中,可使用适当的方法(例如,纯化、消化等)从核酸制备物中除去未杂交的引物。在一些实施方案中,核酸酶(例如核酸外切酶i)用于从制备物中除去引物。在一些实施方案中,此类核酸酶在引物消化后被热失活。一旦核酸酶失活,可以将另一组引物与其他合适的组分(例如酶、缓冲液)一起添加以进行进一步的扩增反应。
在一些实施方案中,本文提供的方法的步骤任选地包括居间样品纯化步骤。在一些实施方案中,样品纯化步骤包括洗涤步骤。在一些实施方案中,样品纯化步骤包括spri净化(例如,ampure)。例如,制备用于分析的核酸的方法可包括:(a)通过使用rna制备物作为模板进行随机引发的第一链合成反应和使用随机引发的第一链合成反应的产物作为模板进行第二链合成反应来制备cdna,其中rna制备物包含靶核苷酸序列;(b)对cdna进行末端修复以产生包含靶核苷酸序列的平末端双链核酸;(c)将平末端双链核酸固定在顺磁性基底或表面上;(d)洗涤该经固定的的平末端双链核酸;(e)从顺磁性基底或表面释放经洗涤的经固定的平末端双链核酸;(f)将一个或更多个核苷酸添加至释放的平末端双链核酸的3’端;(g)将包含可连接双链体部分和单链突出端序列的衔接子与步骤(f)所产生的核酸连接以产生连接产物,其中单链突出端序列与一个或更多个核苷酸互补;(h)在不洗涤连接产物的情况下,通过聚合酶链式反应使用与靶核苷酸序列特异性退火的第一靶特异性引物和与衔接子核酸的互补序列特异性退火的第一衔接子引物扩增连接产物;(i)通过聚合酶链式反应使用第二衔接子引物和第二靶特异性引物扩增步骤(h)的扩增产物,其中第二靶特异性引物相对于第一靶特异性引物嵌套;(j)将步骤(i)的扩增产物固定至顺磁性基底或表面;(k)洗涤经固定的扩增产物;(1)从顺磁性基底或表面释放经洗涤的经固定的扩增产物。
在一些实施方案中,本文提供的方法的步骤任选地包括向核酸添加一个或更多个核苷酸,其中一个或更多个核苷酸中的至少一个包含捕获部分,并通过捕获部分和捕获部分的结合配偶体之间的相互作用捕获核酸。例如,制备用于分析的核酸的方法可包括:(a)通过使用核酸制备物作为模板进行随机引发的第一链合成反应和使用随机引发的第一链合成反应的产物作为模板进行第二链合成反应来制备cdna,其中核酸制备物包含靶核苷酸序列;(b)对cdna进行末端修复以产生包含靶核苷酸序列的平末端双链核酸;(c)洗涤平末端双链核酸;(d)将一个或更多个核苷酸添加至步骤(c)中经洗涤的核酸的3’端,任选地其中一个或更多个核苷酸中的至少一个是以捕获部分修饰的核苷酸;(e)洗涤步骤(d)所产生的核酸;(f)将包含可连接双链体部分和单链突出端序列的衔接子核酸与步骤(e)中经洗涤的核酸连接以产生连接产物,其中单链突出端序列与一个或更多个核苷酸互补;(g)通过聚合酶链式反应使用与靶核苷酸序列特异性退火的第一靶特异性引物和与衔接子核酸的互补序列特异性退火的第一衔接子引物来扩增连接产物;(h)通过聚合酶链式反应使用第二衔接子引物和第二靶特异性引物扩增步骤(g)的扩增产物,其中第二靶特异性引物相对于第一靶特异性引物嵌套;以及(j)洗涤步骤(h)的扩增产物。
核酸衔接子
如本文所用,术语“核酸衔接子”或“衔接子”是指可以与包含靶核苷酸序列的核酸连接以在靶核苷酸序列的扩增和/或测序期间提供一种或更多种元件的核酸分子。在一些实施方案中,衔接子是单链的。在一些实施方案中,衔接子是双链的。在一些实施方案中,双链衔接子包含第一可连接双链体末端和第二未配对末端。在一些实施方案中,衔接子包含扩增链和阻断链。在一些实施方案中,扩增链包含5’未配对部分和3’双链体部分。在一些实施方案中,扩增链还包含3’单链突出端。在一些实施方案中,3’单链突出端是3’t单链突出端。在一些实施方案中,扩增链包含与第一和第二衔接子引物相同的核苷酸序列。在一些实施方案中,衔接子的阻断链包含5’双链体部分和不可延伸的3’部分。在一些实施方案中,阻断链还包含3’未配对部分。在一些实施方案中,扩增链和阻断链的双链体部分基本上互补,并且双链体部分具有足够的长度以在连接温度下保持双链体形式。
在一些实施方案中,扩增链的包含与第一和第二衔接子引物相同的核苷酸序列的部分可以至少部分地包含在扩增链的5’未配对部分中。
在一些实施方案中,衔接子可具有“y”形,即第二未配对末端包含扩增链的5’未配对部分和阻断链的3’部分。阻断链的3’未配对部分的长度可以比扩增链的5’未配对部分更短、更长或与其相等。在一些实施方案中,阻断链的3’未配对部分可以比扩增链的5’未配对部分更短。y形衔接子的优点是阻断链的未配对部分在pcr方案期间不会受到3’延伸。
在一些实施方案中,衔接子的阻断链还可包含3’未配对部分,其基本上不与扩增链的5’未配对部分互补,其中阻断链的3’未配对部分基本上不与任何引物互补或相同。在一些实施方案中,阻断链还可包含在退火温度下不与扩增链的5’未配对部分特异性退火的3’未配对部分,其中阻断链的3’未配对部分在退火温度下不与任何引物或其互补物特异性退火。在一些实施方案中,衔接子核酸在最低程度下包含用于多重化的样品索引序列。然而,在一些实施方案中,衔接子核酸还包含随机分子条形码。
扩增
本公开内容的方面涉及可包括一轮或更多轮扩增的技术。在一些实施方案中,使用第一靶特异性引物和第一衔接子引物进行第一轮扩增。
如本文所用,“第一靶特异性引物”是包含核酸序列的寡核苷酸,所述核酸序列可以在合适的退火条件下与模板核酸的靶核苷酸序列特异性退火。在扩增期间,第一靶特异性引物产生与其模板互补的链,并且该互补链能够与第一衔接子引物杂交。
如本文所用,“第一衔接子引物”是包含核酸序列的寡核苷酸,所述核酸序列可以在合适的退火条件下与衔接子核酸的互补序列特异性退火。由于第一衔接子引物因此与衔接子的至少一部分相同,其与由第一靶特异性引物产生的互补链退火以允许进行扩增。
在一些实施方案中,在第一扩增步骤的第一pcr扩增循环中,第一靶特异性引物可以与包含靶核苷酸序列的核酸的模板链特异性退火。在一些实施方案中,取决于设计第一靶特异性引物的取向,靶核苷酸序列上游或下游的序列将合成为与模板链互补的链。在一些实施方案中,如果在pcr的延伸阶段期间,模板链的5’端终止于连接的衔接子中,则新合成的互补链的3’端将包含能够与第一衔接子引物杂交的序列。在随后的pcr扩增循环中,第一靶特异性引物和第一衔接子引物都能够与靶核酸序列的适当链特异性退火,并且可以扩增已知核苷酸靶序列和衔接子之间的序列。在一些实施方案中,使用第二靶特异性引物和第二衔接子引物进行第二轮扩增。
如本文所用,“第二靶特异性引物”是包含核酸序列的寡核苷酸,所述核酸序列可以在合适的退火条件下与由前面的扩增步骤产生的扩增子所包含的靶核苷酸序列的一部分特异性退火。在扩增期间,第二靶特异性引物产生与其模板互补的链,并且该互补链能够与第二衔接子引物杂交。
如本文所用,“第二衔接子引物”是包含核酸序列的寡核苷酸,所述核酸序列可以在合适的退火条件下与衔接子核酸的互补序列特异性退火。由于第一衔接子引物因此与衔接子的至少一部分相同,其与由第二靶特异性引物产生的互补链退火以允许进行扩增。
在一些实施方案中,第二靶特异性引物相对于第一靶特异性引物嵌套。在一些实施方案中,使用嵌套的衔接子引物消除了产生最终的扩增子的可能性,所述扩增子可扩增(例如,在桥式pcr或乳液pcr期间)但不能测序,这是在半嵌套方法期间可能出现的情况。在其他情况下,使用与测序引物相同的引物的半嵌套方法可导致从第一pcr步骤到第二pcr步骤的不需要的扩增产物的遗留,并最终产生人工测序读取。在一些实施方案中,第二靶特异性引物相对于第一靶特异性引物嵌套至少1个核苷酸,例如,1个、2个、3个、4个、5个、6个、7个、8个、9个、10个或更多个核苷酸。在一些实施方案中,第二靶特异性引物相对于第一靶特异性引物嵌套约5个核苷酸至约10个核苷酸、约10个核苷酸至约15个核苷酸、约15个核苷酸至约20个核苷酸,或约20个核苷酸或更多个核苷酸。
在另一些方面,本文描述的技术可涉及使用一种或更多种嵌套引物。在一些实施方案中,由于不期望的引物结合位点的扩增,使用嵌套引物可以减少pcr产物中的非特异性结合。如本文所用,术语“嵌套”用于描述引物对的引物的退火位点与另一引物对的另一引物的退火位点之间的位置关系。例如,在一些实施方案中,第二引物相对于第一引物嵌套1、2、3个或更多个核苷酸,这意味着其与模板链上的位点结合,所述位点移位1、2、3个或更多个核苷酸。
在一些实施方案中,第二靶特异性引物包含与靶核苷酸序列特异性退火的3’部分和不与靶核苷酸序列退火的5’尾。在一些实施方案中,5’尾包含与第二测序引物相同的核酸序列。在一些实施方案中,反应中存在的多个引物(例如,一个或更多个靶特异性引物和/或一个或更多个衔接子引物)可包含相同的5’尾序列部分。
在一些实施方案中,5’尾可以是富含gc的序列。在一些实施方案中,5’尾序列可包含至少50%gc含量、至少55%gc含量、至少60%gc含量、至少65%gc含量、至少70%gc含量、至少75%gc含量、至少80%gc含量或更高的gc含量。在一些实施方案中,5’尾序列可包含至少60%gc含量。在一些实施方案中,5’尾序列可包含至少65%gc含量。
在一些实施方案中,第二轮扩增包含第二靶特异性引物,其包含5’尾、第一衔接子引物和另外的引物。在一些实施方案中,另外的引物包含与第二靶特异性引物的5’尾相同的3’部分。在一些实施方案中,另外的引物可包含位于杂交序列5’的另外的序列,其可包括条形码、索引、衔接子序列或测序引物位点。在一些实施方案中,另外的引物是通用测序衔接子/索引引物。
在一些实施方案中,第一和第二靶特异性引物与靶核酸的相同链基本上互补。在一些实施方案中,与已知靶序列特异性退火的第一和第二靶特异性引物的部分可包含已知靶核苷酸序列的总共至少20个独特碱基,例如20个或更多个独特碱基、25个或更多个独特碱基、30个或更多个独特碱基、35个或更多个独特碱基、40个或更多个独特碱基、或50个或更多个独特碱基。在一些实施方案中,与已知靶序列特异性退火的第一和第二靶特异性引物的部分可包含已知靶核苷酸序列的总共至少30个独特碱基。
在一些实施方案中,第一衔接子引物可包含与衔接子的扩增链的约20个最5’端的碱基相同的核酸序列,并且第二衔接子引物可包含与衔接子的扩增链的约30个碱基相同的核酸序列,其具有5’碱基,其是位于扩增链的5’端的3’的至少1个核苷酸。
在一些实施方案中,衔接子连接的核酸(例如,连接产物)是极少的。在此类实施方案中,可使用第一衔接子引物,其在其3’端含有一部分衔接子核酸序列,然后在其5’端含有另外的序列发生器重要信息。在这样的实施方案中,可使用第二衔接子引物,其在其3’端含有第一衔接子引物的5’端。在此类实施方案中,第二衔接子引物还可具有允许在其5’端测序的核苷酸序列。在这样的实施方案中,可使用pcr产生与测序仪兼容的文库。引物
在一些实施方案中,设计引物(例如,第一和第二靶特异性引物和第一和第二衔接子引物),使得它们将在约61至72℃(例如,约61至69℃、约63至69℃、约63至67℃、约64至66℃)的退火温度下与其互补序列特异性退火。在一些实施方案中,设计引物使得它们在低于72℃的退火温度下与其互补序列特异性退火。在一些实施方案中,设计引物使得它们在低于70℃的退火温度下与其互补序列特异性退火。在一些实施方案中,设计引物使得它们在低于68℃的退火温度下与其互补序列特异性退火。在一些实施方案中,设计引物使得它们在约65℃的退火温度下与其互补序列特异性退火。在一些实施方案中,本文提供的系统被配置成改变容器温度(例如,通过在不同温度范围之间循环)以促进引物退火。
在一些实施方案中,与已知靶核苷酸序列特异性退火的靶特异性引物的部分将在约61至72℃的温度下特异性退火,例如,约61至69℃、约63至69℃、约63至67℃、约64至66℃。在一些实施方案中,与已知靶核苷酸序列特异性退火的靶特异性引物的部分将在pcr缓冲液中在约65℃的温度下特异性退火。
核酸延伸、扩增和pcr
在一些实施方案中,本文描述的方法包括延伸方案或步骤。在此类实施方案中,延伸可以从一个或更多个杂交随机引物使用所述引物与之杂交的核酸分子作为模板进行。本文描述了延伸步骤。在一些实施方案中,一个或更多个随机引物可与样品中的基本上所有核酸杂交,其中许多核酸可不包含靶核苷酸序列。因此,在一些实施方案中,由于与不包含靶核苷酸序列的模板杂交,可能发生随机引物的延伸。
在一些实施方案中,本文描述的方法可涉及聚合酶链式反应(pcr)扩增方案,其包括一个或更多个扩增循环。本文描述的方法的扩增步骤可各自包含pcr扩增方案,即一组聚合酶链式反应(pcr)扩增循环。如本文所用,术语“扩增方案”是指特异性扩增(增加其丰度)目的核酸的过程。在一些实施方案中,当先前聚合酶延伸的产物充当连续轮次延伸的模板时,发生指数扩增。在一些实施方案中,根据本文公开的方法的pcr扩增方案可包含至少一个,并且在一些情况下至少5个或更多个迭代循环。在一些实施方案中,每个迭代循环包括以下步骤:1)链分离(例如,热变性);2)寡核苷酸引物与模板分子退火;3)退火引物的核酸聚合酶延伸。应当理解,可使用这些步骤中的每一个中涉及的任何合适的条件和时间。在一些实施方案中,所选择的条件和时间可取决于长度、序列含量、解链温度、二级结构特征或与反应中使用的核酸模板和/或引物相关的其他因素。在一些实施方案中,根据本文所述方法的扩增方案在热循环仪中进行,该热循环仪中的许多是可商购的。在一些实施方案中,本文描述的方法可包括线性扩增。例如,在一些实施方案中,使用嵌套引物进行的扩增步骤可使用线性扩增进行。在一些实施方案中,可使用基于核酸序列的扩增(nucleicacidsequence-basedamplification,nasba)进行扩增。例如,在一些实施方案中,扩增包括t7介导的nasba反应。
在一些实施方案中,核酸延伸反应涉及使用核酸聚合酶。如本文所用,短语“核酸聚合酶”是指催化核苷三磷酸的模板依赖性聚合以形成与模板核酸序列互补的引物延伸产物的酶。核酸聚合酶在退火的引物的3’端开始合成,并在朝向模板的5’端的方向上进行。许多核酸聚合酶是本领域已知的并且是可商购的。一组核酸聚合酶是热稳定的,即它们在经受足以使互补核酸的退火链变性的温度(例如94℃,或有时更高)后保持功能。用于扩增的方案的非限制性实例涉及在以下条件下使用聚合酶(例如,phoenixtaq,veraseq):98℃持续30秒,随后是14至22个循环,每个循环包括在98℃下熔化10秒,随后在68℃下退火30秒,接着在72℃下延伸3分钟,然后在4℃下保持反应。但是,也可使用其他适当的反应条件。在一些实施方案中,可以调节退火/延伸温度以引起盐浓度的差异(例如,高3℃以得到更高的盐浓度)。在一些实施方案中,减慢升温速率(例如,1℃/s、0.5℃/s、0.28℃/s、0.1℃/s或更慢),例如,从98℃至65℃,改善了高度多重化样品的引物性能和覆盖均匀性。在一些实施方案中,本文提供的系统被配置成改变容器温度(例如,通过在不同温度范围之间循环,具有受控的升温或降温速率)以促进扩增。
在一些实施方案中,核酸聚合酶在酶进行模板依赖性延伸的条件下使用。在一些实施方案中,核酸聚合酶是dna聚合酶i、taq聚合酶、phoenixtaq聚合酶、phusion聚合酶、t4聚合酶、t7聚合酶、klenow片段、klenowexo-、phi29聚合酶、amv逆转录酶、m-mulv逆转录酶、hiv-1逆转录酶、verasequltra聚合酶、veraseqhf2.0聚合酶、enzscript,或其他合适的聚合酶。在一些实施方案中,核酸聚合酶不是逆转录酶。在一些实施方案中,核酸聚合酶作用于dna模板。在一些实施方案中,核酸聚合酶作用于rna模板。在一些实施方案中,延伸反应包括对rna进行逆转录以产生互补dna分子(rna依赖性dna聚合酶活性)。在一些实施方案中,逆转录酶是小鼠莫洛尼鼠白血病病毒(moloneymurineleukemiavirus,m-mlv)聚合酶、amv逆转录酶、rsv逆转录酶、hiv-1逆转录酶、hiv-2逆转录酶,或其他合适的逆转录酶。
在一些实施方案中,核酸扩增反应涉及包括链分离步骤的循环,其通常包括加热反应混合物。如本文所用,术语“链分离”或“对链进行分离”是指处理核酸样品,使得互补的双链分子分离成可用于与寡核苷酸引物退火的两条单链。在一些实施方案中,根据本文所述方法的链分离通过将核酸样品加热至其解链温度(tm)以上来实现。在一些实施方案中,对于在适合于核酸聚合酶的反应制备物中的含有核酸分子的样品,加热至94℃足以实现链分离。在一些实施方案中,合适的反应制剂含有一种或更多种盐(例如,1至100mmkcl,0.1至10mmmgcl2)、至少一种缓冲剂(例如,1至20mmtris-hcl)和载体(例如,0.01至0.5%bsa)。合适缓冲液的非限制性实例包括50mmkcl,10mmtris-hcl(在25℃下ph8.8),0.5至3mmmgcl2和0.1%bsa。合适缓冲液的另一个非限制性实例包括50mmkcl,10mmtris-hcl(在25℃下ph8.8),0.5至5mm(例如,约0.5mm、约1mm、约2mm、约3mm、约4mm、约5mm)mgcl2和0.1%bsa。
在一些实施方案中,核酸扩增包括将引物与具有靶核酸特征链的核酸模板退火。在一些实施方案中,靶核酸链可以用作模板核酸。如本文所用,术语“退火”是指在两个核酸之间形成一个或更多个互补碱基对。在一些实施方案中,退火涉及杂交在一起的两条互补或基本上互补的核酸链。在一些实施方案中,在延伸反应的背景下,退火涉及引物与模板的杂交,从而形成模板依赖性聚合酶的引物延伸底物。在一些实施方案中,退火(例如,在引物和核酸模板之间)的条件可以基于引物的长度和序列而变化。在一些实施方案中,退火的条件基于引物的tm(例如,经计算的tm)。在一些实施方案中,延伸方案的退火步骤包括在链分离步骤后将温度降低至基于引物的tm(例如,经计算的tm)的温度,持续足以允许这种退火的时间。在一些实施方案中,可使用许多算法中的任意一种来确定tm(例如,oligotm(molecularbiologyinsightsinc.colorado)引物设计软件和ventrontitm(invitrogen,inc.california)引物设计软件和可获自互联网的程序,包括primer3、oligocalculator和netprimer(premierbiosoft;paloalto,ca;以及可免费在万维网(例如,在premierbiosoft.com/netprimer/netprlaunch/help/xnetprlaunch.html)上获得的那些)。在一些实施方案中,引物的tm可使用下式计算,该公式由netprimer软件使用并且在frieir等的pnas198683:9373-9377中更详细地描述,该文献通过引用整体并入本文。
tm=δh/(δs+r*ln(c/4))+16.6log([k+]/(1+0.7[k+]))-273.15
其中:δh是螺旋形成的焓;δs是螺旋形成的熵;r是摩尔气体常数(1.987cal/℃*mol);c是核酸浓度;[k+]是盐浓度。对于大多数扩增方案,退火温度选择为比预测的tm低约5℃,尽管可以使用接近和高于tm(例如,比预测的tm低1℃至5℃或比预测的tm高1℃至5℃),同样可以使用例如比预测的tm低5℃以上的温度(例如,低6℃、低8℃、低10℃或更低)。在一些实施方案中,退火温度越接近tm,退火越具有特异性。在一些实施方案中,在延伸反应期间(例如,在pcr扩增方案的背景下)用于引物退火的时间至少部分地基于反应的体积来确定(例如,其中较大体积涉及较长时间)。在一些实施方案中,在延伸反应期间(例如,在pcr扩增方案的背景下)用于引物退火的时间至少部分地基于引物和模板浓度来确定(例如,其中较高的引物与模板的相对浓度涉及比较低相对浓度更短的时间)。在一些实施方案中,取决于体积和相对引物/模板浓度,延伸反应中(例如,在扩增方案的情况下)的引物退火步骤可以在1秒至5分钟、10秒至2分钟,或30秒至2分钟的范围内。如本文所用,“基本上退火”是指当在pcr扩增方案的上下文中使用时,在两个核酸之间形成互补碱基对的程度足以产生可检测水平的特异性扩增产物。
如本文所用,术语“聚合酶延伸”是指通过核酸聚合酶将至少一个互补核苷酸模板依赖性地添加至与核酸模板退火的引物的3’端。在一些实施方案中,聚合酶延伸添加多于一个核苷酸,例如,直至并包括对应于模板全长的核苷酸。在一些实施方案中,聚合酶延伸的条件至少部分基于所用聚合酶的特性。在一些实施方案中,用于聚合酶延伸的温度基于酶的已知活性特性。在一些实施方案中,其中退火温度低于酶的最佳温度,使用较低的延伸温度可以是可接受的。在一些实施方案中,在低于其最佳延伸温度的情况下,酶可以保持至少部分活性。在一些实施方案中,聚合酶延伸(例如,用热稳定聚合酶例如taq聚合酶及其变体进行)在65℃至75℃或68℃至72℃下进行。在一些实施方案中,本文提供的方法涉及引物的聚合酶延伸,所述引物在pcr扩增方案的每个循环时与核酸模板退火。在一些实施方案中,使用具有相对强的链置换活性的聚合酶进行聚合酶延伸。在一些实施方案中,出于检测融合(例如,5’融合)的目的,具有强链置换的聚合酶可用于制备核酸。在一些实施方案中,具有5’→3’外切核酸酶活性的聚合酶(例如taq聚合酶)可用于产生长文库片段。
在一些实施方案中,引物延伸在允许退火的寡核苷酸引物延伸的条件下进行。如本文所用,术语“允许退火的寡核苷酸延伸以使得产生延伸产物的条件”是指一组条件(例如,温度、盐和辅因子浓度、ph和酶浓度),在该条件下核酸聚合酶催化引物延伸。在一些实施方案中,这样的条件至少部分基于所用的核酸聚合酶。在一些实施方案中,聚合酶可以在合适的反应制备物中进行引物延伸反应。
在一些实施方案中,合适的反应制备物含有一种或更多种盐(例如,1至100mmkcl,0.1至10mmmgcl2)、至少一种缓冲剂(例如,1至20mmtris-hcl)、载体(例如,0.01至0.5%bsa),和一种或更多种ntp(例如,datp、dttp、dctp和dgtp每种10至200μm)。一组非限制性条件是在72℃下50mmkcl,10mmtris-hcl(在25℃下,ph8.8),0.5至3mmmgcl2,200μm每种dntp和0.1%bsa,在该温度下聚合酶(例如,taq聚合酶)催化引物延伸。
在一些实施方案中,合适的反应制备物含有一种或更多种盐(例如,1至100mmkcl,0.5至5mmmgcl2)、至少一种缓冲剂(例如,1至20mmtris-hcl)、载体(例如,0.01至0.5%bsa),和一种或更多种ntp(例如,datp、dttp、dctp和dgtp每种50至350μm)。一组非限制性条件是在72℃下50mmkcl,10mmtris-hcl(在25℃下,ph8.8),3mmmgcl2、200μm每种dntp和0.1%bsa,在该温度下聚合酶(例如,taq聚合酶)催化引物延伸。另一组非限制性条件是在72℃下50mmkcl,10mmtris-hcl(在25℃下,ph8.8),3mmmgcl2、266μmdatp,200μmdctp,133μmdgtp,200μmdttp和0.1%bsa,在该温度下聚合酶(例如,taq聚合酶)催化引物延伸。
在一些实施方案中,起始和延伸的条件可包含在合适的缓冲液中存在一种、两种、三种或四种不同的脱氧核苷三磷酸(例如,选自datp、dttp、dctp和dgtp)和聚合诱导剂,例如dna聚合酶或逆转录酶。在一些实施方案中,“缓冲液”可包括溶剂(例如,水性溶剂)加上影响ph、离子强度等的适当的辅因子和试剂。在一些实施方案中,两种、三种或四种不同的脱氧核苷三磷酸以等摩尔浓度,或大约等摩尔浓度存在。在一些实施方案中,两种、三种或四种不同的脱氧核苷三磷酸以不同浓度存在,所述浓度已经通过实验确定为适合于该技术的特定实施。
在一些实施方案中,核酸扩增涉及多至5轮、多至10轮、多至20轮、多至30轮、多至40轮或更多轮(循环)的扩增。在一些实施方案中,核酸扩增可包括一组长度为5个循环至20个循环的pcr扩增方案的循环。在一些实施方案中,扩增步骤可包括一组长度为10个循环至20个循环的pcr扩增方案的循环。在一些实施方案中,每个扩增步骤可包括一组长度为12个循环至16个循环的pcr扩增方案的循环。在一些实施方案中,退火温度可低于70℃。在一些实施方案中,退火温度可低于72℃。在一些实施方案中,退火温度可为约65℃。在一些实施方案中,退火温度可为约61至约72℃。
在多种实施方案中,本文所述的方法和组合物涉及用本文所述的一种或更多种类型的引物进行pcr扩增方案。如本文所用,“引物”是指这样的寡核苷酸,其能够与核酸模板特异性退火并提供充当模板依赖性聚合酶的底物的3’端,以产生与模板互补的延伸产物。在一些实施方案中,引物是单链的,使得引物及其互补物可以退火以形成两条链。根据本文所述的方法和组合物的引物可包含杂交序列(例如,与核酸模板退火的序列),其长度为小于或等于300个核苷酸,例如,长度为小于或等于300个、或250个、或200个、或150个、或100个、或90个、或80个、或70个、或60个、或50个、或40个、或30个或更少、或20个或更少、或15个或更少,但至少6个核苷酸。在一些实施方案中,引物的杂交序列可以长度为6至50个核苷酸、6至35个核苷酸、6至20个核苷酸、10至25个核苷酸。
任何合适的方法可用于合成寡核苷酸和引物。在一些实施方案中,商业来源提供了适合于提供用于本文所述方法和组合物之引物的寡核苷酸合成服务(例如,invitrogentm定制dna寡核苷酸(lifetechnologies,grandisland,ny)或来自integrateddnatechnologies(coralville,ia)的定制dna寡核苷酸)。
靶核酸
如本文所用,术语“靶核酸”和“包含靶核苷酸序列的核酸”是指目的核酸分子(例如,待制备用于分析的核酸)。在一些实施方案中,靶核酸包含靶核苷酸序列(例如,已知或预先确定的核苷酸序列)和待确定的相邻核苷酸序列(其可称为未知序列)二者。靶核酸可以具有任何合适的长度。在一些实施方案中,靶核酸是双链的。在一些实施方案中,靶核酸是dna。在一些实施方案中,靶核酸包含基因组或染色体dna(gdna)。在一些实施方案中,靶核酸包含互补dna(cdna)。在一些实施方案中,靶核酸是单链的。在一些实施方案中,靶核酸包含rna(例如,mrna、rrna、trna、cfdna、cfrna、长非编码rna、微rna)。
许多适用于本文所述方法的测序方法提供了具有数十至数百个核苷酸碱基的最佳读取长度的测序运行(例如,iontorrent技术可产生200至400bp的读取长度)。例如,由基因组dna或mrna构成的靶核酸可以由基本上长于该最佳读取长度的核酸分子构成。为了使由第二扩增步骤产生的扩增的核酸部分具有合适的长度(例如,多至100bp、200bp、300bp、400bp、500bp、1kb、2kb)用于特定测序技术,已知靶核苷酸序列和衔接子可以与之连接的靶核酸末端之间的距离应该尽可能接近所选技术的最佳读取长度。例如,如果给定测序技术的最佳读取长度是200bp,则根据本文所述方法扩增的核酸分子应具有约400bp或更短的平均长度。然而,应当理解,在一些实施方案中,当核酸分子的长度超过400bp时,可以实施本文描述的技术。例如,在一些实施方案中,核酸片段可以是约400个或更多个核苷酸、500个或更多个核苷酸、600个或更多个核苷酸、700个或更多个核苷酸、800个或更多个核苷酸、900个或更多个核苷酸、1000个或更多个核苷酸、1500个或更多核苷酸、2000个或更多个核苷酸、2500个或更多个核苷酸、3000个或更多个核苷酸、4000个或更多个核苷酸、5000个或更多个核苷酸、10000个或更多个核苷酸。
由例如基因组dna或mrna构成的靶核酸可以被剪切,例如机械或酶促地剪切,以产生具有任何所需尺寸的片段。机械剪切过程的非限制性实例包括超声处理、雾化和可从covaris(wobum,ma)获得的afatm剪切技术。在一些实施方案中,可通过超声处理机械剪切由基因组dna构成的靶核酸。
在一些实施方案中,当靶核酸由rna构成时,可以对样品进行逆转录酶方案以产生dna模板。在一些实施方案中,然后可以剪切dna模板。在一些实施方案中,dna模板未被剪切。例如,在一些实施方案中,可以调节在逆转录酶方案期间使用的引物浓度,使得产物cdna具有合适的“片段化”长度。在一些实施方案中,可以在进行逆转录酶方案之前剪切靶rna。在一些实施方案中,包含靶rna的样品可用于本文所述的方法,所述方法使用从新鲜或降解的样品中提取的总核酸;无需去除基因组dna以进行cdna测序;无需清除核糖体rna以进行cdna测序;在任意步骤中都无需机械或酶促剪切;通过使用随机六聚体对rna进行双链cdna合成;和通过使核酸进行末端修复、磷酸化和腺苷酸化。
在一些实施方案中,靶核苷酸序列可包含基因重排。本文描述的方法适用于确定基因重排的存在和/或身份,因为基因重排的仅一半必须先前已知(即,将被基因特异性引物靶向的基因重排的一半)。在一些实施方案中,基因重排可包含癌基因。在一些实施方案中,基因重排可包含融合癌基因。在一些实施方案中,基因重排可包含v(d)j重组产物。
如本文所用,术语“已知靶核苷酸序列”或“靶核苷酸序列”是指靶核酸的一部分,该部分的序列(例如,核酸的核苷酸碱基的身份和顺序)是已知的。例如,在一些实施方案中,已知靶核苷酸序列是核酸的核苷酸序列,其是已知的或在探询核酸的相邻未知序列之前已经确定的。已知靶核苷酸序列可以具有任何合适的长度。
在一些实施方案中,靶核苷酸序列(例如,已知靶核苷酸序列)长度为10个或更多个核苷酸、30个或更多个核苷酸、40个或更多个核苷酸、50个或更多个核苷酸、100个或更多个核苷酸、200个或更多个核苷酸、300个或更多个核苷酸、400个或更多个核苷酸、500个或更多个核苷酸、600个或更多个核苷酸、700个或更多个核苷酸、800个或更多个核苷酸、900个或更多个核苷酸、1000个或更多个核苷酸、1500个或更多个核苷酸、2000个或更多个核苷酸、2500或更多个核苷酸、3000或更多个核苷酸、4000个或更多个核苷酸、5000个或更多个核苷酸、10000个或更多个核苷酸。在一些实施方案中,靶核苷酸序列(例如,已知靶核苷酸序列)长度为10至100个核苷酸、10至500个核苷酸、10至1000个核苷酸、100至500个核苷酸、100至1000个核苷酸、500至1000个核苷酸、500至5000个核苷酸。
在一些实施方案中,本文提供了用于确定核酸的邻接(或相邻)部分的序列的方法。如本文所用,术语“与……邻接的核苷酸序列”是指紧邻另一核苷酸序列(例如,已知核苷酸序列)的上游或下游的核酸分子(例如,靶核酸)的核苷酸序列。在一些实施方案中,与已知靶核苷酸序列邻接的核苷酸序列可具有任何合适的长度。在一些实施方案中,与已知靶核苷酸序列邻接的核苷酸序列包含1kb或更短的核苷酸序列,例如1kb或更短的核苷酸序列、750bp或更短的核苷酸序列、500bp或更短的核苷酸序列、400bp或更短的核苷酸序列、300bp或更短的核苷酸序列、200bp或更短的核苷酸序列、100bp或更短的核苷酸序列。在一些实施方案中,其中样品包含含有已知靶核苷酸序列的不同靶核酸(例如,其中已知靶核苷酸序列在其基因组中或在分开的、不同的染色体上多次出现的细胞),存在包含“与已知靶核苷酸序列邻接的核苷酸序列”的多个序列。如本文所用,术语“确定核苷酸序列”是指确定核酸的核苷酸碱基的身份和相对位置。
在一些实施方案中,已知靶核酸可含有由基因重排产生的融合序列。在一些实施方案中,本文描述的方法适合于确定基因重排的存在和/或身份。在一些实施方案中,基因重排的一部分的身份是先前已知的(例如,将由基因特异性引物靶向的基因重排的部分),并且其他部分的序列可使用本文公开的方法确定。在一些实施方案中,基因重排可涉及癌基因。在一些实施方案中,基因重排可包含融合癌基因。
分子条形码和索引序列
在一些实施方案中,引物和/或衔接子可含有另外的序列,例如标识符序列(例如条形码、索引)、测序引物杂交序列(例如,rd1)和衔接子序列。在一些实施方案中,衔接子序列是与下一代测序系统一起使用的序列。在一些实施方案中,衔接子序列是基于illumina的测序技术的p5和p7序列。在一些实施方案中,衔接子序列是与iontorrent测序技术兼容的p1和a。
在一些实施方案中,如本文所用,“条形码”、“分子条形码”和“分子条形码标签”可互换使用,并且通常是指衔接子核酸的区域,其可用作与其连接的特定核酸的标识符。在一些实施方案中,分子条形码包含随机化核酸序列,其为与其连接的核酸提供独特的标识符。在一些实施方案中,分子条形码可用于识别独特片段并从样品中对测序读取进行“去重复”。在一些实施方案中,分子条形码可用于识别和去除pcr重复。在一些实施方案中,分子条形码可以长度为2至25个核苷酸、长度为2至15个核苷酸、长度为2至10个核苷酸、长度为2至6个核苷酸。在一些实施方案中,分子条形码包含至少2个、3个、4个、5个、6个、7个、8个、9个、10个、11个、12个、13个、14个、15个、16个、17个、18个、19个、20个、21个、22个、23个、24个或至少25个核苷酸。在一些实施方案中,分子条形码包含8个核苷酸。
在一些实施方案中,如本文所用,“索引”、“索引序列”、“索引区域”和“样品索引”可互换使用,并且通常是指衔接子核酸的区域,该区域可用作连接核酸所属群体的标识符。在一些实施方案中,索引包含固定的核酸序列,其可用于识别属于共有文库的序列集合。例如,索引可用于识别对应于核酸的样品。在一些实施例中,索引可用作,例如,源标识符,位置标识符,日期或时间标识符(例如,取样或处理的日期或时间),或核酸的与共享或共有特性相关的(例如,在文库的其他核酸中共有的)其他标识符。在一些实施方案中,此类索引序列可用于识别核酸群体中存在的核酸的不同方面。在一些实施方案中,索引序列可提供靶核酸的来源或位置标识符。例如,索引序列可用于识别从中获得核酸的患者。在一些实施方案中,索引序列使得能够在单个反应上(例如,在单个流动单元中进行)对多个不同样品进行测序。在一些实施方案中,出于检测个体测序反应的目的,索引序列可用于对序列成像仪进行定向。在一些实施方案中,索引序列可以长度为2至25个核苷酸、长度为2至15个核苷酸、长度为2至10个核苷酸、长度为2至6个核苷酸。在一些实施方案中,索引包含至少2个、3个、4个、5个、6个、7个、8个、9个、10个、11个、12个、13个、14个、15个、16个、17个、18个、19个、20个、21个、22个、23个、24个或至少25个核苷酸。
在一些实施方案中,当根据本文描述的方法使用一群加尾随机引物时,在扩增之后可存在多种可区分的扩增产物。在一些实施方案中,因为加尾随机引物在样品的所有核酸分子中的多个位置杂交,一组靶特异性引物可以使由多于1个杂交事件产生的延伸产物杂交(和扩增),例如,一个加尾随机引物可以在与靶特异性引物杂交位点相隔第一距离(例如,100个核苷酸)处杂交,并且另一个加尾随机引物可以在与靶特异性引物杂交位点相隔第二距离(例如,200个核苷酸)处杂交,从而产生了两种扩增产物(例如,包含约100bp的第一扩增产物和包含约200bp的第二扩增产物)。在一些实施方案中,可使用下一代测序技术对这些多重扩增产物每种进行测序。在一些实施方案中,这些多重扩增产物的测序是有利的,因为其提供了多个重叠序列读取,其可以彼此比较以检测在扩增或测序过程中引入的序列错误。在一些实施方案中,可以比对单独的扩增产物(例如,来源于单个分子),并且当它们在特定碱基处存在的序列不同时,可以存在pcr和/或测序的伪象或错误。
dna剪切/片段化
本文所述的核酸分子可以被剪切(例如,机械或酶促地剪切、通过喷雾器剪切)以产生具有任何所需尺寸的片段。机械剪切过程的非限制性实例包括超声处理、雾化和可从covaris(woburn,ma)获得的afatm剪切技术。在一些实施方案中,可通过超声处理机械剪切核酸。在一些实施方案中,靶核酸未经剪切或消化。在一些实施方案中,制备步骤的核酸产物(例如延伸产物、扩增产物)未经剪切或酶促消化。
在一些实施方案中,当靶核苷酸序列包含rna时,可以对样品进行逆转录酶方案以产生dna模板,然后可以剪切dna模板。在一些实施方案中,可以在进行逆转录酶方案之前剪切靶rna。在一些实施方案中,包含靶rna的样品可用于本文所述的方法中,所述方法使用从新鲜或降解的样品中提取的总核酸;无需去除基因组dna以进行cdna测序;无需清除核糖体rna以进行cdna测序;在任意步骤中都无需机械或酶促剪切;通过使用随机六聚体对rna进行双链cdna合成。
测序
在一些方面,本文描述的技术涉及富集核酸样品用于寡核苷酸测序的方法。在一些实施方案中,可通过下一代测序方法进行测序。如本文所用,“下一代测序”是指寡核昔酸测序技术,其在高于通过常规测序方法(例如,sanger测序)可能的速率的速率下能够对寡核苷酸进行测序,因为同时进行和读出数千至数百万个测序反应。下一代测序方法/平台的非限制性实例包括大规模平行签名测序(lynxtherapeutics);454焦磷酸测序(454lifesciences/rochediagnostics);固相可逆染料-终止子测序(solexa/illumina);solid技术(appliedbiosystems);离子半导体测序(iontorrent);dna纳米球测序(completegenomics);和可从pacificbiosciences、intelligenbio-systems和oxfordnanoporetechnologies获得的技术。在一些实施方案中,测序引物可包含与所选择的下一代测序方法相容的部分。下一代测序技术以及相关测序引物的限制和设计参数是本领域公知的(参见,例如,shendure等,“next-generationdnasequencing,”nature,2008,第26卷,第10期,1135-1145;mardis,“theimpactofnext-generationsequencingtechnologyongenetics”,trendsingenetics,2007,第24卷,第3期,第133至141页;su等,“next-generationsequencinganditsapplicationsinmoleculardiagnostics”,expertrevmoldiagn,2011,11(3):333-43;zhang等,“theimpactofnext-generationsequencingongenomics”,jgenetgenomics,2011,38(3):95-109;(nyren,p等,analbiochem208:17175(1993);bentley,d.r.curropingenetdev16:545-52(2006);strausberg,r.l.等,drugdisctoday13:569-77(2008);美国专利no.7,282,337;美国专利no.7,279,563;美国专利no.7,226,720;美国专利no.7,220,549;美国专利no.7,169,560;美国专利no.6,818,395;美国专利no.6,911,345;美国公开号2006/0252077;2007/0070349;和20070070349;其通过引用整体并入本文。)
在一些实施方案中,测序步骤依赖于第一和第二测序引物的使用。在一些实施方案中,选择第一和第二测序引物以与本文所述的下一代测序方法相容。
将测序读取与基因组和/或cdna序列的已知序列数据库比对的方法是本领域公知的,并且该过程的软件可商购获得。在一些实施方案中,没有完整地定位到野生型序列数据库的读取(较少的测序引物和/或衔接子核苷酸序列)可以是基因组重排或大的插入缺失突变。在一些实施方案中,包含定位到基因组中多个位置的序列的读取(较少的测序引物和/或衔接子核苷酸序列)可以是基因组重排。在一些实施方案中,可以构建重叠成邻接序列或“重叠群(contig)”的读取的从头组装,并用于测序读取的比对。在一些实施例中,可以利用不依赖于可公开访问的基因组数据库的热点参考。
样品
在一些实施方案中,核酸(例如,靶核酸、包含靶核苷酸序列的核酸)存在于或获得自合适的样品中(例如,食物样品、环境样品、生物样品(例如血液样品等))。在一些实施方案中,靶核酸是获得自对象的生物样品。在一些实施方案中,样品可以是获得自对象的诊断样品。在一些实施方案中,样品还可包含蛋白质、细胞、流体、生物流体、防腐剂和/或其他物质。作为非限制性实例,样品可以是颊部拭子、血液、血清、血浆、痰、脑脊髓液、尿液、泪液、肺泡分离物、胸膜液、心包液、囊液、肿瘤组织、组织、活组织检查、唾液、吸出物,或其组合。在一些实施方案中,可通过切除或活组织检查获得样品。
在一些实施方案中,样品可以获得自需要治疗与遗传改变相关的疾病(例如癌症或遗传性疾病)的对象。在一些实施方案中,已知靶序列存在于疾病相关基因中。
在一些实施方案中,样品获得自需要治疗癌症的对象。在一些实施方案中,样品包含肿瘤细胞群,例如至少一个肿瘤细胞。在一些实施方案中,样品包括肿瘤活组织检查,包括但不限于未经处理的活组织检查组织或经处理的活组织检查组织(例如,福尔马林固定的和/或石蜡包埋的活组织检查组织)。
在一些实施方案中,样品是新鲜收集的。在一些实施方案中,在用于本文所述的方法和组合物之前储存样品。在一些实施方案中,样品是未经处理的样品。如本文所用,“未经处理的样品”是指除了在溶液中稀释和/或悬浮之外没有任何先前样品预处理的生物样品。在一些实施方案中,样品获得自对象并在用于本文所述的方法和组合物之前进行保存或加工。作为非限制性实例,样品可以包埋在石蜡中、冷藏或冷冻。根据本文所述的方法和组合物,在确定核酸的存在之前,可以解冻冷冻的样品。在一些实施方案中,样品可以是经加工或处理的样品。用于处理或加工样品的示例性方法包括但不限于离心、过滤、超声处理、均化、加热、冷冻和解冻、与防腐剂(例如,抗凝血剂或核酸酶抑制剂)接触,及其任意组合。在一些实施方案中,可以用化学和/或生物试剂处理样品。可使用化学和/或生物试剂以在加工和/或储存期间保护样品或由样品构成的核酸和/或维持样品或由样品构成的核酸的稳定性。作为补充或替代,可使用化学和/或生物试剂以从样品的其他组分中释放核酸。作为非限制性实例,在用于本文所述的方法和组合物之前,可以用抗凝血剂处理血液样品。用于核酸分析的样品的加工、保存或处理的合适的方法和过程可用于本文公开的方法中。在一些实施方案中,样品可以是澄清的流体样品。在一些实施方案中,可通过低速离心(例如,3,000xg或更低)澄清样品并收集包含澄清的流体样品的上清液。
在一些实施方案中,可以在用于本文所述的方法和组合物之前分离、富集或纯化样品中存在的核酸。可使用从样品中分离、富集或纯化核酸的合适方法。例如,用于从多种样品类型中分离基因组dna的试剂盒是可商购的(例如,目录号51104、51304、56504和56404;qiagen;germantown,md)。在一些实施方案中,本文描述的方法涉及富集靶核酸的方法,例如,在靶核酸测序之前。在一些实施方案中,在测序之前不知道待富集的靶核酸的一端的序列。在一些实施方案中,本文描述的方法涉及在使用下一代测序技术确定核苷酸序列之前富集特定核苷酸序列的方法。在一些实施方案中,富集特定核苷酸序列的方法不包括杂交富集。
靶基因和治疗应用
在本文所述技术的一些实施方案中,确定与已知寡核苷酸靶序列邻接的序列可提供与疾病治疗相关的信息。因此,在一些实施方案中,本文公开的方法可用于帮助治疗疾病。在一些实施方案中,样品可以来自需要治疗与遗传改变相关的疾病的对象。在一些实施方案中,已知靶序列是疾病相关基因(例如癌基因)的序列。在一些实施方案中,与已知寡核苷酸靶序列邻接的序列和/或该已知寡核苷酸靶序列可包含与疾病相关的突变或遗传异常,例如snp、插入、缺失和/或基因重排。在一些实施方案中,样品中存在的与已知靶序列邻接的序列和/或已知靶序列包含基因重排产物的序列。在一些实施方案中,基因重排可以是癌基因,例如融合癌基因。
癌症的某些治疗对于包含某些癌基因的肿瘤特别有效,例如,靶向给定融合癌基因的作用或表达的治疗剂可以对包含该融合癌基因的肿瘤有效,但对缺乏该融合癌基因的肿瘤无效。本文描述的方法可以有助于确定揭示癌基因状态(例如,突变、snp和/或重排)的特定序列。在一些实施方案中,本文描述的方法还可允许在侧翼区域的序列已知时确定特定序列,例如,本文描述的方法可确定涉及已知基因(例如癌基因)的基因重排的存在和身份,其中在进行本文描述的方法之前,精确位置和/或重排配偶体是未知的。
在一些实施方案中,对象需要治疗肺癌(例如,用egfr-tki,一种靶向癌症治疗)。在一些实施方案中,例如,当从需要治疗肺癌的对象获得样品时,已知靶序列可包含来自选自alk、ros1和ret的基因的序列。因此,在一些实施方案中,基因重排导致涉及alk、ros1或ret的融合。涉及alk、ros1或ret的基因排列的非限制性实例描述于例如soda等,nature2007448561-6:rikova等,cell2007131:1190-1203;kohno等,naturemedicine201218:375-7;takouchi等,naturemedicine201218:378-81;其通过引用整体并入本文。然而,应该理解的是,基因重排的精确位置和参与重排的第二基因的身份可能不是事先已知的。因此,在本文所述的方法中,可以检测这种重排的存在和身份,而不必须知道重排的位置或参与基因重排的第二基因的身份。
在一些实施方案中,已知靶序列可包含来自选自下组的基因的序列:alk、ros1和ret。
在一些实施方案中,从对象的肿瘤获得的样品中的alk的基因重排的存在可表明肿瘤易于用选自下组的治疗进行治疗:alk抑制剂;egfr;克唑替尼(pf-02341066);ap26113;ldk378;3-39;af802;ipi-504;asp3026;ap-26113;x-396;gsk-1838705a;ch5424802;alk激酶活性的二氨基和氨基嘧啶抑制剂,例如nvp-tae684和pf-02341066(参见,例如,galkin等,procnatlacadsciusa,2007,104:270-275;zou等,cancerres,2007,67:4408-4417;hallberg和palmerf1000medreports20113:21;sakamoto等,cancercell201119:679-690;以及wo04/079326中公开的分子)。所有前述参考文献都通过引用整体并入本文。alk抑制剂可包括降低alk或其部分的表达和/或激酶活性的任何药剂,包括例如降低alk或其部分的表达和/或活性的寡核苷酸、小分子和/或肽。如本文所用,“间变性淋巴瘤激酶”或“alk”是指通常以野生型形式参与神经元调节的跨膜tyros1ine激酶。alk基因和mrna的核苷酸序列对于许多物种是已知的,包括人(例如,如根据ncbi基因id:238所注释)。
在一些实施方案中,获得自对象的肿瘤的样品中的ros1的基因重排的存在可表明肿瘤易于用选自下组的治疗进行治疗:ros1抑制剂和如上所述的alk抑制剂(例如,克唑替尼)。ros1抑制剂可包括降低ros1或其部分的表达和/或激酶活性的任何药剂,包括例如降低ros1或其部分的表达和/或活性的寡核苷酸、小分子和/或肽。如本文所用,“c-ros癌基因1”或“ros1”(在本领域中也称为ros-1)是指果蝇sev(sevenless)亚家族的跨膜酪氨酸激酶,其与ptpn6相互作用。rosl基因和mrna的核苷酸序列对于许多物种是已知的,包括人(例如,如根据ncbi基因id:6098所注释)。
在一些实施方案中,获得自对象的肿瘤的样品中的ret的基因重排的存在可表明肿瘤易于用选自下组的治疗进行治疗:ret抑制剂;dp-2490、dp-3636、su5416;bay43-9006、bay73-4506(瑞戈非尼)、zd6474、nvp-ast487、索拉非尼、rpi-1、xl184、凡德他尼、舒尼替尼、伊马替尼、帕唑帕尼、阿西替尼、莫特塞尼、吉非替尼和醉茄素a(参见例如samadi等,surgery2010148:1228-36;cuccuru等,jnci200413:1006-1014;akeno-stuart等,cancerresearch200767:6956;grazma等,jclinoncol201028:15s5559;mologni等,jmolendocrinol200637:199-212;calmomagno等,journalnci200698:326-334;mologni,currmedchem201118:162-175;以及wo06/034833;美国专利公开2011/0201598和美国专利8,067,434中公开的化合物)。所有前述参考文献都通过引用整体并入本文。ret抑制剂可包括降低ret或其部分的表达和/或激酶活性的任何药剂,包括例如降低ret或其部分的表达和/或活性的寡核苷酸、小分子和/或肽。如本文所用,“在转染期间重排”或“ret”是指钙黏蛋白超家族的受体酪氨酸激酶,其参与神经嵴发育并识别神经胶质细胞系来源的神经营养因子家族信号传导分子。ret基因和mrna的核苷酸序列对于许多物种是已知的,包括人(例如,如根据ncbi基因id:5979所注释)。
在一些实施方案中,已知靶序列可包含选自表2的基因。
表2.已知靶序列
本文描述的方法的应用的另外的非限制性实例包括检测血液恶性标志物及其组(例如,包括检测淋巴瘤和白血病中的基因组重排的那些)、检测肉瘤相关的基因组重排及其组;和检测igh/tcr基因重排及其组用于淋巴瘤测试。
在一些实施方案中,本文描述的方法涉及用针对癌症的治疗来治疗患有或诊断为患有例如癌症的对象。患有癌症的对象可以由医生使用当前诊断癌症的方法来识别。例如,表征这些病症并有助于诊断的肺癌症状和/或并发症是本领域公知的,其包括但不限于呼吸微弱、锁骨上方淋巴结肿大、肺部异常声音、当胸部被敲击时有浊音,和胸部疼痛。可以帮助诊断例如肺癌的测试包括但不限于x射线、针对高水平的某些物质(例如钙)的血液测试、ct扫描和肿瘤活组织检查。肺癌的家族史或暴露于肺癌的风险因素(例如,吸烟或暴露于烟雾和/或空气污染)也可有助于确定对象是否可能患有肺癌或有助于进行肺癌癌症的诊断。
癌症可包括但不限于癌,包括腺癌、淋巴瘤、胚细胞瘤、黑素瘤、肉瘤、白血病、鳞状细胞癌、小细胞肺癌、非小细胞肺癌、胃肠癌、霍奇金和非霍奇金淋巴瘤、胰腺癌、成胶质细胞瘤、基底细胞癌、胆道癌、膀胱癌、包括成胶质细胞瘤和成神经管细胞瘤在内的脑癌;乳腺癌、宫颈癌、绒毛膜癌;结肠癌、结直肠癌、子宫内膜癌、子宫内膜癌;食管癌、胃癌;多种类型的头颈部癌症、包括鲍恩病(bowen’sdisease)和佩吉特病(paget’sdisease)在内的上皮内肿瘤;包括急性淋巴细胞白血病和急性髓细胞性白血病在内的血液肿瘤;卡波西肉瘤(kaposi’ssarcoma)、毛细胞白血病;慢性髓细胞性白血病、艾滋病相关白血病和成人t细胞白血病淋巴瘤;肾癌,例如肾细胞癌、t细胞急性淋巴细胞白血病/淋巴瘤、包括霍奇金病和淋巴细胞淋巴瘤在内的淋巴瘤;肝癌例如肝癌和肝癌、梅克尔细胞癌(merkelcellcarcinoma)、黑素瘤、多发性骨髓瘤;成神经细胞瘤;包括鳞状细胞癌在内的口腔癌;包括由上皮细胞引起的卵巢癌在内的卵巢癌、包括平滑肌肉瘤、横纹肌肉瘤、脂肪肉瘤、fibros1肉瘤和骨肉瘤在内的肉瘤;胰腺癌;包括黑素瘤、间质细胞、生殖细胞和间充质细胞在内的皮肤癌;prosltate癌症,直肠癌;外阴癌,包括腺癌在内的肾癌;睾丸癌,其包括生殖器肿瘤,例如精原细胞瘤、非精原细胞瘤(畸胎瘤、绒毛膜癌)、间质瘤和生殖细胞肿瘤;包括甲状腺腺癌和髓样癌在内的甲状腺癌;食管癌、唾液腺癌和肾母细胞瘤。在一些实施方案中,癌症可以是肺癌。
多重方法
本文描述的方法可以以多重形式使用。在本文所述方法的实施方案中,多重应用可包括确定与一种或更多种已知靶核苷酸序列邻接的核苷酸序列。如本文所用,“多重扩增”是指涉及在一个或更多个反应容器中同时扩增多于一种靶核酸的过程。在一些实施方案中,方法涉及使用一组或更多组引物随后确定多重扩增产物的序列。多重可以指在单个反应中检测约2至1,000个不同的靶序列。然而,在一些实施方案中,多重可以指在单个反应中检测约1,000至10,000个不同的靶序列。在一些实施方案中,多重可以指在单个反应中检测约10,000至100,000个不同的靶序列。如本文所用,多重是指在单个反应中检测2至1,000个不同的靶序列之间的任何范围,例如,5至500个、25至1,000个或10至100个不同的靶序列等。术语“多重”在应用于pcr时意味着在同一pcr反应中存在对至少两种不同靶序列具有特异性的引物。
在一些实施方案中,可以用多个引物(例如,多个第一和第二靶特异性引物)扩增样品中的靶核酸或样品的分离部分。在一些实施方案中,多个引物(例如,多个第一和第二靶特异性引物)可以存在于单一反应混合物中,例如,可以在同一反应混合物中产生多个扩增产物。在一些实施方案中,多个引物(例如,多组第一和第二靶特异性引物)可以与由单独的基因构成的已知靶序列特异性退火。在一些实施方案中,至少两组引物(例如,至少两组第一和第二靶特异性引物)可以与已知靶序列的不同部分特异性退火。在一些实施方案中,至少两组引物(例如,至少两组第一和第二靶特异性引物)可以与由单个基因构成的已知靶序列的不同部分特异性退火。在一些实施方案中,至少两组引物(例如,至少两组第一和第二靶特异性引物)可以与包含已知靶序列的基因的不同外显子特异性退火。在一些实施方案中,多个引物(例如,第一靶特异性引物)可包含相同的5’标签序列部分。
在本文所述方法的实施方案中,多重应用可包括在一个测序反应或测序运行中确定与多个样品中的一个或更多个已知靶核苷酸序列邻接的核苷酸序列。在一些实施方案中,多个样品可以具有不同的来源,例如来自不同组织和/或不同对象。在此类实施方案中,引物(例如,加尾随机引物)还可包含条形码部分。在一些实施方案中,可以将具有独特条形码部分的引物(例如,加尾随机引物)添加至每个样品中并与其中的核酸连接;随后可以合并样品。在此类实施方案中,扩增产物的每个所得测序读取将包含条形码,其识别含有扩增产物所来源的模板核酸的样品。
实施例
以下实施例旨在说明本文所述的某些实施方案,包括本发明的某些方面,但不是举例说明本发明的全部范围。
实施例1:技术特异性衔接子核酸的设计
设计并产生适用于多种下一代测序技术的衔接子核酸和相应的衔接子引物。
可用于illumina特定应用的衔接子核酸和衔接子引物的实例如下所示:
illumina特异性衔接子核酸和衔接子引物
顶部(扩增)链(5’→3’):
,其中“n”代表分子条形码序列的核苷酸,“*t”代表具有硫代磷酸酯键的t。
底部(阻断)链(5’→3’):
5phosctcctggcggttt(seqidno.:2),其中“t”代表经修饰的胸腺嘧啶核碱基(例如反向的胸腺嘧啶)
第一衔接子引物(5’→3’):
第二衔接子引物(5’→3’):
如所示出的,第一和第二衔接子引物含有与顶部(扩增)链的一部分相同的序列。作为该设计的结果,每个引物能够分别在第一和第二pcr步骤期间引发由第一和第二靶特异性引物产生的互补链。该实施例中的第二衔接子引物含有两个另外的核苷酸,并且相对于第一衔接子引物嵌套。
可用于离子半导体特定应用的衔接子核酸和衔接子引物的实例如下所示:
离子特异性衔接子核酸和衔接子引物
顶部(扩增)链(5’→3’):
,其中“n”代表分子条形码序列的核苷酸,“*t”代表具有硫代磷酸酯键的t。
底部(阻断)链(5’→3’):
5phosgatcggaagagct(seqidno.:6),其中“t”代表经修饰的胸腺嘧啶核碱基(例如反向的胸腺嘧啶)
第一衔接子引物(5’→3’):
第二衔接子引物(5’→3’):
如所示出的,第一和第二衔接子引物含有与顶部(扩增)链的一部分相同的序列。作为该设计的结果,每个引物能够分别在第一和第二pcr步骤期间引发由第一和第二靶特异性引物产生的互补链。该实施例中的第二衔接子引物含有10个另外的核苷酸,并且相对于第一衔接子引物嵌套。
实施例2:制备用于分析的核酸样品
说明制备用于分析的核酸样品的方法的工作流程的实例示于图5中。用随机引物对rna分子样品进行退火。例如,通过向样品中添加随机六聚体,然后在65℃下加热5分钟,可以实现这种退火。退火后,使用逆转录酶通过引物延伸(例如,在室温下)实现第一链cdna合成以产生dna/rna杂交体。
此时,可以进行“preseq”rnaqc测定以评估文库复杂性。使用该测定中,600ng随机六聚体(在65℃下退火5分钟)与使用100ng随机六聚体(在65℃下退火5分钟)进行比较。“ct”值的确定提供了文库复杂性的指示以及在后续步骤中分子条形码膨胀的可能性的预测。通常,阈值ct为28用作基准,低于该阈值的值是最理想的。发现提高随机引物浓度有利地使ct最小化。
在任选的preseq测定之后,例如通过用rna酶h处理样品来切割dna/rna杂合体的rna。所得的与dna保持杂交的rna片段用作第二链cdna合成的引物。这是使用dnapoli并将样品例如在16℃下孵育60分钟来实现的。在此期间之后,通过加热(例如,通过在75℃下孵育样品20分钟)使dnapoli失活。发现dnapoli的热失活极大地提高了后续样品制备步骤中的样品完整性。
如图6所示,与没有进行热失活相比,dnapoli产生的样品的热失活在第二链合成之后通过凝胶色谱法显示出更干净的条带。假定dnapoli在末端修复期间变得活跃并且由于其5’→3’和/或3’→5’核酸外切酶活性而破坏片段——第二链合成之后dnapoli的热失活阻止了这种情况的发生。
对双链cdna样品进行末端修复以使cdna产生平末端并使5’端磷酸化。在该步骤中,将过量的t4dna聚合酶和t4多核苷酸激酶与足够的dntp一起添加至样品中并使其孵育(例如,在25℃下孵育30分钟)。在此期间之后进行ampure净化(2.5x)是至关重要的,因为它在用生物素标记的datp加尾之前从文库制备物中去除了剩余的datp。该净化步骤阻止用datp而不是生物素-datp标记文库片段,这将导致在捕获步骤期间丢失错误标记的片段。
在第一次连接步骤中使用klenow片段(3’-5’exo-)用生物素标记的datp对文库片段的3’端进行a加尾。例如,这可通过将样品和必要组分在37℃下孵育15分钟来实现。a加尾之后的ampure净化(2.5x)是至关重要的,因为它在捕获步骤之前从文库制备物中去除剩余的生物素标记的datp。该净化防止游离生物素-datp使链霉抗生物素蛋白结合位点饱和,导致捕获期间文库片段的丢失。
在第二连接步骤中,使用dna连接酶将衔接子核酸与生物素-a-加尾的文库片段连接。有趣的是,发现向连接混合物中添加拥挤剂极大地提高了所有末端碱基的连接效率。如图7所示,不管5’端碱基,包含10%peg进一步使非连接片段(无)和单连接片段(l1)最小化,同时伴随提高双连接片段(l2)。此外,与在60分钟内进行的“标准”方案相比,在10%peg的情况下,在5分钟内实现了衔接子连接。进一步的数据表明,20%peg更进一步提高了连接效率(未示出)。
图8a示出了在这些实验中使用的核酸衔接子。如所示出的,顶链(扩增链)在5’→3’方向上含有通用衔接子引物位点区域、样品索引区域、测序引物位点区域、分子条形码区域、3’双链体部分和3’t单链突出端。底链(阻断链)含有与顶链的3’双链体部分形成双链的共有区域、5’磷酸化末端和防止链延伸的反向dt碱基。
在衔接子连接后,通过链霉抗生物素蛋白包被的珠捕获文库片段来进行连接净化。这是使用m-280链霉抗生物素蛋白dynabead(10mg/ml浓度,储存在pbs±0.1%bsa+0.02%叠氮化物中)进行的。在将珠添加至样品中之前,将存储缓冲液与连接净化缓冲液(1mnacl,1mmedta,0.1%吐温,10mmtrisph8)交换。将连接的dna产物(50μl)与连接净化珠(50μl,总共100μl)混合。随后将磁场施加至样品上以捕获文库片段,并除去上清液。然后将结合文库的珠转移至单独的组分混合物中用于第一pcr步骤。
使用第一靶特异性引物和第一衔接子引物进行第一轮pcr。第一衔接子引物与扩增链的至少一部分相同,使得其与由第一靶特异性引物产生的互补链退火。使用第二靶特异性引物和第二衔接子引物进行第二轮pcr,后者与扩增链的一部分类似地相同。第二靶特异性引物相对于第一靶特异性引物嵌套,并通过另外的引物进一步接触。
如图8b所示,第二靶特异性引物含有不与靶特异性区域杂交的5’尾。包含另外的引物,其包含与5’尾相同的区域以及第二样品索引区域和测序衔接子区域。以这种方式,第二靶特异性引物引发模板链以产生具有非共有加尾区域的互补链。如在第一轮pcr中,第二衔接子引发该互补链以产生模板链的拷贝。由于模板链的这个拷贝将包含与5’尾序列互补的区域,含有第二样品索引区和测序衔接子区的另外的引物将引发该序列以产生可用于测序的底链。
等同物
虽然本文描述并举例说明了本发明的几个实施方案,但本领域普通技术人员将容易预见到用于执行本文所述的功能和/或获得结果和/或一种或更多种优势的多种其他手段和/或结构,并且每种这样的改变和/或修改都被认为在本文所述的本发明的范围之内。更一般地,本领域技术人员将容易理解,本文所描述的所有参数、尺寸、材料和构造都意在为示例性的,并且实际的参数、尺寸、材料和/或构造将根据使用本发明教导的具体应用。本领域技术人员将认识到,或能够仅使用常规实验确定本文所描述的本发明具体实施方案的许多等效方案。因此,应当理解的是,前面的实施方案仅仅通过实例的方式展示,并且除非特别描述并要求,本发明的实施方案可以在所附权利要求范围及其等同的范围内实施。本公开内容的本发明的实施方案涉及本文所描述的每个单独的特征、系统、制品、材料、套件和/或方法。此外,如果该特征、系统、制品、材料、套件和/或方法并非互不相同,则任何两个或更多个该特征、系统、制品、材料、套件和/或方法的组合也包含在本公开内容的本发明的范围内。
如本文所定义和使用的所有定义应理解为支配所定义项目的字典定义、在被合并以作参考的文献中的定义以及/或者其通常含义。
本文公开的所有参考文献、专利和专利申请均关于其所引用的主题通过引用并入本文,该主题在某些情况下可涵盖整个文件。
除非明确相反指明,否则本文在说明书和权利要求中所使用的不定冠词“一个/种”应理解为意指“至少一个/种”。
本文在说明书和权利要求中使用的短语“和/或”应理解为意指相关联的要素(即在某些情况下相关联存在,而在其他情况下不相关联地存在的要素)中的“任意一个或二者”。用“和/或”列出的多个元素应以相同的方式解释,即,如此结合的“一个或更多个”元素。除了被“和/或”分句特别地确定的要素之外,其他要素可以任选地存在,无论其与特别确定的那些要素是否相关。因此,作为一个非限制实例,提及“a和/或b”,当与开放性语句如“包含/括”结合使用时,在一个实施方案中,可指仅有a(任选地,包括除了b之外的要素);在另一个实施方案中,指仅有b(任选地,包括除了a之外的要素);在另一个实施方案中,指a与b二者(任选地,包括其他要素);等。
本文在说明书和权利要求中使用的“或”应该理解为与上文定义的“和/或”具有相同含义。例如,当分离列表中的项时,“或”或者“和/或”应被解释为包括性的,即在许多要素或要素列表中,以及任选地另外的未列出的项中,包括至少一个/种,但也包括多于一个/种的要素。仅当术语明确相反指明,例如“只有其中之一”或“恰好其中之一”,或者当在权利要求中使用“由……组成”时,将指包含许多要素或要素列表中的恰好一个/种要素。一般而言,当前面是排他性术语例如“任一”、“其中之一”、“仅其中之一”或“恰好其中之一”时,本文所使用的术语“或”应当仅被解释为排除性的选择(即,“一个或另一个,但并非二者全部”)。当在权利要求中使用“基本上由……组成”时,应当具有其用于专利法领域中的通常含义。
本文在说明书和权利要求中使用的短语“至少一个/种”涉及一系列的一个/种或更多个/种要素,应当被理解为意指在要素列表中,选自任何一个/种或更多个/种要素的至少一个/种要素,但未必包括该要素列表中具体列出的各个/种和每个/种要素中的至少一个/种,并且不排除该要素列表中的任何要素的组合。该定义也允许除了在要素列表中被具体确定的、短语“至少一个/种”所指的要素以外,其他要素可任选的存在,无论是否与具体确定的那些要素相关。因此,作为一个非限制性实例,“a和b中的至少一个/种”(或等同的,“a或b中的至少一个/种”,或等同的,“a和/或b中的至少一个/种”)在一个实施方案中可指至少一个/种(任选地包括多于一个/种)a,而不存在b(且任选地包括除b之外的要素);在另一个实施方案中,指至少一个/种(任选地包括多于一个/种)b,而不存在a(且任选地包括除a之外的要素);在另一个实施方案中,指至少一个/种(任选地包括多于一个/种)a,和至少一个/种(任选地包括多于一个/种)b(并且任选地包括其他要素);等。
还应该理解,除非明确相反地指出,否则在本文要求保护的包括多于一个步骤或操作的任何方法中,该方法的步骤或操作的顺序不一定限于所记载的该方法的步骤或操作的顺序。
在权利要求以及在上述的说明书中,所有的过渡短语如“包含”、“包括”、“带有”、“具有”、“含有”、“涉及”、“保持”、“由……构成”等应理解为开放式的,即意为包括但不限于。如美国专利局的专利审查程序手册(theunitedstatespatentofficemanualofpatentexaminingprocedures),2111.03章所述,只有过渡短语“由……组成”和“基本上由……组成”应分别为封闭式或半封闭式过渡短语。应当理解,在作为替选的实施方案中,在本文件中描述的使用开放式过渡短语(例如,“包含/括”)的实施方案也被认为是“由开放式过度短语所述的特征组成”和“基本上由开放式过度短语所述的特征组成”。例如,如果本公开内容描述了“包含a和b的组合物”,则本公开内容还考虑了作为替选的实施方案“由a和b组成的组合物”和“基本上由a和b组成的组合物”。
序列表
<110>archerdx,inc.
<120>核酸样品制备方法
<130>a1100.70013
<150>us62/395,339
<151>2016-09-15
<160>8
<170>patentinversion3.5
<210>1
<211>91
<212>dna
<213>人工序列
<220>
<223>合成寡核苷酸
<220>
<221>misc_feature
<222>(71)..(78)
<223>nisa,c,g,ort
<400>1
aatgatacggcgaccaccgagatctacacatccgtacacactctttccctacacgacgct60
cttccgatctnnnnnnnnaaccgccaggagt91
<210>2
<211>13
<212>dna
<213>人工序列
<220>
<223>合成寡核苷酸
<400>2
ctcctggcggttt13
<210>3
<211>26
<212>dna
<213>人工序列
<220>
<223>合成寡核苷酸
<400>3
aatgatacggcgaccaccgagatcta26
<210>4
<211>28
<212>dna
<213>人工序列
<220>
<223>合成寡核苷酸
<400>4
atgatacggcgaccaccgagatctacac28
<210>5
<211>61
<212>dna
<213>人工序列
<220>
<223>合成寡核苷酸
<220>
<221>misc_feature
<222>(41)..(48)
<223>nisa,c,g,ort
<400>5
ccatctcatccctgcgtgtctccgactcagctaaggtaacnnnnnnnngctcttccgatc60
t61
<210>6
<211>13
<212>dna
<213>人工序列
<220>
<223>合成寡核苷酸
<400>6
gatcggaagagct13
<210>7
<211>20
<212>dna
<213>人工序列
<220>
<223>合成寡核苷酸
<400>7
ccatctcatccctgcgtgtc20
<210>8
<211>30
<212>dna
<213>人工序列
<220>
<223>合成寡核苷酸
<400>8
ccatctcatccctgcgtgtctccgactcag30
- 还没有人留言评论。精彩留言会获得点赞!