一种抗肿瘤多肽及其应用的制作方法
本发明涉及多肽药物
技术领域:
,特别涉及一种抗肿瘤多肽及其应用。
背景技术:
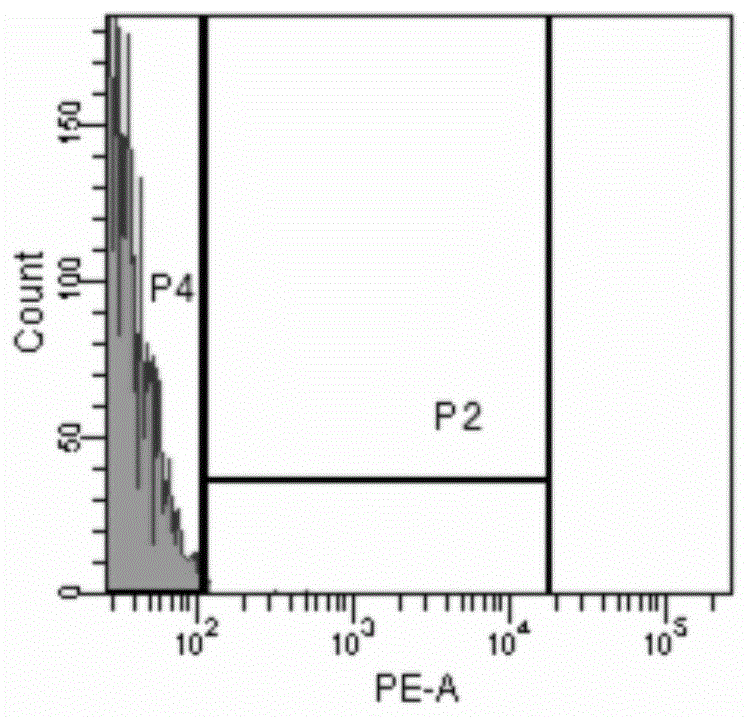
:多肽是由一种或多种氨基酸以肽键连接在一起而形成的化合物,通常由10~100个氨基酸分子脱水缩合而成,它们的分子量<10000da。多肽是蛋白质发挥作用的活性基团,是涉及生物体内各种细胞功能的生物活性物质,参与调控各种生理功能,因而在临床应用上具有非常重要的开发价值。活性多肽的来源分为天然活性多肽、基于天然产物的人工修饰多肽以及人工合成的活性多肽。天然多肽的来源十分广泛,可分为动物生物活性多肽和植物多肽。随着科技的发展,天然多肽已经不是唯一的多肽来源,取而代之的是基因重组多肽和化学合成的多肽。生物活性肽的合成方法包括液相合成、固相合成、酶促合成和组合生物合成。液相合成有逐步合成和片段合成2种策略,对于合成较少氨基酸的多肽方便快速,纯度高,且能大量合成。固相合成是将氨基酸的c末端固定在不溶性树脂上,然后依次缩合氨基酸的方法。该方法简化了每一步反应的后处理操作,具有较高产率,缺点是每步中间产物不能纯化,且终产物必须通过可靠的分离手段进行纯化。液相合成和固相合成都属于化学合成,目前开发上市的多肽药物中,90%为化学合成,应用广泛。酶促合成是利用某些特定的酶来催化反应的生物合成方法,反应条件温和、立体专一性强,缺点是存在许多不良反应、酶容易变性失活。组合生物合成是通过对微生物代谢途径中一些酶编码基因进行操作,从而获得新的产物。由于该方法成本昂贵,并且有真核基因表达易形成不恰当折叠及翻译后修饰等问题,从而阻碍了其广泛应用。目前局部癌症虽然可以成功地运用外科手术和放射疗法治疗,但化学疗法仍是常规治疗晚期或转移性肿瘤的首选。由于化疗药物存在选择性低、不良反应大、多药耐药等缺陷,很大程度上限制了其使用。单抗类肿瘤靶向疗法虽然解决了靶向性的问题,但其蛋白分子量大,免疫原性高,易产生过敏及免疫交叉反应,且由于研发成本高,研发难度大,产能有限等原因导致其售价高昂,普通癌症患者很难普及使用,同时单抗类药物存在剂型比较单一,给药方式多为静脉注射或滴注,无法口服等问题,使得药物应用十分不便。受技术条件的制约,多数抗肿瘤肽类药物的半衰期较短,但抗肿瘤多肽具有其独特的优势:与小分子化学药物相比,对目标肿瘤具有更高的亲和力和更强的特异性,并且不良反应低,还可以增加肿瘤对其他治疗方法的敏感度;与抗体相比,由于它们体积微小,因此更容易渗透到组织中;可以化学合成,并且可以运用多种手段进行化学修饰,有助于设计和研究新型活性多肽。新型抗肿瘤活性多肽具有高亲和力、强特异性、低不良反应的特点,此外大多数还具选择性靶向肿瘤细胞的性质,因而在临床应用上具有非常重要的开发价值,作为抗肿瘤化合物具有较好的前景。技术实现要素:本发明所要解决的技术问题:针对目前单抗类药物和化疗类药物在治疗肿瘤中存在的诸多缺点,本发明提供一种抗肿瘤多肽及在制备抗肿瘤药物中的应用。为解决上述技术问题,本发明提供以下的技术方案:一种抗肿瘤多肽,包含ccndeglemrik和gdaslkmdksdav两段氨基酸序列,多肽的氨基酸序列为ccndeglemrik-linker-gdaslkmdksdav;或gdaslkmdksdav-linker-ccndeglemrik;或gdaslkmdksdavccndeglemrik。优选地,所述linker的氨基酸序列为dptgg或g3s重复1-2遍。优选地,多肽氨基酸序列为(1)ccndeglemrik-dptgg-gdaslkmdksdav;或(2)gdaslkmdksdav-dptgg-ccndeglemrik;或(3)ccndeglemrik-gggsgggs-gdaslkmdksdav;或(4)gdaslkmdksdav-gggsgggs-ccndeglemrik;或(5)ccndeglemrik-gggs-gdaslkmdksdav;或(6)gdaslkmdksdav-gggs-ccndeglemrik或(7)gdaslkmdksdavccndeglemrik。优选地,所述多肽采用fmoc固相合成法制备,包括如下具体步骤:(1)称取适量fmoc-ala(otbu)-wangresin加入多肽固相合成管并加入dcm,溶胀树脂30min;(2)溶胀后抽干,加入dmf洗涤三次并再次抽干,加入脱帽液;(3)密封后放入摇床中震荡反应20min,抽干后每次加入50mldmf洗涤5次并抽干;(4)取30g处理好的树脂加入验色剂,在100℃水浴锅中加热1.5min,观察颜色;(5)验色通过后按照多肽的氨基酸序列进行第二个氨基酸的缩合,投料量与树脂的摩尔比为3:1,35℃反应60min后抽干,50mldmf洗涤5次并抽干;(6)取缩合后的树脂30g加入验色剂,100℃加热90s,树脂无色透明,溶液淡黄色即验色通过;(7)重复步骤(4)~(6),直至将最后一个氨基酸缩合完成,脱去保护基团fmoc,50mldmf洗涤9次后再用50mldcm及50ml无水甲醇各洗涤三次,抽干,真空干燥即得干燥肽树脂;(8)取1g干燥肽树脂加入10ml切割液,在室温密闭反应2h,砂芯漏斗抽滤,收集滤液;(9)将滤液加入无水乙醚中,滤液与无水乙醚的体积比为1:10,多肽析出后抽滤,收集滤饼,35℃真空干燥4h,得到多肽粗品;(10)采用反相液相色谱对多肽粗品进行纯化,色谱柱采用c18反相硅胶柱。上述的抗肿瘤多肽在制备抗肿瘤药物中的应用。优选地,所述多肽可用于治疗实体瘤,所述实体瘤包括胃癌、食道鳞癌、非小细胞肺癌、结肠癌、肝癌、黑色素瘤、口腔鳞癌、乳腺癌。优选地,所述抗类风湿性关节炎药物包含有效剂量的抗类风湿性关节炎多肽及其他药学上可接受的辅料或载体,所述药物载体包括有机和无机载体,口服和肠道给药途径适合加入有机载体,有机载体包括淀粉、乳糖、氧化钙硬脂酸盐、植物油、有机增溶剂中的一种或多种,所述有机增溶剂包括聚乙二醇、甘油、水溶性的有机和无机碱中的一种或多种,抗类风湿性关节炎药物被制成固体形式或液体形式,这些各种形式的抗类风湿性关节炎药物制备完成后被灭菌。优选地,所述抗肿瘤药物的剂型为片剂、注射剂、喷雾剂、胶囊或包衣药丸,所述注射剂的给药方式为静脉、皮下或肌肉注射。优选地,所述抗肿瘤药物的给药部位包括全身给药和局部给药,全身给药为口服、静脉注射或滴注、皮下注射或肌肉注射,局部给药为肿瘤组织内注射、肿瘤周边组织注射。本发明获得的有益效果:(1)本发明的多肽可以靶向至肿瘤新生血管,抑制新生血管形成,达到预防或治疗肿瘤的目的;本发明的多肽还可以cd47-sirpα阻断免疫检查点,解除肿瘤细胞对免疫细胞的抑制,抑制免疫逃逸,在抑制血管新生的同时促进自身免疫系统对肿瘤的攻击,达到预防或治疗肿瘤的目的;(2)本发明的多肽对肿瘤的靶向性、亲和性较高,还可以增加肿瘤对其他治疗方法的敏感度;与阻断抗体相比,免疫原性低,不良反应率低,可通过化学方法合成,制备和纯化过程更为简单,生产效率高;(3)本发明的多肽分子量较小,可穿多种生理屏障,有利于全身给药时药物在目标位置的扩散和靶向。(4)本发明的氨基酸序列中采用柔性肽段连接两个功能片段,可有效提高药效,增强药物稳定性,延长半衰期。(5)本发明的多肽具有多种抗肿瘤功效,可对多种不同起源的肿瘤细胞增殖具有较高的抑制率,在有效给药浓度下,对黑色素瘤、胃癌、肝癌的抑制率达到60%以上;在有效给药浓度下,对食道鳞癌、非小细胞肺癌、结肠癌、口腔鳞癌、乳腺癌的抑瘤率可达50%以上。附图说明图1:空白组流式细胞术荧光强度图;图2:pe标记序列2多肽组流式细胞术荧光强度图;图3:pe标记序列4多肽组流式细胞术荧光强度图;图4:pe标记序列6多肽组流式细胞术荧光强度图;图5:pe标记序列7多肽组流式细胞术荧光强度图;图6:鼠抗人sirpα单抗+pe标记序列2多肽组流式细胞术荧光强度图;图7:鼠抗人sirpα单抗+pe标记序列4多肽组流式细胞术荧光强度图;图8:鼠抗人sirpα单抗+pe标记序列6多肽组流式细胞术荧光强度图;图9:鼠抗人sirpα单抗+pe标记序列7多肽组流式细胞术荧光强度图;具体实施方式本发明中的ccndeglemrik序列来源于人vegf165蛋白ccndegle为86~93位氨基酸残基,mrik为107~110位氨基酸残基,二者皆为vegf165与其受体的表面结合位点,将两个肽段的氨基酸序列整合后人工合成新的氨基酸序列可有效结合vegf受体,但无受体激活结构域,因而无受体激活的能力,竞争性的抑制vegf信号通路,从而抑制肿瘤组织中强烈的血管新生。gdaslkmdksdav序列来源于人cd47蛋白94~106位氨基酸残基,此序列位于cd47胞外段的免疫球蛋白样结构域,免疫球蛋白样结构域是cd47与其配体sirp-α相互识别和结合的区域,人工合成的gdaslkmdksdav序列可特异性的结合于巨噬细胞表面的sirp-α蛋白上,竞争性的抑制sirp-α与cd47的结合,cd47与sirp-α免疫检查点阻断后可解除肿瘤细胞对巨噬细胞的抑制作用,使得巨噬细胞识别并攻击肿瘤细胞,从而达到杀伤和抑制肿瘤细胞增殖的目的。抗肿瘤多肽靶向结合巨噬细胞表面的sirp-α分子后,在促进巨噬细胞吞噬肿瘤细胞的同时与肿瘤组织内的血管内皮细胞上的vegfr2结合,进一步抑制肿瘤组织内的血管新生,阻断肿瘤组织内的血供,使肿瘤组织缺乏氧气和营养供给,改变肿瘤组织微环境,最终抑制肿瘤细胞增殖和杀伤肿瘤细胞。下面通过对实施例的描述,对本发明的具体实施方式作进一步详细的说明,以帮助本领域的技术人员对本发明的发明构思、技术方案有更完整、准确和深入的理解。实施例1:本发明中抗肿瘤多肽采用fmoc固相合成法制备,具体方法如下:(1)称取5gfmoc-ala(otbu)-wangresin加入多肽固相合成管并加入50mldcm,溶胀树脂30min;(2)溶胀后抽干,加入50mldmf洗涤三次并再次抽干,加入脱帽液50ml;(3)密封后放入摇床中震荡反应20min,抽干后每次加入50mldmf洗涤5次并抽干;(4)取30g处理好的树脂加入验色剂,在100℃水浴锅中加热1.5min,观察颜色,若树脂棕黄色,溶液蓝紫色,说明fmoc已被脱除,若树脂无色,溶液颜色很淡则需要重复上述脱帽步骤至验色通过;(5)验色通过后按照多肽的氨基酸序列进行第二个氨基酸的缩合,投料量与树脂的摩尔比为3:1,35℃反应60min后抽干,50mldmf洗涤5次并抽干;(6)取缩合后的树脂30g加入验色剂(茚三酮、苯酚、吡啶各100μl),100℃加热90s,树脂无色透明,溶液淡黄色即验色通过;(7)重复步骤(4)~(6),按照表1中的氨基酸序列逐个缩合氨基酸原料,直至将最后一个氨基酸缩合完成。脱去保护基团fmoc,50mldmf洗涤9次后再用50mldcm及50ml无水甲醇各洗涤三次,抽干,真空干燥即得干燥肽树脂;(8)取1g干燥肽树脂加入10ml切割液,在室温密闭反应2h,砂芯漏斗抽滤,收集滤液;(9)将滤液加入无水乙醚中,滤液与无水乙醚的体积比为1:10,多肽析出后抽滤,收集滤饼,35℃真空干燥4h,得到多肽粗品;(10)采用反相液相色谱对多肽粗品进行纯化,色谱柱采用c18反相硅胶柱(具体纯化方法和条件参见zhux,robertsonjt,sackshs,dohanfc,tsengjl,desideriodm.peptides.,1995,16(6):1097一1107)。表1多肽氨基酸序列表编号氨基酸序列1ccndeglemrik-dptgg-gdaslkmdksdav2gdaslkmdksdav-dptgg-ccndeglemrik3ccndeglemrik-gggsgggs-gdaslkmdksdav4gdaslkmdksdav-gggsgggs-ccndeglemrik5ccndeglemrik-gggs-gdaslkmdksdav6gdaslkmdksdav-gggs-ccndeglemrik7gdaslkmdksdavccndeglemrik其中,dptgg、gggsgggs、gggs均为柔性连接肽。纯化后多肽的纯度为92.3%,用于后续的动物体内抗肿瘤药效实验。实施例2:抗肿瘤药物的制备按如下配方制备组合物片剂:表2抗肿瘤药物组分表组分含量氨基酸序列1多肽50mg玉米淀粉278mg乳糖70mg氧化钙硬脂酸盐2mg共计400mg采用实施例1中制备的多肽(氨基酸序列1)和乳糖通过玉米淀粉糊粘结形成颗粒,干燥后,加入玉米淀粉和氧化钙硬脂酸盐,混合物被制片机压制成2毫米厚,400mg重,9sce硬度的片剂。实施例3:抗肿瘤药物的制备按如下配方制备组合物栓剂:表3抗肿瘤药物组分表组分含量氨基酸序列2多肽50mg滑石粉250mg植物油25mg碳酸氢钠25mg平均分子量为4000的聚乙二醇50mg共计400mg按照常规药物制剂方法(参考《现代药剂学》)制备以实施例1中制备的多肽(氨基酸序列2)为主要活性成分的栓剂。实施例4:抗肿瘤药物的制备按如下配方制备组合物胶囊:表4抗肿瘤药物组分表以食用明胶作为胶囊壳,按照常规药物制剂方法(参考《现代药剂学》)制备以实施例1中制备的多肽(氨基酸序列3)为主要活性成分的胶囊。实施例5:抗肿瘤药物注射液的制备注射液母液配方如下:表5抗肿瘤药物组分表组分含量氨基酸序列4多肽10mg甘油0.01ml二乙醇胺0.005ml生理盐水0.985ml各组分充分混合溶解后0.22μm滤膜过滤除菌,无菌分装入填充有氮气的安瓿瓶中,使用时采用生理盐水将母液稀释1000倍作为工作液。实施例6:抗肿瘤药物注射液的制备注射液母液配方如下:表6抗肿瘤药物组分表组分含量氨基酸序列5多肽25mg甘油0.1ml二乙醇胺0.15ml生理盐水0.75ml各组分充分混合制备完成后0.22μm滤膜过滤除菌,无菌分装入填充有氮气的安瓿瓶中,使用时采用生理盐水将母液稀释1000倍作为工作液。实施例7:抗肿瘤药物乳剂的制备组合物配方如下:表7抗肿瘤药物组分表组分含量氨基酸序列6多肽1mg甘油0.2ml生理盐水0.8ml力保肪宁9ml精确称量氨基酸序列6的多肽,溶于生理盐水中,再加入甘油和力保肪宁充分搅拌后分装,辐照灭菌。实施例8:抗肿瘤药物注射剂的制备组合物配方如下:表8抗肿瘤药物组分表组分含量氨基酸序列7多肽40mg甘露醇0.2ml生理盐水1.8ml制备及使用方法同实施例6。实施例9:采用实施例2中制备的抗肿瘤药物进行抗肿瘤体内实验。实验材料:18~22g雄性裸小鼠50只;肿瘤细胞株为胃癌mgc-803,将实施例2中制备的抗肿瘤药物溶于无菌生理盐水中,使终浓度为0.2mg/ml,0.22微米滤膜过滤后无菌分装,4℃保存备用。avastin和多西他赛注射液,均购自江苏先声再康医药有限公司。实验方法:(1)将mgc-803细胞在37℃,5%co2培养箱中培养至密度80%以上,培养基为含10%fbs的dmem高糖培养基,用0.25%的胰蛋白酶消化液消化收集细胞,1000rpm离心弃上清,生理盐水洗涤三遍后重悬计数至5×107/ml,4℃保存备用。(2)将肿瘤细胞细胞悬液接种至裸小鼠前肢腋下,0.1ml/只,空白对照组不处理,接种后每三天观察出瘤情况,在肿瘤体积达到0.1mm3时分组给药。(3)设置空白对照组、模型组、实施例2给药组和阳性对照组,每组8只小鼠,阳性药采用avastin和多西他赛注射液,avastin的给药剂量为15mg/kg,每三天给药一次,多西他赛注射液的给药剂量为5mg/kg每7天给药一次,阳性药的给药方式均为静脉注射。空白对照组不做任何处理,模型组在造模后给予生理盐水灌胃,给药体积0.1ml/10g,给药组给予抗肿瘤药物溶液灌胃,给药体积0.1ml/10g,每日给药一次。(4)给药21天后测量肿瘤体积,计算抑瘤率,计算公式如下:抑瘤率(%)=(模型组肿瘤体积-给药组肿瘤体积)/模型组肿瘤体积实验结果如下:表9各组药物抗肿瘤药效组别有效成分抑瘤率(%)实施例2序列1多肽68.6avastin单抗61.2多西他赛注射液紫杉醇51.9实施例10:采用实施例3中制备的抗肿瘤药物进行抗肿瘤体内实验。实验材料:18~22g雄性裸小鼠50只;肿瘤细胞株为食道鳞癌kyse-30,将实施例3中制备的抗肿瘤药物溶于无菌生理盐水中,使终浓度为0.2mg/ml,0.22微米滤膜过滤后无菌分装,4℃保存备用。avastin和多西他赛注射液,均购自江苏先声再康医药有限公司。实验方法:同实施例1实验结果如下:表10各组药物抗肿瘤药效实施例11:采用实施例4中制备的抗肿瘤药物进行抗肿瘤体内实验。实验材料:18~22g雄性裸小鼠50只;肿瘤细胞株为黑色素瘤b16f10,将实施例4中制备的抗肿瘤药物溶于无菌生理盐水中,使终浓度为0.2mg/ml,0.22微米滤膜过滤后无菌分装,4℃保存备用。avastin和多西他赛注射液,均购自江苏先声再康医药有限公司。实验方法:同实施例1实验结果如下:表11各组药物抗肿瘤药效组别有效成分抑瘤率(%)实施例4序列3多肽66.4avastin单抗65.9多西他赛注射液紫杉醇55.8实施例12:采用实施例5中制备的抗肿瘤药物进行抗肿瘤体内实验。实验材料:18~22g雄性裸小鼠60只;肿瘤细胞株为结肠癌hct-116,将实施例5中制备的抗肿瘤药物采用无菌生理盐水稀释1000倍后给药,药物终浓度为10μg/ml,0.22微米滤膜过滤后无菌分装,4℃保存备用。avastin和多西他赛注射液,均购自江苏先声再康医药有限公司。实验方法:(1)将hct-116细胞在37℃,5%co2培养箱中培养至密度80%以上,培养基为含10%fbs的dmem高糖培养基,用0.25%的胰蛋白酶消化液消化收集细胞,1000rpm离心弃上清,生理盐水洗涤三遍后重悬计数至5×107/ml,4℃保存备用。(2)将肿瘤细胞细胞悬液接种至裸小鼠前肢腋下,0.1ml/只,空白对照组不处理,接种后每三天观察出瘤情况,在肿瘤体积达到0.1mm3时分组给药。(3)设置空白对照组、模型组、实施例5给药组、溶媒组和阳性对照组,每组8只小鼠,阳性药采用avastin和多西他赛注射液,avastin的给药剂量为20mg/kg,每三天给药一次,多西他赛注射液的给药剂量为5mg/kg每7天给药一次,阳性药的给药方式均为尾静脉注射。空白对照组不做任何处理,模型组在造模后尾静脉注射生理盐水,给药体积0.1ml/10g,溶媒组和给药组分别尾静脉注射溶媒和抗肿瘤药物注射液,给药体积0.1ml/10g,每日给药一次。(4)给药21天后测量肿瘤体积,计算抑瘤率,计算公式如下:抑瘤率(%)=(模型组肿瘤体积-实验组肿瘤体积)/模型组肿瘤体积实验结果如下:表12各组药物抗肿瘤药效组别有效成分抑瘤率(%)实施例5序列4多肽58.4溶媒组无-0.5avastin单抗65.9多西他赛注射液紫杉醇55.8实施例13:采用实施例6中制备的抗肿瘤药物进行抗肿瘤体内实验。实验材料:18~22g雄性裸小鼠60只;肿瘤细胞株为肝癌smmc-7721,将实施例6中制备的抗肿瘤药物采用无菌生理盐水稀释1000倍后给药,药物终浓度为25μg/ml,0.22微米滤膜过滤后无菌分装,4℃保存备用。avastin和多西他赛注射液,均购自江苏先声再康医药有限公司。与实施例12的实验方法不同之处在于模型组、溶媒组和给药组给药方式为皮下注射给药。实验结果如下:表13各组药物抗肿瘤药效组别有效成分抑瘤率(%)实施例6序列5多肽65.9溶媒组无1.1avastin单抗60.2多西他赛注射液紫杉醇53.1实施例14:采用实施例7中制备的抗肿瘤药物进行抗肿瘤体内实验。实验材料:18~22g雄性裸小鼠60只;肿瘤细胞株为肺癌a549,药物终浓度为100μg/ml,0.22微米滤膜过滤后无菌分装,4℃保存备用。avastin和多西他赛注射液,均购自江苏先声再康医药有限公司。与实施例12的实验方法不同之处在于模型组、溶媒组和给药组给药方式为后肢肌肉注射给药。给药体积为0.02ml/10g。实验结果如下:表14各组药物抗肿瘤药效组别有效成分抑瘤率(%)实施例7序列6多肽59.1溶媒组无2.5avastin单抗59.9多西他赛注射液紫杉醇61.2实施例15:采用实施例8中制备的抗肿瘤药物进行抗肿瘤体内实验。实验材料:18~22g雄性裸小鼠60只;肿瘤细胞株为口腔鳞癌tca8113,将实施例8中制备的抗肿瘤药物采用无菌生理盐水稀释1000倍后给药,药物终浓度为20μg/ml,0.22微米滤膜过滤后无菌分装,4℃保存备用。avastin和多西他赛注射液,均购自江苏先声再康医药有限公司。与实施例12的实验方法不同之处在于模型组、溶媒组和给药组给药方式为肿瘤组织内注射给药。给药体积为0.01ml/10g。实验结果如下:表15各组药物抗肿瘤药效组别有效成分抑瘤率(%)实施例8序列7多肽51.2溶媒组无0.3avastin单抗65.4多西他赛注射液紫杉醇60.7实施例16:采用实施例8中制备的抗肿瘤药物进行抗肿瘤体内实验。实验材料:18~22g雌性裸小鼠60只;肿瘤细胞株为乳腺癌mda-mb-231,将实施例8中制备的抗肿瘤药物采用无菌生理盐水稀释1000倍后给药,药物终浓度为20μg/ml,0.22微米滤膜过滤后无菌分装,4℃保存备用。avastin和多西他赛注射液,均购自江苏先声再康医药有限公司。与实施例12的实验方法不同之处在于模型组、溶媒组和给药组给药方式为肿瘤周围组织皮下注射给药。给药体积为0.1ml/10g。实验结果如下:表16各组药物抗肿瘤药效组别有效成分抑瘤率(%)实施例8序列7多肽50.5溶媒组无3.3avastin单抗66.8多西他赛注射液紫杉醇62.3根据上述实验结果,本发明的多肽具有多种抗肿瘤功效,可对多种不同起源的肿瘤细胞增殖具有较高的抑制率,在有效给药浓度下,对黑色素瘤、胃癌、肝癌的抑制率达到60%以上;在有效给药浓度下,对食道鳞癌、非小细胞肺癌、结肠癌、口腔鳞癌、乳腺癌的抑瘤率可达50%以上。流式细胞术检测多肽与巨噬细胞的结合作用:取sirpα高表达的人thp-1细胞株作为实验用巨噬细胞。取悬浮培养的thp-1细胞,加入终浓度100ng/ml的pma诱导分化12h贴壁,胰蛋白酶消化后收集细胞,1×pbs洗涤两遍后重悬并调整细胞浓度至107/ml,将细胞分为9组,分别为空白组,pe标记多肽2组,pe标记多肽4组,pe标记多肽6组,pe标记多肽7组,鼠抗人sirpα单抗+pe标记多肽2组,鼠抗人sirpα单抗+pe标记多肽4组,鼠抗人sirpα单抗+pe标记多肽6组,鼠抗人sirpα单抗+pe标记多肽7组,每组取细胞悬液100μl,再空白组加入20μlpbs孵育细胞2.5h。pe标记多肽各组加入10μlpbs,37℃孵育细胞2h后加入pe标记多肽10μl避光反应30min,pe标记多肽终浓度为1μg/μl;sirpα单抗+pe标记多肽各组先加入10μl鼠抗人sirpα单抗(10μg/ml),37℃孵育细胞2h后加入pe标记多肽10μl避光反应30min,pe标记多肽终浓度为1μg/μl;将上述9组细胞用预冷1×pbs洗涤后离心(1000rmp/10min)3次,用200μl预冷1×pbs重悬,各组细胞用流式细胞仪分别进行检测。相关统计分析由spss10.0软件完成,主要方法为单因素方差分析。若p<0.05提示差异有统计学意义,结果见图1~9。图1~5结果显示,单独孵育pe标记多肽后,细胞表面荧光强度显著增加,表明pe标记多肽大量结合于细胞表面,而图6~9显示,在预先用sirpα单抗处理细胞后再孵育pe标记多肽时,荧光强度接近空白对照组,表明细胞表面较少或没有pe标记多肽结合,sirpα单抗与多肽的结合位点相同,因此本发明多肽可特异性地结合于巨噬细胞表面的sirpα上。巨噬细胞与肿瘤细胞共培养实验:取sirpα高表达的人thp-1细胞株作为实验用巨噬细胞,取cd47高表达的mgc-803细胞作为肿瘤细胞;收集悬浮培养的thp-1细胞,1×pbs洗涤两遍后重悬计数,24孔板内加入细胞悬液并控制thp-1总数为104/孔,加入终浓度100ng/ml的pma诱导分化12h贴壁,加入收获计数后的mgc-803细胞,thp-1与mgc-803的细胞总数之比为1:15,同时分别加入sirpα单抗(终浓度10μg/ml)、序列1~7多肽(终浓度10μg/ml),空白对照组仅加入1mlpbs,肿瘤细胞组仅加入等量的mgc-803细胞,不做任何处理,上述每组设三个复孔。37℃,5%co2条件下共培养细胞48h后,mtt法测定细胞活力,并计算肿瘤抑制率:肿瘤抑制率=(肿瘤细胞组吸光度平均值-实验组吸光度平均值)/肿瘤细胞组吸光度平均值*100%结果见表17:表17多肽对巨噬细胞和肿瘤细胞共培养的影响上述结果表明本发明多肽通过与巨噬细胞表面的sirp-α结合,阻断cd47与sirp-α信号通路,解除了肿瘤细胞对巨噬细胞的免疫抑制作用,有效的促进了巨噬细胞对肿瘤细胞的抑制作用,使得各多肽的肿瘤抑制率显著高于共培养空白对照组。鸡胚绒毛尿囊膜血管生成抑制实验取11日龄鸡胚,于检卵灯下标记气室及胎位,并在胎位附近无大血管处画一记号用碘酒,乙醇消毒气室顶部和记号处,然后在气室顶部钻一小孔,同时用磨卵器在记号处将卵壳磨一个和纵轴平行的裂痕,勿伤及壳膜。将卵平放,轻轻将裂痕处卵壳去掉,勿伤及壳膜,于壳膜上刺破一小缝但不伤及下面的绒毛尿囊膜,滴加无菌生理盐水一滴于壳膜上。用橡皮乳头从气室端小孔处缓缓将气室内空气吸去,造成气室负压,此时可见生理盐水下沉,绒毛尿囊膜下陷,壳膜与尿囊膜之间形成人工气室。揭开人工气室上的壳膜,暴露该处的绒毛尿囊(cam)膜,滴加0.2-0.5ml药物悬液于绒毛尿囊膜上,加入样品后,用无菌透明胶带封闭窗口,孵育3天,每12小时观察一次,用无菌胶布封口。将鸡胚横卧,于37度孵育,避免翻动,以免人工气室移位。5天后取出收获。用碘酒,乙醇消毒接种部位及四周,撕去封闭处卵壳,用无菌镊子扩大开口处,轻轻夹起绒毛尿囊膜用无菌剪刀剪下接种面及周围的膜,甲醛固定。取固定后的cam膜,乙醇脱水,石蜡包埋,沿平行与cam方向,连续切片,厚度8μm。0.5%甲苯胺蓝染色。取标本于250倍视野下计数微血管的横截面,分别随机6个不重复的高倍视野,取其平均值作为该标本的单位面积下的mvd(微血管密度)结果如下:血管生成抑制率=(空白组mvd值-实验组mvd值)/空白组mvd值*100%表18血管新生抑制药效测定表11结果表明本发明不仅可以阻断cd47和sirp-α信号通路,还可显著抑制血管新生,效果接近或好于vegf单抗(贝伐单抗)组。以上实施例仅为说明本发明的技术思想,不能以此限定本发明的保护范围,凡是按照本发明提出的技术思想,在技术方案基础上所做的任何改动,均落入本发明保护范围之内;本发明未涉及的技术均可通过现有技术加以实现。sequencelisting<110>南京萌萌菌业有限公司<120>一种抗肿瘤多肽及其应用<130>11204<160>7<170>patentinversion3.5<210>1<211>30<212>prt<213>人工序列<400>1cyscysasnaspgluglyleuglumetargilelysaspprothrgly151015glyglyaspalaserleulysmetasplysseraspalaval202530<210>2<211>30<212>prt<213>人工序列<400>2glyaspalaserleulysmetasplysseraspalavalaspprothr151015glyglycyscysasnaspgluglyleuglumetargilelys202530<210>3<211>33<212>prt<213>人工序列<400>3cyscysasnaspgluglyleuglumetargilelysglyglyglyser151015glyglyglyserglyaspalaserleulysmetasplysseraspala202530val<210>4<211>33<212>prt<213>人工序列<400>4glyaspalaserleulysmetasplysseraspalavalglyglygly151015serglyglyglysercyscysasnaspgluglyleuglumetargile202530lys<210>5<211>29<212>prt<213>人工序列<400>5cyscysasnaspgluglyleuglumetargilelysglyglyglyser151015glyaspalaserleulysmetasplysseraspalaval2025<210>6<211>29<212>prt<213>人工序列<400>6glyaspalaserleulysmetasplysseraspalavalglyglygly151015sercyscysasnaspgluglyleuglumetargilelys2025<210>7<211>25<212>prt<213>人工序列<400>7glyaspalaserleulysmetasplysseraspalavalcyscysasn151015aspgluglyleuglumetargilelys2025当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1