用于乳腺癌HER2基因检测的引物组、试剂盒及方法与流程
本发明涉及基因检测
技术领域:
,具体涉及用于乳腺癌her2基因检测的引物组、试剂盒及方法。
背景技术:
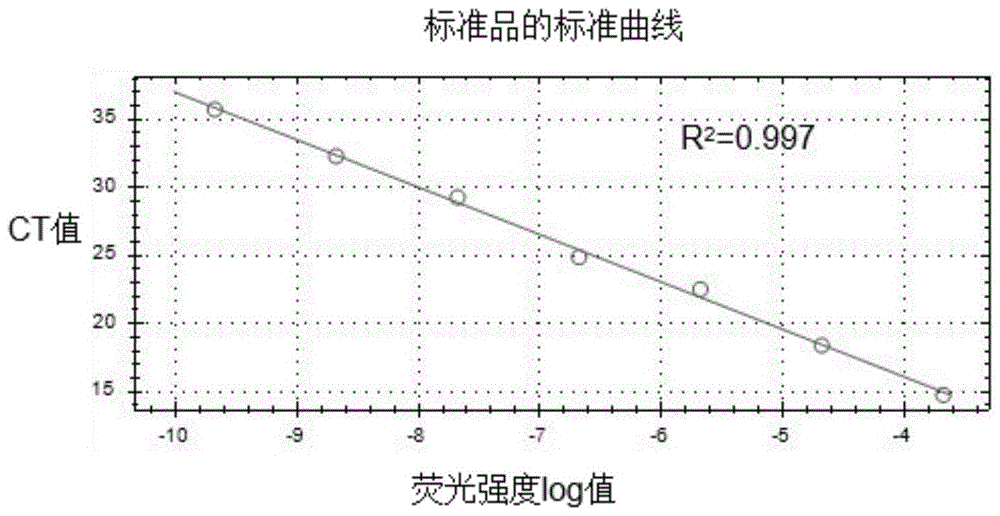
:原癌基因人类表皮生长因子受体2(humanepidermalgrowthfactorreceptor-2,her2)基因,即c-erbb-2基因,定位于染色体17q12-21.32上,具有酪氨酸激酶活性。它会抑制细胞凋亡,促进增殖,增加肿瘤细胞的侵袭力。her2基因突变检测是预测her2靶向疗法潜在效果的生物标志。大约有20%-30%原发浸润性乳腺癌患者表现为her2阳性,就是细胞表面her2蛋白受体表达大量增加,导致her2基因细胞核内拷贝数增加。相较于其它类型的乳腺癌,her2阳性乳腺癌进展速度更快、恶性程度更高,同时也更容易发生其他部位的转移,预后情况也相对较差。赫赛汀是一种可以抑制her2过表达肿瘤细胞增殖的单抗药物,所以对于her2阳性乳腺癌患者而言,准确的判断对确保最有可能获益的患者接受her2靶向治疗至关重要;同时,那些不太可能获益的人可以避免与这些药物有关的副作用和成本。目前临床已有的检测方法包括免疫组化和原位杂交。免疫组化就是利用免疫显色反应在蛋白水平上对福尔马林固定的石蜡切片进行her2过表达检测。原位杂交就是利用特别设计的核酸探针与固定的细胞内her2基因进行序列杂交,缺点是耗时较长,价格较高,无法得到确切的阳性结果。对于her2免疫组化阳性结果不确定的情况,还需要用fish方法检测确定her2基因扩增状态。虽然fish技术被认为是目前检测her2基因是否扩增的“金标准”。但是其检测操作繁琐,流程较长,不同的抗体敏感性存在差异,在实验室很难进行标准化的检测。技术实现要素:针对上述传统乳腺癌her2基因检测方法中存在的操作繁琐、准确性低、敏感性不高、难以标准化等问题,本发明基于hs-msh技术提供了用于乳腺癌her2基因检测的引物组、试剂盒及方法,操作简单、准确性高、敏感性高且统一化标准。为了实现上述目的,本发明采用的技术方案为:本发明提供了一种用于乳腺癌her2基因检测的引物组,包括her2正向引物和her2反向引物,所述her2正向引物和her2反向引物包括:her2正向引物f1:5'-acatcctgctgtggaggact-3',her2反向引物r1:5'-cgccacgactggctaattt-3';her2正向引物f2:5'-actagttattgggccggaca-3',her2反向引物r2:5'-cgccacgactggctaattt-3';her2正向引物f3:5'-tttgctacagtgcaaagacac-3',her2反向引物r3:5'-ggtggtctcgaactcctgac-3'。优选地,上述引物组还包括tsn内参基因的引物:tsn正向引物f4:5'-f1cccatcacaggaccagaagt-3',tsn反向引物r4:5'-agctgccaagcctcctttat-3'。本发明还提供了一种包括上述引物组的试剂盒。优选地,上述试剂盒还包括pcr反应液、标准品、阳性对照品、阴性对照品和饱和荧光染料。进一步地,所述pcr反应液包括:pcrbuffer、dntps、taq酶和无核酸酶水。优选地,所述pcr反应液中pcrbuffer为5×pcrbuffer,dntps终浓度为0.2mm。优选地,her2正向引物、her2反向引物、tsn正向引物f4和tsn反向引物r4的终浓度均为0.4μm。本发明还提供了一种用于乳腺癌her2基因检测的方法,包括如下步骤:1)提取待检测样本dna,作为pcr扩增的模板;2)使用上述引物组对所述模板进行荧光定量pcr扩增,pcr扩增程序为:3)使用ms-hrm分析软件自动计算不同样品的相对荧光强度,用于检测her2基因的扩增。优选地,步骤2)中采用的扩增体系为pcrbuffer10μl,dntps1μl,正向引物和反向引物各1μl,taq酶0.1μl,模板2μl,用无核酸酶水补至25μl。本发明的有益效果如下:1.利用本发明的检测试剂盒可以简便、高通量地检测乳腺癌患者中her2基因是否发生扩增,与检测金标准fish法相比,具有检测灵敏度高、时间短、价格低廉、通量高的优势,适合于大规模临床开展。2.本发明的检测试剂盒通过荧光定量pcr扩增,由溶解曲线确定是否存在her2基因扩增,进而,可为临床医生选择靶向药物提供参考,降低治疗风险以及减轻患者负担。附图说明图1显示的是以标准品dna为模板的pcr结果绘制的标准曲线。图2显示的是以样品dna为模板的pcr结果的高分辨溶解曲线。具体实施方式为了更好的理解本发明,下面结合附图和实施例进一步阐明本发明的内容,但本发明不仅仅局限于下面的实施例。实施例1乳腺癌her2阳性细胞系skbr3和her2阴性细胞系zr-75-1均购自上海细胞所。分别从中提取基因组dna,按照突变频率从1%到10%的比例掺入基因组dna,建立her2/tsn比值梯度的模型。使用上述pcr扩增反应液加入相应反应成分。扩增体系为:5×pcrbuffer5μldntps(10mm)0.5μl正向引物(10μm)1μl反向引物(10μm)1μltaq酶(5u/μl)0.1μl模板2μl无核酸酶水15.4μl总体积25μl按照如下反应程序对标准品进行扩增。采用her2阳性细胞和her2阴性细胞的dna,使用泊松公式计算tsn和her2的绝对浓度,并应用z-检验对logher2/tsn比值(呈近似正态分布)对突变dna量进行显著性检验。二者的比值差为1.23±0.04,0.19±0.06,-0.02±0.01,所以,通过这种方法,我们能够显著地检测突变dna的存在。标准曲线如图1所示。本发明所述的阴性对照品和阳性对照品均为常规对照品,均为her2基因片段和fas基因片段的混合物。实施例2(1)使用qiaampcirculatingnucleicacidkit(qiagen,cat:55114)提取乳腺癌患者的游离核酸(经患者同意,医院收集的乳腺癌样品),操作过程按照试剂盒说明书,最后把80μlbufferave加入到qiaampmini吸附柱中,20,000rpm离心1min,收集提取的核酸,然后使用nanodropone超微量分光光度计对所提取的样品进行检测,260/280范围是1.8-2.1,浓度不高于10ng/μl;(2)pcr体系把pcr反应液配制成mastermix,含有dntps0.5μl和taq酶0.1μl。荧光检测通道使用hex检测通道。mastermix10μl正向引物(10μm)0.8μl反向引物(10μm)0.8μl模板2μl无核酸酶水11.4μl总体积25μl(3)反应程序在appliedbiosystems7500快速荧光定量pcr仪上进行,所需要用到的pcr程序为:(4)选择2号染色体上的tsn(内参基因)和her2基因同时扩增。这种检测方法能够绝对定量her2拷贝数,并区分her2扩增和17号染色体多倍体,避免her2扩增情况被错误评估。(5)pcr结果的计算:通过实时监测升温过程中双链dna荧光染料与pcr扩增产物的结合情况,仪器可以自动记录高分辨率溶解曲线,如图2所示,从而实现对待测样品的检测。使用ms-hrm分析软件自动计算不同样品的随着时间变化的荧光强度,由仪器输出的溶解曲线的峰形,再与阴性对照品、阳性对照品的峰形相比较,就可以检测患者是否存在her2基因的扩增。当仪器根据扩增的溶解曲线自动计算的f的值在0.35-0.47时,判断her2基因扩增,当f的值小于0.35时,判断her2基因未扩增。因此本试剂盒通过hrm分析就能够有效区分不同样品her2基因的扩增情况。实施例3选取21例乳腺癌患者和5例健康人群(经患者同意,医院收集的检验样本)分别使用上述检测试剂盒和罗氏的her2基因扩增检测试剂盒,它的原理是根据her2基因与参照基因扩增反应的ct值差异(经参照样本的δct校正后即为δδct)比较拷贝数差异,从而间接计算her2基因的扩增。比较两个试剂盒检测结果的准确性。统计结果如下:fish技术被认为是目前检测her2基因是否扩增的“金标准”,使用fish技术再次对上述样品进行检测,结果与本发明一致。说明本发明可以满足临床her2检测的稳定性、精密度的要求对于本领域技术人员而言,显然本发明不限于上述示范性实施例的细节,而且在不背离本发明的精神或基本特征的情况下,能够以其他的具体形式实现本发明。因此,无论从哪一点来看,均应将实施例看作是示范性的,而且是非限制性的,本发明的范围由所附权利要求而不是上述说明限定,因此旨在将落在权利要求的等同要件的含义和范围内的所有变化囊括在本发明内。当前第1页1 2 3
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1