吲哚与喹唑酮类生物碱及其医药用途
:
1.本发明属于医药技术领域,涉及吲哚与喹唑酮类生物碱及其医药用途,尤其涉及从植物崧蓝叶(大青叶)中提取制备的光学纯的吲哚类与喹唑酮类生物碱及这类化合物在制备神经保护药物中的应用。
背景技术:
:
2.崧蓝(isatis indigotica fortune):为十字花科(cruciferae),菘蓝属植物。原产我国,全国各地均有栽培。古时为重要的染料资源,其根(板蓝根)、叶(大青叶)均可入药,有清热解毒、凉血消斑、利咽止痛的功效。临床上主要用于治疗温热病热毒入于营血温热病初期和外感风热症。另外,近些年对该属植物抗衰老、美容等保健作用的研究,给本属植物的保健食品及新药开发研究提供了较好的发展前景。
3.氧化应激(oxidative stress,os):指机体内活性氧产生过多,导致氧化和抗氧化系统失衡,引起细胞或组织氧化损伤的一种病理状态。活性氧(reactive oxygen species,ros)造成dna、蛋白质和脂质等氧化损伤,破坏细胞结构和功能的完整性,引起细胞凋亡或坏死,与多种疾病发生相关。
4.国内外研究氧化应激的模型大体分为动物模型和体外细胞培养模型两种,其中应用最广泛的体外细胞培养模型是h2o2氧化损伤模型。h2o2作为活性氧类物质之一,不仅极易透过细胞膜,与细胞内铁离子反应生成高活性自由基,而且易于获得,性质稳定,已成为国内外研究各类细胞氧化损伤的重要工具。
5.衰老(senility)与氧化应激:衰老是一个复杂的生命过程,它涉及生命的方方面面。诸如基因调控障碍、细胞凋亡、自由基损伤、物质代谢失衡、抗氧化酶活性降低、免疫功能紊乱、神经内分泌失调、组织细胞退行性改变、生理功能下降等。其中自由基衰老学说认为自由基损伤在衰老中扮演着重要的角色,是导致机体衰老的主要“微损伤”因子。也因此,通过对抗或减弱体内ros产生过多导致的氧化和抗氧化系统失衡是延缓机体衰老,减弱细胞损伤有效途径
技术实现要素:
:
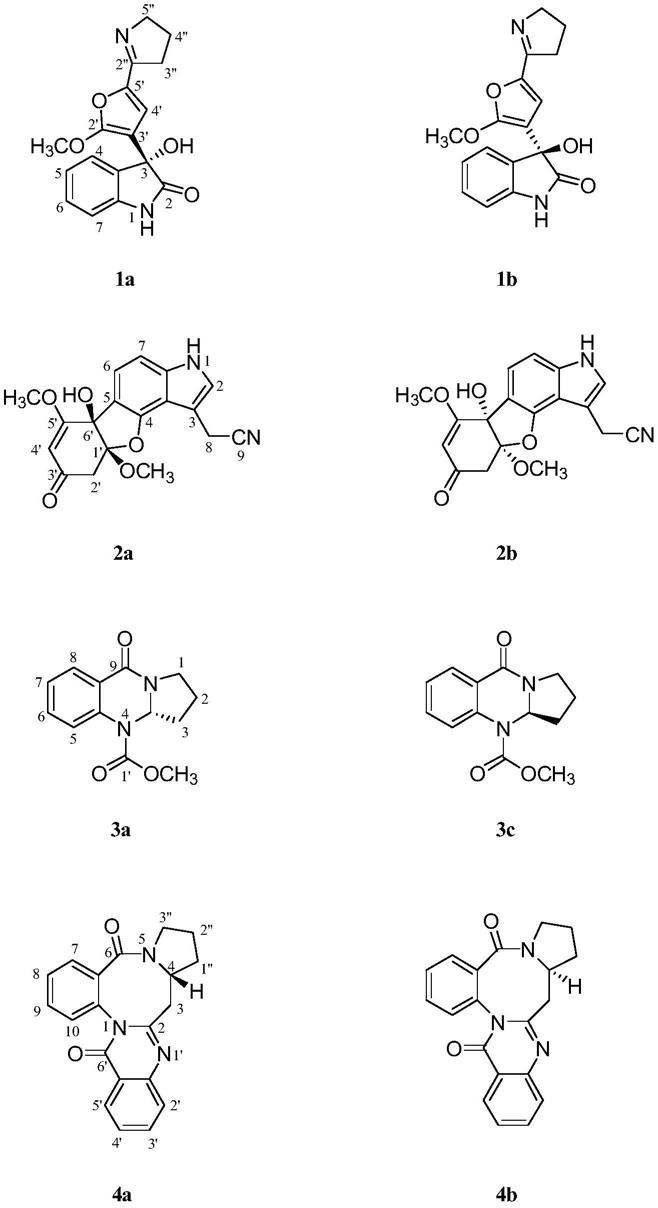
6.本发明提供了四种吲哚与喹唑酮类生物碱或其盐,结构如下:
[0007][0008]
本发明所述的吲哚与喹唑酮类生物碱是从十字花科菘蓝属崧蓝(isatis indigotica fortune)叶(大青叶)中分离得到的。
[0009]
本发明所述的吲哚与喹唑酮类生物碱的制备技术方案包括如下步骤:
[0010]
(1)取干燥的崧蓝叶以70-80%工业乙醇提取,浓缩提取液得浸膏,浸膏采用二氯甲烷萃取。
[0011]
(2)将二氯甲烷萃取液所得浸膏经硅胶柱色谱,以二氯甲烷-甲醇系统100:1-3:1
2”),24.1(c-3”)相关,证明了一个3,4-二氢吡咯片段的存在,根据剩余信号确定化合物还含有一个呋喃环;呋喃环上的双键氢δ6.16(1h,s,h-4')与δ141.5(c-2”)相关,表明3,4-二氢吡咯连在呋喃环c-5'位;羟基氢δ6.53(1h,br s,oh-3)与δ133.7(c-3a),112.9(c-3')相关,表明存在羟基连在c-3位;δ3.42(3h,s,och
3-2')与δ160.4(c-2')相关,表明甲氧基连在呋喃环的c-2'位。从而确定了化合物1的平面结构。
[0022]
通过daicel chiralpak ig手性色谱柱对化合物1进行拆分,得到1aig手性色谱柱对化合物1进行拆分,得到1a和比例约为3:2,cd谱呈镜像关系。它们的绝对构型是通过比较计算和实测ecd来确定的。1a的实验cd曲线与预设为3r构型的计算ecd曲线吻合,而1b的实验cd曲线与3s构型的计算ecd曲线吻合。因此确定了1a和1b的绝对构型分别为3r和3s,并分别命名为isatindigotindoline e1和isatindigotindoline e2。
[0023]
化合物2:黄色油状物hresims给出准分子离子峰m/z 363.0951[m+na]
+
(计算为c
18
h
16
n2o5na 363.0951),结合1h,
13
c-nmr数据确定其分子式为c
18
h
16
n2o5,计算不饱和度为12。1h-nmr(400mhz,dmso-d6)谱中,δ7.16(1h,d,j=8.3hz,h-6),7.01(1h,d,j=8.3hz,h-7)提示存在一个1,2,3,4-四取代的苯环系统,δ11.27(1h,brs,h-1)显示为一个氮氢信号,δ7.28(1h,d,j=1.9hz,h-2),5.36(1h,s,h-4')显示为双键上的氢信号;此外氢谱还显示了两组亚甲基信号δ4.00(1h,d,j=18.2hz,h-8),3.94(1h,d,j=18.2hz,h-8)和δ3.09(1h,d,j=16.4hz,h-2'),2.88(1h,d,j=16.4hz,h-2'),一个羟基信号δ6.27(1h,s,oh-6'),两个甲氧基信号δ3.35(3h,s,och
3-1'),3.62(3h,s,och
3-5')。
13
c-nmr(100mhz,dmso-d6)谱中给出18个碳信号,低场区有12个碳信号,其中包括六个苯环的碳信号和四个双键碳信号,还有一个羰基碳信号和一个氰基碳信号;高场区有6个碳信号,包括两个连氧季碳信号、两个亚甲基碳信号、两个甲氧基碳信号。在hmbc谱中,δ7.16(1h,d,j=8.3hz,h-6)与δ149.4(c-4),139.2(c-7a)存在远程相关,δ7.01(1h,d,j=8.3hz,h-7)与δ111.7(c-3a),117.8(c-5)存在远程相关,氮氢δ11.27(1h,brs,h-1)与δ102.2(c-3),111.7(c-3a),105.4(c-7)相关,δ7.28(1h,d,j=1.9hz,h-2)与δ111.7(c-3a),139.2(c-7a)相关,δ4.00(1h,d,j=18.2hz,h-8),3.94(1h,d,j=18.2hz,h-8)与δ124.3(c-2),111.7(c-3a),119.4(c-9)相关,以上相关信号表明化合物2含有3-吲哚乙腈的结构片段;δ3.09(1h,d,j=16.4hz,h-2')与δ109.4(c-1'),192.4(c-3'),78.7(c-6')相关,δ5.36(1h,s,h-4')与δ40.7(c-2'),78.7(c-6')相关,表明化合物2含有环己烯酮的片段,根据化合物不饱和度12以及剩余的碳氢信号和原子数目,可以说明化合物还存在一个呋喃环与环己烯酮骈合于c-1'位和c-6'位两个连氧季碳上。羟基信号δ6.27(1h,s,oh-6')与δ117.8(c-5),173.8(c-5')相关,甲氧基δ3.35(3h,s,och
3-1')与δ109.4(c-1')相关,甲氧基δ3.62(3h,s,och
3-5')与δ173.8(c-5')相关,证明羟基连在c-6'位,两个甲氧基分别连在c-1'位和c-5'位;根据δ7.16(1h,d,j=8.3hz,h-6)与δ149.4(c-4),78.7(c-6')相关,可以证明呋喃环与3-吲哚乙腈骈合,共用碳原子为c-4和c-5。从而确定了化合物2的平面结构。
[0024]
化合物2的相对构型是通过noesy谱来确定的,在noesy谱中,c-6'位的羟基氢和c-1'位的甲氧基氢存在相关,说明这两个基团位于同侧,从而确定该化合物的相对构型c-6'位的羟基与c-1'的甲氧基为β取向。
[0025]
通过daicel chiralpak ic手性色谱柱对化合物2进行拆分,得到ic手性色谱柱对化合物2进行拆分,得到和比例约为1:1,它们的cd谱近似呈镜像关系。它们的绝对构型是通过比较计算和实测ecd来确定的。2a和2b的实验cd曲线分别与预设为1'r,6'r和1's,6's构型的计算ecd曲线吻合。因此确定了2a和2b的绝对构型分别为1'r,6'r和1's,6's,并命名为isatindoleacetonitriline a1和isatindoleacetonitriline a2。
[0026]
化合物3:白色晶体hresims给出准分子离子峰m/z 269.0881[m+na]
+
(计算为c
13
h
14
n2o3na 269.0897),结合1h,
13
c-nmr数据确定其分子式为c
13
h
14
n2o3,计算不饱和度为8。1h-nmr(400mhz,dmso-d6)谱中,δ7.24(1h,m,h-5),7.51(1h,overlap,h-6),7.51(1h,overlap,h-7),7.81(1h,d,j=7.7hz,h-8)提示存在一组邻位取代的苯环质子信号,δ5.15(1h,dd,j=9.1,5.4hz,h-3a)显示为一个次甲基信号,化学位移值为δ5.15提示其可能与氮相连,δ3.53(2h,m,h-1),2.00(1h,m,h-2)和1.80(1h,m,h-2),2.59(1h,m,h-3)和2.45(1h,m,h-3)提示为三个亚甲基信号,δ3.74(3h,s,och
3-1')为甲氧基信号。
13
c-nmr(100mhz,dmso-d6)谱共给出13个碳信号。δ160.3(c-9)为酰胺的羰基碳信号,δ160.0(c-3a)为双键的碳信号,化学位移值向低场位移,提示与氮相连。δ140.6(c-4a),124.3(c-5),132.1(c-6),122.4(c-7),126.7(c-8),122.9(c-8a)为一组苯环的碳信号,δ72.0(c-3a)为次甲基碳信号,δ43.7(c-1),21.6(c-2),32.1(c-3)为三个饱和亚甲基碳信号。该化合物的平面结构与文献报道的一致,但文献中并未给出碳氢数据,其构型也未确定。因此,根据hsqc谱对该化合物进行了碳氢直接相关归属,并根据hmbc谱对碳氢远程相关进行归属。在hmbc谱中,δ7.81(1h,d,j=7.7hz,h-8)与δ140.6(c-4a),132.1(c-6)160.3(c-9)相关,δ7.51(1h,overlap,h-7)与δ124.3(c-5),122.9(c-8a)有相关,δ7.24(1h,m,h-5)与δ122.4(c-7),122.9(c-8a)相关,δ5.15(1h,dd,j=9.1,5.4hz,h-3a)与δ32.1(c-3),153.1(c-1')相关,δ3.53(2h,m,h-1),2.00(1h,m,h-2)都与δ72.0(c-3a)有相关,δ2.59(1h,m,h-3)与δ43.7(c-1)有相关。根据上述相关,确定该化合物的平面构型。
[0027]
通过chiralpak ad-h手性色谱柱对化合物3进行拆分,得到和比例约为1:1,它们的cd谱呈镜像关系。它们的绝对构型是通过比较计算和实测ecd来确定的。3a和3b的实验cd曲线分别与预设为3as和3ar构型的计算ecd曲线吻合。因此确定了3a和3b的绝对构型分别为3as和3ar。并命名为deoxyvsicinone a1和deoxyvsicinone a2。。
[0028]
化合物4:黄色油状物hresims给出准分子离子峰m/z332.1404[m+na]
+
(计算为c
20
h
18
n3o
2 332.1394),结合1h,
13
c-nmr数据确定其分子式为c
20
h
17
n3o2,计算不饱和度为14。1h-nmr(600mhz,dmso-d6)谱中,δ7.57(1h,overlap,h-7),7.63(1h,td,j=7.6,1.2hz,h-8),7.66(1h,td,j=7.6,1.2hz,h-9),7.53(1h,br d,j=7.6hz,h-10)以及δ7.72(1h,br d,j=8.0hz,h-2'),7.87(1h,td,j=8.0,1.2hz,h-3'),7.55(1h,overlap,h-4'),8.11(1h,br d,j=8.0hz,h-5')提示存在两个邻位二取代的苯环系统,δ3.79(1h,m,h-4)提示存在一个连氮的次甲基信号,δ2.84(1h,dd,j=13.9,9.0hz,h-3)和2.79(1h,dd,j=13.9,2.4hz,h-3),2.16(1h,m,h-1”)和2.05(1h,m,h-1”),1.89(1h,m,h-2”)和1.74(1h,m,h-2”),3.54(1h,m,h-3”)和2.96(1h,m,h-3”)提示结构中含有四个亚甲
基,且化学位移值为δ3.54(1h,m,h-3”),2.96(1h,m,h-3”)的这个亚甲基可能与氮相连。
13
c-nmr(100mhz,dmso-d6)谱中给出20个碳信号,低场区有15个双键碳信号,除了与氢信号相对应的两组苯环的碳信号之外,还存在两个羰基碳信号δ166.1(c-6),160.5(c-6')和一个连氮双键碳信号δ154.7(c-2);在高场区,δ55.7(c-4)提示为次甲基碳信号,δ41.4(c-3),34.8(c-1”),22.1(c-2”),46.8(c-3”)为与氢信号相对应的四个亚甲基碳信号。根据化合物不饱和度为14,提示该结构除了存在两个苯环外,可能还存在三个环。在hmbc谱中,苯环质子信号δ7.57(1h,overlap,h-7)与酰胺羰基碳δ166.1(c-6)以及连氮苯环碳信号δ133.6(c-10a)存在相关,表明苯环邻位分别与酰胺羰基和一个氮原子相连;在1h-1
h cosy谱中,h-7/h-8/h-9/h-10,h-2'/h-3'/h-4'/h-5'以及h-3/h-4/h-1”/h-2”/h-3”存在同核质子偶合相关,可以推断出邻位质子偶合的片段,结合hmbc的相关信号δ1.89(1h,m,h-2”),1.74(1h,m,h-2”)与δ55.7(c-4)相关,δ3.54(1h,m,h-3”),2.96(1h,m,h-3”)与δ55.7(c-4),34.8(c-1”)相关,证明了结构中存在一个吡咯烷的片段,并且根据δ3.79(1h,m,h-4)与δ154.7(c-2)相关,δ3.54(1h,m,h-3”)与δ166.1(c-6)相关,可以推断出有一个八元二氮杂环与苯环骈合,且吡咯烷与八元二氮杂环骈合于c-4和n-5位;另一苯环质子信号δ8.11(1h,br d,j=8.0hz,h-5')与酰胺羰基碳δ160.5(c-6')以及连氮苯环碳信号δ147.0(c-2'a)存在相关,表明另一苯环邻位也分别与酰胺羰基和一个氮原子相连,根据剩余的c、h、o、n原子的数目,得出结构中还含有一个喹唑酮片段,与八元二氮杂环骈合于n-1和c-2位。从而确定了化合物4的平面结构。
[0029]
通过daicel chiralpak ig手性色谱柱对化合物4进行拆分,得到ig手性色谱柱对化合物4进行拆分,得到和比例约为3:2,它们的cd谱近似呈镜像关系。它们的绝对构型是通过比较计算和实测ecd来确定的。4a的实验cd曲线与预设为4r构型的计算ecd曲线比较吻合,而4b的实验cd曲线与4s构型的计算ecd曲线比较吻合。从而确定了4a和4b的绝对构型分别为4r和4s,并命名为cycloanthranilylproline a1和cycloanthranilylproline a2。
[0030]
化合物1a/1b、2a/2b、3a/3b、4a/4b的核磁数据如下表所示:
[0031]
表1 1a/1b、2a/2b、3a/3b、4a/4b在dmso-d6中1h(400mhz)与
13
c(100mhz)nmr数据
[0032]
[0033][0034]
对发明所述四个新的生物碱类化合物对h2o2诱导的人sh-sy5y神经细胞损伤的神经保护作用进行了考察,体外细胞试验结果表明,本发明所述的吲哚及喹唑酮类生物碱具有神经细胞保护作用,尤其化合物1a与4b对h2o2诱导的人sh-sy5y细胞氧化损伤具有显著的保护作用。
附图说明:
[0035]
图1化合物1的uv谱;
[0036]
图2化合物1的hresims谱;
[0037]
图3化合物1的hmbc谱(600mhz,cdcl3);
[0038]
图4化合物1的hsqc谱(600mhz,cdcl3);
[0039]
图5化合物1的手性拆分色谱图;
[0040]
图6化合物1a的cd谱;
[0041]
图7化合物1b的cd谱;
[0042]
图8化合物2的uv谱;
[0043]
图9化合物2的hresims谱;
[0044]
图10化合物2的hmbc谱(600mhz,cdcl3);
[0045]
图11化合物2的hsqc谱(600mhz,cdcl3);
[0046]
图12化合物2的手性拆分色谱图;
[0047]
图13化合物2a的cd谱;
[0048]
图14化合物2b的cd谱;
[0049]
图15化合物3的uv谱;
[0050]
图16化合物3的hresims谱;
[0051]
图17化合物3的hmbc谱(600mhz,cdcl3);
[0052]
图18化合物3的hsqc谱(600mhz,cdcl3);
[0053]
图19化合物3的手性拆分色谱图;
[0054]
图20化合物3a的cd谱;
[0055]
图21化合物3b的cd谱;
[0056]
图22化合物4的uv谱;
[0057]
图23化合物4的hresims谱;
[0058]
图24化合物4的hmbc谱(600mhz,cdcl3);
[0059]
图25化合物4的hsqc谱(600mhz,cdcl3);
[0060]
图26化合物4的手性拆分色谱图;
[0061]
图27化合物4a的cd谱;
[0062]
图28化合物4b的cd谱;
[0063]
图29化合物1、2、3、4的计算ecd谱;
具体实施方式:
[0064]
下面所列实施例有助于本领域技术人员更好地理解本发明,但不以任何方式限制本发明。
[0065]
实施例1:化合物1a/1b-4a/4b的制备。
[0066]
利用崧蓝叶制备吲哚与喹唑酮类生物碱类化合物的方法,取干燥的崧蓝叶以80%工业乙醇回流提取两次,每次4个小时,合并提取液浓缩得4280g浸膏,浸膏先采用二氯甲烷萃取,上清液再采用正丁醇萃取。其中二氯甲烷层共得粗馏分864g,经硅胶柱色谱,以二氯甲烷-甲醇系统100:1-3:1进行梯度洗脱,共收集到4个馏分a、b、c、d。
[0067]
馏分c(864g)经聚酰胺,以30%乙醇-水,60%乙醇-水及90%乙醇-水进行洗脱,得三个组分c1、c2、c3。
[0068]
随后将组分c1(88.9g)利用hp-20柱色谱以醇-水系统0:100-90:10进行梯度洗脱,得到了3个组分c
1.1
、c
1.2
、c
1.3
。
[0069]
将c
1.3
(15.5g)进一步经ods柱色谱以醇-水系统10:90-90:10进行梯度洗脱得到了2个组分c
1.3.1
、c
1.3.2
。
[0070]
所得组分c
1.3.1
(6.0g)经硅胶柱色谱以石油醚-乙酸乙酯系统50:1-1:1进行梯度洗
脱,并将所得组分经制备及半制备hplc(乙腈-水18:82)得到了化合物1(4.1mg,t
r
=42min)、2(5.8mg,t
r
=50min)、3(4.4mg,t
r
=54min)、4(18.1mg,t
r
=56min)。
[0071]
随后使用手性柱色谱对四个化合物进行拆分,利用daicel chiralpak ig以乙腈:水53:47得到化合物1a(2.8mg,t
r
=14.8min)和1b(1.9mg,t
r
=19.5min),并利用daicel chiralpak ic色谱柱以正己烷:异丙醇3:1得到了化合物2a(1.8mg,t
r
=41min)和2b(1.5mg,t
r
=45min)。利用chiralpak ad-h以正己烷:异丙醇8:1得到了化合物3a(11.0mg,t
r
=20.8min)和3b(8.0mg,t
r
=25.0min)。利用daicel chiralpak ig以正己烷:异丙醇1:1得到了4a(2.2mg,t
r
=60.9min)和4b(1.4mg,t
r
=89.7min)。
[0072]
实施例2:化合物1a/1b-2a/2b在体外对h2o2诱导的人sh-sy5y神经细胞损伤保护作用的考察。
[0073]
利用mtt实验,考察化合物对h2o2诱导的sh-sy5y细胞损伤的保护作用。将细胞放置在96孔板中,以100μl培养液静置12h,使用不同浓度的化合物1a/1b-4a/4b(12.5,25,50μm)预处理sh-sy5y神经细胞1h,并用h2o2(1mm)处理细胞36h。随后将培养液替换为含有0.5mg/ml mtt的磷酸盐缓冲溶液并在37℃下放置4h。除去上清液并加入dmso(150ml/孔),以h2o2(1mm)单独处理的细胞为对照组,检测不同浓度处理的细胞在490nm波长下利用紫外分光光度计进行检测(thermo scientific multiskan mk3,上海,中国)。细胞的存活程度以存活百分比表示,并利用graphpad prism 6软件进行分析。结果显示,化合物1a/1b-4a/4b不同浓度下均表现出显著的保护作用。1a/1b、3a、4a/4b在50μm浓度下作用最强,相较于阳性药的67.9
±
4.23%,其细胞存活率达到了77.2
±
2.88%、69.9
±
1.42%、63.1
±
1.03%、61.1
±
3.15%。2b、3b在12.5μm浓度下作用最强,相较于阳性药的64.1
±
4.89%,其细胞存活率达到了65.8
±
3.29%、64.4
±
2.03%。2a、4b在25μm浓度下作用最强,相较于阳性药的65.2
±
1.98%,其细胞存活率达到了63.7
±
3.54%、72.1
±
0.98%。
[0074]
表2给药后细胞存活百分比
[0075][0076]
模型组相比于对照组的细胞存活百分比
###
p<0.001;实验组相比于模型组的细胞存活百分比**p<0.01,***p<0.01。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1