一种酶法合成西那卡塞中间体(R)-1-(1-萘基)乙胺的方法与流程
本发明属于生物催化领域,具体涉及到一种酶法合成西那卡塞中间体(r)-1-(1-萘基)乙胺的方法。
背景技术:
(r)-1-(1-萘基)乙胺是盐酸西那卡塞(cinacalceti)的关键手性中间体,其结构式为:
盐酸西那卡塞是由amgen公司研发的第二代拟钙剂药物,能激活甲状旁腺中的钙受体,从而降低甲状旁腺素(pth)的分泌,适用于治疗进行透析的慢性肾病(ckd)患者的继发性甲状旁腺功能亢进(spth)、甲状旁腺癌患者的高血钙症和治疗不能接受甲状旁腺切除术的原发性甲状旁腺功能亢进引起的严重高血钙症。
目前,(r)-1-(1-萘基)乙胺的合成方法主要分为不对称拆分法和不对称合成法。不对称拆分法主要以1-(1-萘基)乙胺消旋体为原料,通过化学拆分剂或者酶拆分获得手性纯(r)-1-(1-萘基)乙胺,此方法理论产率最高仅为50%。wo2008058235中以1-萘乙酮为原料经还原胺化得到1-(1-萘基)乙胺消旋体,再经d-(+)-萘普生拆分获得(r)-1-(1-萘基)乙胺,该方法存在拆分剂价格贵,反应步骤多,有机试剂用量大等缺点。cn103420845b采用d-酒石酸作为拆分剂,制备过程需使用大量有机试剂甲醇,经拆分萃取后收率仅为37.8%。cn104630322b公开了一种酶法拆分的方法,采用南极假丝酵母脂肪酶b对1-(1-萘基)乙胺消旋体进行选择性酯化,然后将(r)-1-(1-萘基)乙胺酯化物与(s)-1-(1-萘基)乙胺分离,最后将(r)-1-(1-萘基)乙胺酯化物水解得到(r)-1-(1-萘基)乙胺,该方法步骤较多,其中选择性酯化反应还需在有机溶剂正己烷中进行,最终收率仅为47.5%。相比而言,不对称合成法主要以1-萘乙酮或1-(1-萘基)乙酮肟为原料,经不对称催化反应生成手性纯(r)-1-(1-萘基)乙胺,其理论产率可达100%。cn105294449b公开了一种(r)-1-(1-萘基)乙胺的不对称合成方法,最终产物手性纯度为96%ee,收率为90%。该方法中使用的手性催化剂氯{[(1r,2r)-(-)-2-氨-1,2-二苯乙基](4-甲苯磺酰)氨}(p-异丙基甲苯)钌(ii))价格昂贵,存在重金属污染,反应需在有机溶剂中进行,不利于环境保护,同时产物手性纯度并不高。
因此,本领域亟需一种反应具有反应条件温和、效率高、立体选择性强、环境友好的(r)-1-(1-萘基)乙胺的合成方法,以期在药物合成方面具有较好的应用。
技术实现要素:
本部分的目的在于概述本发明的实施例的一些方面以及简要介绍一些较佳实施例。在本部分以及本申请的说明书摘要和发明名称中可能会做些简化或省略以避免使本部分、说明书摘要和发明名称的目的模糊,而这种简化或省略不能用于限制本发明的范围。
鉴于上述和/或现有技术中存在的问题,提出了本发明。
因此,本发明的目的是,克服现有技术中的不足,提供一种酶法合成西那卡塞中间体(r)-1-(1-萘基)乙胺的方法。
为解决上述技术问题,本发明提供了如下技术方案:一种酶法合成西那卡塞中间体(r)-1-(1-萘基)乙胺的方法,包括,在ph6.5~8.5的磷酸钾缓冲液中,分别添加1-萘乙酮、氨基供体、辅酶、助溶剂、甲酸脱氢酶以及d-氨基酸脱氢酶组成反应混合液,在30~40℃下进行反应24~48h,生成(r)-1-(1-萘基)乙胺;其中,所述d-氨基酸脱氢酶,其基因序列如seqidno.1所示,氨基酸序列如seqidno.2所示;所述反应混合液中1-萘乙酮浓度为50~300mmol/l,氨基供体的浓度为100~600mmol/l,辅酶浓度为0.1~0.5g/l,助溶剂浓度为5%~10%,辅酶循环酶浓度为1~3g/l,d-氨基酸脱氢酶浓度为0.5~2g/l,磷酸钾缓冲液的浓度为50~100mmol/l。
作为本发明所述酶法合成西那卡塞中间体(r)-1-(1-萘基)乙胺的方法一种优选方案,其中:所述氨基供体为无机铵盐。
作为本发明所述酶法合成西那卡塞中间体(r)-1-(1-萘基)乙胺的方法一种优选方案,其中:所述无机铵盐包括甲酸铵。
作为本发明所述酶法合成西那卡塞中间体(r)-1-(1-萘基)乙胺的方法一种优选方案,其中:所述辅酶为nad+、nadp+、nadh、nadph中任意一种或几种的组合。
作为本发明所述酶法合成西那卡塞中间体(r)-1-(1-萘基)乙胺的方法一种优选方案,其中:所述辅酶为nad+。
作为本发明所述酶法合成西那卡塞中间体(r)-1-(1-萘基)乙胺的方法一种优选方案,其中:所述助溶剂为二甲基亚砜、异丙醇、四氢呋喃的任意一种或几种的组合。
作为本发明所述酶法合成西那卡塞中间体(r)-1-(1-萘基)乙胺的方法一种优选方案,其中:所述助溶剂为二甲基亚砜。
作为本发明所述酶法合成西那卡塞中间体(r)-1-(1-萘基)乙胺的方法一种优选方案,其中:所述反应混合液中1-萘乙酮浓度为300mmol/l,甲酸铵浓度为600mmol/l,辅酶nad+浓度为0.5g/l,二甲基亚砜的浓度为10%,缓冲液浓度为100mmol/l,甲酸脱氢酶浓度为3g/l,d-氨基酸脱氢酶浓度为2g/l。
本发明有益效果:
(1)本发明提供了一种酶法催化1-萘乙酮合成(r)-1-(1-萘基)乙胺的方法,所用d-氨基酸脱氢酶可通过构建大肠杆菌基因工程菌和发酵培养大量制备,相对廉价易得,且反应转化率(95%以上)和产物手性纯度(99%ee)均较高,大大提高了(r)-1-(1-萘基)乙胺的制备效率;
(2)本发明提供了一种酶法催化1-萘乙酮合成(r)-1-(1-萘基)乙胺的方法,反应为“一锅煮”式,所有原料同时加入,反应后直接得到终产物(r)-1-(1-萘基)乙胺,中间无需分离提纯,反应条件温和,有机溶剂用量小,反应体系更绿色环保,具有较好的工业应用前景。
附图说明
为了更清楚地说明本发明实施例的技术方案,下面将对实施例描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图仅仅是本发明的一些实施例,对于本领域普通技术人员来讲,在不付出创造性劳动性的前提下,还可以根据这些附图获得其它的附图。其中:
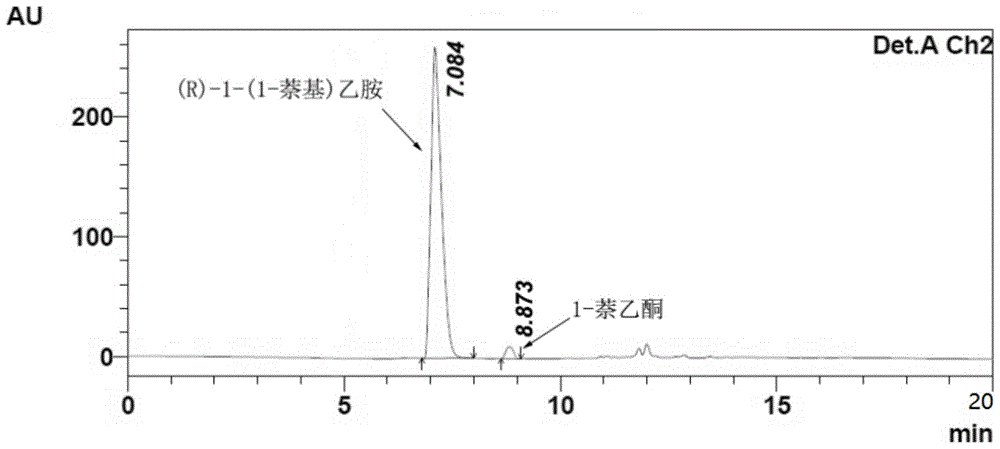
图1为本发明实施例3中d-氨基酸脱氢酶催化1-萘乙酮合成(r)-1-(1-萘基)乙胺反应的转化率检测结果图。
图2为本发明实施例3中d-氨基酸脱氢酶催化1-萘乙酮合成(r)-1-(1-萘基)乙胺反应的产物手性纯度检测结果图。
具体实施方式
为使本发明的上述目的、特征和优点能够更加明显易懂,下面结合说明书实施例对本发明的具体实施方式做详细的说明。
在下面的描述中阐述了很多具体细节以便于充分理解本发明,但是本发明还可以采用其他不同于在此描述的其它方式来实施,本领域技术人员可以在不违背本发明内涵的情况下做类似推广,因此本发明不受下面公开的具体实施例的限制。
其次,此处所称的“一个实施例”或“实施例”是指可包含于本发明至少一个实现方式中的特定特征、结构或特性。在本说明书中不同地方出现的“在一个实施例中”并非均指同一个实施例,也不是单独的或选择性的与其他实施例互相排斥的实施例。
实施例1
(1)本发明重组d-氨基酸脱氢酶基因工程菌的构建:
全基因合成序列如seqidno.1所示,选择ndei和hindiii两个酶切位点插入pet-41a(+)表达载体,采用氯化钙法转化大肠杆菌jm109感受态细胞;挑取阳性转化子测序鉴定后,得到重组表达载体;将含有目的基因的重组表达载体采用氯化钙法转入大肠杆菌bl21(de3)感受态细胞后,即可获得可以诱导表达重组d-氨基酸脱氢酶的基因工程菌。
(2)本发明重组d-氨基酸脱氢酶的制备:
将(1)中获得的基因工程菌接种至5ml含卡那霉素的lb试管培养基中活化培养(37℃培养12h),按1%接种量转接活化培养物至400ml含卡那霉素的lb液体培养基中,37℃培养菌体浓度a600至0.6-0.8,加入iptg(终浓度0.1mmol/l)于28℃诱导培养12h,离心收集菌体。取0.1g菌体重悬于10ml磷酸钾缓冲液(10mmol/l,ph7.5)中,冰水浴中超声破碎15min,离心收集上清液,-20℃预冻后真空冷冻干燥48h后碾碎,即得d-氨基酸脱氢酶酶粉。
(3)(r)-1-(1-萘基)乙胺的制备:
在ph6.5的磷酸钾缓冲液中,分别添加1-萘乙酮、辅酶nad+、甲酸铵、甲酸脱氢酶以及重组d-氨基酸脱氢酶组成反应混合液,在30℃水浴进行还原反应24h,生成(r)-1-(1-萘基)乙胺,通过hplc分析,测得转化率为95%,反应液用20%氢氧化钠溶液调节ph≥10,分别用等体积乙酸乙酯萃取3次,合并有机相,用无水硫酸钠干燥,过滤后减压蒸馏去除乙酸乙酯得油状液体产物,计算收率为88%,手性纯度(r)为99%ee。
其中,反应混合液:1-萘乙酮浓度为50mmol/l,甲酸铵浓度为100mmol/l,辅酶nad+浓度为0.1g/l,dmso的浓度为5%(v/v),缓冲液浓度为50mmol/l,甲酸脱氢酶浓度为1g/l,d-氨基酸脱氢酶浓度为0.5g/l。
实施例2
(r)-1-(1-萘基)乙胺的制备:
在ph8.5的磷酸钾缓冲液中,分别添加1-萘乙酮、辅酶nad+、甲酸铵、甲酸脱氢酶以及重组d-氨基酸脱氢酶组成反应混合液,在35℃水浴下进行还原反应40h,生成(r)-1-(1-萘基)乙胺,通过hplc分析,测得转化率为97%。反应液用20%氢氧化钠溶液调节ph≥10,分别用等体积乙酸乙酯萃取3次,合并有机相,用无水硫酸钠干燥,过滤后减压蒸馏去除乙酸乙酯得油状液体产物,计算收率为90%,手性纯度(r)为99%ee。
其中,反应混合液:1-萘乙酮浓度为150mmol/l,甲酸铵浓度为300mmol/l,辅酶nad+浓度为0.25g/l,dmso的浓度为5%(v/v),缓冲液浓度为100mmol/l,甲酸脱氢酶浓度为2g/l,d-氨基酸脱氢酶浓度为1g/l。1-萘乙酮,氨基供体,辅酶,助溶剂,缓冲液,辅酶循环酶和d-氨基酸脱氢酶按一定比例混合反应得到产物(r)-1-(1-萘基)乙胺,反应流程为:
实施例3
(r)-1-(1-萘基)乙胺的制备:
在ph7.5的磷酸钾缓冲液中,分别添加1-萘乙酮、辅酶nad+、甲酸铵、甲酸脱氢酶以及重组d-氨基酸脱氢酶组成反应混合液,在40℃水浴下进行还原反应45h,生成(r)-1-(1-萘基)乙胺,通过hplc分析,测得转化率为98%(见图1)。
反应液用20%氢氧化钠溶液调节ph≥10,分别用等体积乙酸乙酯萃取3次,合并有机相,用无水硫酸钠干燥,过滤后减压蒸馏去除乙酸乙酯得油状液体产物,计算收率为91%,手性纯度(r)为99%ee(见图2)。
其中,反应混合液:1-萘乙酮浓度为300mmol/l,甲酸铵浓度为600mmol/l,辅酶nad+浓度为0.5g/l,dmso的浓度为10%(v/v),缓冲液浓度为100mmol/l,甲酸脱氢酶浓度为3g/l,d-氨基酸脱氢酶浓度为2g/l。
实施例4
按照实施例1(1)和(2)的方法制备corynebacteriumglutamicumatcc13032来源的d-氨基酸脱氢酶酶粉。按实施例2所述在ph8.5的磷酸钾缓冲液中,分别添加1-萘乙酮、辅酶nad+、甲酸铵、甲酸脱氢酶以及来源于corynebacteriumglutamicumatcc13032的重组d-氨基酸脱氢酶酶粉组成反应混合液,在30℃水浴进行还原反应24h,通过hplc分析,无明显产物生成。
由此可知,并非所有的d-氨基酸脱氢酶都能催化此反应,只有本发明中公开的d-氨基酸脱氢酶能催化1-萘乙酮生成(r)-1-(1-萘基)-乙胺。
实施例5
与实施例1中(3)相比,调整ph为9.5,其余条件相同,转化率仅为38%,详见如下:
在ph9.5的柠檬酸钠缓冲液中,分别添加1-萘乙酮、辅酶nad+、甲酸铵、甲酸脱氢酶以及重组d-氨基酸脱氢酶组成反应混合液,在30℃水浴进行还原反应24h,生成(r)-1-(1-萘基)乙胺,通过hplc分析,测得转化率为38%。
其中,反应混合液:1-萘乙酮浓度为50mmol/l,甲酸铵浓度为100mmol/l,辅酶nad+浓度为0.1g/l,dmso的浓度为5%(v/v),缓冲液浓度为50mmol/l,甲酸脱氢酶浓度为1g/l,d-氨基酸脱氢酶浓度为0.5g/l。
实施例6
与实施例1中(3)相比,调整调整反应温度为50℃,其余条件相同,转化率仅为32%,详见如下:
在ph6.5的磷酸钾缓冲液中,分别添加1-萘乙酮、辅酶nad+、甲酸铵、甲酸脱氢酶以及重组d-氨基酸脱氢酶组成反应混合液,在50℃水浴进行还原反应24h,生成(r)-1-(1-萘基)乙胺,通过hplc分析,测得转化率为32%。
其中,反应混合液:1-萘乙酮浓度为50mmol/l,甲酸铵浓度为100mmol/l,辅酶nad+浓度为0.1g/l,dmso的浓度为5%(v/v),缓冲液浓度为50mmol/l,甲酸脱氢酶浓度为1g/l,d-氨基酸脱氢酶浓度为0.5g/l。
实施例7
与实施例1中(3)相比,底物与氨基供体(甲酸铵)的浓度比由1:2调整为1:1,同时不添加助溶剂dmso,其余条件相同,转化率仅为46%,详见工艺如下:
在ph6.5的磷酸钾缓冲液中,分别添加1-萘乙酮、辅酶nad+、甲酸铵、甲酸脱氢酶以及重组d-氨基酸脱氢酶组成反应混合液,在30℃水浴进行还原反应24h,生成(r)-1-(1-萘基)乙胺,通过hplc分析,测得转化率为46%。
其中,反应混合液:1-萘乙酮浓度为50mmol/l,甲酸铵浓度为50mmol/l,辅酶nad+浓度为0.1g/l,缓冲液浓度为50mmol/l,甲酸脱氢酶浓度为1g/l,d-氨基酸脱氢酶浓度为0.5g/l。
现有技术主要采用化学不对称合成方法和不对称拆分法,其中化学不对称合成方法所使用的催化剂含有重金属,价格昂贵,存在重金属污染,反应需在有机溶剂中进行,不利于环境保护,同时产物手性纯度并不高;不对称拆分法涉及化学法和生物法,这一类方法理论最高收率仅50%,同时拆分试剂价格昂贵,需要大量使用有机溶剂,环境污染严重。本发明提出了利用d-氨基酸脱氢酶不对称催化合成(r)-1-(1-萘基)乙胺,最终反应转化率大于95%,产物收率大于88%,产物手性纯度达到99%ee,本发明方法反应条件温和,有机溶剂用量小,反应体系更绿色环保,转化率高,大大提高了(r)-1-(1-萘基)乙胺的制备效率,具有较好的工业应用前景。
d-氨基酸脱氢酶能不对称催化羰基化合物合成手性胺类化合物,已有授权专利公布了利用该酶催化合成(r)-3-氨基丁醇等手性胺;本发明通过筛选不同来源的d-氨基酸脱氢酶,发现本发明中公开的d-氨基酸脱氢酶能催化1-萘乙酮生成(r)-1-(1-萘基)-乙胺,而并非所有的d-氨基酸脱氢酶都能催化此反应。
本发明优化各反应物的添加比例,(r)-1-(1-萘基)乙胺最终反应转化率大于95%,产物收率大于88%,产物手性纯度达到99%ee,反应条件温和,有机溶剂用量小,反应体系更绿色环保,转化率高,大大提高了(r)-1-(1-萘基)乙胺的制备效率,具有较好的工业应用前景。
应说明的是,以上实施例仅用以说明本发明的技术方案而非限制,尽管参照较佳实施例对本发明进行了详细说明,本领域的普通技术人员应当理解,可以对本发明的技术方案进行修改或者等同替换,而不脱离本发明技术方案的精神和范围,其均应涵盖在本发明的权利要求范围当中。
序列表
<110>泰州学院
<120>一种酶法合成西那卡塞中间体(r)-1-(1-萘基)乙胺的方法
<141>2020-02-03
<160>2
<170>siposequencelisting1.0
<210>1
<211>900
<212>dna
<213>artificialsequence
<400>1
atggacaaactgcgtgttgctgttgttggttacggtaacgttggtcgttacgctctggaa60
gctgttcaggctgctccggacatggaactggttggtgttgttcgtcgtaaagttctggct120
gctaccccgccggaactgaccggtgttcgtgttgttaccgacatctctcagctggaaggt180
gttcagggtgctctgctgtgcgttccgacccgttctgttccggaatacgctgaagctatg240
ctgcgtcgtggtatccacaccgttgactcttacgacatccacggtgacctggctgacctg300
cgtcgtcgtctggacccggttgctcgtgaacacggtgctgctgctgttatctctgctggt360
tgggacccgggtaccgactctatcatccgtgctctgctggaattcatggctccgaaaggt420
atcacctacaccaacttcggtccgggtatgtctatgggtcactctgttgctgttaaagct480
atcccgggtgttcgtgacgctctgtctatgaccatcccggctggtatgggtgttcacaaa540
cgtgctgtttacgttgaactggaaccgggtgctgacttcgctgaagttgaacgtgctatc600
aaaaccgacccgtacttcgttcgtgacgaaacccgtgttacccaggttgagtctgtaagc660
gctctgatggacgttggtcacggtgttgttatggaacgtaaaggtgtttctggtgctacc720
cacaaccagctgttccgtttcgaaatgcgtatcaacaacccggctctgaccgctcaggtt780
atggttgctgctctgcgtgctgctgctcgtcagaaaccgggttgctacaccatgatcgaa840
atcccggttatcgactacctgccgggtgaccgtgaagcgtggatccgtaaactggtttaa900
<210>2
<211>299
<212>prt
<213>artificialsequence
<400>2
metalaleuleualavalalavalvalglythrglyalavalglyala
151015
thralaleuglyalavalglyalaalaproalametglyleuvalgly
202530
valvalalaalaleuvalleualaalathrproproglyleuthrgly
354045
valalavalvalthralaileserglyleuglyglyvalglyglyala
505560
leuleucysvalprothralaservalproglythralaglyalamet
65707580
leualaalaglyilehisthrvalalaserthralailehisglyala
859095
leualaalaleualaalaalaleualaprovalalaalaglyhisgly
100105110
alaalaalavalileseralaglythralaproglythralaserile
115120125
ilealaalaleuleuglyprometalaproleuglyilethrthrthr
130135140
alaproglyproglymetsermetglyhisservalalavalleuala
145150155160
ileproglyvalalaalaalaleusermetthrileproalaglymet
165170175
glyvalhisleualaalavalthrvalglyleuglyproglyalaala
180185190
proalaglyvalglyalaalaileleuthralaprothrprovalala
195200205
alaglythralavalthrglyvalglyservalseralaleumetala
210215220
valglyhisglyvalvalmetglyalaleuglyvalserglyalathr
225230235240
hisalaglyleuproalaproglymetalailealaalaproalaleu
245250255
thralaglyvalmetvalalaalaleualaalaalaalaalaglyleu
260265270
proglycysthrthrmetileglyileprovalilealathrleupro
275280285
glyalaalaglyalathrilealaleuleuval
290295
- 还没有人留言评论。精彩留言会获得点赞!