一种探针组合物及其在核酸原位检测中的应用的制作方法
本发明属于生物技术领域,涉及一种探针组合物及其在核酸原位检测中的应用,尤其涉及一种探针组合物、核酸原位检测试剂盒、核酸原位检测方法及其在制备疾病诊断试剂中的应用。
背景技术:
核酸原位检测技术是一种在细胞内检测核酸表达和分布的技术。随着pcr(polymerasechainreaction)和高通量测序的发展,将生物样本作为整体进行研究,获得的基因表达谱和基因表达量是整个生物样本的平均值,而组织中不同位置、不同功能的细胞的基因表达具有异质性,采用传统的方法无法获得这一差异,细胞间的差异淹没在了平均值中。而了解基因在不同功能细胞中的差异性表达,有助于精准揭示基因功能、准确研究疾病原因,为疾病的精准治疗提供有效方案。
现有的免疫荧光、免疫组化、细胞流式等技术能够通过标记的抗体研究单细胞中的蛋白质,但是不适用于单细胞的核酸检测;同时,上述方法受到商品化抗体的限制,如果缺少特异性抗体,则很难对相应靶标进行检测;另外,此类方法也难以准确检测分泌型蛋白。单细胞测序是近年来新兴的研究单细胞基因表达的方法,但是将单细胞实验结果还原到组织结构中时,需要考虑组织位置分布及微环境对细胞基因表达的影响,单纯的单细胞测序结果仍然不能准确反映组织细胞的异质性。
为了解决上述技术问题,核酸原位检测技术也得到了快速发展。核酸原位检测技术能够在组织切片中对不同细胞的基因表达情况进行检测,fish(fluorescenceinsituhybridization)作为最经典的核酸原位检测技术,但存在耗时长、信号低、背景高、特异性差等缺点,研究人员在此基础上也逐渐开发出了许多新方法。
wo2018175779a1、us20160108458a1利用滚环扩增的方式进行核酸的原位检测,设计的探针结合在靶核酸的相邻位置上,两条探针游离的一端供搭桥探针和成环探针结合,通过连接酶将搭桥探针和成环探针连接成闭合的环状序列后,以一条探针的3’端为引物、以形成的环状序列为模板,进行滚环扩增检测。上述两种方案虽然具有较好的特异性,但是需要加入搭桥探针和成环探针并进行连接反应,操作复杂,耗时较长。
wang等(thejournalofmoleculardiagnostics,vol.14,no.1,january2012)设计一对“z”型探针结合在靶核酸的相邻位置上,体系中需要加入与两个“z”型探针结合的延伸探针,供大量的检测探针结合,从而进行信号放大。该方法特异性好,但是探针设计复杂,影响了检测效率,且成本高。
larsson等(naturemethods,vol.7,no.5,may2010)利用lna逆转录引物和逆转录酶将rna逆转录为cdna后,采用锁式探针识别靶序列,通过滚环扩增放大检测信号。但是该方法需要采用lna逆转录引物识别目标mrna并进行逆转录,lna逆转录引物的合成成本高,逆转录过程延长了检测时间;另外,滚环扩增以cdna的3’端为引物,因此一条cdna链只能结合一个锁式探针进行扩增,信号放大程度受到限制。
另外,chen等(science,vol.348,issue6233,april2015)设计多达96条探针进行原位检测,每条探针包含中间识别序列和两端的游离序列,探针复杂、成本较高,方法特异性弱。
因此,有必要提供一种更加简便、高效、特异、低成本的核酸原位检测技术。
技术实现要素:
针对现有技术的不足和实际需求,本发明提供了一种探针组合物及其在核酸原位检测中的应用,采用环状探针和发夹探针组成的探针组合物与原位核酸互补结合,探针结构简单,反应过程中不需要进行连接反应,实现了快速、特异、准确、低成本的核酸原位检测。
为达此目的,本发明采用以下技术方案:
第一方面,本发明提供了一种探针组合物,所述探针组合物包括环状探针和发夹探针;
所述环状探针包括第一结合序列和非第一结合序列;
所述发夹探针包括5’折叠序列、第二结合序列和3’结合序列;
所述第一结合序列与靶核酸的第一结合位点互补;
所述第二结合序列与靶核酸的第二结合位点互补;
所述发夹探针的3’结合序列与所述环状探针中除第一结合序列的部分或全部序列互补。
本发明中,环状探针和发夹探针依靠各自的结合序列结合在原位核酸处,结合序列的设计可以与靶核酸的序列具有70~100%的吻合程度。环状探针和发夹探针分别与靶核酸结合时,发夹探针的3’结合序列与相邻位置的环状探针的部分或全部非第一结合序列相结合,发夹探针的3’结合序列作为滚环扩增的引物、环状探针作为滚环扩增的模板,进行滚环扩增反应,在原位核酸处得到含有大量重复序列的扩增产物。
本发明中,为进一步提高检测特异性,将发夹探针的5’折叠序列设计为能够与3’结合序列结合,形成茎环结构,在发夹探针未与靶核酸结合的情况下,发夹探针呈茎环结构,3’结合序列无法与环状探针结合,不发生滚环扩增反应;当发夹探针与靶核酸结合后,茎环结构打开,3’结合序列与环状探针结合,从而引发滚环扩增反应。另外,发夹探针也可通过自身序列互补折叠,将3’结合序列与第二结合位点部分序列互补,实现无靶核酸情况下,3’结合序列无法与环状探针结合,而有靶核酸情况下,能够释放出3’结合序列,与环状探针结合。sanjaytyagi等(naturebiotechnology,vol.14,march1996)研究表明,拥有茎环结构的分子信标具有极高的特异性,设计合理的分子信标甚至可以识别出单碱基的差异,当非特异核酸与靶核酸只存在单个碱基差异时,分子信标也不会打开茎环结构。因此采用5’折叠序列和3’结合序列互补结合的发夹探针能够显著提高检测特异性,可检测单碱基突变。同时,本发明通过扩增出的重复序列带来的信号放大,实现了简单、灵敏、特异的核酸原位检测效果。另外茎环结构打开后5’折叠序列可以与靶核酸互补结合,也可以呈游离状态作为检测探针的结合位点、与检测探针结合,增强检测信号。
优选地,所述第一结合位点和所述第二结合位点相邻。
本发明中,环状探针和发夹探针结合在靶核酸的相邻位置,只有当环状探针和发夹探针同时结合在靶核酸相邻位置,降低了3’结合序列与环状探针的结合难度,有利于发夹探针的3’结合序列特异、高效地互补结合在环状探针的非第一结合序列上,才能引发滚环扩增,从而更加提高了检测的特异性。
优选地,所述第一结合位点位于所述第二结合位点的5’端或3’端,优选为所述第一结合位点位于所述第二结合位点的5’端。
优选地,发夹探针未与靶核酸结合时,3’结合序列与5’折叠序列相互结合形成茎环结构,当发夹探针与靶核酸结合后,茎环结构打开。
本发明中,当不存在靶核酸序列时,发夹探针的5’折叠序列与所述3’结合序列通过氢键结合或化学键结合,优选为5’折叠序列与所述3’结合序列通过watson-crick配对结合或通过hoogsteen配对结合;当5’折叠序列与所述3’结合序列通过hoogsteen配对结合时,可通过多聚鸟苷酸形成g-四链体(g-quadruplex)结构(a.bourdoncleetal.j.am.chem.soc.2006),从而形成类似茎环结构。在发夹探针未与靶核酸结合的情况下,3’结合序列和5’折叠序列结合在一起,不会造成非特异扩增。
优选地,所述5’折叠序列与所述3’结合序列可以通过碱基互补结合,形成茎环结构。
本发明中,可以通过对环状探针、发夹探针进行化学修饰,提高其结合靶核酸的稳定性和特异性,同时能够增强探针对核酸酶的耐受能力。
优选地,所述环状探针和发夹探针的部分或全部核苷酸修饰有核酸类似物。
优选地,所述核酸类似物包括lna(lockednucleicacid,锁式核酸)-dna、lna-rna、2’-frna、2’-nh2rna、2’-o-merna或2’-o-moerna中的任意一种或至少两种的组合。
本发明还可以优化探针设计,调整相互结合的碱基数,优化杂交缓冲液、洗脱液配方,调整反应温度,反应时间,探针加入顺序,来降低非特异性结合、提高反应灵敏度、简化操作步骤。
优选地,所述环状探针的长度为15~100nt,例如可以是15nt、20nt、25nt、30nt、35nt、40nt、45nt、50nt、55nt、60nt、65nt、70nt、75nt、80nt、85nt、90nt、95nt或100nt。
优选地,所述发夹探针的长度为15~80nt,例如可以是15nt、20nt、25nt、30nt、35nt、40nt、45nt、50nt、55nt、60nt、65nt、70nt、75nt或80nt。
优选地,所述环状探针采用酶连接反应制备得到。
优选地,所述酶连接反应包括:
人工合成与环状探针具有相同核酸序列的线性化核酸分子;
向所述线性化核酸分子中加入搭桥引物和连接酶,连接得到所述环状探针;
所述搭桥引物的两端分别与所述线性化核酸分子的两端互补结合,优选地所述搭桥引物的5’端与所述线性化核酸分子的5’端反向互补,所述搭桥引物的3’端与所述线性化核酸分子的3’端反向互补。
优选地,所述搭桥引物可以是dna片段,也可以是rna片段。
优选地,所述连接酶可以是dna连接酶如t4dnaligase、splintr或rna连接酶如t4rnaligase中的一种或至少两种的组合。
本发明中,环状探针可以通过人工有机合成方法直接获得,也可以通过连接反应制备得到;在连接反应中,搭桥引物将线性化核酸分子的5’端和3’端拉近,在连接酶的作用下发生连接反应,得到环状探针。
搭桥引物的3’端需要进行封闭修饰,例如可以采用双脱氧胞苷(dideoxy-c,ddc)进行修饰,以防止搭桥引物的3’端在滚环扩增中进行延伸;优选地,搭桥引物也可以不进行3’端封闭修饰,当环状探针封闭成环后,可以加入核酸外切酶iii消化去除搭桥引物。
优选地,所述线性化核酸分子的5’端修饰有磷酸基团。
本发明中,为促进连接反应的发生,可以在线性化核酸分子的5’端通过人工有机合成添加磷酸基团,或通过磷酸激酶进行磷酸化处理,以便于连接反应进行。
第二方面,本发明提供了一种核酸原位检测方法,所述方法包括:
(1)向生物样本中加入一对或多对第一方面所述的探针组合物,探针组合物中的环状探针和发夹探针结合在靶核酸的相邻位点;
(2)发夹探针的3’结合序列与环状探针的部分或全部非第一结合序列互补结合,发夹探针的3’结合序列作为引物、环状探针作为模板发生滚环扩增反应;
(3)加入一种或多种检测探针,与滚环扩增产物和/或发夹探针的5’折叠序列结合;
(4)对检测探针的标记基团进行检测,得到核酸原位检测结果。
优选地,步骤(1)所述多对第一方面所述的探针组合物结合生物样本的相同和/或不同靶核酸。
本发明中,可以采用多对探针组合物结合同一靶核酸的不同位点,提高检测灵敏度,多对环状探针和发夹探针的结合序列与同一靶核酸的不同位置结合,每对探针组合物中的环状探针和发夹探针结合在靶核酸的相邻位点;多个环状探针含有相同或不同的检测探针结合序列。
本发明中,还可以采用多对探针组合物结合不同的靶核酸,实现原位多重检测,也可同时针对不同的靶核酸,每个靶核酸采用多对探针组合物进行检测。
优选地,步骤(2)所述滚环扩增反应的温度为25~65℃,例如可以是25℃、26℃、27℃、28℃、29℃、30℃、31℃、32℃、33℃、34℃、35℃、36℃、37℃、38℃、39℃、40℃、41℃、42℃、43℃、44℃、45℃、46℃、47℃、48℃、49℃、50℃、51℃、52℃、53℃、54℃、55℃、56℃、57℃、58℃、59℃、60℃、61℃、62℃、63℃、64℃或65℃,优选为37℃。
优选地,步骤(3)所述多种检测探针修饰有相同和/或不同的标记基团。
优选地,所述核酸包括dna和/或rna。
优选地,所述rna包括信使rna(messengerrna,mrna)、核糖体rna(ribosomalrna,rrna)、转移rna(transferrna,trna)、非编码rna(non-codingrna,ncrna)或调控rna(regulatoryrna)中的任意一种或至少两种的组合。
优选地,所述核酸位于细胞、囊泡或组织切片中。
优选地,所述细胞包括真核细胞和/或原核细胞。
优选地,所述细胞包括动物细胞、植物细胞、真菌细胞、原生生物细胞或人工细胞中的任意一种或至少两种的组合。
优选地,所述细胞包括固定后的细胞或活细胞。
优选地,所述囊泡包括微囊泡、外泌体、凋亡小体或人工囊泡、颗粒中的任意一种或至少两种的组合。
优选地,所述组织切片包括冰冻切片和/或石蜡切片。
优选地,在靶核酸含量很低的情况下,可以将本发明的方法与酪胺信号放大技术(tyramidesignalamplification,tsa)相结合。洗脱未结合的检测探针后,加入针对检测探针标记基团的第一抗体,再加入识别第一抗体的辣根过氧化物酶(horseradishperoxidase,hrp)酶标二抗,再加入tsa荧光化合物,tsa荧光化合物在hrp催化下与靶点附近的酪氨酸残基结合,生成稳定的荧光化合物,将检测信号放大10~1000倍。
优选地,所述方法在步骤(1)之前还包括对生物样本进行预处理的步骤,所述预处理包括裂解处理和/或透化处理。
优选地,所述方法在步骤(4)之后还包括对生物样本进行免疫组化分析、免疫荧光分析、流式细胞分析或细胞分选的步骤。
本发明中,可以采用人工方法或自动设备对信号进行识别分析,分析信号位置和信号强度,采用机器算法对细胞、囊泡中的核酸进行统计,进行原位核酸的定性、定量分析;在某些情况下还可以根据核酸检测结果,对细胞、囊泡进行分类识别。
第三方面,本发明提供了一种核酸原位检测试剂盒,所述试剂盒包括第一方面所述的探针组合物。
优选地,所述试剂盒还包括检测探针。
优选地,所述检测探针的序列与所述环状探针的部分序列相同。
本发明中,以环状探针的部分序列作为检测探针的序列,使环状探针中含有一个或多个与检测探针相同的序列,有利于检测探针互补结合在以环状探针为模板的扩增产物的一个或多个位点上。
优选地,所述检测探针的序列与所述发夹探针的5’折叠序列互补。
本发明中,检测探针还可以结合在发夹探针的5’折叠序列互补上,增强检测信号。
优选地,所述检测探针修饰有标记基团。
优选地,所述标记基团包括荧光标记物、生物发光标记物、化学发光标记物、同位素标记物或纳米颗粒、蛋白酶、催化剂或金属中的任意一种,优选为荧光标记物。
本发明中,检测探针还可以通过化学修饰提高其结合力、特异性以及对核酸酶的耐受性。
优选地,所述检测探针的部分或全部核苷酸修饰有核酸类似物。
优选地,所述核酸类似物包括lna-dna、lna-rna、2’-frna、2’-nh2rna、2’-o-merna或2’-o-moerna中的任意一种或至少两种的组合。
本发明中,当在一个循环体系中检测多个靶核酸时,针对不同的靶核酸采用不同的检测探针,检测探针修饰不同的标记基团(如cy3、cy5、fam等),从而根据不同的信号对靶核酸进行区分;还可以采用多循环体系检测多个靶核酸,一个循环完成后,去除检测探针,或使用淬灭剂淬灭检测信号,再进行下一个循环,完成后去除检测探针或淬灭检测信号,重复循环,直至完成所有的核酸检测。
优选地,所述检测探针的长度为5~100nt,例如可以是5nt、10nt、20nt、30nt、40nt、50nt、60nt、70nt、80nt、90nt或100nt。
优选地,所述试剂盒还包括聚合酶,例如可以是dna聚合酶和/或rna聚合酶。
优选地,所述聚合酶为具有链置换活性的聚合酶,例如可以是phi29、bsu、bst或vent(exo-)dnapolymerase中的任意一种或至少两种的组合。
优选地,所述试剂盒还包括聚合酶反应液、杂交缓冲液、洗脱液或样本处理液中的任意一种或至少两种的组合。
第四方面,本发明提供了一种第一方面所述的探针组合物和/或第二方面所述的试剂盒在制备疾病诊断试剂中的应用。
与现有技术相比,本发明具有如下有益效果:
(1)本发明利用预先制备好的环状探针进行检查,省略了现有方法中的连接成环的步骤,操作简便、快捷;
(2)本发明利用发夹探针的结构特点,在没有靶核酸的情况下,发夹探针保持茎环结构,无法与环状探针互补结合,不会引发扩增反应,使检测反应具有较高的特异性,在保证了检测的高特异性的同时节省了操作时间,降低了实验成本。
附图说明
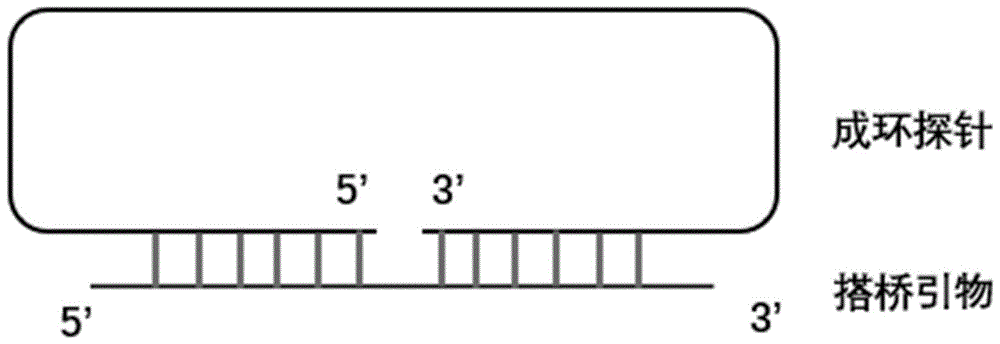
图1为环状探针的制备方法示意图;
图2a为单基因核酸原位检测原理图,图2b为多基因核酸原位检测原理图;
图3a为滚环扩增产物的电泳图,其中,t为阳性实验组,加入反应所需全部试剂,c1为对照组1,去离子水替代靶标序列,c2为对照组2,去离子水替代发夹探针和靶标序列,图3b为滚环扩增产物的电泳图,其中,t为阳性实验组,加入反应所需全部试剂,c3为对照组3,随机序列代替靶标序列,m为dnamarker;
图4为采用g-四链体设计的发夹探针进行滚环扩增产物的电泳图,其中,t为阳性实验组,加入反应所需全部试剂,c为对照组,加入随机序列代替靶标序列,其余反应成分相同,m为dnamarker;
图5a为人源hela细胞中gapdh的mrna原位检测结果,图5b为相应的对照组结果;
图6a为小鼠3t3细胞中scnn1b的mrna原位检测结果,图6b为相应的对照组结果;
图7a为使用3’互补序列与5’折叠序列不互补结合的发夹探针,在小鼠3t3细胞中进行scnn1b的mrna原位检测结果,图7b为相应的对照组结果;
图8为小鼠气管冰冻切片中sma(绿色荧光)和col1α1(红色荧光)的mrna原位检测结果。
具体实施方式
为进一步阐述本发明所采取的技术手段及其效果,以下结合实施例和附图对本发明作进一步地说明。可以理解的是,此处所描述的具体实施方式仅仅用于解释本发明,而非对本发明的限定。
实施例中未注明具体技术或条件者,按照本领域内的文献所描述的技术或条件,或者按照产品说明书进行。所用试剂或仪器未注明生产厂商者,均为可通过正规渠道商购获得的常规产品。
实施例1环状探针的合成和核酸原位检测原理
环状探针可以通过人工合成方法直接获得,也可以通过连接反应制备得到。本实施例首先采用连接反应的方法制备环状探针,示意图如图1所示,步骤如下:
(1)人工合成与环状探针具有相同核酸序列的线性化核酸分子;
(2)向线性化核酸分子中加入搭桥引物和连接酶,搭桥引物的5’端与线性化核酸分子的5’端互补,搭桥引物的3’端与线性化核酸分子的3’端互补,搭桥引物将线性化核酸分子的5’端和3’端拉近,在连接酶的作用下发生连接反应,得到环状探针。
基于制备的环状探针和发夹探针,实现核酸原位检测,原理图如图2a和图2b所示:
在进行单基因检测时,将生物样本与一对或多对探针组合物共孵育,探针组合物中的环状探针和发夹探针结合在靶核酸的相邻位点,发夹探针的茎环结构打开,3’结合序列与环状探针的非第一结合序列互补结合,发夹探针的3’结合序列作为引物、环状探针作为模板发生滚环扩增反应(rollingcircleamplification,rca);滚环扩增后,再加入检测探针,与滚环扩增产物和/或发夹探针的5’折叠序列结合,通过对检测探针的标记基团进行检测,进行核酸原位检测。
还可以向体系中加入针对不同靶核酸的环状探针、发夹探针和检测探针,实现靶核酸的原位多重检测。
实施例2滚环扩增
(1)探针设计
本实施例以humanglyceraldehyde-3-phosphatedehydrogenase(hgapdh)mrna序列为模板,选择合适的区域进行探针设计,序列如下:
环状探针(seqidno:1):
5’-p-aatagctaagtcgcgatcttgattttggagggatctcgcatcagcacga-3’;
其中,5’端添加磷酸化修饰,ttgattttggagggatctcg与靶标序列中的部分序列互补,cgcgatc与发夹探针的3’结合序列互补,5’端和3’端的其余序列与搭桥引物互补;
发夹探针(seqidno:2):
5’-cgcgatccagcgccagcatcgccccacgatcgcg-3’;
其中,cagcgccagcatcgccccac与靶标序列中的部分序列互补,5’折叠序列cgcgatc与3’结合序列gatcgcg反向互补,形成茎环结构;
搭桥引物(seqidno:3):
5’-acttagctatttcgtgctgatg-3’;
靶标序列(seqidno:4):
5’-aggagcgagatccctccaaaatcaagtggggcgatgctggcgctgagtac-3’;
随机序列(seqidno:5):
5’-gtcacgagagtcgagctgaagcgaatacggcaagtggtccaggtcagtcc-3’;
合成的序列采用te溶液(10mmtris,1mmedta,ph8.0)配制为100μm的储存液,再稀释成10μm工作液。发卡探针95℃加热5min后,缓慢降至室温,以形成稳定的茎环结构。
(2)环状探针的制备
向5μl线性化探针中加入5μl搭桥引物,再加入10μl杂交液(2×ssc,10%甲酰胺,0.3mg肝素),混合均匀后置于37℃反应1h;取出5μl反应产物,加入2μl10×t4ligasebuffer(neb)、0.5μlt4dnaligase(neb),加去离子水至20μl,置于37℃反应1h,反应产物即为连接好的环状探针;
向连接好的环状探针中加入2μl核酸外切酶iii(takara),37℃孵育3h,80℃孵育20min,使外切酶热失活,置于4℃冰箱保存待用。
(3)rca扩增
取2μl核酸外切酶处理后的环状探针,加入0.2μl发夹探针、0.2μl靶标序列、2μl10×phi29聚合酶(neb)、2μl10×phi29聚合酶缓冲液(neb)、1μl10mmdntp,加入去离子水至20μl,置于37℃反应,分别在2h、8h后取出进行电泳检测;对照组1按照上述配方,用去离子水替代靶标序列;对照组2按照上述配方,用去离子水替代发夹探针和靶标序列;对照组3按照上述配方,用随机序列代替靶标序列。
(4)电泳检测
取各组的反应产物5μl,加入1μl6×上样缓冲液,在1%琼脂糖凝胶上进行电泳检测。
电泳结果如图3a和图3b所示,实验组有长度较长的核酸条带,对照组均未见条带,说明在没有靶标序列的情况下,发夹探针不与环状探针结合,不会进行序列扩增。
实施例3滚环扩增
本实施例同样以hgapdhmrna序列为模板,发夹探针采用g-四链体设计,进行功能验证,序列如下:
环状探针(seqidno:6):
5’-p-aatagctaagtccctaacccttgattttggagggatctcgcatcagcacga-3’;
发夹探针(seqidno:7):
5’-gggttagggcagcgccagcatcgccccacgggttaggg-3’;
搭桥引物(seqidno:3):
5’-acttagctatttcgtgctgatg-3’;
靶标序列(seqidno:4):
5’-aggagcgagatccctccaaaatcaagtggggcgatgctggcgctgagtac-3’;
随机序列(seqidno:5):
5’-gtcacgagagtcgagctgaagcgaatacggcaagtggtccaggtcagtcc-3’;
(2)环状探针的制备
使用实施例2制备的环状探针。
(3)rca扩增
按照实施例2的方法进行rca扩增,扩增反应时间为8h;对照组采用随机序列代替靶标序列。
(4)电泳检测
按照实施例2的方法进行电泳检测。
电泳结果如图4所示,实验组有长度较长的核酸条带,对照组未见条带,说明在没有靶标序列的情况下,发夹探针保持茎环结构,不与环状探针结合,不会进行序列扩增。
实施例4人源肿瘤细胞涂片的核酸原位检测
(1)hela细胞培养
将hela细胞加入dmem培养基(含10%fbs,1%青链霉素)中,置于37℃、5%co2细胞培养箱中培养至适当密度,准备收集细胞,制备细胞涂片,原位检测hgapdhmrna。
(2)细胞涂片制备
hela细胞采用0.25%胰酶消化后,加入全培养基终止消化,吹打细胞,将细胞悬液加入15ml离心管中;800rpm离心3min,收集细胞,并用pbs(ph7.4)清洗两次;向细胞中加入0.5ml4%pfa,进行细胞固定20min;800rpm离心3min,弃上清,用pbs清洗两次,加入0.1mlpbs悬浮细胞;
取5μl细胞悬液滴加在载玻片中央,用另一载玻片边缘将细胞悬液推开,使细胞分散在载玻片上,室温放置20min,风干载玻片,-80℃保存。
(3)环状探针的制备
按照实施例2的方法制备环状探针,并使用外切酶iii进行消化,使用2对探针组合物,在细胞涂片上原位检测hgapdhmrna的表达;
环状探针1(seqidno:1):
5’-p-aatagctaagtcgcgatcttgattttggagggatctcgcatcagcacga-3’;
环状探针2(seqidno:8):
5’-p-aatagctaagtcgcgatcttcccgttcagctcagggatcatcagcacga-3’;
发夹探针1(seqidno:2):
5’-cgcgatccagcgccagcatcgccccacgatcgcg-3’;
发夹探针2(seqidno:9):
5’-cgcgatcggaaggccatgccagtgagcgatcgcg-3’;
搭桥引物(seqidno:3):
5’-acttagctatttcgtgctgatg-3’;
检测探针(seqidno:10):
5’-fam-catcagcacgaaatagctaagt-3’;
(4)rna原位检测
取出-80℃保存的细胞涂片,室温风干20min,浸入100%乙醇脱水5min,室温10min风干,再依次放入80%乙醇、60%乙醇和pbs中各3min;
按照每个环状探针10μl、1μlrnaseout加入79μl杂交液(depc水配制,2×ssc,10%甲酰胺,0.3mg肝素)的比例配制所需溶液,滴加到玻片样本上全部覆盖样本表面;将玻片放置于湿盒中,在37℃下孵育1h,用杂交液清洗玻片三次;
按照每个发夹探针1μl、1μlrnaseout加入97μl杂交液的比例配制所需溶液,滴加到玻片样本上全部覆盖样本表面;将玻片放置于湿盒中,在37℃下孵育1h,用杂交液清洗玻片三次;
按照下述比例配制rca反应液,6μlphi29聚合酶、10μl10×phi29聚合酶缓冲液、2μl10mmdntps、2μlbsa(25mg/ml)、80μldepc水,滴加至样本表面覆盖样本;将玻片放置于湿盒中,在37℃下孵育过夜;
实验组加入反应所需全部试剂,对照组不加入发夹探针,其余操作步骤同实验组;
第二天,用杂交液清洗玻片三次,按照1μl检测探针加入99μl杂交液的比例配制所需体积溶液,滴加到玻片样本上全部覆盖样本表面;将玻片放置于湿盒中,在37℃下孵育1h,用杂交液清洗玻片三次;
滴加核染料dapi(1ng/ml)到玻片样本上全部覆盖样本表面,37℃孵育10min,加入洗脱液(pbs,ph7.4)洗三次;
滴加抗荧光猝灭封片液(碧云天)进行封片,荧光显微镜下观察结果。
结果如图5a和图5b所示,实验组可见点状绿色荧光分布在细胞核周围,而对照组无绿色荧光,说明该方法可以原位检测细胞中的基因表达。
实施例5小鼠细胞涂片核酸原位检测
(1)3t3小鼠成纤维细胞培养
将3t3小鼠成纤维细胞加入α-mem培养基(含10%fbs,1%青链霉素)中,置于37℃、5%co2细胞培养箱中培养至适当密度,准备收集细胞,制作细胞涂片,原位检测小鼠sodiumchannel,nonvoltage-gated1beta(scnn1b)mrna。
(2)细胞涂片制备
3t3细胞采用0.25%胰酶消化后,加入全培养基终止消化,吹打细胞,将细胞悬液加入15ml离心管中;800rpm离心3min,收集细胞,并用pbs(ph7.4)清洗两次;向细胞中加入0.5ml4%pfa,进行细胞固定20min;800rpm离心3min,弃上清,用pbs清洗两次,加入0.1mlpbs悬浮细胞;
取5μl细胞悬液滴加在载玻片中央,用另一载玻片边缘将细胞悬液推开,使细胞分散在载玻片上,室温放置20min,风干载玻片,-80℃保存。
(3)环状探针的制备
按照实施例2的方法制备环状探针,并使用外切酶iii进行消化,序列如下;
环状探针1(seqidno:11):
5’-p-aatagctaagtcgcgatcatgcgatcaggggcatagcccatcagcacga-3’;
环状探针2(seqidno:12):
5’-p-aatagctaagtcgcgatcacggatcatgtggtcttggacatcagcacga-3’;
环状探针3(seqidno:13):
5’-p-aatagctaagtcgcgatcttgacaatacccttcctgctcatcagcacga-3’;
发夹探针1(seqidno:14):
5’-cgcgatccaaacaggcaagctaggattgatcgcg-3’;
发夹探针2(seqidno:15):
5’-cgcgatctagtggccacaactgcagttgatcgcg-3’;
发夹探针3(seqidno:16):
5’-cgcgatccttggaagtagatattgagcgatcgcg-3’;
搭桥引物(seqidno:3):
5’-acttagctatttcgtgctgatg-3’;
检测探针(seqidno:10):
5’-fam-catcagcacgaaatagctaagt-3’;
(4)rna原位检测
将3对环状探针、发夹探针组合物同时加入进行检测,按每个环状探针10μl、每个发夹探针1μl、rnaseout1μl加入66μl杂交液的比例,配制所需溶液,滴加到玻片样本上全部覆盖样本表面,37℃孵育1h,杂交液洗三次。接下来按照实施例4的rna原位检测方法进行后续步骤,在细胞涂片上原位检测小鼠scnn1bmrna的表达。实验组加入反应所需全部试剂,对照组不加入环状探针,其余操作步骤同实验组。
结果如图6a和图6b所示,实验组中的细胞核周围可见绿色荧光斑点,而对照组中则未见。本实施例还证明了不同物种的细胞,人源细胞、鼠源细胞,都可以采用该方法进行mrna的原位检测。
实施例6小鼠细胞涂片核酸原位检测
本实施例采用5’折叠序列与3’结合序列并不互补结合的发夹探针,进行小鼠scnn1bmrna的原位检测。
(1)3t3小鼠成纤维细胞培养
按照实施例5方法进行细胞培养。
(2)细胞涂片制备
按照实施例5方法进行细胞涂片制备。
(3)环状探针的制备
按照实施例2的方法制备环状探针,并使用外切酶iii进行消化,序列如下;
环状探针1(seqidno:11):
5’-p-aatagctaagtcgcgatcatgcgatcaggggcatagcccatcagcacga-3’;
环状探针2(seqidno:12):
5’-p-aatagctaagtcgcgatcacggatcatgtggtcttggacatcagcacga-3’;
环状探针3(seqidno:13):
5’-p-aatagctaagtcgcgatcttgacaatacccttcctgctcatcagcacga-3’;
发夹探针1(seqidno:17):
5’-ttccaaacaggcaagctaggattgatcgcg-3’;
发夹探针2(seqidno:18):
5’-aagtagtggccacaactgcagttgatcgcg-3’;
发夹探针3(seqidno:19):
5’-actcttggaagtagatattgagcgatcgcg-3’;
搭桥引物(seqidno:3):
5’-acttagctatttcgtgctgatg-3’;
检测探针(seqidno:10):
5’-fam-catcagcacgaaatagctaagt-3’;
(4)rna原位检测
按照实施例4的rna原位检测方法,依次加入环状引物、发夹引物,使用3对探针组合物,在细胞涂片上原位检测小鼠scnn1bmrna的表达。对照组不加环状探针,其余操作步骤同实验组。
结果如图7a和图7b所示,采用5’折叠序列与3’结合序列并不互补结合的发夹探针,也同样能够得到与实施例5相似的结果,在实验组中能检测到荧光信号,而对照组无荧光信号。
实施例7小鼠组织冰冻切片核酸原位检测
(1)环状探针的制备
在小鼠气管冰冻切片上进行smoothmuscleactin(sma)和collagentypeialpha1(col1α1)基因的mrna检测;
按照实施例2的方法分别制备col1α1和sma的环状探针,并使用外切酶iii进行消化,序列如下:
sma:
环状探针1(seqidno:20):
5’-p-aatagctaagtcgcgatctgggacgtcccacgatggatcatcagcacga-3’;
环状探针2(seqidno:21):
5’-p-aatagctaagtcgcgatctcggccagccaagtccagaccatcagcacga-3’;
环状探针3(seqidno:22):
5’-p-aatagctaagtcgcgatctgatgtcaatatcacacttccatcagcacga-3’;
发夹探针1(seqidno:23):
5’-cgcgatcaaccattactccctgatgtcgatcgcg-3’;
发夹探针2(seqidno:24):
5’-cgcgatcatgaggtagtcggtgagatcgatcgcg-3’;
发夹探针3(seqidno:25):
5’-cgcgatcgttagcatagagatccttccgatcgcg-3’;
搭桥引物(seqidno:3):
5’-acttagctatttcgtgctgatg-3’;
检测探针(seqidno:10):
5’-fam-catcagcacgaaatagctaagt-3’;
col1α1:
环状探针1(seqidno:26):
5’-p-cgtcctgacgatcggctgaggtccaggaggtccacgtcagacatct-3’;
环状探针2(seqidno:27):
5’-p-cgtcctgacgatcggctggaagaccagctgcaccactcagacatct-3’;
环状探针3(seqidno:28):
5’-p-cgtcctgacgatcggcttgtcaccacgggggccttgtcagacatct-3’;
发夹探针1(seqidno:29):
5’-gatcggccaggcaatccacgagcacccgccgatc-3’
发夹探针2(seqidno:30):
5’-gatcggccctctgtcacccttaggaccgccgatc-3’;
发夹探针3(seqidno:31):
5’-gatcggccttgttcgcctgtctcacccgccgatc-3’;
搭桥引物(seqidno:32):
5’-gtcaggacgagatgtctga-3’;
检测探针(seqidno:33):
5’-cy5-tcagacatctcgtcctgac-3’;
(2)小鼠气管冰冻切片处理
冰冻切片按常规方法进行制备,组织采用4%pfa固定,组织冰冻切片包埋剂进行包埋,在冰冻切片机中进行切片,-80℃保存。
冰冻切片从冰箱取出后,室温风干20min,浸入100%乙醇脱水5min,室温10min风干,再依次放入75%乙醇、50%乙醇和pbs中各3min;
(3)rna原位检测
按照实施例5的rna原位检测方法,同时加入6对探针组合物,在冰冻切片上原位检测col1α1和smamrna的表达。
结果如图8所示,小鼠气管冰冻切片染色可见绿色和红色荧光,在小鼠平滑肌细胞中可见大量sma绿色荧光,在纤维细胞和平滑肌细胞中可见col1α1红色荧光。荧光位置与基因表达的空间分布相符合,也证明了该方法良好的特异性。
综上所述,本发明采用环状探针和发夹探针组成的探针组合物与原位核酸互补结合,反应过程中不需要进行连接反应,节省了操作时间,探针结构简单,当发夹探针采用3’结合序列与5’折叠序列相互结合设计时,发夹探针在没有靶核酸的情况下保持茎环结构,不与环状探针互补结合,不会引发扩增反应,使检测反应具有较高的特异性,实现了快速、特异、准确、低成本的核酸原位检测。
申请人声明,本发明通过上述实施例来说明本发明的详细方法,但本发明并不局限于上述详细方法,即不意味着本发明必须依赖上述详细方法才能实施。所属技术领域的技术人员应该明了,对本发明的任何改进,对本发明产品各原料的等效替换及辅助成分的添加、具体方式的选择等,均落在本发明的保护范围和公开范围之内。
sequencelisting
<110>深圳百纳心致生命科学有限公司
<120>一种探针组合物及其在核酸原位检测中的应用
<130>20200519
<160>33
<170>patentinversion3.3
<210>1
<211>49
<212>dna
<213>人工序列
<400>1
aatagctaagtcgcgatcttgattttggagggatctcgcatcagcacga49
<210>2
<211>34
<212>dna
<213>人工序列
<400>2
cgcgatccagcgccagcatcgccccacgatcgcg34
<210>3
<211>22
<212>dna
<213>人工序列
<400>3
acttagctatttcgtgctgatg22
<210>4
<211>50
<212>dna
<213>人工序列
<400>4
aggagcgagatccctccaaaatcaagtggggcgatgctggcgctgagtac50
<210>5
<211>50
<212>dna
<213>人工序列
<400>5
gtcacgagagtcgagctgaagcgaatacggcaagtggtccaggtcagtcc50
<210>6
<211>51
<212>dna
<213>人工序列
<400>6
aatagctaagtccctaacccttgattttggagggatctcgcatcagcacga51
<210>7
<211>38
<212>dna
<213>人工序列
<400>7
gggttagggcagcgccagcatcgccccacgggttaggg38
<210>8
<211>49
<212>dna
<213>人工序列
<400>8
aatagctaagtcgcgatcttcccgttcagctcagggatcatcagcacga49
<210>9
<211>34
<212>dna
<213>人工序列
<400>9
cgcgatcggaaggccatgccagtgagcgatcgcg34
<210>10
<211>22
<212>dna
<213>人工序列
<400>10
catcagcacgaaatagctaagt22
<210>11
<211>49
<212>dna
<213>人工序列
<400>11
aatagctaagtcgcgatcatgcgatcaggggcatagcccatcagcacga49
<210>12
<211>49
<212>dna
<213>人工序列
<400>12
aatagctaagtcgcgatcacggatcatgtggtcttggacatcagcacga49
<210>13
<211>49
<212>dna
<213>人工序列
<400>13
aatagctaagtcgcgatcttgacaatacccttcctgctcatcagcacga49
<210>14
<211>34
<212>dna
<213>人工序列
<400>14
cgcgatccaaacaggcaagctaggattgatcgcg34
<210>15
<211>34
<212>dna
<213>人工序列
<400>15
cgcgatctagtggccacaactgcagttgatcgcg34
<210>16
<211>34
<212>dna
<213>人工序列
<400>16
cgcgatccttggaagtagatattgagcgatcgcg34
<210>17
<211>30
<212>dna
<213>人工序列
<400>17
ttccaaacaggcaagctaggattgatcgcg30
<210>18
<211>30
<212>dna
<213>人工序列
<400>18
aagtagtggccacaactgcagttgatcgcg30
<210>19
<211>30
<212>dna
<213>人工序列
<400>19
actcttggaagtagatattgagcgatcgcg30
<210>20
<211>49
<212>dna
<213>人工序列
<400>20
aatagctaagtcgcgatctgggacgtcccacgatggatcatcagcacga49
<210>21
<211>49
<212>dna
<213>人工序列
<400>21
aatagctaagtcgcgatctcggccagccaagtccagaccatcagcacga49
<210>22
<211>49
<212>dna
<213>人工序列
<400>22
aatagctaagtcgcgatctgatgtcaatatcacacttccatcagcacga49
<210>23
<211>34
<212>dna
<213>人工序列
<400>23
cgcgatcaaccattactccctgatgtcgatcgcg34
<210>24
<211>34
<212>dna
<213>人工序列
<400>24
cgcgatcatgaggtagtcggtgagatcgatcgcg34
<210>25
<211>34
<212>dna
<213>人工序列
<400>25
cgcgatcgttagcatagagatccttccgatcgcg34
<210>26
<211>46
<212>dna
<213>人工序列
<400>26
cgtcctgacgatcggctgaggtccaggaggtccacgtcagacatct46
<210>27
<211>46
<212>dna
<213>人工序列
<400>27
cgtcctgacgatcggctggaagaccagctgcaccactcagacatct46
<210>28
<211>46
<212>dna
<213>人工序列
<400>28
cgtcctgacgatcggcttgtcaccacgggggccttgtcagacatct46
<210>29
<211>34
<212>dna
<213>人工序列
<400>29
gatcggccaggcaatccacgagcacccgccgatc34
<210>30
<211>34
<212>dna
<213>人工序列
<400>30
gatcggccctctgtcacccttaggaccgccgatc34
<210>31
<211>34
<212>dna
<213>人工序列
<400>31
gatcggccttgttcgcctgtctcacccgccgatc34
<210>32
<211>19
<212>dna
<213>人工序列
<400>32
gtcaggacgagatgtctga19
<210>33
<211>19
<212>dna
<213>人工序列
<400>33
tcagacatctcgtcctgac19
- 还没有人留言评论。精彩留言会获得点赞!