检测野生型腺相关病毒的通用引物及其应用的制作方法
1.本发明涉及生物工程技术领域的病毒检测方法,具体涉及一种检测野生型腺相关病毒的通用引物、检测方法及其应用。
背景技术:
2.腺相关病毒(adeno-associatedvirus,aav)属于微小病毒科依赖病毒属b19家族,无包膜,含线性单链的脱氧核糖核酸—约4.7kbp,含rep和cap两个开放阅读框,两端分别有末端重复序列(itr)。aav颗粒呈二十面体,直经约20nm,分子量约为5.5-6.2
×
106da。目前没有直接证据表明aav与人类疾病相关。aav在宿主中的复制需要宿主细胞或其他病毒的协助才能完成,如腺病毒和疱疹病毒,因此被称为腺相关病毒。aav是作为腺病毒的污染成分被发现的,fda在《人体细胞和基因治疗指导原则》中对腺病毒生产的aav污染残留的质量控制有明确规定。目前已发现的不同血清型、突变型aav种类达上百种。过去,国内外在质量控制中主要采用pcr扩增常见腺相关病毒1-8血清型的保守序列来进行质量控制。如高凯等(高凯,毕华,丁有学等.重组复制型溶瘤腺病毒p53的质量控制方法.药学学报,2011,46(12):1476-1482),使用引物组合aav-f1/r1对重组复制型溶瘤腺病毒p53中的aav残留进行检测;李永红等(李永红,饶春明,赵阳等.重组腺病毒人内皮抑素的质量标准研究.中国肿瘤生物治疗杂志,2005,12(2):138-142)使用引物组合pan1/2对重组腺病毒人内皮抑素中的aav残留进行检测。下载ncbi数据库中的aav1-aav12的序列进行比对与分析,推测,aav-f1/r1对aav3、5、11、12的扩增效率较低,pan1/2对aav3的扩增效率较低。
3.目前,尚未发现可快速高效、定量的检测12种血清型的野生型aav(aav1-12)的方法。
技术实现要素:
4.本发明旨在至少在一定程度上解决相关技术中的技术问题之一。为此,本发明的一个目的在于提供一种可用于检测12种血清型的野生型腺相关病毒的通用引物对/组合,利用该引物组合,可实现12种血清型的野生型腺相关病毒的qpcr检测。相比传统的野生型腺相关病毒pcr检测方法,利用该引物组合的qpcr检测方法可有效提高检测灵敏度和准确性,更快捷、可定量。
5.为此,本发明第一方面提供一种检测野生型腺相关病毒的通用引物对/组合。根据本发明的实施例,所述通用引物对/组合包括第一引物和第二引物,所述第一引物的序列为5
’-
tggtgggaggagggvaagatgac-3’,其中简并碱基v为c、g或a;所述第二引物的序列为5
’-
crcacatgttkgtrttgg-3’,其中简并碱基r为g或a,简并碱基k为g或t。
6.国内外在腺病毒质量控制中主要采用pcr扩增常见腺相关病毒1-8血清型的保守序列来进行质量控制。目前尚未发现可快速高效、定量的检测12种血清型的野生型aav(aav1~12)的方法。而本发明提供的检测野生型腺相关病毒的通用引物,可同时用于检测12种血清型的野生型aav。基于该引物组合开发的sybr green i qpcr检测方法,其灵敏度
可达100个拷贝/反应,比此前传统的pcr检测方法提高至少1个数量级。
7.本发明第二方面提供一种试剂盒。根据本发明的实施例,包含第一方面所述的通用引物对/组合。
8.本发明提供的包含所述第一引物和第二引物的试剂盒,可用于检测12种野生型腺相关病毒。
9.本发明第三方面提供第一方面所述的通用引物对/组合在制备试剂盒中的用途,所述试剂盒用于检测野生型腺相关病毒。根据本发明的实施例,所述野生型腺相关病毒为12种血清型的野生型腺相关病毒,所述12种血清型的野生型腺相关病毒为avv1~12。
10.本发明第四方面提供第一方面所述的通用引物对/组合或第二方面所述的检测试剂盒在检测野生型腺相关病毒中的应用。根据本发明的实施例,所述野生型腺相关病毒为12种血清型的野生型腺相关病毒,所述12种血清型的野生型腺相关病毒为avv1~12。
11.本发明第五方面提供第一方面所述的通用引物对/组合在利用pcr或qpcr检测样品中野生型腺相关病毒的应用。根据本发明的实施例,所述野生型腺相关病毒为12种血清型的野生型腺相关病毒,所述12种血清型的野生型腺相关病毒为avv1~12。
12.在本发明的一些优选的实施例中,利用qpcr检测样品中野生型腺相关病毒,相比传统的野生型腺相关病毒pcr检测方法,能够有效提高检测灵敏度和准确性,可定量且更快捷。
13.荧光定量pcr检测方法相对于pcr凝胶电泳鉴定方法通常具有更高的灵敏度、稳定性且更快捷、可定量。在本发明的一些实施例中,使用sybr green i qpcr方法利用通用引物进行野生型腺相关病毒检测。当然,基于本发明中通用引物也可以采用taqman探针pcr检测方法进行野生型腺相关病毒检测。
14.本发明第六方面提供一种利用第一方面所述的通用引物对/组合的野生型腺相关病毒的qpcr检测方法。根据本发明的实施例,所述方法包括步骤:
15.1)提取待测样品中总dna;
16.2)以总dna为模板,利用所述通用引物进行qpcr扩增;
17.3)根据扩增结果,判定待测样品中是否存在野生型腺相关病毒,并对待测样品中野生型腺相关病毒的含量进行定量,
18.其中,所述野生型腺相关病毒为12种血清型的野生型腺相关病毒,所述12种血清型的野生型腺相关病毒为avv1~12。
19.在本发明的一些实施例中,提取待测样品中总dna可以采用本领域常规的提取dna的方法,或者根据需要选择市售的基因组dna提取试剂盒。
20.在本发明的一些实施例中,还可以具有如下附加的技术特征:
21.在本发明的一些实施例中,进行qpcr扩增时的退火温度为50-60℃。而当退火温度不在此范围内时,如低于50℃,进行qpcr扩增则会产生非特异性扩增,影响后续待测样品中野生型腺相关病毒的含量的定量结果,若高于60℃,则扩增效率将降低。
22.在本发明的一些优选的实施例中,进行qpcr扩增时的退火温度为53-57℃。
23.在本发明的一些进一步优选的实施例中,进行qpcr扩增时的退火温度为54-56℃。
24.在本发明的一些更为优选的实施例中,进行qpcr扩增时的退火温度为55℃。
25.在本发明的一些实施例中,所述qpcr包括sybr green i qpcr和taqman探针法
qpcr中的至少之一。
26.在本发明的一些优选的实施例中,利用第一方面所述的通用引物对/组合,通过sybr green i qpcr检测野生型腺相关病毒。该方法中灵敏度可达100个拷贝/反应,比此前传统的pcr检测方法提高至少1个数量级。
27.在本发明的一些实施例中,所述待测样品为血液、细胞、组织样品或病毒样品。
28.例如,所述待测样品可以是293ft细胞、hek293细胞、ad293细胞、293f细胞、重组腺病毒制品、重组疱疹病毒、重组aav等,通过检测这些样品中野生型腺相关病毒的含量,来评估样品中野生型腺相关病毒的残留,进而对待测样品中野生型腺相关病毒残留进行质量控制。
29.在本发明的一些实施例中,所述野生型腺相关病毒的qpcr检测方法,还包括对dna提取的步骤进行质控,通过添加定量重组aav来监测dna提取步骤相关样品的回收率。
30.定量重组aav颗粒是已知滴度的基因组拷贝的参考品,可以单独设为对照组进行dna提取和qpcr,用以评估某次dna提取试验的整体回收率水平(取若干重复的平均值),校正各样品的qpcr含量测定值;也可以定量添加到各待检样品中,进行dna提取和qpcr,分别计算回收率,再计算差值获得各样品中待检野生型aav含量。
31.本发明基于检测某重组复制型溶瘤腺病毒生产过程中的野生型aav污染需要,在系统比对分析12种血清型aav基因组序列后,设计了一系列引物/引物组合,并从中筛选到最优的可同时用于检测12种血清型aav的引物对组合。相比传统的野生型腺相关病毒pcr检测方法,利用该引物组合的qpcr检测方法可有效提高检测灵敏度和准确性,可定量且更快捷。
32.本发明从10个引物组合中筛选到1个最优的引物组合,可同时用于检测至少12种血清型的野生型aav。基于该引物组合开发的sybr green i qpcr检测方法,其灵敏度可达100个拷贝/反应,比此前传统的pcr检测方法提高至少1个数量级。并且sybr green i qpcr省略了凝胶电泳检测过程,还可通过已知拷贝数(浓度)的参考品标准曲线来计算并待测样品中的aav残留量。
33.本发明的附加方面和优点将在下面的描述中部分给出,部分将从下面的描述中变得明显,或通过本发明的实践了解到。
附图说明
34.本发明的上述和/或附加的方面和优点从结合下面附图对实施例的描述中将变得明显和容易理解,其中:
35.图1为12种血清型的野生型相关病毒aav1~aav12的核酸序列比对结果(部分展示);
36.图2a-2b为分别以引物组合a、b、c、d、e、f、g、h、i、j,在不同的退火温度下,进行pcr获得的电泳结果图;
37.图3为构建成功的phs-bvc-lj018质粒图谱;
38.图4为构建成功的puc57-partial aav3质粒图谱;
39.图5a为对pcr模板进行梯度稀释,分别以引物组合a、b、c、d进行pcr获得的电泳结果图;
40.图5b为对pcr模板进行梯度稀释,分别以引物组合e、f、g、h、i、j进行pcr获得的电泳结果图,ck-表示空白对照;
41.图5c为电泳结果图,其中,泳道2-11为对pcr模板进行梯度稀释,以引物组合pan1/pan2进行pcr获得的电泳结果;泳道12为以293ft细胞基因组(293)、腺病毒基因组(ad)作为模板,pan1/pan2为引物进行pcr获得的电泳结果;泳道13为以293ft细胞基因组(293)、腺病毒基因组(ad)以及含aav2序列的phs-bvc-lj018质粒(p)的混合物作为模板,pan1/pan2为引物进行pcr获得的电泳结果;泳道14为以293ft细胞基因组(293)、腺病毒基因组(ad)作为模板,以引物组合f进行pcr获得的电泳结果;泳道15为以293ft细胞基因组(293)、腺病毒基因组(ad)以及含aav2序列的phs-bvc-lj018质粒(p)的混合物作为模板,以引物组合f进行pcr获得的电泳结果;图5a-5c中,ck+指pcr阳性对照,即以质粒phs-bvc-lj018(含aav2全序列)为模板;ck-为空白对照,即没有加入模板;0-8为10n拷贝数;
42.图6为以含有aav3部分序列的puc57-partial aav3质粒为模板,分别以引物组合pan1/pan2及引物组合f进行pcr,获得的电泳结果图,泳道数字表示模板添加量10n拷贝/反应,ck为空白对照,未加模板;
43.图7为含aav2序列的phs-bvc-lj018质粒进行梯度稀释后作为模板,以引物组合f进行sybr greeni qpcr,获得的标准曲线;
44.图8为含aav2序列的phs-bvc-lj018质粒进行梯度稀释后作为模板,以引物组合f进行sybr greeni qpcr,获得的扩增曲线;
45.图9为含aav2序列的phs-bvc-lj018质粒进行梯度稀释后作为模板,以引物组合f进行sybr greeni qpcr,获得的熔解曲线;
46.图10为以待测样本为模板,以引物组合f进行sybr greeni qpcr,获得的熔解曲线。
具体实施方式
47.下面详细描述本发明的实施例。下面描述的实施例是示例性的,仅用于解释本发明,而不能理解为对本发明的限制。实施例中未注明具体技术或条件的,按照本领域内的文献所描述的技术或条件或者按照产品说明书进行。所用试剂或仪器未注明生产厂商者,均为可以通过市购获得的常规产品。
48.实施例1引物设计以及引物组合筛选过程
49.1.引物设计
50.本实施例中的12种血清型的野生型腺相关病毒aav1-aav12的基因序列可由ncbi基因组数据库下载,网址https://www.ncbi.nlm.nih.gov/,其中avv1序列号nc_002077,avv2序列号nc_001401,avv3序列号nc_001729,avv4序列号u89790,avv5序列号nc_006152,avv6序列号af028704,avv7序列号nc_006260,avv8序列号nc_006261,avv9序列号lq870208,avv10序列号ay631965,avv11序列号ay631966,avv12序列号dq813647。
51.本实施例中的序列比对软件为dnaman v7(使用多序列比对模块中的full alignment下的默认参数)。序列比对结果表明所选择的12种血清型的野生型腺相关病毒的同源性为79.74%。
52.在本实施例中,根据序列比对结果,优选了6个位于rep和cap阅读框内同源性较高
的区域,设计了8条引物(ld-aav-001/002/003/004/005/006/007/008),并筛选10个引物组合(见表1)。附图1中部分展示了12种血清型的野生型腺相关病毒aav1~aav12的核酸序列比对结果。
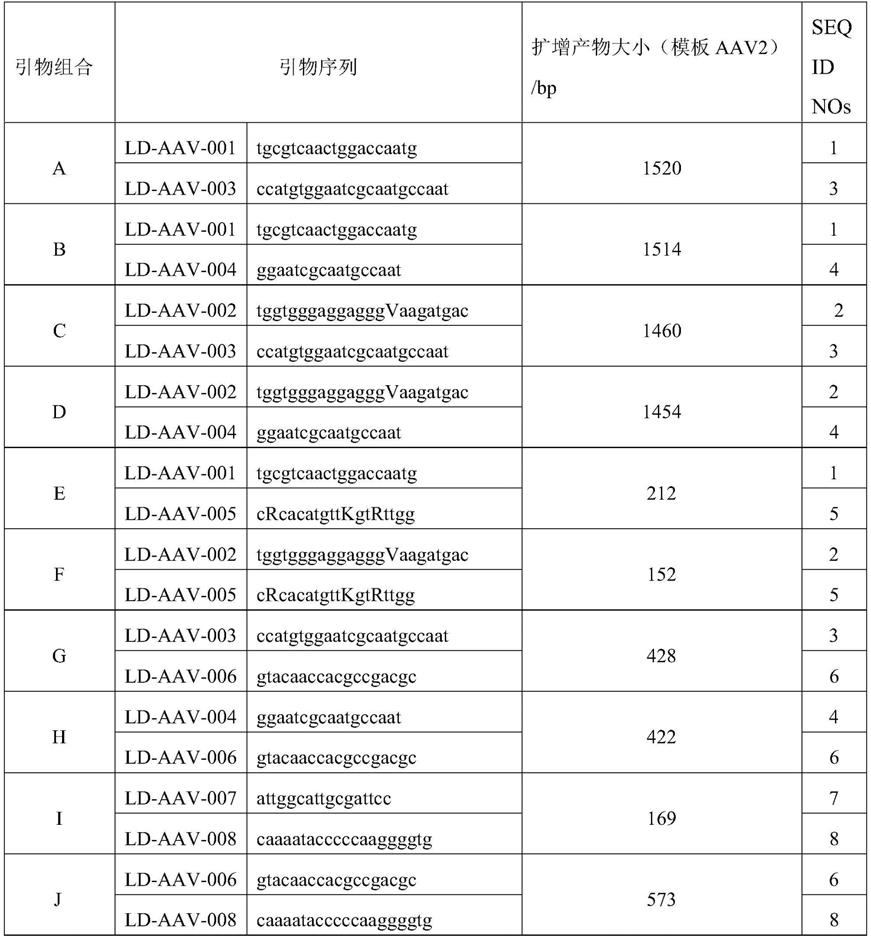
53.表1用于检测aav的10个引物组合
[0054][0055]
2.引物组合退火温度的优化
[0056]
以含aav2序列的phs-bvc-lj018质粒(质粒图谱参见附图3,插入片段为rep基因和cap基因的编码序列,分别如seq id no:9和seq id no:10所示)为pcr模板(1ng/μl),分别以引物组合a、b、c、d、e、f、g、h、i、j为引物,在不同的退火温度下,进行pcr扩增,所用2x taq mix购自北京擎科新业生物技术有限公司。
[0057]
10μl pcr体系如下:
[0058]
f primer:0.5μl
[0059]
r primer:0.5μl
[0060]
模板(1ng/μl):1μl
[0061]
h2o:3μl
[0062]
2x taq mix:5μl
[0063]
pcr扩增程序如下:
[0064]
95℃-5min
[0065]
(95℃-30s,ta-30s,72℃-1min)
×
35
[0066]
72℃-10min
[0067]
15℃-hold
[0068]
pcr产物经1.5%琼脂糖凝胶电泳检测,检测结果如图2a和2b。本实施例中,对琼脂糖凝胶电泳进行拍照时,设置的参数相同。因此,条带的亮度与扩增产物的量呈正相关。结果表明引物组合a和b的非特异性扩增较明显,其他引物组合的较优退火温度介于50-60℃,后续测试优选55℃的退火温度。
[0069]
3.引物的灵敏度以及特异性测定
[0070]
将含aav2序列的phs-bvc-lj018质粒(p)(由通用生物系统(安徽)有限公司合成aav2序列)进行梯度稀释后作为pcr模板测试各引物组合的灵敏度,质粒图谱见图3;同时,将293ft细胞(购自atcc美国模式培养物集存库(american type culture collection))基因组(293)、腺病毒基因组(ad)作为模板,测试各引物组合的特异性。
[0071]
使用天根离心柱型血液/细胞/组织基因组dna提取试剂盒提取293ft细胞基因组。使用磁珠法dna提取试剂盒提取腺病毒基因组。发明人使用申科磁珠法样品dna前处理试剂盒及康为磁珠法dna提取试剂盒提取病毒制品的dna。
[0072]
10μl pcr体系如下:
[0073]
f primer:0.5μl
[0074]
r primer:0.5μl
[0075]
模板(1ng/μl):1μl
[0076]
h2o:3μl
[0077]
2x taq mix:5μl
[0078]
pcr扩增程序如下:
[0079]
95℃-5min
[0080]
(95℃-30s,55℃-30s,72℃-1min)
×
35
[0081]
72℃-10min
[0082]
15℃-hold
[0083]
pcr产物经1.5%琼脂糖凝胶电泳检测,本实施例中,对琼脂糖凝胶电泳进行拍照时,设置的参数相同。因此,条带的亮度与扩增产物的量呈正相关。检测结果如5a-5c所示,图5a显示引物组合a-d引物灵敏度不高,仅接近107拷贝/反应,图5b、5c显示引物组合f的灵敏度最高,且比已报道的引物组合pan1/pan2灵敏度稍高;且引物组合f在293ft细胞基因组及腺病毒基因组中未见扩增产物,说明引物组合f的特异性较高。
[0084]
将含aav3部分序列的puc57-partial aav3质粒(p)(由通用生物系统(安徽)有限公司合成并构建)(质粒图谱参见附图4,插入片段为aav3的部分编码序列,如seq id no:11所示)进行梯度稀释后作为pcr模板测试引物组合f和pan1/pan2的灵敏度(质粒图谱见图4),pcr反应体系同上,图6中泳道数字表示模板添加量10n拷贝/反应,结果显示,引物组合f
比pan1/pan2的灵敏度高近三个数量级。
[0085]
上述结果充分说明,在进行pcr时,引物组合f对含有aav2或aav3的核酸序列的样品的检测灵敏度更高,当样品中含有的aav2或aav3的核酸浓度较低时,引物组合pan1/pan2可能无法检测aav2或aav3的存在,而引物组合f却能够检测到。因此,当需要检测待测样品中是否含有野生型腺相关病毒时,可以采用引物组合f,即便待测样品中野生型腺相关病毒丰度较低,也能够检测出,并且该引物组合特异性较好。
[0086]
实施例2sybr greeni qpcr测试
[0087]
使用含aav2序列的phs-bvc-lj018质粒进行梯度稀释后作为模板,以引物组合f作为qpcr引物,使用擎科2x master qpcr mix-sybr(+udg)或擎科2x t5 fast sybr green i qpcr mix进行sybr greeni qpcr。测试引物组合f的扩增效率、熔解曲线、线性相关性。
[0088]
表2不同浓度标准品(三次重复;添加量1μl/反应)进行qpcr获得的ct值
[0089][0090]
表2结果表明基于引物组合f的qpcr检测方法其灵敏度可达100拷贝/反应,扩增效率90-100%,线性相关性较佳,无非特异性扩增。
[0091]
图9显示质粒标准曲线熔解曲线单峰,基本无非特异性扩增。
[0092]
图10显示待测样品熔解曲线单峰,基本无非特异性扩增。待测样品是含重组腺病毒的293ft细胞总dna,来源于生产重组腺病毒过程中的料液(含293ft细胞)。
[0093]
当检测样品中是否含有野生型腺相关病毒aav1~12时,可首先提取待测样品中总dna,以总dna为模板,利用引物组合f进行qpcr扩增,根据扩增结果,判定待测样品中是否存在野生型腺相关病毒,同时利用图7中所示的标准曲线,可对待测样品中野生型腺相关病毒的含量进行定量。
[0094]
关于待测样品总dna的提取:
[0095]
对于检测含293ft细胞的样品是否污染aav,可使用细胞基因组提取试剂盒。在本发明中,使用了天根离心柱型血液/细胞/组织基因组dna提取试剂盒提取细胞样品的dna。
[0096]
对于检测经纯化的重组腺病毒制品,乃至重组疱疹病毒、重组aav中野生aav的残留时,可以使用磁珠法dna提取试剂盒。在本发明中,使用了申科磁珠法样品dna前处理试剂盒及康为磁珠法dna提取试剂盒提取病毒制品的dna。
[0097]
建议对dna提取步骤进行质控,可通过添加定量重组aav或同质野生型aav参考品
来监测dna提取步骤相关样品的回收率,一方面可规避因dna提取步骤异常(dna提取率低或操作过程失误)造成假阴性检测结果,另一方面可通过计算参考品dna提取回收率来校正定量结果。在本实验中,构建并包装纯化了两个重组aav(非野生型aav,以避免野生型aav污染腺病毒制品的生产)及其qpcr定量用的标准质粒和相应的引物组合(不同于引物组合f)用于dna提取步骤的质控。
[0098]
在本说明书的描述中,参考术语“一个实施例”、“一些实施例”、“示例”、“具体示例”、或“一些示例”等的描述意指结合该实施例或示例描述的具体特征、结构、材料或者特点包含于本发明的至少一个实施例或示例中。在本说明书中,对上述术语的示意性表述不必须针对的是相同的实施例或示例。而且,描述的具体特征、结构、材料或者特点可以在任一个或多个实施例或示例中以合适的方式结合。此外,在不相互矛盾的情况下,本领域的技术人员可以将本说明书中描述的不同实施例或示例以及不同实施例或示例的特征进行结合和组合。
[0099]
尽管上面已经示出和描述了本发明的实施例,可以理解的是,上述实施例是示例性的,不能理解为对本发明的限制,本领域的普通技术人员在本发明的范围内可以对上述实施例进行变化、修改、替换和变型。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1