一种血清二氧化碳检测试剂盒及其制备方法与流程
本发明涉及二氧化碳检测
技术领域:
,具体涉及一种血清二氧化碳检测试剂盒及其制备方法。
背景技术:
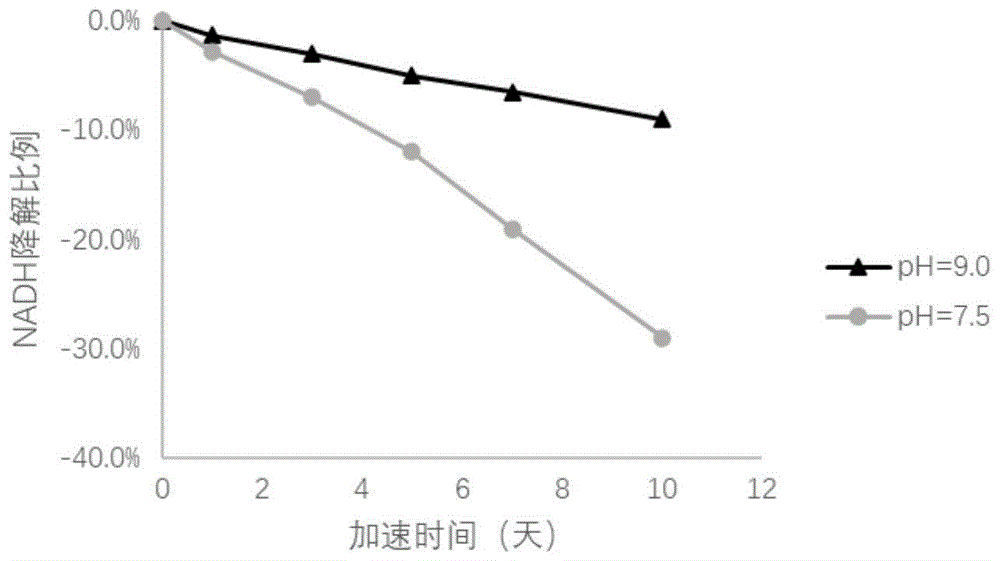
:血清中二氧化碳与hco3-处于平衡状态,它们共同形成了血清的缓冲体系,二氧化碳的总浓度是血清电解质平衡的最佳指标,在临床上,二氧化碳的总浓度用以辅助诊断呼吸系统及代谢的酸碱平衡。血清中co2主要以hco3-形式存在,其变化主要反映代谢性酸碱平衡紊乱。血清中co2增高,常见于幽门梗阻、库欣综合征、服碱性药物过多等。呼吸性酸中毒:如肺心病、呼吸中枢抑制、呼吸机麻痹、肺气肿、支气管扩张和气胸等。血清中co2减低,常见于严重腹泻、肾衰竭、糖尿病酮症、感染性休克、服酸性药物过多等。慢性呼吸性碱中毒:由于长期呼吸增速、肺泡中co2减低,肾小管代偿性hco3-排出增多。临床上根据样品中co2含量,可以初步判断机体酸碱失衡状态。co2酶法测定在临床实验室属常规开展的检验项目,apadh-apad+是生化检测试剂常用的显色系统之一。公开号为cn105928937a的专利申请公开一种测定二氧化碳的试剂盒及其制备方法,该专利申请中公开nadh被氧化成nad+,通过测定相应波长吸光度,可计算出样本中碳酸氢根的含量。而nadh在ph>9的溶液中比较稳定,但部分试剂ph值呈现弱碱性,如二氧化碳试剂ph为7.5。此时nadh降解速度比较快,引起试剂质量下降。技术实现要素:本发明所要解决的技术问题在于现有技术二氧化碳测定试剂盒中的nadh在ph7.5的条件下发生降解,引起试剂质量下降,同时试剂盒稳定性较差。本发明通过以下技术手段实现解决上述技术问题的:本发明提供一种血清二氧化碳检测试剂盒,包括试剂r,所述试剂r包括以下浓度的原料:50-150mmol/ltris缓冲盐、0.4-1.0g/l乙二胺四乙酸二钠盐(edta)、1.0-3.0g/l乙酸镁、1.0-3.0g/l草氨酸钠、10-20g/l葡萄糖、0.3-1.7g/l磷酸烯醇式丙酮酸、0.2-2.2g/l还原型3-乙酰吡啶腺嘌呤二核苷酸(apadh)、1.2-3.8ku/l苹果酸脱氢酶、0.5-2.5ku/l磷酸烯醇式丙酮酸羧化酶、1.0-2.0ku/l葡萄糖脱氢酶,溶剂为纯化水。反应原理:在碳酸氢根存在的前提下,磷酸烯醇式丙酮酸由磷酸烯醇式丙酮酸羧化酶催化生成草酰乙酸和磷酸,在还原型3-乙酰吡啶腺嘌呤二核苷酸存在的前提下,草酰乙酸经由苹果酸脱氢酶的催化作用生成苹果酸,同时还原型3-乙酰吡啶腺嘌呤二核苷酸(apadh)脱氢生成氧化型3-乙酰吡啶腺嘌呤二核苷酸(apad+),apad+与葡萄糖在葡萄糖脱氢酶作用下生成apadh,apadh在405nm有特征性吸收峰,而apad+在405nm无特征性吸收峰,根据405nm吸光度的变化,可以测定二氧化碳的活性或浓度。有益效果:试剂r中加入葡萄糖脱氢酶和葡萄糖,可以形成一个apadh再生体系,将氧化后的apad+通过酶促反应还原,使试剂中的apadh维持在一定浓度范围内,解决了在ph7.5条件下apadh降解,引起试剂质量下降的问题,同时确保在不显著增加成本的情况下解决apadh不稳定的问题,从而提高试剂盒的稳定性。试剂r中草氨酸钠作为部分抑制葡萄糖脱氢酶的存在,使得再生体系缓慢的生成apadh。优选地,所述试剂r的ph为7.50±0.05。有益效果:试剂r的ph为7.50±0.05范围内,由于ph>9.0的情况下,试剂盒稳定性好,而不选ph>9.0的原因是,在ph>9.0的情况下,试剂盒中的葡萄糖脱氢酶、苹果酸脱氢酶等会失去活性。而选择ph为7.50±0.05范围内是因为试剂盒中大部分酶的最适ph值都在这个范围内,同时由于循环再生体系的存在,使得apadh处于一个相对稳定的水平。优选地,所述tris缓冲液的ph值为6-9。有益效果:葡萄糖脱氢酶最适ph下限6,apadh在偏碱性ph>9稳定性比较好,因此tris缓冲液的ph值设置在6-9的范围内。优选地,所述试剂r具体包括以下浓度的原料:100mmol/ltris缓冲盐、0.7g/l乙二胺四乙酸二钠盐(edta)、2.0g/l乙酸镁、2.0g/l草氨酸钠、15g/l葡萄糖、1.0g/l磷酸烯醇式丙酮酸、1.2g/lapadh、2.5ku/l苹果酸脱氢酶、1.5ku/l磷酸烯醇式丙酮酸羧化酶、1.5ku/l葡萄糖脱氢酶,溶剂为纯化水。优选地,所述试剂r具体包括以下浓度的原料:150mmol/ltris缓冲盐、1.0g/l乙二胺四乙酸二钠盐(edta)、2.0g/l乙酸镁、3.0g/l草氨酸钠、20g/l葡萄糖、1.0g/l磷酸烯醇式丙酮酸、1.2g/lapadh、2.5ku/l苹果酸脱氢酶、1.5ku/l磷酸烯醇式丙酮酸羧化酶、2.0ku/l葡萄糖脱氢酶,溶剂为纯化水。优选地,所述试剂r具体包括以下浓度的原料:50mmol/ltris缓冲盐、0.7g/l乙二胺四乙酸二钠盐(edta)、1.0g/l乙酸镁、1.0g/l草氨酸钠、10g/l葡萄糖、1.0g/l磷酸烯醇式丙酮酸、1.2g/lapadh、2.5ku/l苹果酸脱氢酶、1.5ku/l磷酸烯醇式丙酮酸羧化酶、1.0ku/l葡萄糖脱氢酶,溶剂为纯化水。优选地,所述试剂r的制备方法包括以下步骤:按浓度将各原料混合,即制得试剂r。优选地,所述试剂r的制备方法包括以下步骤:将tris缓冲盐溶于纯化水中,然后加入乙二胺四乙酸二钠盐、乙酸镁、草氨酸钠、葡萄糖,搅拌后,再加入磷酸烯醇式丙酮酸和apadh,调节溶液ph值至7.50±0.05范围内,最后加入磷酸烯醇式丙酮酸羧化酶,苹果酸脱氢酶,葡萄糖脱氢酶,混合后,即制得试剂r。本发明还提供一种血清二氧化碳检测试剂盒的制备方法,所述试剂盒包括试剂r,所述试剂r的制备方法包括以下步骤:按浓度将各原料混合,即制得试剂r。有益效果:本发明中的试剂盒制备方法简单,底物、工具酶价格便宜,试剂成本无显著增加。优选地,所述试剂r的制备方法包括以下步骤:将tris缓冲盐溶于纯化水中,然后加入乙二胺四乙酸二钠盐、乙酸镁、草氨酸钠、葡萄糖,搅拌后,再加入磷酸烯醇式丙酮酸和apadh,调节溶液ph值至7.50±0.05范围内,最后加入磷酸烯醇式丙酮酸羧化酶,苹果酸脱氢酶,葡萄糖脱氢酶,混合后,即制得试剂r。本发明的优点在于:试剂r中加入葡萄糖脱氢酶和葡萄糖,可以形成一个apadh再生体系,将氧化后的apad+通过酶促反应还原,使试剂中的apadh维持在一定浓度范围内,解决了在ph7.5条件下apadh降解,引起试剂质量下降的问题,同时确保在不显著增加成本的情况下解决apadh不稳定的问题,从而提高试剂盒的稳定性。本发明试剂盒中底物、工具酶稳定,开瓶12天后性能无显著下降。底物、工具酶价格便宜,试剂成本无显著增加。试剂r中乙酸镁主要作为参与反应过程酶的激活剂,edta主要作用是螯合掉试剂中的杂质-重金属离子等,草氨酸钠作为部分抑制葡萄糖脱氢酶的作用,使得葡萄糖在葡萄糖脱氢酶作用下,源源不断的生成apadh,因为葡萄糖脱氢酶的正常酶活力较高,会一次性生成大量的apadh,而不是缓慢的源源不断的生成,因此需要加入草氨酸钠这一成分,使葡萄糖脱氢酶的酶活力下降,生成apadh的速度缓慢进行。附图说明图1为本发明中ph值对溶液中apadh稳定性的影响结果图;图2为本发明试剂盒反应原理图;图3为本发明对比例1、实施例1-实施例3中apadh稳定性的变化趋势图;图4为本发明实施例3中试剂盒的校准曲线;图5为本发明实施例3中试剂盒的线性范围相关性图。具体实施方式为使本发明实施例的目的、技术方案和优点更加清楚,下面将结合本发明实施例,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有作出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。下述实施例中所用的试验材料和试剂等,如无特殊说明,均可从商业途径获得。实施例中未注明具体技术或条件者,均可以按照本领域内的文献所描述的技术或条件或者按照产品说明书进行。实施例1血清二氧化碳检测试剂盒及其制备方法试剂r:其溶剂为纯化水,最终,采用饱和trisbuffer及1mhcl将溶液ph值调整在7.50±0.05范围内。试剂r的制备方法包括以下步骤:将上述配比的tris缓冲盐溶于纯化水中,然后加入上述配比的乙二胺四乙酸二钠盐、乙酸镁、草氨酸钠、葡萄糖,搅拌后,再加入磷酸烯醇式丙酮酸和apadh,调节溶液ph值至7.50±0.05范围内,最后加入磷酸烯醇式丙酮酸羧化酶,苹果酸脱氢酶,葡萄糖脱氢酶,混合后,即制得试剂r,本实施例中试剂盒的反应原理如图2所示。实施例2血清二氧化碳检测试剂盒及其制备方法试剂r:其溶剂为纯化水,最终,采用饱和trisbuffer及1mhcl将溶液ph值调整在7.50±0.05范围内。试剂r的制备方法包括以下步骤:将上述配比的tris缓冲盐溶于纯化水中,然后加入上述配比的乙二胺四乙酸二钠盐、乙酸镁、草氨酸钠、葡萄糖,搅拌后,再加入磷酸烯醇式丙酮酸和apadh,调节溶液ph值至7.50±0.05范围内,最后加入磷酸烯醇式丙酮酸羧化酶,苹果酸脱氢酶,葡萄糖脱氢酶,混合后,即制得试剂r,本实施例中试剂盒的反应原理如图2所示。实施例3血清二氧化碳检测试剂盒及其制备方法其溶剂为纯化水,最终,采用饱和trisbuffer及1mhcl将溶液ph值调整在7.50±0.05范围内。试剂r的制备方法包括以下步骤:将上述配比的tris缓冲盐溶于纯化水中,然后加入上述配比的乙二胺四乙酸二钠盐、乙酸镁、草氨酸钠、葡萄糖,搅拌后,再加入磷酸烯醇式丙酮酸和apadh,调节溶液ph值至7.50±0.05范围内,最后加入磷酸烯醇式丙酮酸羧化酶,苹果酸脱氢酶,葡萄糖脱氢酶,混合后,即制得试剂r,本实施例中试剂盒的反应原理如图2所示。对比例1试剂r:其溶剂为纯化水。最终,采用饱和trisbuffer及1mhcl将溶液ph值调整在7.50±0.05范围内。对比例2对apadh在不同ph值下的稳定性进行测定测定结果:如表1和图1所示,测试结果出现较大偏差,表1为对apadh在不同ph值下的测定结果,图1为ph值对溶液中apadh稳定性的影响,图1中位于上方的曲线表示ph=9.5条件下apadh降解比例,图1中位于下方的曲线表示ph=7.5条件下apadh降解比例。表1apadh在不同ph值下的测定结果apadh不稳定主要是在弱碱性ph下易被氧化为apad+,为了使试剂中的apadh维持在一定浓度范围内,需要将氧化后的apad+通过酶促反应还原。有许多工具酶和相应的底物可以完成这一反应,如乙醇在乙醇脱氢酶的作用下和+生成,但是乙醇不稳定,易挥发,但是很难保证具有良好的稳定性。对对比例1、实施例1-实施例3中的试剂r的稳定性进行测定。(一)测定方法包括以下步骤:操作参数如表2所示。加速稳定性测定方法:由于实时稳定性难以在短时间内完成,为考察试剂的稳定性,通过测试试剂在37℃保存时的稳定性来推测试剂的有效期。通常认为试剂37℃条件下加速一天,代表实时稳定性1.5月。具体操作方法如下:将待检试剂避光密封置37℃恒温箱进行加速实验,自开始之日起每隔2~3天开启密封试剂进行空白吸光度、样本偏差测试。测试过程中,以冷藏试剂当天的样本测定均值为基准值,当加速试剂的样本测定偏差无法满足要求时停止实验。开瓶稳定性测定方法:试剂在使用过程中往往不会使用完后加盖,很多情况下都是开瓶后一直使用到试剂耗尽,因此,试剂的开瓶稳定性是一个非常重要的性能指标。试剂的开瓶稳定性评估方法如下:将待检试剂避光密封置生化分析仪中进行开瓶实验,开瓶实验开展过程中待检试剂始终处于不加瓶盖状态。然后自开始之日起每隔2~3天对开瓶试剂的空白吸光度、样本偏差进行测试,测试过程中均以第一次样本测试结果作为基准。开瓶测试过程中若出现样本偏差超过要求的情况,即停止实验。表2为本发明试剂盒的操作参数表(二)测定结果:测定结果如表1和图3所示,表3为试剂盒开瓶稳定性测定结果,图3为对比例1、实施例1-实施例3中apadh稳定性的变化趋势。表3为试剂盒开瓶稳定性测定结果表从表3可以看出,实施例3中试剂盒的开瓶稳定性最佳,在20天后,试剂盒检测偏差在-4.59%,而对比例1中没有再生体系,在20天后,测定的偏差已经达到了-42.93%,说明了其稳定性差,实施例1-实施例3中试剂盒的稳定性均高于对比例1,表明再生体系的加入,能够提高试剂盒的稳定性。从图2可以明显看出,加入再生体系后,apadh降解比例明显降低。实施例4对公开号为cn105928937a的专利申请中公开的试剂盒的开瓶稳定性和加速稳定性进行测定,测定方法与实施例3中相同。测定结果如表4和表5所示。表4为现有二氧化碳试剂盒与本发明试剂盒加速稳定性对比结果表表5为现有二氧化碳试剂盒与本发明试剂盒开瓶稳定性对比结果表质控n代表正常值,p代表异常值,从表4和表5可以看出,本发明试剂盒的加速稳定性和开瓶稳定性均有所提高,现有技术中的试剂盒在第3天加速稳定性相对偏差已达到-10%以上,而本发明的试剂盒在第3天加速稳定性相对偏差不到-5%。现有技术中的试剂盒在开瓶13天时,测定结果相对偏差已达到10%以上,而本发明中的试剂盒在开瓶第30天,测定结果相对偏差仍不到10%。对实施例3中的二氧化碳检测试剂盒的性能进行测定,采用实施例4中的操作参数进行测定。(1)定标:使用校准品进行定标,定标方法为两点定标。(2)线性范围检测:采用高值样本,通过倍比稀释的方式,稀释成至少5个不同梯度浓度(xi),每个稀释浓度样品测定2次,分别求出测试结果的均值(yi)。以稀释浓度(xi)为自变量,以测定结果均值(yi)为因变量求出线性回归方程,同时计算绝对偏差或相对偏差。(3)重复性测定:对同一待测样本进行多次反复测定,对所得结果进行sd和cv的计算。(4)检测限测定:以生理盐水为样本,重复测定20次,计算20次结果的平均值和标准偏差s空白,则:lld=x空白+3s空白上式表示当检测样品响应值在x空白+3s空白以上时,有99.7%的可能性属于样品中含有被检测物。(四)测定结果(1)空白和校准品的反应度如表6所示,校准曲线如图4所示,表6为两点定标,空白(0.0)和校准品(30.0)吸光度od值,定标两水平校准品的反应度。表6为空白和校准品的吸光度表浓度0.0(mmol/l)30.0(mmol/l)od值11.751.63od值21.771.60均值1.761.615(2)线性范围如表7和图5所示,表7中的10a:0b表示不包含样品。本实施例中的试剂盒稳定性有明显改善,并符合产品的技术要求指标。表7为线性范围测定结果表(3)表8为对质控n和质控p的重复测定结果,其中质控n=13.5mmol/l质控p=35.8mmol/l,可以看出,本发明试剂盒的精密度较好。表8为重复性测定结果表重复次数质控n(mmol/l)质控p(mmol/l)113.8035.18212.6735.42314.0935.58413.1035.44514.1435.28613.6634.88713.8235.25814.2236.38913.2135.171013.1235.481113.6835.191213.0234.651313.8535.131412.8335.321512.8935.161613.2334.811713.5634.651812.8834.651912.8134.902012.8735.42平均值mean13.3735.20标准偏差sd0.500.40变异系数cv3.75%1.14%(4)表9为检测限测定结果,从表9可以看出,本发明中的试剂盒符合产品行业标准,标准要求≤5%。重复次数水(mmol/l)10.0120.0130.0140.0450.0360.0370.058-0.0190.07100.04110.05120.04130.07140.05150.09160.04170.04180.06190.07200.08平均值mean0.04标准偏差sd0.03lld0.12(5)对实施例3中的物料成本进行核算,核算成本如表10所示。表10为实施例3中试剂盒的物料成本cn105928937a专利申请中公开的试剂盒的物料成本(元)实际物料成本(元)下降比例1.000.8713%从表10可以看出,本发明中的试剂盒不仅能够提高稳定性,同时还能降低物料成本。以上实施例仅用以说明本发明的技术方案,而非对其限制;尽管参照前述实施例对本发明进行了详细的说明,本领域的普通技术人员应当理解:其依然可以对前述各实施例所记载的技术方案进行修改,或者对其中部分技术特征进行等同替换;而这些修改或者替换,并不使相应技术方案的本质脱离本发明各实施例技术方案的精神和范围。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1