一种细胞过滤器的制作方法
本发明涉及医疗机械技术领域,具体涉及一种细胞过滤器。
背景技术:
在基于细胞形态大小(iset)的肿瘤细胞俘获技术上,通过真空系统产生的过高负压容易导致肿瘤细胞的破坏和死亡。目前,iest的检测需要对血液进行预处理,运用甲醛来固定细胞,使细胞失去活力,不能用于下一阶段的基因学研究。本发明不需要优先处理血液,尽可能保护细胞,同时俘获的细胞是活的肿瘤细胞。
ctc是指来源于肿瘤组织而在血液中循环的肿瘤细胞。ctc是化疗作用的靶点,也是肿瘤转移和复发的元凶。现研究证实肿瘤在原位癌的阶段就向患者的血中释放ctc,不过大都被机体的免疫系统所清除。直到肿瘤的大小达到一定的阶段时,患者的血中就可以检测出ctc,但此时影像学尚不能发现肿瘤。因此,对高危人群血中ctc的监测,有机会发现早期肿瘤。但此时,血中ctc的数目少,需要一种高灵敏度的检测装置。ctc的基因学检测可以实时提供患者包括基因突变在内的肿瘤负载信息,也可以用作fish染色体重组检测,ngs基因测序,pcr基因表达水平检测和细胞培养等,为肿瘤患者的精准治疗提供解决方案。
ctc的俘获和富集基于原理,共分为物理方法和化学方法。物理方法基于ctc的形态大小和密度。化学方法则基于ctc细胞表面的上皮细胞特定的标记物,利用磁珠包裹的相对应的抗体和抗原特异性的反应来达到分离ctc的目的。根据原理又分为阳性和阴性两种方法。化学方法由于步骤较多,对ctc的破坏较大,容易引起细胞的凋亡。ctc的俘获率和纯度较低,
目前,国内的基因检测公司多集中于肿瘤的靶向药物治疗,涉及肿瘤的早期诊断或筛查的比较少。最主要的原因是肿瘤的早期ctc在血中的含量非常的少,缺乏高灵敏度的检测方法。从肿瘤不可以检测到能够在影像学上被检测出大约需要5~10年的时间。当肿瘤的体积达到0.5cm时,它才能够被影像学检测出。这时候,对应的肿瘤细胞数目大约是109,即10亿个。其实肿瘤在生长过程中,不停的向外周血中释放肿瘤细胞。当然,在肿瘤的早期,大部分的肿瘤细胞被机体的免疫系统所清除或屏蔽。但仍然有部分的肿瘤细胞可以在血中被检测出。如果血液中能够检测到ctc,但影像学检查还未发现到肿瘤;这种情况,需要连续几次的检测才能发现早期肿瘤。
现有的检测系统根据肿瘤细胞与血细胞的细胞尺寸(iset)及细胞变形能力的差异,应用滤膜过滤来进行富集。膜上有近20万个大、小一致的圆孔,圆孔以一定规格排列的,整齐有序。膜放在一个6毫升的圆柱状过滤器的底部。一次性的把血液样本全部加入过滤器中。此时,由于血液全部覆盖在膜上,膜上所有的孔均被堵住,所以需要非常大的负压。据报道超过400kpa~600kpa(0.4~0.6mpa)(工业级别的真空泵)的负压才能让血液中的细胞通过过滤膜。为了防止过高的负压吸附导致膜完全变形,孔径扭曲堵塞,在膜的下面加了一层金属的网丝作为膜的撑垫。
综上,现有的相关技术存在以下技术缺点:
1)、过高的负压过滤:iset方法中血液样本一次性的全部加入到过滤器中,膜上的孔径全部被堵住了。这样腔内的负压梯度被消除了,使腔内压降为零。所以需要很大的外部压力(400~600pka),才能把血液过滤出去。在如此大的压力下,膜的孔径变形,部分肿瘤细胞通过变形的孔而被过滤掉,导致肿瘤细胞的俘获效率较低;同时拌有细胞结构的改变,会导致部分肿瘤细胞的死亡。
2)、没有活的肿瘤细胞:为了降低过高的负压对血细胞的破坏,维持细胞正常的结构,血液必须要预处理。一般都采用不同浓度的甲醛,来固定细胞。这样,没有活的肿瘤细胞用于下一步的基因学检测。
3)、以聚碳酸刻蚀膜的iset技术膜孔的大小和排列均不一致,容易致使白细胞在膜上的积聚,污染膜,导致低的ctc俘获率和俘获纯度。
4)、自动化程度较低:血液过滤器人工清洗,不能有效的应对大规模的样本检测。
技术实现要素:
本发明提出的一种细胞过滤器,可解决如何在低的压力条件下,尽可能的俘获血液中活的肿瘤细胞。
为实现上述目的,本发明采用了以下技术方案:
一种细胞过滤器,包括壳体,还包括分别置于壳体内的血液吸取装置、血液过滤装置和血液回收装置,所述血液回收装置包括废液瓶与真空泵,真空泵与废液瓶连通;
所述血液吸取装置通过管道与血液过滤装置的入口密封连通,所述血液过滤装置的出口通过管道与血液回收装置的废液瓶密封连通;
其中,
所述血液吸取装置内设置血液吸取针头;
所述血液过滤装置从下往下依次对应设置上密封腔、可移动支撑平板和下密封腔,下密封腔固定在升降系统上;
上密封腔包括上腔体和固定在上腔体底部的上密封圈,上密封腔的顶部密封连接血液流入针头;
可移动支撑平板放置在上密封腔和下密封腔之间,通过启动升降系统上下移动可使下密封腔和可移动支撑平板依次与上密封腔分离和闭合;
可移动支撑平板的中心设置过滤孔,过滤孔上设置过滤膜;
下密封腔包括下腔体和固定在下腔体顶部的下密封圈,下密封腔内密封连通血液回收管道入口;
血液通过血液吸取装置的血液吸取针头到血液过滤装置的血液流入针头,再滴入到过滤膜后流出,经血液回收管道出口流入到废液瓶;
所述血液吸取针头的口径小于血液流入针头的口径。
进一步的,所述血液吸取针头是通过针头附着装置固定在上、下钢性夹板之间,上、下钢性夹板固定在壳体上。
进一步的,所述针头附着装置是一个两头大小不一,中空的塑料结构;血液吸取针头贯穿针头附着装置内;
针头附着装置的上半部设置弹簧,通过弹簧把针头固定在两块钢板之间。
进一步的,所述针头附着装置的下半部还设置出气管。
进一步的,所述上腔体、下腔体及可移动支撑平板都相应的设置凹槽,用于嵌入密封圈,保持密封效果。
进一步的,所述升降系统包括升降台和步进电机;
升降台的上表面上固定有下密封腔;
通过步进电机的转动推动升降台的上升,使上密封腔、可移动支撑平板和下密封腔完整结合,形成一个密封的腔。
进一步的,所述壳体内分别对应设置六组血液吸取装置和血液过滤装置,一个血液吸取装置对应一个血液过滤装置,六个血液过滤装置的回收管道通过一个分配阀,归结到一个出口管道而进入废液瓶。
进一步的,所述血液吸取针头的和血液流入针头的口径大小d的范围为g15≤d≤g23。
进一步的,所述过滤膜上设置多个槽孔,所述槽孔排列整齐,大小均一。
进一步的,所述可移动支撑平板的外侧面设置手柄。
由上述技术方案可知,本发明的细胞过滤器,为一个低压(可在-0.5~-5.0kpa)的过滤装置,产生一个低压俘获系统,尽量在不损伤/破坏肿瘤细胞的前提下,俘获肿瘤细胞。
具体的说,本发明的细胞过滤器,存在以下优点:
1、本发明为低压血液过滤系统,通过分别在输入端设置血液吸取针头,输出端设置血液流入针头,并且血液吸取针头的口径小于血液流入针头,使可采用极低的负压对血液进行过滤,低压对细胞的破坏作用较小。
2、本发明不用预先处理血液,可直接进行过滤检测,保证了细胞的活力,分离的活细胞可以培养,用于后续的基因检测;
3、本发明采用新型膜孔结构,孔的大小和排列形式一致,避免白细胞对膜孔的污染。膜可以采用芯片的形式,增加膜孔/单位面积上孔的密度,最大限度的俘获肿瘤细胞,俘获肿瘤细胞的效率和纯度都高。
4、本发明检测可实现自动化,即血液的吸取、转运、过滤和管道的清洗均全自动化,适合大规模的样本检测。
附图说明
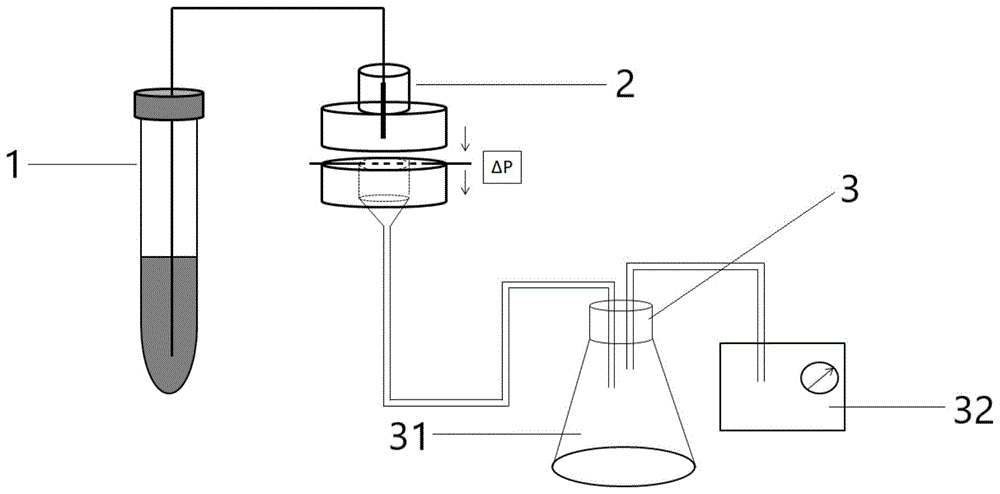
图1是本发明的结构示意图;
图2是本发明的血液吸取装置结构示意图;
图3是本发明的血液过滤装置结构示意图;
图4是本发明的可移动支撑平板结构示意图;
图5是本发明的过滤膜结构示意图;
图6是本发明的升降系统结构示意图;
图7是本发明实施例真空泵的输出压力图表;
图8是本发明实施例血液导管入口端压力与真空泵的输出压力压力差的曲线图;
图9是本发明实施例的血液回收装置的结构示意图;
图10是本发明实施例血液流入管道入口端压力的检测实验图;
图11是本发明实施例密封腔内压力下降的动态观察曲线图;
图12是本发明的工作流程示意图;
图13是本发明实施例的电缆布局图;
图14是本发明实施例的电气安装板布局图;
图15是本发明实施例的主电源电路图;
图16是本发明实施例的n线和pe线分配图;
图17是本发明实施例的开关电源电路示意图;
图18是本发明实施例的24v电源分配图;
图19是本发明实施例的plc模块电路图;
图20是本发明实施例扩展模块电路图;
图21是本发明实施例中间继电器电路图;
图22是本发明实施例触摸屏及接近开关电路图;
图23是本发明实施例开关阀电路图;
图24是本发明实施步进电机驱动电路图;
图25是本发明实施例的步进电机电路图;
图26是本发明实施例真空泵控制电路图;
图27是本发明实施例的肺癌上皮细胞a549(局部)实验结果。
具体实施方式
为使本发明实施例的目的、技术方案和优点更加清楚,下面将结合本发明实施例中的附图,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例是本发明一部分实施例,而不是全部的实施例。
目前,iest的检测需要对血液进行预处理,运用甲醛来固定细胞,使细胞失去活力,不能用于下一阶段的基因学研究。本发明不需要优先处理血液,尽可能保护细胞,同时俘获的细胞是活的肿瘤细胞。
如图1所示,本实施例所述的细胞过滤器,包括分别置于壳体内的血液吸取装置1、血液过滤装置2和血液回收装置3,所述血液吸取装置1通过管道与血液过滤装置2的入口连通,所述血液过滤装置2的出口通过管道与血液回收装置3连通;所述血液回收装置3包括废液瓶31与真空泵32,真空泵32与废液瓶31连通;
其中,如图2所示,血液吸取装置用于血液的吸取,具体包括:血液样本试管本体13,血液样本试管本体13的管口密封,血液样本试管本体13内设置血液吸取针头14,血液吸取针头14连通血液样本试管本体13内外,血液吸取针头14固定在针头附着装置17上,针头附着装置17固定在试管本体13的管口处,针头附着装置17的上半部套设弹簧16;
具体的说,针头附着装置17如下,血液吸取针头14是通过特殊的附着装置17固定在上、下钢性夹板之间的。针头附着装置17是一个两头大小不一,中空的塑料结构,便于针头从中插入。它的上半部通过弹簧16的作用,把针头14固定在上下夹板11即两块钢板之间,上下夹板11通过螺丝12固定在壳体上;针头附着装置17的下半部除针头14穿过外,尚有一开口即连通出气管15,其作用是维持血液样本管子内、外压力的一致。只有这样,在负压的作用下,血液才能被针头吸取而转运。
血液经负压作用从血液吸取针头14的出口经管道流入到血液过滤装置2,血液过滤装置2的入口设置血液流入针头21,即血液经血液流入针头21流入到血液过滤装置2内,血液吸取针头14和血液流入针头21两种针头的口径是大小不一的,具体的是所述血液吸取针头14的口径小于血液流入针头21的口径;这样的设计保证流出端的血液是一滴一滴的流到膜上,并且会快速的通过膜而被过滤掉。
关于血液的运输:血液在负压的作用下被吸取到入口端针头14上部的塑料管子,经由塑料管子被转用到血液过滤装置2,管道直径的大小影响血液吸取的速率。
如图3所示,本发明实施例的血液过滤装置2包括上下对应的上密封腔213和下密封腔214,上密封腔213和下密封腔214之间放置可移动支撑平板25;
上密封腔213底部设置密封圈23,上密封圈23固定在上密封圈固定在上腔体22上,上密封腔213的顶部设置血液流入针头21;
可移动支撑平板25的中心设置过滤孔27,过滤孔27上设置过滤膜26;
下密封腔214的顶部设置下密封圈29,下密封圈29固定在下密封圈固定附着装置28上,下密封腔214内设置血液回收管道210,血液经过滤膜26流出,流入血液回收管道的入口211,再从血液回收管道的出口212流出;
所述过滤膜26上设置多个槽孔,所述槽孔排列整齐,大小均一;所述槽孔为矩形槽孔,所述矩形槽孔的长度和宽度分别为20-100μm和4-10μm。
总体来说,血液过滤装置2的密封腔由三个部分组成的。分别由上、下密封腔和中间的平板构成。没有平板时,仅形成一个密封腔;当有平板插入时,就会形成上、下两个腔。密封腔的压力与真空泵相关。通过压力计可以测量出上、下腔的压力,下腔直接与真空泵相通,所以下腔的压力就代表了真空泵的输出压力。而上腔是插入的平板与上密封圈构成的腔室,平板中间有孔。在无膜的情况下,上、下腔的压力是相等的。而在血液过滤过程中,膜的孔径瞬间被堵塞或者部分的孔径被长时间的堵塞,导致过滤膜26可以实际通透的面积减小。这样会引起上腔的压力较下腔低。
血液从吸取装置1流出后经管道到流入针头21与上密封腔相连接,这样血液管道入口端的压力可以用来反映密封圈上腔的压力。由于管道阻力的存在,导致血液管道入口端的压力比上腔的压力低。这种压力差对血液的过滤是有益的。既减缓了血液样本的吸取速度,同时又避免了血液在膜上的积聚。由此可见,在血液过滤过程中,上、下腔内的压力是动态变化的。
具体的说,本发明实例的血液过滤装置2的具备以下特点:
低压:由于密封性能非常的好,非常低的压力条件下就能够把液体从血液管中吸取,压力甚至可低于-0.5kpa,过滤过程中对肿瘤细胞的破坏作用较小。
所述上腔体22、下腔体28及可移动支撑平板25都相应的设置凹槽,用于嵌入密封圈,保持密封效果。密封圈被设置在凹槽内,这样不但确保密封,而且不影响液体对密封胶的破坏作用。
本实施例的密封圈采用橡胶,密封效果较好;因为检测时上下密封圈都要与平板的紧密接触,所以材料的选择非常重要。
具体的说,如图4所示,所述支撑平板25中心设置过滤孔27,所述支撑平板25的外部侧面设置手柄251,方便拿取;具体的说,支撑平板25是一圆形扁平结构,并带有柄。其结构为平板的中心有一圆型的中心孔;该孔是血液过滤产物的通道,血液中主要的红细胞,白细胞及其它非肿瘤细胞通过此孔而流走。同时,中心孔也是血液过滤系统负压的形成和维持通道。作用:平板是膜的载体,通过平板把膜放入血液过滤系统,用于肿瘤细胞的俘获。特点:非常方便的通过插入或拿出方式就实现了对血液样本的循环检测。
如图5所示,本实施例的过滤膜26是一种既耐酸、耐碱、耐腐蚀同时又具有一定的硬度的材料。在膜的中间有高密度的槽孔,排列整齐,大小均一。具体槽孔可以为矩形槽孔,所述矩形槽孔的长度和宽度分别为20-100μm和4-10μm。膜孔完全覆盖在平板中间孔的上方。在低压条件下,血液通过一定的速度通过膜而被过滤,血中的肿瘤细胞由于体积比较大而留在膜的表面。血液过滤结束后,拿出平板,把膜从平板上取下,用于肿瘤细胞的染色鉴定。而平板则经过简单的清洗后用于下一阶段的样本检测。相对比聚碳酸刻蚀膜的膜孔大小不一和排列杂乱无章,本发明的膜芯片上的膜孔大小一致,排列整齐。
图5上p1/p2:表示密封性能/膜的过滤或通透性能的;v1/v2:表示膜的通透/过滤性能的,膜的通透性主要由膜孔的大小和孔的密度和膜的厚度/膜两侧的压力差决定的。膜孔的面积与液滴大小的关系:尽量控制液滴体积的大小,使之滴到膜上的面积小于膜孔的面积;液滴的大小控制主要由出口针头的大小,管道直径的大小来决定的,本发吗实施例的管道直径范围在1~10mm,不会在膜上有任何的积聚。
同时,上腔体22它上面有凹槽,上密封圈23固定在凹槽中。通过其上部的螺纹和外在的螺母,它被固定在上层铝板上,上腔体22在检测中是固定不动的,它与升降台系统4共同推动了上、下密封腔的结合和密封腔的形成。
下腔体28,它上面也有凹槽,下密封圈29固定在凹槽中,下腔体28固定在升降台的上表面平板上。
如图6所示,升降台系统4的构成:该系统由升降台和步进电机组成。升降台的上表面平板上固定有下腔体28,通过由步进电机的转动推动升降台的上升,使下腔体与上腔体完整结合,形成一个密封的腔。步进电机通过脉冲电信号刺激步进电机转动。步进电机与升降台相连接,推动升降台的上升和下降,产生密封圈的开、合。
具体的说,如图6所示,下密封腔214固定在升降台系统4的升降台41的上表面上,图6上标记200是血液回收管道,电机43通过电机轴42驱动升降支架44进而带动升降台41做上下运动,进而实现下密封腔214做上下往复运动。
本发明实施例血液过滤低压系统的评估:
血液导管入口端的压力检测:以直径为2.0mm的血液管道为例子,测试在不同口径的血液流出针头的条件下,血液导管入口端的压力与真空泵的输出压力/密封圈下腔的压力关系。血液导管入口端的压力是决定血液样本的吸取速率的。它反映的是上密封腔的压力和血液吸取管道的阻力。
结果如图7和图8所示,取负压的绝对值来作图,便于观察;在相同的真空泵输出压力条件下,血液流出端针头直径越大,血液导管入口端的压力就越大。入口端压力大就意味着更快速的血液吸取。对直径大的针头而言也就意味着相对低的真空泵的输出压力就能够把血液从末端吸取。
关于膜上、下表面的压力差说明如下:
通过真空泵的连续负压作用吸取血管内的血液;当膜上面的膜孔没有被堵塞时,膜上、下面的压力差δp≈0;真空泵的压力作用于血管的针头端开始抽取血液;
当血液开始滴到膜的上表面,血液中细胞可能堵塞了膜的孔(无论是瞬间的还是长期的堵塞);这种堵塞一方面使上腔内的负压变大(绝对值变小)导致针头端对血液的抽取能力降低,使血液流速变慢,这种变慢有助于肿瘤细胞在膜上被俘获;另一方面膜下腔的负压维持不变(等于真空泵的负压),这个相对增强的负压(相对于膜上腔)驱使膜上的血液通过膜,使膜上的血液不至于积聚在膜上,造成膜孔的完全堵塞。
一旦膜孔全部被堵塞,膜上腔的压力为0,也就没有负压的存在,不能把血管中的血液再抽取。
而本发明实施例的过滤膜保证了即使有细胞在膜孔,也不会完全堵塞膜孔,这就保证了膜上、下压力差处于一个合理的范围,使得血液不断的被抽取,通过膜而被过滤,肿瘤细胞被留在膜上。这个设计是低的负压的原理。
可见,血液导管入口端与真空泵的输出压力差随着真空泵输出压力的增加而增加,这种增加反映了针头直径对压力改变的影响是非常大的。可见选择一个合适的血液流出端针头的重要性。
综上所述,本实施例血液的吸取是通过血液入口端针头来实现的。血液的吸取主要取决于负压压力的大小、针头的口径。负压是由过滤单位末端的真空泵所产生并调控的。负压越大,血液吸取的速度就越大。当血液吸取速度大于血液从膜上过滤的速度,会造成血液在膜上面的积聚,而影响后续血液的过滤和肿瘤细胞的俘获。
低压的负压,是本发明实施例的最突出的特点,现有的比如武汉某公司的产品一开始就把血液全部放在膜上,一旦开始工作,血液中的细胞就全部占住了膜孔,堵塞膜孔;血液和膜是在一个密封的管子内的,管子内的压力为0,就不存在一个压力差;为了克服膜孔被堵塞,唯一能够做的就是增大负压的值,靠强大的负压把细胞从膜上吸附通过膜;他们的压力大到400~600kpa,相当于本实施例的300倍,而高的压力在过滤过程中会造成肿瘤细胞的变形和破坏,所以他们需要预先处理血液—利用甲醛固定细胞,维持细胞的形态。这样做的坏处是得到是没有活性的肿瘤细胞;会产生和维持高的负压需要工业级别的真空泵,体积大,成本高;而本实施例的低压系统不需要预先处理血液,所需要的压力较低,不会破坏细胞。整套设备体积较小,方便。
最后,如图9所示,血液回收系统3是通过真空泵产生的负压来实现的。血液回收系统3包括废液瓶31,血液经血液过滤装置2过滤后经血液回收管道入口210流入到废液瓶31,废液瓶31与真空泵33连通。过滤后的血液通过管道进入废液瓶31中,本发明实施例设置6个血液过滤单元,每个血液过滤单元的回收管道通过一个分配阀,归结到一个出口管道而进入废液瓶。定期检查废液瓶内废液的量以防废液被吸入到真空泵。
同时,如图10实验结果所示,血液流入管道入口端压力的检测,可见血液流入管道入口端的压力决定了血液的吸取速度和量。该压力受真空泵的负压、血液流入管道的直径和血液流出端针头直径三个因素的影响。本实验在血液流入管道直径为2.0mm的前提下,观察了真空泵压力和血液流出端针头直径的改变对血液流入管道入口端压力的影响。
如图11所示,为了观察血液在过滤过程中,密封腔内压力的变化,一个多通道的压力监测仪连接到密封腔的上下端。本实施例采用6毫升的血液用来检测,随着血液的流入,膜孔逐渐的被堵塞,密封腔内的压力逐渐增大(负值向零靠近)。腔内存在压力的下降。当膜孔完全堵塞时,腔内压力降为0,管子内的血液将不能被抽取。用pbs清洗后,膜孔逐渐被冲开,腔内负压又重新出现,压力的下降变低。
本发明实施例有6个血液过滤单位,每个单位是独立的;还可以并联更多的过滤单位,一次检测会有更多的样本被检测。整个过程分为三个部分:血液的吸取、血液的过滤和血液的回收,如图12所示。
本发明实施例对应的装置,具体采用自动控制,相关控制电路如图13-图26所示,在使用时,本发明按照说明书上的指示,启动机器。在显示屏上选择“检测”程序,输入待测血液样本的数目。把膜放在平板上并插入倒“t”型的孔中,把装有血液样本的管子插入针头装置上。按启动检测键,仪器开始工作。血液从针头的末端被吸取,在负压的作用下通过血液导管转运到血液过滤单位。血液通过平板上的过滤膜时,异常的细胞就被留在膜上。当血液吸取结束后,检测程序进入到清洗过程,自动的对针头、血液转运管道、血液过滤单位及血液回收管道进行清洗。清洗的目的是为了对下一批次的血液样本进行检测,这样过程的循环往复,直到所有的血液样本被检测结束。
以下是应用本实施例的具体实验:
实验一:肿瘤细胞的截留率(spiked-in)检测
1.取2.4x106/ml肺癌上皮细胞a549200ul,加入2mmcalcein-am100ul,室温下染色15分钟。离心200g5分钟,倒掉上清液,用pbs冲洗细胞两次,以去除多余的染料。然后,将细胞重新悬浮在含有2mmedta和0.5%bsa的pbs中。
2.通过连续稀释的统计取样,将细胞稀释至10-100个细胞/50μl的理想浓度。随后,使用微量移液管将50μl稀释细胞悬浮液转移至96孔微量滴定板中,在显微镜下计数移植悬浮液中的细胞数。重复计数三次,以确定悬浮液中细胞的实际数量。重复这些操作后,调整用于加入1ml全血中细胞悬浮的体积,以制备肿瘤细胞加标样本。
3.一定量的肿瘤细胞加入到1ml健康人的全血中,混溶。血液上机检测;本实验中的膜孔的大小为6x40um,膜孔的总面积为6x6mm,真空泵的压力为2.0±0.1kpa,流速为500ul/min。
4.膜上活的肿瘤细胞的计数。由于calcein-am只与活细胞的细胞核结合,在荧光显微镜蓝光的激发下发出绿光,而被观察和计数。
实验结果:
如图27所示,在10x物镜下,观察并计数显微镜视野下绿色荧光细胞的数目即可得出所俘获肿瘤细胞的数目。肿瘤细胞a549的俘获率为92±3%。
实验二:肿瘤病人外周血中ctc的俘获
1.11个患有各种恶性肿瘤的病人,用edta的抗凝管抽取病人的外周血3毫升,用pbs按1:1稀释成6毫升。
2.稀释的血液上机,进行过滤,膜的孔径为6x40um,真空泵的压力为2.0±0.1kpa,流速为500ul/min。
3.血液过滤结束后取出膜,用瑞姬氏染色法(wright’sstaining)对膜进行染色并对循环肿瘤细胞(ctc)进行鉴定和计数。
4.ctc的判定标准:a.细胞外形异常,大小不均一;b.细胞核直径大于24um;c.细胞核异形;d.高核质比(细胞核/细胞质)e.细胞核膜增厚且不规则,呈立体感。(满足以上4条者即判定为恶性肿瘤细胞);
实验结果如下:
综上所述,本发明是基于肿瘤细胞的体积较正常血液细胞大的原理,在血液过滤时,因无法通过膜上芯片的孔径而被滞留在膜的表面,从而被俘获。这种俘获是①低压力条件下的,对肿瘤细胞的破坏非常的小,血液流动过程中的切变力对细胞的损伤也非常的小;尽可能的保护好肿瘤细胞;②血液无需预先处理:目前国内采用iset的方法均需要对血液进行预先处理,主要是用1%左右的甲醛溶液处理血液细胞,固定细胞膜和细胞结构。这样俘获的细胞是死细胞,不能进行细胞培养等后续的一系列检测。③提供活的肿瘤细胞。④全自动化,高效的俘获肿瘤细胞,适合大规模的样本检测。
相对而言,本发明实施例具备以下优点:
1、低压力下检测:
目前,iset面临的主要问题是如何在低的压力条件下,尽可能的俘获血液中活的肿瘤细胞。国内现行的技术是通过加大的负压把细胞从膜上俘获。高的负压需要工业量级的真空泵。工业量级的真空泵一方面增加资本的投入,同时产生大的噪音和大的体积,使整套设备体积变得非常的大。高负压下产生的血流切变力的改变也会破坏血细胞和肿瘤细胞。如何在非常低的压力条件下,把肿瘤细胞俘获是个关键性问题。低的压力(-1.0~-5.0kpa)一方面保护细胞另一方面使整个装置小型化。
2、血液不需要预处理;步骤少,对肿瘤细胞的破坏少。
3、实用方便:低压力的实现是通过本实施例独特的过滤单位来实现,既方便又实用。整套系统通过由升降台推动的上、下密封腔的快速开合和平板/膜的插入和拿出等步骤来快速实现的。非常适合大规模的样本检测。
4、低成本:仅膜是消耗品;
5、检测过程包括过滤和清洗均全自动化精准控制。
总而言之,本发明实施例在过滤结果方面的优点如下:
a)、高的俘获效率;
b)、活的肿瘤细胞;
c)、细胞可以用于后续的基因学检测;
d)、大规模的样本检测:极短的样本处理过程和快速的检测过程。
以上实施例仅用以说明本发明的技术方案,而非对其限制;尽管参照前述实施例对本发明进行了详细的说明,本领域的普通技术人员应当理解:其依然可以对前述各实施例所记载的技术方案进行修改,或者对其中部分技术特征进行等同替换;而这些修改或者替换,并不使相应技术方案的本质脱离本发明各实施例技术方案的精神和范围。
- 还没有人留言评论。精彩留言会获得点赞!