一种氨基脲类似物化合物、制备方法及应用与流程
1.本发明涉及医药生产技术领域,具体涉及一种氨基脲类似物化合物、制备方法及应用。
背景技术:
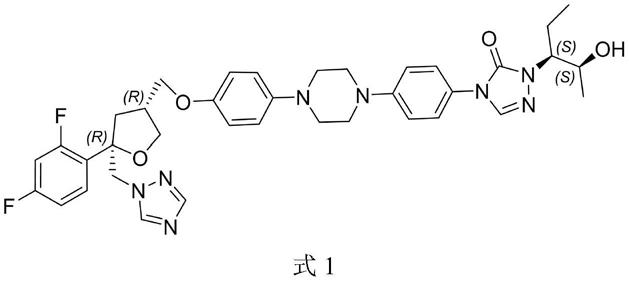
2.泊沙康唑,英文名:posaconazole。化学名为4-[4-[4-[4-[[(3r,5r)-5-(2,4-二氟苯基)-5-(1,2,4-三唑-1-基甲基)氧杂戊环-3-基]甲氧基]苯基]哌嗪-1-基]苯基]-2-[(2s,3s)-2-羟基戊-3-基]-1,2,4-三唑-3-酮,结构如下式1。
[0003][0004]
泊沙康唑由德国先灵葆雅公司(现在的默克公司)研制开发,并首先于2005年10月在爱尔兰获批上市。2006年9月,美国fda批准了泊沙康唑口服混悬液(规格:40mg/ml);2013年11月至2014年3月美国fda先后批准了泊沙康唑缓释片(规格:100mg/片)和注射液(规格:0.3g/16.7ml)。目前已在全球70多个国家、地区获批,并在美国、欧盟等40多个国家、地区上市。是第二代广谱三唑类抗真菌药物,用于预防侵袭性真菌感染,适用于13岁和13岁以上因重度免疫缺陷而导致侵袭性曲霉菌和念珠菌感染风险增加的患者,包括造血干细胞移植(hsct)后发生移植物抗宿主病(gvhd)的患者或化疗导致长时间中性粒细胞减少症的血液系统恶性肿瘤患者的侵袭性真菌感染的预防治疗。由于其高效低毒的特点,且临床应用范围广,为临床侵袭性真菌感染的治疗提供了选择空间。
[0005]
泊沙康唑作为上市人药,其药品质量需受到严格控制。处于人体给药安全考虑,任何一种药品有效成分(api)在商业化之前需要由国家和国际相关管理局建立药理毒理学上杂质鉴定的极低下限。由于杂质一般不具有治疗作用,但对人体机能会有一定的伤害作用,因此杂质在药品或有效成分(api)必须得到有效控制。我们知道杂质从来源方面分为一般杂质和特殊杂质,泊沙康唑有效成分(api)中的杂质很大可能来源于自身的合成和降解过程。主要包括未反应完原料;原料中原存在的杂质及其衍生物、合成副产物和降解产物等、主反应多位点反应合成的杂质等。
[0006]
药品中的杂质可能给人体带来不良反应,造成严重后果。因此需要清楚杂质的化学结构及其药理毒理性质成为了必须且必要之事。这就要求需要制备纯度较高的杂质对照品。一般在api化学合成中,成分复杂、副产物及降解产物等影响使得目标杂质的分离、纯化等变得极其困难。因此,高效且简易制备高纯度杂质对照品能够找到一条可行路径显得非
常重要。
技术实现要素:
[0007]
本发明旨在提供一种氨基脲类似物化合物、制备方法及应用,具体涉及一种高效、简易的制备泊沙康唑杂质对照品的方法,建立一个可靠、稳定的杂质合成工艺。该工艺合成路线短,仅一步就能得到目标杂质氨基脲类似物(化合物3),且不存在安全性问题,分离和纯化手段简单易行,经济可靠。合成路线具体如下:
[0008]
为了实现上述目的,本发明具体采用如下技术方案
[0009]
一种氨基脲类似物化合物,所述化合物结构为:
[0010][0011]
前述化合物的制备方法为,化合物1和化合物2,在催化剂及有机弱碱的存在下,反应合成目标化合物,也即化合物3:
[0012][0013]
所述的催化剂为dmap。其中,化合物1是一种丁二酸肼盐类似物。
[0014]
优选的,所述有机弱碱选自三乙胺、二乙胺、咪唑、吡啶或苯胺。
[0015]
优选的,所述制备方法的具体步骤如下:
[0016]
(1)将化合物1和化合物2溶于有机溶剂中,加入催化剂及有机弱碱搅拌溶清;
[0017]
(2)将步骤(1)溶液于25℃~95℃下继续搅拌反应;
[0018]
(3)反应毕,将步骤(2)所得反应液滴入水中,加入有机溶剂萃取;
[0019]
(4)将步骤(3)的有机相减压浓缩得有色油状物;
[0020]
(5)将步骤(4)所得油状物进行柱层析纯化得目标化合物。
[0021]
优选的,步骤(1)所述有机溶剂选自dmf、dmac、dmso、甲苯或nmp。
[0022]
优选的,步骤(2)反应温度为50~80℃。
[0023]
优选的,步骤(3)中的萃取用有机溶剂选自乙酸乙酯、二氯甲烷或甲基叔丁醚。
[0024]
优选的,步骤(5)所述柱层析洗脱剂选自石油醚:乙酸乙酯=1:1或1:2;或正己烷:乙酸乙酯=1:1或1:2;或二氯甲烷:甲醇=20:1。
[0025]
优选的,所述的催化剂用量与化合物1的摩尔比为0.1~5:1;所述的化合物2与化合物1的摩尔比为1.1~2.5;所述的有机弱碱与化合物1的摩尔比为1~8:1。
[0026]
优选的,所述的催化剂用量与化合物1的摩尔比为0.5~2:1;所述的化合物2与化合物1的摩尔比为1.2~2.0;所述的有机弱碱与化合物1的摩尔比为1.5~3.5:1。
[0027]
前述所述化合物在制备泊沙康唑中间体杂质对照品或制备泊沙康唑杂质对照品中的应用。
[0028]
有益效果:
[0029]
本发明制备方法高效、简易、可靠、稳定;
[0030]
该工艺合成路线短,仅一步就能得到目标杂质氨基脲类似物(化合物3);
[0031]
本发明工艺不存在安全性问题,分离和纯化手段简单易行,经济可靠;
[0032]
本发明制备所得产品纯度更高。
附图说明
[0033]
图1为实施例7合成杂质(化合物3)的核磁1h-nmr谱图。
[0034]
图2为实施例7合成杂质(化合物3)的ms谱图。
[0035]
图3为实施例9合成杂质(化合物3)的核磁1h-nmr谱图。
[0036]
图4为实施例9合成杂质(化合物3)的ms谱图。
[0037]
图5为实施例9合成杂质(化合物3)的hplc谱图。
[0038]
图6为实施例10合成杂质(化合物3)的核磁1h-nmr谱图。
[0039]
图7为实施例10合成杂质(化合物3)的ms谱图。
[0040]
图8泊沙康唑合成工艺得到的中间体化合物5产品hplc图
[0041]
图9中间体化合物5和加标后的hplc图
具体实施方式
[0042]
下面将结合本发明实施例中的附图,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。以下对至少一个示例性实施例的描述实际上仅仅是说明性的,决不作为对本发明及其应用或使用的任何限制。基于本发明中的实施例,本领域普通技术人员在没有作出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
[0043]
需要注意的是,这里所使用的术语仅是为了描述具体实施方式,而非意图限制根据本技术的示例性实施方式。如在这里所使用的,除非上下文另外明确指出,否则单数形式也意图包括复数形式,此外,还应当理解的是,当在本说明书中使用术语“包含”和/或“包括”时,其指明存在特征、步骤、操作、器件、组件和/或它们的组合。
[0044]
除非另外具体说明,否则在这些实施例中阐述的部件和步骤的相对布置、数字表达式和数值不限制本发明的范围。对于相关领域普通技术人员已知的技术、方法和设备可能不作详细讨论,但在适当情况下,所述技术、方法和设备应当被视为授权说明书的一部分。
[0045]
下面结合实例对本发明进行详细说明,以方便本领域技术人员理解本发明,另外以下实例杂质合成体系均与泊沙康唑合成工艺中该杂质产生的体系一致。
[0046]
文献(structural characterization ofimpurities and degradation products 164-177)报道过泊沙康唑中部分杂质,但该杂质(化合物3)未见报道过。本发明
中该杂质(化合物3)是在泊沙康唑合成工艺其中一个中间体(化合物5)合成体系中发现的,该中间体的合成路线如下:
[0047][0048]
从路线中看出化合物4(草酸肼盐类似物)与化合物2在催化剂下合成了泊沙康唑中间体(化合物5),该中间体成品的hplc图如图8所示。
[0049]
谱图中rt=14.208min(rrt=1.0)是化合物5,rt=15.883min(rrt=1.12)是未知杂质,发现其含量选超我们限度(标准≤0.10%);针对于该未知杂质,我们猜测应该是反应中产生而不是后续处理引入的,而体系中杂质产生无非是产物降解或是原料中杂质产生的副反应生,而化合物5我们做过稳定性实验,在该体系中是稳定的,所以该杂质很大可能是原料中自带杂质参与反应生成的副产物(化合物3),对此我们查询到化合物1是买来的起始原料,该原料厂家coa显示原料中一个最主要杂质(化合物1)与化合物4结构很相似,对此我们猜测化合物5中的未知杂质应该是化合物1与化合物2反应生成的化合物3。对此我们设计了实验,在与泊沙康唑中间体相同反应体系下用化合物1与化合物2合成化合物3,通过加标实验来达到确定泊沙康唑中间体(化合物5)成品中的杂质(rrt=1.12)与化合物3是否为同一化合物的目的。通过分离手段得到化合物5纯净品,核磁质谱确定了其化学结构。我们用化合物3做了加标实验,所谓的加标实验就是向含有未知杂质(rrt=1.12)的化合物5中加入化合物3得到混合物,该混合物通过hplc检测,验证未知杂质与化合物3出峰位置是否一致。如果一致,可以说明化合物5中未知杂质(rrt=1.12)的结构就是化合物3,反之不是。对此我们同时测了含未知杂质(rrt=1.12)的中间体(化合物5)和加标后的hplc图,谱图如图9所示。
[0050]
从加标实验与化合物5的hplc谱图中我们可以看出,加标后未知杂质(rrt=1.12)含量明显增长,化合物3出峰位置与未知杂质完全重合,从而确证了化合物5中未知杂质的化学结构就是化合物3。该杂质的发现对泊沙康唑杂质研究的完善及药物不良反应的控制起着关键积极作用。
[0051]
实施例1
[0052]
依次加入3.0g化合物1,2.27g化合物2,0.32g dmap,0.54g咪唑,3ml dmso搅拌溶解,25℃反应24h,将反应液滴至30ml水中,100ml二氯甲烷萃取,减压浓缩得深棕色油状液体,柱层析(使用18*160mm玻璃层析柱,300~400目硅胶,石油醚与乙酸乙酯体积比为1:1的混合溶剂作洗脱剂)3次纯化得浅黄色固体(化合物3)0.24g,收率8.9%,纯度98.1%。
[0053]
实施例2
[0054]
依次加入3.0g化合物1,2.27g化合物2,0.32g dmap,0.54g咪唑,3ml dmso搅拌溶解,45℃反应24h,将反应液滴至30ml水中,100ml二氯甲烷萃取,减压浓缩得深棕色油状液体,柱层析(使用18*160mm玻璃层析柱,300~400目硅胶,石油醚与乙酸乙酯体积比为1:1的混合溶剂作洗脱剂)3次纯化得浅黄色固体(化合物3)0.33g,收率12.5%,纯度98.5%。
[0055]
实施例3
[0056]
依次加入3.0g化合物1,2.27g化合物2,0.32g dmap,0.54g咪唑,3ml dmso搅拌溶解,70℃反应24h,将反应液滴至30ml水中,100ml二氯甲烷萃取,减压浓缩得深棕色油状液体,柱层析(使用18*160mm玻璃层析柱,300~400目硅胶,石油醚与乙酸乙酯体积比为1:1的混合溶剂作洗脱剂)3次纯化得浅黄色固体(化合物3)0.55g,收率20.5%,纯度98.6%。
[0057]
实施例4
[0058]
依次加入3.0g化合物1,2.27g化合物2,0.32g dmap,0.54g咪唑,3ml dmso搅拌溶解,95℃反应24h,将反应液滴至30ml水中,100ml二氯甲烷萃取,减压浓缩得深棕色油状液体,柱层析(使用18*160mm玻璃层析柱,300~400目硅胶,石油醚与乙酸乙酯体积比为1:1的混合溶剂作洗脱剂)3次纯化得浅黄色固体(化合物3)0.53g,收率20.1%,纯度98.5%。
[0059]
实施例5
[0060]
依次加入3.0g化合物1,2.27g化合物2,0.32g dmap,0.54g咪唑,3ml dmso搅拌溶解,70℃反应8h,将反应液滴至30ml水中,100ml二氯甲烷萃取,减压浓缩得深棕色油状液体,柱层析(使用18*160mm玻璃层析柱,300~400目硅胶,石油醚与乙酸乙酯体积比为1:1的混合溶剂作洗脱剂)3次纯化得浅黄色固体(化合物3)0.54g,收率20.3%,纯度98.6%。
[0061]
实施例6
[0062]
依次加入3.0g化合物1,2.27g化合物2,0.32g dmap,0.54g咪唑,3ml dmso搅拌溶解,70℃反应8h,将反应液滴至30ml水中,100ml二氯甲烷萃取,减压浓缩得深棕色油状液体,柱层析(使用18*160mm玻璃层析柱,300~400目硅胶,石油醚与乙酸乙酯体积比为1:1的混合溶剂作洗脱剂)3次纯化得浅黄色固体(化合物3)0.54g,收率20.3%,纯度98.6%。
[0063]
实施例7
[0064]
依次加入3.0g化合物1,3.09g化合物2,0.65g dmap,0.54g咪唑,3ml dmso搅拌溶解,70℃反应8h,将反应液滴至水30ml中,100ml二氯甲烷萃取,减压蒸馏得深棕色油状液体,柱层析(使用18*160mm玻璃层析柱,300~400目硅胶,石油醚与乙酸乙酯体积比为1:1的混合溶剂作洗脱剂)3次得浅黄色固体(化合物3)0.67g,收率25.3%,纯度98.7%。
[0065]
1h nmr(400mhz,dmso)δ8.88(s,1h),8.86(s,1h),7.42(d,j=8.9hz,2h),7.34(t,j=7.4hz,5h),6.92(d,j=9.0hz,2h),6.87(d,j=8.9hz,2h),6.70(d,j=8.9hz,2h),4.62(d,j=11.8hz,1h),4.40(d,j=11.8hz,1h),4.29(s,2h),4.23(dd,j=10.6,5.3hz,1h),3.76
–
3.68(m,1h),3.19(d,j=5.0hz,4h),3.12(d,j=4.4hz,4h),1.78(d,j=10.6hz,1h),1.55(dd,j=7.0,2.2hz,1h),1.18(d,j=6.2hz,3h),0.83(t,j=7.3hz,3h).esi
+-ms[m+h]504.6,[m+na]526.6.
[0066]
实施例8
[0067]
依次加入3.0g化合物1,3.09g化合物2,1.03g dmap,0.54g咪唑,3ml dmso搅拌溶解,70℃反应8h,将反应液滴至水30ml中,100ml二氯甲烷萃取,减压蒸馏得深棕色油状液
体,柱层析(使用18*160mm玻璃层析柱,300~400目硅胶,石油醚与乙酸乙酯体积比为1:1的混合溶剂作洗脱剂)3次得浅黄色固体(化合物3)0.66g,收率25.1%,纯度98.7%。
[0068]
实施例9
[0069]
依次加入3.0g化合物1,3.09g化合物2,0.65g dmap,0.79g咪唑,3ml dmso搅拌溶解,70℃反应8h,将反应液滴至水30ml中,100ml二氯甲烷萃取,减压蒸馏得深棕色油状液体,柱层析(使用18*160mm玻璃层析柱,300~400目硅胶,石油醚与乙酸乙酯体积比为1:1的混合溶剂作洗脱剂)3次得浅黄色固体(化合物3)0.81g,收率30.3%,该化合物的核磁氢谱图如图1所示,ms谱图如图2所示,hplc如图3所示,产物纯度99.2%。
[0070]1h nmr(400mhz,dmso)δ9.02(s,1h),8.89(s,1h),7.42(d,j=9.0hz,2h),7.36
–
7.27(m,5h),6.91(d,j=9.1hz,2h),6.88
–
6.84(m,2h),6.72(dd,j=9.6,2.8hz,2h),4.61(d,j=11.8hz,1h),4.39(d,j=11.8hz,1h),4.30(s,2h),4.26
–
4.20(m,1h),3.76
–
3.68(m,1h),3.19(dd,j=6.4,2.9hz,4h),3.13
–
3.09(m,4h),1.78(s,1h),1.54(dd,j=7.0,2.2hz,1h),1.18(d,j=6.2hz,3h),0.82(t,j=7.3hz,3h).esi
+-ms[m+h]504.6,[m+na]526.6.
[0071]
实施例10
[0072]
依次加入3.0g化合物1,3.09g化合物2,0.65g dmap,1.08g咪唑,3ml dmso搅拌溶解,70℃反应8h,将反应液滴至水30ml中,100ml二氯甲烷萃取,减压蒸馏得深棕色油状液体,柱层析(使用18*160mm玻璃层析柱,300~400目硅胶,石油醚与乙酸乙酯体积比为1:1的混合溶剂作洗脱剂)3次得浅黄色固体(化合物3)0.80g,收率30.1%,纯度99.1%。
[0073]
1h nmr(400mhz,dmso)δ9.00(s,1h),8.48(s,1h),7.40
–
7.34(m,4h),7.33
–
7.25(m,3h),6.93
–
6.81(m,4h),6.76
–
6.68(m,2h),4.76(s,1h),4.60(d,j=11.8hz,1h),4.46(d,j=11.8hz,1h),3.70
–
3.55(m,1h),3.18(dd,j=6.5,2.8hz,4h),3.14
–
3.08(m,4h),2.72(s,2h),1.94(s,1h),1.61
–
1.50(m,1h),1.19(d,j=6.3hz,3h),0.95(t,j=7.4hz,3h).esi
+-ms[m+h]504.6,[m+na]526.6.
[0074]
实施例11
[0075]
依次加入3.0g化合物1,3.09g化合物2,0.65g dmap,0.79g咪唑,3ml dmso搅拌溶解,70℃反应6h,将反应液滴至水30ml中,100ml二氯甲烷萃取,减压蒸馏得深棕色油状液体,柱层析(使用18*160mm玻璃层析柱,300~400目硅胶,石油醚与乙酸乙酯体积比为1:1的混合溶剂作洗脱剂)3次得浅黄色固体(化合物3)0.79g,收率29.9%,纯度99.1%。
[0076]
以上所述实施例仅表达了本发明的几种实施方式,其描述较为具体和详细,但并不能因此而理解为对本发明专利范围的限制。应当指出的是,对于本领域的普通技术人员来说,在不脱离本发明构思的前提下,还可以做出若干变形和改进,这些都属于本发明的保护范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1