多肽化合物及其在预防或治疗非酒精性脂肪肝炎中的应用的制作方法
7.其中,r1=
‑
nh2或-oh;
8.xaa2=lys或ser;
9.xaa5=ser或tyr;
10.xaa6=pro或lys;
11.xaa8=leu或ala。
12.本发明多肽化合物,优选的xaa6=pro。
13.本发明多肽化合物,优选的xaa2=lys。
14.本发明的多肽化合物为如下化合物1
‑
8中的任一种:
15.化合物1(seq id no.1):
16.cys
‑
lys
‑
lys
‑
asn
‑
ser
‑
pro
‑
thr
‑
ala
‑
cys
17.ckknsptac
18.化合物2(seq id no.2):
19.cys
‑
lys
‑
lys
‑
asn
‑
tyr
‑
pro
‑
thr
‑
leu
‑
cys
20.ckknyptlc
21.化合物3(seq id no.3):
22.cys
‑
lys
‑
lys
‑
asn
‑
tyr
‑
pro
‑
thr
‑
ala
‑
cys
23.ckknyptac
24.化合物4(seq id no.4):
25.cys
‑
lys
‑
lys
‑
asn
‑
ser
‑
pro
‑
thr
‑
leu
‑
cys
26.ckknsptlc
27.化合物5(seq id no.5):
28.cys
‑
ser
‑
lys
‑
asn
‑
tyr
‑
pro
‑
thr
‑
leu
‑
cys
29.csknyptlc
30.化合物6(seq id no.6):
31.cys
‑
ser
‑
lys
‑
asn
‑
ser
‑
pro
‑
thr
‑
leu
‑
cys
32.csknsptlc
33.化合物7(seq id no.7):
34.cys
‑
ser
‑
lys
‑
asn
‑
ser
‑
pro
‑
thr
‑
ala
‑
cys
35.csknsptac
36.化合物8(seq id no.8):
37.cys
‑
ser
‑
lys
‑
asn
‑
tyr
‑
pro
‑
thr
‑
ala
‑
cys
38.csknyptac。
39.本发明的另一方面是提供一种组合物,该组合物包含上述多肽化合物。
40.本发明的组合物为药物组合物,以本发明的多肽化合物作为活性成分添加药学上可接受载体和/或辅料制成药物组合物。
41.本发明的再一方面是提供本发明的多肽化合物的药物用途。通过细胞和动物实验显示,本发明的多肽化合物没有不良反应发生,可用于预防或治疗非酒精性脂肪肝炎。
42.本领域技术人员可以理解,本发明的药物组合物适用于各种给药方式,例如口服给药、经皮给药、静脉给药、肌肉内给药、局部给药、经鼻给药等。根据所采用的给药方式,可
将本发明的多肽化合物的药物组合物制成各种合适的剂型,其中包含至少一种有效剂量的本发明的多肽化合物和至少一种药学上可接受的药用载体。适当剂型的实例为片剂、胶囊、糖衣片剂、粒剂、口服溶液和糖浆,用于皮肤表面的油膏和药贴,气雾剂、鼻喷剂,以及可用于注射的无菌溶液。
43.含有本发明多肽化合物的药物组合物可以制成溶液或者冻干粉末以用于胃肠外给药,在使用前可加入适当溶剂或其他可药用的载体将粉末重新配置,液体配方一般是缓冲液、等渗溶液和水溶液。
44.本发明的药物组合物的用量可以在一个较大范围内变动,本领域技术人员可以根据一些客观的因素,如根据疾病的种类、病情严重程度、病人体重、剂型以及给药途径等因素很容易的加以确定。
45.本发明的优点:
46.1)本发明的多肽化合物具有良好的生物学活性;
47.2)本发明的多肽化合物对于非酒精性脂肪肝炎具有良好的治疗效果;
48.3)本发明的多肽化合物在药物的药代实验中显示出显著的药物活性;
49.4)本发明的多肽化合物在药物的药代实验中显示出良好的安全性和稳定性;
50.5)本发明的多肽化合物合成产率高,稳定性好,易于放大生产,且成本低。
51.本发明中所用缩写具体含义如下:
52.fmoc为芴甲氧羰基,resin为树脂,mpeg为单甲氧基聚乙烯二醇,cys为半胱氨酸,lys为赖氨酸,ser为丝氨酸,asn为天冬酰胺,tyr为酪氨酸,thr为苏氨酸,ala为丙氨酸,leu为亮氨酸,pro为脯氨酸。
附图说明
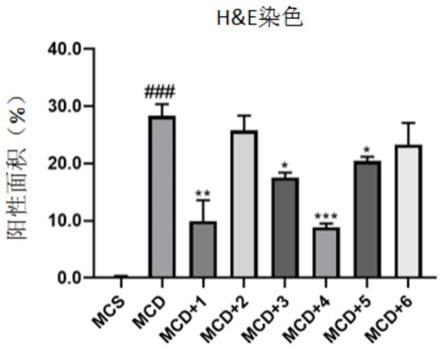
53.图1为在mcd(蛋氨酸胆碱缺乏)饲料诱导的小鼠肝脏非酒精性脂肪肝炎模型中,分别给予150μg/kg的化合物1、化合物2、化合物3、化合物4、化合物5和化合物6后小鼠肝脏的h&e染色病理切片图。
54.图2为在mcd饲料诱导的小鼠肝脏非酒精性脂肪肝炎模型中,分别给予80μg/kg的化合物1、化合物2、化合物3、化合物4、化合物5和化合物6后小鼠肝脏脂质积累柱状分析图;其中,*:表示置信度>95%,差异有统计学意义(p<0.05);**:表示置信度>99%,两者差别有非常显著意义(p<0.01);***:表示置信度>99.9%,两者差别有极其显著性意义(p<0.001);###:表示模型组与对照组相比有极其显著性差异(p<0.001)。
55.图3为在mcd饲料诱导的小鼠肝脏非酒精性脂肪肝炎模型中,分别给予80μg/kg的化合物1、化合物2、化合物3、化合物4、化合物5和化合物6后小鼠肝脏的油红o染色病理切片图。
56.图4为在mcd饲料诱导的小鼠肝脏非酒精性脂肪肝炎模型中,分别给予80μg/kg的化合物1、化合物2、化合物3、化合物4、化合物5和化合物6后小鼠肝脏脂质积累柱状分析图;其中,*:表示置信度>95%,差异有统计学意义(p<0.05);**:表示置信度>99%,两者差别有非常显著意义(p<0.01);***:表示置信度>99.9%,两者差别有极其显著性意义(p<0.001);###:表示模型组与对照组相比有极其显著性差异(p<0.001)。
57.图5为在mcd饲料诱导的小鼠肝脏非酒精性脂肪肝炎模型中,分别给予80μg/kg的
化合物1、化合物2、化合物3、化合物4、化合物5和化合物6后小鼠肝脏的天狼星红染色病理切片图。
58.图6为在mcd饲料诱导的小鼠肝脏非酒精性脂肪肝炎模型中,分别给予80μg/kg的化合物1、化合物2、化合物3、化合物4、化合物5和化合物6后小鼠肝脏脂质积累柱状分析图;其中,*:表示置信度>95%,差异有统计学意义(p<0.05);**:表示置信度>99%,两者差别有非常显著意义(p<0.01);***:表示置信度>99.9%,两者差别有极其显著性意义(p<0.001);###:表示模型组与对照组相比有极其显著性差异(p<0.001)。
具体实施方式
59.下面将结合实施例对本发明的实施方案进行详细描述,但是本领域技术人员将会理解,下列实施例仅用于说明本发明,而不应视为限定本发明的范围。实施例中未注明具体条件者,按照常规条件或制造商建议的条件进行。所用试剂或仪器未注明生产厂商者,均为可以通过市购获得的常规产品。
60.实施例1多肽化合物的合成
61.材料:
62.所有的氨基酸购自吉尔生化(上海)有限公司。如果没有特别说明,其他所有试剂均为分析纯,sigma品牌试剂。采用protein technologies prelude 6通道多肽合成仪。phenomenex luna c18制备柱(46mm x 250mm)用来纯化多肽。高效液相色谱仪为waters公司产品。质谱分析采用agilent质谱仪进行测定。
63.实验方法:
64.化合物采用fmoc固相多肽的合成法,由羧基端向氨基端方向合成,按照上述氨基酸序列顺序依次连接。具体步骤如下:首先采用mbhar(amide
‑
mbha
‑
resin酰胺保护的mbha树脂)或者王树脂,脱fmoc保护基合成。用茚检试剂进行检测,其中茚检试剂的使用量为试剂1:试剂2:试剂3=l:2:l(滴),沸水中加热3
‑
10min。处理树脂,称取一定量mbha树脂于合成仪中,加入dcm搅拌30min,抽干,再用dmf洗4次,每次2min,挑取少量树脂进行茚检,若树脂颜色无改变,表明正常,可使用。脱fmoc保护:20%哌啶洗4次,在第3次洗之后茚检,如果茚检显蓝紫色说明可接下一个氨基酸。如此重复操作,直至合肽完成为止。最后利用冰乙醚洗涤沉淀切割后的多肽,然后进行高效液相色谱纯化。
65.基于以上合成步骤,合成本发明的如下多肽化合物(表1):
66.表1.本发明实施例中所合成的多肽化合物结构:
67.化合物编号序列1seq id no.1cys
‑
lys
‑
lys
‑
asn
‑
ser
‑
pro
‑
thr
‑
ala
‑
cys2seq id no.2cys
‑
lys
‑
lys
‑
asn
‑
tyr
‑
pro
‑
thr
‑
leu
‑
cys3seq id no.3cys
‑
lys
‑
lys
‑
asn
‑
tyr
‑
pro
‑
thr
‑
ala
‑
cys4seq id no.4cys
‑
lys
‑
lys
‑
asn
‑
ser
‑
pro
‑
thr
‑
leu
‑
cys5seq id no.5cys
‑
ser
‑
lys
‑
asn
‑
tyr
‑
pro
‑
thr
‑
leu
‑
cys6seq id no.6cys
‑
ser
‑
lys
‑
asn
‑
ser
‑
pro
‑
thr
‑
leu
‑
cys7seq id no.7cys
‑
ser
‑
lys
‑
asn
‑
ser
‑
pro
‑
thr
‑
ala
‑
cys8seq id no.8cys
‑
ser
‑
lys
‑
asn
‑
tyr
‑
pro
‑
thr
‑
ala
‑
cys
68.实施例2本发明的多肽化合物对mcd诱导的小鼠非酒精性脂肪肝炎的改善治疗作用
69.本实施例选用多肽化合物1、多肽化合物2、多肽化合物3、多肽化合物4、多肽化合物5、多肽化合物6为例研究本发明的多肽化合物对小鼠非酒精性脂肪炎的改善治疗作用,其具体方法如下。
70.模型的建立:
71.受试药物:多肽化合物1,多肽化合物2,多肽化合物3,多肽化合物4,多肽化合物5和多肽化合物6,保存条件
‑
20℃。
72.造模方法:将48只雄性c57bl/6j小鼠,周龄8周(购自北京维通利华实验动物技术有限公司),随机分为8组,分别为:1)对照组(mcs)+生理盐水,腹腔注射,n=6;2)模型组(mcd)+生理盐水,腹腔注射,n=6;3)模型组(mcd)+150μg/kg化合物1,n=6;4)模型组(mcd)+150μg/kg化合物2,n=6;5)模型组(mcd)+150μg/kg化合物3,n=6;6)模型组(mcd)+150μg/kg化合物4,n=6;7)模型组(mcd)+150μg/kg化合物5,n=6;8)模型组(mcd)+150μg/kg化合物6,n=6。
73.在喂养蛋氨酸
‑
胆碱缺乏的饲料(mcd)(购自江苏美迪森生物医药有限公司)4周后,对小鼠进行给药或给生理盐水处理,给药后3周取材,进行病理观察。
74.实验方法:
75.h&e染色:烘片、脱蜡;苏木素染色7分钟、自来水冲洗干净、1%盐酸乙醇分化1s、自来水冲洗、伊红染色、自来水冲洗、脱水透明、晾干、树胶封片。
76.油红o染色:将冰冻切片(厚度为4
‑
8μm)常温干燥15
‑
20min;100%异丙醇孵育5分钟(避免把水带入油红o);0.5%的油红o溶液孵育7
‑
8分钟(在60℃烤箱);85%异丙醇溶液洗3分钟;双脱水洗;苏木素染1
‑
1.5min;双脱水洗;封片剂封片。
77.天狼星红染色:烘片、脱蜡;双蒸水中静置5.0分钟;暗室中天狼星红染色60
‑
80分钟;0.5%冰醋酸涮洗5s;脱水透明,封片,拍照。
78.在mcd诱导的小鼠非酒精性脂肪肝炎模型中,小鼠的表现特征为:脂质代谢异常和肝脏中大量的甘油三酯(tg)积累等。在给予本发明的多肽化合物治疗3周之后,处理小鼠并进行取材,取肝脏组织用于病理学分析。
79.在mcd诱导的小鼠肝脏非酒精性脂肪肝炎模型中,分别给予150μg/kg的多肽化合物1、多肽化合物2、多肽化合物3、多肽化合物4、多肽化合物5和多肽化合物6后,小鼠肝脏的h&e染色结果及脂质积累分析结果如图1至图2所示;小鼠肝脏的油红o染色结果及脂质积累分析结果如图3至图4所示;小鼠肝脏的天狼星红染色结果及脂质积累分析结果如图5至图6所示。
80.从图1至图6的结果可以看出,小鼠给予mcd饲料之后,小鼠肝脏中甘油三酯的积累明显增多,在给予本发明的多肽化合物治疗之后得到了小鼠肝脏内甘油三酯的积累明显得到了明显改善。由此可以证明,本发明的多肽化合物对于非酒精性脂肪肝炎具有良好的治疗效果。
81.当然,本发明还可有其它多种实施例,在不背离本发明精神及其实质的情况下,熟悉本领域的技术人员当可根据本发明作出各种相应的改变和变形,但这些相应的改变和变形都应属于本发明所附的权利要求书所界定的保护范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1