芳胺类有机化合物、混合物、组合物及有机电子器件的制作方法
芳胺类有机化合物、混合物、组合物及有机电子器件
1.本技术要求于2020年11月19日提交中国专利局、申请号为2020113011194、发明名称为“一种芳胺化合物及其在有机电子器件上的应用”的中国专利申请的优先权,其全部内容通过引用结合在本技术中。
技术领域
2.本发明涉及有机电致发光材料技术领域,特别是涉及一种芳胺类有机化合物、混合物、组合物及有机电子器件。
背景技术:
3.有机光电材料在合成上具有多样性,制造成本相对较低以及优良的光学与电学性能。有机发光二极管(oled)在光电器件(例如平板显示器和照明)的应用方面具有广视角、反应时间快、工作电压低、面板厚度薄等优势,因而具有广阔的发展潜力。
4.有机电致发光现象是指利用有机物质将电能转化为光能的现象。利用有机电致发光现象的有机电致发光元件通常具有正极与负极以及在它们中间包含有机功能层的结构。为了提高有机电致发光元件的效率与寿命,有机功能层具有多层结构,每一层包含有不同的有机物质。具体的,可以包括空穴注入层、空穴传输层、发光层、电子传输层、电子注入层等。在这种有机电致发光元件中,在两个电极之间施加电压,则由正极向有机功能层注入空穴,由负极向有机功能层注入电子,当注入的空穴与电子相遇时形成激子,该激子跃迁回基态时发出光。这种有机电致发光元件具有自发光、高亮度、高效率、低驱动电压、广视角、高对比度等特性。
5.近些年,有机电致发光二极管(oled)的发光效率有了很大的提升,但是其内部量子效率已经接近理论极限。空穴和电子的迁移率的差异导致复合区域并不能完全均匀分散于发光层,降低了器件的发光效率。通过进一步改善材料结构与器件结构,可以提升空穴迁移率,降低空穴和电子迁移率间的差异,避免复合区域的偏移,从而提升器件的发光效率和器件寿命。
技术实现要素:
6.鉴于上述现有技术的不足,本发明的目的在于提供一类基于芳香胺的有机化合物、混合物、组合物及有机电子器件,旨在解决提供一类新型的电子阻挡或空穴传输材料用于有机发光二极管中,提高器件的稳定性和寿命。
7.本发明的技术方案如下:
8.一种芳胺类有机化合物,具有如式(1)所示的结构:
[0009][0010]
其中,
[0011]
ar1、ar2分别独立选自取代或未取代的环原子数为6至40的芳香基团,或取代或未取代环原子数为5至40的杂芳香基团;
[0012]
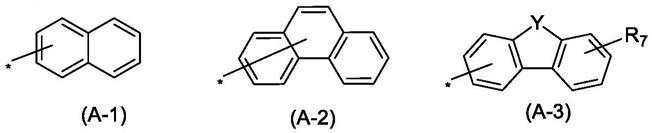
ar3选自(a-1)-(a-3)任一所示的基团:
[0013][0014]
x选自o、s、cr1r2、nr3;
[0015]
y选自o、s、cr4r5、nr6;
[0016]r1-r6每次出现时,分别独立选自-h,-d,或具有1至20个c原子的直链烷基,具有1至20个c原子的直链烷氧基,具有1至20个c原子的直链硫代烷氧基,具有3至20个c原子的支链烷基或环状的烷基,具有3至20个c原子的支链烷氧基或环状的烷氧基,具有3至20个c原子的支链硫代烷氧基或环状的硫代烷氧基,或甲硅烷基,或具有1至20个c原子的酮基,或具有2至20个c原子的烷氧基羰基,或具有7至20个c原子的芳氧基羰基,氰基,卤甲酰基,甲酰基,异氰基,异氰酸酯基,硫氰酸酯基或异硫氰酸酯基,羟基,硝基,烯基,胺基,cf3,cl,br,f,可交联的基团,或者取代或未取代的环原子数为6至60的芳香基团,或取代或未取代的环原子数为5至60的杂芳香基团,或环原子数为6至60的芳氧基,或环原子数为5至60的杂芳氧基基团,或这些基团的组合;
[0017]
r1与r2相互成环或不成环;
[0018]
r4与r5相互成环或不成环;
[0019]
r7选自h或苯基;
[0020]
*表示连接位点。
[0021]
本发明还提供一种混合物,所述混合物包括上述的芳胺类有机化合物,及至少一种有机功能材料,所述有机功能材料选自空穴注入材料、空穴传输材料、电子传输材料、电子注入材料、电子阻挡材料、空穴阻挡材料、发光材料、主体材料和有机染料中的至少一种。
[0022]
本发明还提供一种组合物,所述组合物包括上述的芳胺类有机化合物,或上述的混合物,及至少一种有机溶剂。
[0023]
本发明还提供一种有机电子器件,包含第一电极、第二电极、位于第一电极和第二电极之间的一个或多个有机功能层,所述有机功能层包含上述的芳胺类有机化合物,或上述的混合物,或由上述的组合物制备而成。
[0024]
与现有技术相比,本发明具有如下有益效果:
[0025]
本发明提供的芳胺类有机化合物,因苯基相邻基团之间的位阻作用分子结构会发生扭曲,有利于载流子的传输,可作为电子阻挡材料用于有机电子器件中,提高器件的发光效率和寿命。
具体实施方式
[0026]
以下结合具体实施例对本发明作进一步详细的说明。本发明可以以许多不同的形式来实现,并不限于本文所描述的实施方式。相反地,提供这些实施方式的目的是使对本发明公开内容理解更加透彻全面。
[0027]
除非另有定义,本文所使用的所有的技术和科学术语与属于本发明的技术领域的技术人员通常理解的含义相同。本文中在本发明的说明书中所使用的术语只是为了描述具体的实施例的目的,不是旨在于限制本发明。本文所使用的术语“和/或”包括一个或多个相关的所列项目的任意的和所有的组合。
[0028]
在本发明中,“取代”表示被取代基中的氢原子被取代基所取代。
[0029]
在本发明中,同一取代基多次出现时,可独立选自不同基团。如通式含有多个r1,则r1可独立选自不同基团。例如苯环上6个r1可以彼此相同或不同。
[0030]
本发明中,“取代或未取代”表示所定义的基团可以被取代,也可以不被取代。当所定义的基团被取代时,应理解为任选被本领域可接受的基团所取代,包括但不限于:c
1-30
烷基、含有3-20个环原子的杂环基、含有5-20个环原子的芳基、含有5-20个环原子的杂芳基、硅烷基、羰基、烷氧基羰基、芳氧基羰基、氨基甲酰基、卤甲酰基、甲酰基、-nrr
′
、氰基、异氰基、异氰酸酯基、硫氰酸酯基、异硫氰酸酯基、羟基、三氟甲基、硝基或卤素,且上述基团也可以进一步被本领域可接受取代基取代;可理解的,-nrr
′
中的r和r
′
各自独立地为本领域可接受的基团所取代,包括但不限于h、c
1-6
烷基、含有3-8个环原子的环烷基、含有3-8个环原子的杂环基、含有5-20个环原子的芳基或含有5-10个环原子的杂芳基;所述c
1-6
烷基、含有3-8个环原子的环烷基、含有3-8个环原子的杂环基、含有5-20个环原子的芳基或含有5-10个环原子的杂芳基任选进一步被一个或多个以下基团取代:c
1-6
烷基、含有3-8个环原子的环烷基、含有3-8个环原子的杂环基、卤素、羟基、硝基或氨基。
[0031]
在本发明中,“环原子数”表示原子键合成环状而得到的结构化合物(例如,单环化合物、稠环化合物、交联化合物、碳环化合物、杂环化合物)的构成该环自身的原子之中的原子数。该环被取代基所取代时,取代基所包含的原子不包括在成环原子内。关于以下所述的“环原子数”,在没有特别说明的条件下也是同样的。例如,苯环的环原子数为6,萘环的环原子数为10,噻吩基的环原子数为5。
[0032]
在本发明中,“烷基”可以表示直链、支链和/或环状烷基。烷基的碳数可以为1至50、1至30、1至20、1至10或1至6。包含该术语的短语,例如,“c
1-9
烷基”是指包含1~9个碳原子的烷基,每次出现时,可以互相独立地为c1烷基、c2烷基、c3烷基、c4烷基、c5烷基、c6烷基、c7烷基、c8烷基或c9烷基。烷基的非限制性实例包括甲基、乙基、正丙基、异丙基、正丁基、仲丁基、叔丁基、异丁基、2-乙基丁基、3,3-二甲基丁基、正戊基、异戊基、新戊基、叔戊基、环戊基、1-甲基戊基、3-甲基戊基、2-乙基戊基、4-甲基-2-戊基、正己基、1-甲基己基、2-乙基己基、2-丁基己基、环己基、4-甲基环己基、4-叔丁基环己基、正庚基、1-甲基庚基、2,2-二甲基庚基、2-乙基庚基、2-丁基庚基、正辛基、叔辛基、2-乙基辛基、2-丁基辛基、2-己基辛基、3,7-二甲基辛基、环辛基、正壬基、正癸基、金刚烷基、2-乙基癸基、2-丁基癸基、2-己基癸基、2-辛基癸基、正十一烷基、正十二烷基、2-乙基十二烷基、2-丁基十二烷基、2-己基十二烷基、2-辛基十二烷基、正十三烷基、正十四烷基、正十五烷基、正十六烷基、2-乙基十六烷基、2-丁基十六烷基、2-己基十六烷基、2-辛基十六烷基、正十七烷基、正十八烷基、正十九烷基、正二十烷基、2-乙基二十烷基、2-丁基二十烷基、2-己基二十烷基、2-辛基二十烷基、正
二十一烷基、正二十二烷基、正二十三烷基、正二十四烷基、正二十五烷基、正二十六烷基、正二十七烷基、正二十八烷基、正二十九烷基、正三十烷基、金刚烷等。
[0033]“芳基、芳香基或芳香基团”指至少包含一个芳环的烃基。“杂芳香基或杂芳香基团”指包含至少一个杂原子的芳香烃基。杂原子优选选自si、n、p、o、s和/或ge,特别优选选自si、n、p、o和/或s。稠环芳香基团指芳香基团的环可以具有两个或多个环,其中两个碳原子被两个相邻的环共用,即稠环。稠杂环芳香基团指包含至少一个杂原子的稠环芳香烃基。对于本发明的目的,芳香基团或杂芳香基团不仅包括芳香环的体系,而且包含非芳香族的环系。因此,比如吡啶、噻吩、吡咯、吡唑、三唑、咪唑、噁唑、噁二唑、噻唑、四唑、吡嗪、哒嗪、嘧啶、三嗪、卡宾等体系,对于该发明目的同样认为是芳香基团或杂环芳香基团。对于本发明的目的,稠环芳香族或稠杂环芳香族环系不仅包括芳香基团或杂芳香基团的体系,而且,其中多个芳香基团或杂环芳香基团也可以被短的非芳族单元间断(《10%的非h原子,优选小于5%的非h原子,比如c、n或o原子)。因此,比如9,9'-螺二芴,9,9-二芳基芴,三芳胺,二芳基醚等体系,对于该发明目的同样认为是稠环芳香族环系。
[0034]
在某个优选的实施例中,所述的芳香基团选自:苯、萘、蒽、荧蒽、菲、苯并菲、二萘嵌苯、并四苯、芘、苯并芘、苊、芴、及其衍生物;杂芳香基团选自三嗪、吡啶、嘧啶、咪唑、呋喃、噻吩、苯并呋喃、苯并噻吩、吲哚、咔唑、吡咯并咪唑、吡咯并吡咯、噻吩并吡咯、噻吩并噻吩、呋喃并吡咯、呋喃并呋喃、噻吩并呋喃、苯并异噁唑、苯并异噻唑、苯并咪唑、喹啉、异喹啉、邻二氮萘、喹喔啉、菲啶、伯啶、喹唑啉、喹唑啉酮、二苯并噻吩、二苯并呋喃、咔唑及其衍生物。
[0035]“胺基”是指胺的衍生物,具有式-n(x)2的结构特征,其中每个“x”独立地是h、取代的或未被取代的烷基、取代的或未被取代的环烷基、取代的或未被取代的杂环基等。胺基的非限制性类型包括-nh2、-n(烷基)2、-nh(烷基)、-n(环烷基)2、-nh(环烷基)、-n(杂环基)2、-nh(杂环基)、-n(芳基)2、-nh(芳基)、-n(烷基)(芳基)、-n(烷基)(杂环基)、-n(环烷基)(杂环基)、-n(芳基)(杂芳基)、-n(烷基)(杂芳基)等。
[0036]
本发明中,与单键相连的“*”表示连接或稠合位点。
[0037]
本发明中,基团中未指明连接位点时,表示基团中任选可连接位点作为连接位点;
[0038]
本发明中,基团中未指明稠合位点时,表示基团中任选可稠合位点作为稠合位点,优选基团中处于邻位的两个或多个位点为稠合位点;
[0039]
本发明中,取代基相连的单键贯穿相应的环,表述该取代基可与环的任选位置连接,例如中r与苯环的任一可取代位点相连。
[0040]
在本发明中,“成环”的意思是形成脂肪族环、芳香族环、杂芳香族环、脂肪族杂环或它们组合后的形态。
[0041]
本发明的技术方案如下:
[0042]
一种芳胺类有机化合物,具有如式(1)所示的结构:
[0043]
[0044]
其中,
[0045]
ar1、ar2分别独立选自取代或未取代的环原子数为6至40的芳香基团,或取代或未取代环原子数为5至40的杂芳香基团;
[0046]
ar3选自(a-1)-(a-3)任一所示的基团:
[0047][0048]
x选自o、s、cr1r2、nr3;
[0049]
y选自o、s、cr4r5、nr6;
[0050]r1-r6每次出现时,分别独立选自-h,-d,或具有1至20个c原子的直链烷基,具有1至20个c原子的直链烷氧基,具有1至20个c原子的直链硫代烷氧基,具有3至20个c原子的支链烷基或环状的烷基,具有3至20个c原子的支链烷氧基或环状的烷氧基,具有3至20个c原子的支链硫代烷氧基或环状的硫代烷氧基,或甲硅烷基,或具有1至20个c原子的酮基,或具有2至20个c原子的烷氧基羰基,或具有7至20个c原子的芳氧基羰基,氰基,卤甲酰基,甲酰基,异氰基,异氰酸酯基,硫氰酸酯基或异硫氰酸酯基,羟基,硝基,烯基,胺基,cf3,cl,br,f,可交联的基团,或者取代或未取代的环原子数为6至60的芳香基团,或取代或未取代的环原子数为5至60的杂芳香基团,或环原子数为6至60的芳氧基,或环原子数为5至60的杂芳氧基基团,或这些基团的组合;
[0051]
r1与r2相互成环或不成环;
[0052]
r4与r5相互成环或不成环;
[0053]
r7选自h或苯基;
[0054]
*表示连接位点。
[0055]
在一实施例中,所述芳胺类有机化合物选自(2-1)-(2-6)任一通式:
[0056][0057]
进一步,所述芳胺类有机化合物选自(3-1)-(3-3)任一通式:
[0058][0059]
当(a-3)选自时,相邻位点基团的扭转增大,可提高分子内基团间的位阻,减少基团的共轭,提高分子的三线态能级,减少发光层激子的非辐射跃迁。
[0060]
在一实施例中,y优选自o或s。稠环基团拥有较高的载流子迁移率,有益于实现器件内空穴与电子的平衡,提高发光效率。
[0061]
在一实施例中,x优选自cr1r2;进一步,r
1-r2每次出现时,分别独立选自-h,-d,或具有1至10个c原子的直链烷基,具有3至10个c原子的支链烷基或环状的烷基,或者取代或未取代的环原子数为6至30的芳香基团,或取代或未取代的环原子数为5至30的杂芳香基团;r1与r2不成环,或r1与r2相互形成环原子数为5至20的脂肪族环系;优选地,x优选自c(ch3)2。
[0062]
进一步,通式(1)中选自选自
[0063]
在一实施例中,ar1、ar2选自取代或未取代的环原子数为6至20的芳香基团,或取代或未取代环原子数为6至20的杂芳香基团;
[0064]
在一实施例中,ar1、ar2选自环原子数为6至18的芳香基团,或环原子数为6至18的杂芳香基团;或被d、具有1至10个c原子的直链烷基,具有3至10个c原子的支链烷基或环状的烷基,苯或菲取代的具有环原子数为6至18的芳香基团;或被d、具有1至10个c原子的直链烷基,具有3至10个c原子的支链烷基或环状的烷基,苯或菲取代的具有环原子数为6至18的杂芳香基团。
[0065]
进一步,ar1、ar2分别独立选自以下基团:
[0066][0067]
其中:
[0068]
z每次出现独立选自cr8或n;
[0069]
w每次出现独立选自o、s、cr9r
10
或nr9;
[0070]r8-r
10
每次出现时,分别独立选自-h,-d,或具有1至20个c原子的直链烷基,具有1至20个c原子的直链烷氧基,具有1至20个c原子的直链硫代烷氧基,具有3至20个c原子的支
链烷基或环状的烷基,具有3至20个c原子的支链烷氧基或环状的烷氧基,具有3至20个c原子的支链硫代烷氧基或环状的硫代烷氧基,或甲硅烷基,或具有1至20个c原子的酮基,或具有2至20个c原子的烷氧基羰基,或具有7至20个c原子的芳氧基羰基,氰基,卤甲酰基,甲酰基,异氰基,异氰酸酯基,硫氰酸酯基或异硫氰酸酯基,羟基,硝基,烯基,胺基,cf3,cl,br,f,可交联的基团,或者取代或未取代的环原子数为6至60的芳香基团,或取代或未取代的环原子数为5至60的杂芳香基团,或环原子数为6至60的芳氧基,或环原子数为5至60的杂芳氧基基团,或这些基团的组合。
[0071]
当ar1和ar2中的z为连接位点时,z为c;当ar1和ar2中的w为连接位点时,w为cr9、cr
10
或n。
[0072]
进一步,r
8-r
10
每次出现时,分别独立选自-h,-d,或具有1至10个c原子的直链烷基,具有3至10个c原子的支链烷基或环状的烷基,或者取代或未取代的环原子数为6至30的芳香基团,或取代或未取代的环原子数为5至30的杂芳香基团。
[0073]
在一实施例中,ar1、ar2分别独立选自以下基团:
[0074][0075]
其中:*表示连接位点。
[0076]
进一步,r8每次出现时,分别独立选自-h,-d,或具有1至10个c原子的直链烷基,具有3至10个c原子的支链烷基或环状的烷基,或苯基,或萘基。
[0077]
在一实施例中,ar1、ar2分别独立选自以下基团中的任意一种:
[0078][0079]
在一实施例中,ar1选自苯基。
[0080]
进一步,所述芳胺类有机化合物具有通式(4)所示的结构:
[0081]
[0082]
优选地,通式(4)中的y选自o或s。
[0083]
在一实施例中,式(1)中的选自以下所示基团中的任意一种
[0084][0085]
按照本发明所述的芳胺类有机化合物,选自但不限于以下结构:
[0086]
[0087]
[0088]
[0089]
[0090]
[0091]
[0092][0093]
在一实施例中,按照本发明的芳胺类有机化合物用于电子阻挡层中,更进一步,按照本发明的有机化合物用于红光有机电子器件的电子阻挡层中。
[0094]
本发明进一步涉及一种混合物,包含有至少一种以上所述的芳胺类有机化合物,及至少另一种有机功能材料,所述至少另一种的有机功能材料可选于空穴注入材料(him),空穴传输材料(htm),电子传输材料(etm),电子注入材料(eim),电子阻挡材料(ebm),空穴阻挡材料(hbm),发光材料(emitter),主体材料(host)和有机染料。例如在wo2010135519a1,us20090134784a1和wo 2011110277a1中对各种有机功能材料有详细的描述,特此将此3专利文件中的全部内容并入本文作为参考。
[0095]
在一实施例中,所述另一种有机功能材料选自电子传输材料。
[0096]
本发明还涉及一种组合物,包含至少一种如上所述的芳胺类有机化合物或混合物,及至少一种有机溶剂;所述的有机溶剂选自芳族或杂芳族、酯、芳族酮或芳族醚、脂肪族酮或脂肪族醚、脂环族或烯烃类化合物,或硼酸酯或磷酸酯类化合物,或两种及两种以上溶剂的混合物。
[0097]
在一个优选的实施例中,按照本发明的一种组合物,所述的至少的一种有机溶剂选自基于芳族或杂芳族的溶剂。
[0098]
适合本发明的基于芳族或杂芳族溶剂的例子有,但不限制于:对二异丙基苯、戊苯、四氢萘、环己基苯、氯萘、1,4-二甲基萘、3-异丙基联苯、对甲基异丙苯、二戊苯、三戊苯、戊基甲苯、邻二乙苯、间二乙苯、对二乙苯、1,2,3,4-四甲苯、1,2,3,5-四甲苯、1,2,4,5-四甲苯、丁苯、十二烷基苯、二己基苯、二丁基苯、对二异丙基苯、环己基苯、苄基丁基苯、二甲基萘、3-异丙基联苯、对甲基异丙苯、1-甲基萘、1,2,4-三氯苯、4,4-二氟二苯甲烷、1,2-二甲氧基-4-(1-丙烯基)苯、二苯甲烷、2-苯基吡啶、3-苯基吡啶、n-甲基二苯胺、4-异丙基联苯、α,α-二氯二苯甲烷、4-(3-苯基丙基)吡啶、苯甲酸苄酯、1,1-双(3,4-二甲基苯基)乙烷、2-异丙基萘、喹啉、异喹啉、2-呋喃甲酸甲酯、2-呋喃甲酸乙酯等;
[0099]
适合本发明的基于芳族酮溶剂的例子有,但不限制于:1-四氢萘酮,2-四氢萘酮,2-(苯基环氧)四氢萘酮,6-(甲氧基)四氢萘酮,苯乙酮、苯丙酮、二苯甲酮、及它们的衍生物,如4-甲基苯乙酮、3-甲基苯乙酮、2-甲基苯乙酮、4-甲基苯丙酮、3-甲基苯丙酮、2-甲基苯丙酮等;
[0100]
适合本发明的基于芳族醚溶剂的例子有,但不限制于:3-苯氧基甲苯、丁氧基苯、对茴香醛二甲基乙缩醛、四氢-2-苯氧基-2h-吡喃、1,2-二甲氧基-4-(1-丙烯基)苯、1,4-苯并二噁烷、1,3-二丙基苯、2,5-二甲氧基甲苯、4-乙基本乙醚、1,3-二丙氧基苯、1,2,4-三甲氧基苯、4-(1-丙烯基)-1,2-二甲氧基苯、1,3-二甲氧基苯、缩水甘油基苯基醚、二苄基醚、4-叔丁基茴香醚、反式-对丙烯基茴香醚、1,2-二甲氧基苯、1-甲氧基萘、二苯醚、2-苯氧基甲醚、2-苯氧基四氢呋喃、乙基-2-萘基醚;
[0101]
在一些优选的实施例中,按照本发明的组合物,所述的至少一种的有溶剂可选自:脂肪族酮,例如,2-壬酮、3-壬酮、5-壬酮、2-癸酮、2,5-己二酮、2,6,8-三甲基-4-壬酮、葑酮、佛尔酮、异佛尔酮、二正戊基酮等;或脂肪族醚,例如,戊醚、己醚、二辛醚、乙二醇二丁醚、二乙二醇二乙醚、二乙二醇丁基甲醚、二乙二醇二丁醚、三乙二醇二甲醚、三乙二醇乙基甲醚、三乙二醇丁基甲醚、三丙二醇二甲醚、四乙二醇二甲醚等。
[0102]
在另一些优选的实施例中,按照本发明的组合物,所述的至少一种的有溶剂可选自基于酯的溶剂:辛酸烷酯、癸二酸烷酯、硬脂酸烷酯、苯甲酸烷酯、苯乙酸烷酯、肉桂酸烷酯、草酸烷酯、马来酸烷酯、烷内酯、油酸烷酯等。特别优选辛酸辛酯、癸二酸二乙酯、邻苯二甲酸二烯丙酯、异壬酸异壬酯。
[0103]
所述的溶剂可以是单独使用,也可以是作为两种或多种有机溶剂的混合物使用。
[0104]
在某些优选的实施例中,按照本发明的一种组合物,包含至少一种如上所述的有机化合物,或混合物及至少一种有机溶剂,还可进一步包含另一种有机溶剂。另一种有机溶剂的例子包括(但不限于):甲醇、乙醇、2-甲氧基乙醇、二氯甲烷、三氯甲烷、氯苯、邻二氯苯、四氢呋喃、苯甲醚、吗啉、甲苯、邻二甲苯、间二甲苯、对二甲苯、1,4二氧杂环己烷、丙酮、甲基乙基酮、1,2二氯乙烷、3-苯氧基甲苯、1,1,1-三氯乙烷、1,1,2,2-四氯乙烷、醋酸乙酯、
醋酸丁酯、二甲基甲酰胺、二甲基乙酰胺、二甲基亚砜、四氢萘、萘烷、茚和/或它们的混合物。
[0105]
一些优选的实施例中,特别适合本发明的溶剂是汉森(hansen)溶解度参数在以下范围内的溶剂:δd(色散力)在17.0~23.2mpa1/2的范围,尤其是在18.5~21.0mpa1/2的范围;δp(极性力)在0.2~12.5mpa1/2的范围,尤其是在2.0~6.0mpa1/2的范围;δh(氢键力)在0.9~14.2mpa1/2的范围,尤其是在2.0~6.0mpa1/2的范围。
[0106]
按照本发明的组合物,其中有机溶剂在选取时需考虑其沸点参数。本发明中,所述的有机溶剂的沸点≥150℃;优选为≥180℃;较优选为≥200℃;更优为≥250℃;最优为≥275℃或≥300℃。这些范围内的沸点对防止喷墨印刷头的喷嘴堵塞是有益的。所述的有机溶剂可从溶剂体系中蒸发,以形成包含功能材料薄膜。
[0107]
在一个优选的实施方案中,按照本发明的组合物是一溶液。
[0108]
在另一个优选的实施方案中,按照本发明的组合物是一悬浮液。
[0109]
本发明实施例中的组合物中可以包括0.01wt%至10wt%的按照本发明的化合物或混合物,较好的是0.1wt%至15wt%,更好的是0.2wt%至5wt%,最好的是0.25wt%至3wt%。
[0110]
本发明还涉及所述组合物作为涂料或印刷油墨在制备有机电子器件时的用途,特别优选的是通过打印或涂布的制备方法。
[0111]
其中,适合的打印或涂布技术包括(但不限于)喷墨打印,喷印(nozzle printing),活版印刷,丝网印刷,浸涂,旋转涂布,刮刀涂布,辊筒印花,扭转辊印刷,平版印刷,柔版印刷,轮转印刷,喷涂,刷涂或移印,狭缝型挤压式涂布等。首选的是凹版印刷及喷墨印刷。溶液或悬浮液可以另外包括一个或多个组份例如表面活性化合物,润滑剂,润湿剂,分散剂,疏水剂,粘接剂等,用于调节粘度,成膜性能,提高附着性等。有关打印技术,及其对有关溶液的相关要求,如溶剂及浓度,粘度等。
[0112]
本发明还提供一种如上所述的芳胺类有机化合物、混合物或组合物在有机电子器件中的应用,所述的有机电子器件可选于,但不限于,有机发光二极管(oled),有机光伏电池(opv),有机发光电池(oleec),有机场效应管(ofet),有机发光场效应管,有机激光器,有机自旋电子器件,有机传感器及有机等离激元发射二极管(organic plasmon emitting diode)等,特别优选为oled。本发明实施例中,优选将所述芳胺类有机化合物用于oled器件的电子阻挡层。
[0113]
本发明进一步涉及一种有机电子器件,包含第一电极、第二电极、位于第一电极和第二电极之间的一个或多个有机功能层,所述有机功能层包含如上所述的芳胺类有机化合物、混合物或由上述的组合物制备而成。进一步地,所述有机电子器件,包含阴极、阳极和位于阴极和阳极的一个或多个有机功能层。
[0114]
所述的有机电子器件可选于,但不限于,有机发光二极管(oled),有机光伏电池(opv),有机发光电池(oleec),有机场效应管(ofet),有机发光场效应管,有机激光器,有机自旋电子器件,有机传感器及有机等离激元发射二极管(organic plasmon emitting diode)等,特别优选的是有机电致发光器件,如oled,oleec,有机发光场效应管。
[0115]
按照本发明所述的有机功能层可选自空穴注入层(hil)、空穴传输层(htl)、发光层(eml)、电子阻挡层(ebl)、电子注入层(eil)、电子传输层(etl)、空穴阻挡层(hbl)。适合
用于这些功能层中的材料在上面及在wo2010135519a1、us20090134784a1和wo2011110277a1中有详细的描述,特此将此3篇专利文件中的全部内容并入本文作为参考。
[0116]
在一实施例中所述有机功能层至少包含一电子阻挡层,所述电子阻挡层包含如上所述的芳胺类有机化合物。具体芳胺类有机化合物的定义如前文所述。
[0117]
在一实施例中,按照本发明所述的有机电子器件,其包含的发光层材料为金属配合物,其具有通式(6)所示的结构:
[0118][0119]
其中:
[0120]
q选自1或2;
[0121]
ar7多次出现时,独立选自取代或未取代的环原子数为5至40的杂芳香基团;
[0122]
ar8多次出现时,独立选自取代或未取代的环原子数为6至40的芳香基团,或取代或未取代环原子数为5至40的杂芳香基团;
[0123]r11-r
12
每次出现时,分别独立选自-h、-d、具有1至20个c原子的直链烷基、具有3至20个c原子的支链烷基或环状的烷基、取代或未取代的环原子数为6至60的芳香基、取代或未取代的环原子数为5至60的杂芳香基,或这些基团的组合。
[0124]
在一实施例中,ar7多次出现时,独立选自喹啉或异喹啉及其衍生物。
[0125]
在一实施例中,ar8多次出现时,独立选自苯基及其衍生物。
[0126]
优选地,通式(6)选自通式(7-1)~(7-3)任一结构:
[0127][0128]
其中:
[0129]
a选自0、1、2、3、4、5或6,b选自0、1、2、3或4;
[0130]r13-r
14
每次出现时,分别独立选自-d、具有1至20个c原子的直链烷基、具有3至20个c原子的支链烷基或环状的烷基、取代或未取代的环原子数为6至60的芳香基、取代或未取代的环原子数为5至60的杂芳香基,或这些基团的组合。
[0131]
在一实施例中,至少一个r
13
或r
14
选自具有1至20个c原子的直链烷基或具有3至20个c原子的支链烷基或环状的烷基。
[0132]
在一实施例中,至少一个r
13
选自具有1至20个c原子的直链烷基或具有3至20个c原子的支链烷基或环状的烷基。进一步,至少一个r
14
选自具有1至20个c原子的直链烷基或具有3至20个c原子的支链或环状的烷基。
[0133]
按照通式(6)所述的金属配合物,优选自但不限于如下结构,这些结构上的h可以
被任意取代:
[0134]
[0135][0136]
本发明还涉及按照本发明的电致发光器件在各种电子设备中的应用,包含但不限于,显示设备,照明设备,光源,传感器等等。
[0137]
下面将结合优选实施例对本发明进行了说明,但本发明并不局限于下述实施例,应当理解,所附权利要求概括了本发明的范围在本发明构思的引导下本领域的技术人员应意识到,对本发明的各实施例进行的一定的改变,都将被本发明的权利要求书的精神和范围所覆盖。
[0138]
具体实施例
[0139]
1、按照本发明的化合物的合成方法举例,但本发明并不局限于下述实施例。
[0140]
实施例1:化合物p17合成
[0141][0142]
称取z3(7.6g,25mmol),z4(8.75g,25mmol),碳酸钾(10.35g,75mmol),四(三苯基膦)钯(0.86g,0.75mmol)加入250ml的双口烧瓶,加入甲苯及甲醇的混合溶剂,抽通充氮气三次,升温至90℃,搅拌过夜。待反应液冷却至室温后加水,并用乙酸乙酯萃取,硫酸钠干燥,减压蒸馏除去有机溶剂,硅胶拌样柱层析分离得到目标产物z5共7.15g,产率54%。
[0143]
将化合物z5(6.36g,12mmol)、z6(2.94g,12mmol)溶解在无水甲苯中,加入叔丁醇钠(1.34g,14mmol)及三二亚苄基丙酮二钯(0.33g,0.36mmol),置换氮气三次后,加入三叔丁基膦(0.36mmol),逐渐升温至80℃,搅拌反应12小时,移开热源。待体系冷却后,加入去离子水,分离有机层,并用乙酸乙酯萃取三次,减压下浓缩,过硅胶柱得到6.84g产物p17,产率82%;ms:695[m
+
]
[0144]
实施例2:化合物p29合成
[0145][0146]
称取邻氯苯硼酸(3.9g,25mmol),z9-1(9.8g,25mmol),碳酸钠(6.22g,75mmol),四(三苯基膦)钯(0.58g,0.5mmol)加入250ml的双口烧瓶,加入二氧六环及水的混合溶剂,抽通充氮气三次,升温至90℃,搅拌过夜。减压蒸馏除去有机溶剂,硅胶拌样柱层析分离得到z9共6.37g,产率72%。
[0147]
将中间体z7(8.78g,20mmol)溶解在无水四氢呋喃中,加入乙酸钾(5.88g,60mmol),联硼酸频哪醇酯(5.6g,22mmol)及二氯二三苯基膦钯(0.43g,0.6mmol),升温至回流。搅拌反应12小时,待体系冷却,加入水分离有机相,并用乙酸乙酯萃取三次,减压下浓缩,过硅胶柱得到中间体z8共7.3g,产率75%。
[0148]
称取z8(7.3g,15mmol),z9(5.31g,15mmol),碳酸钾(6.21g,45mmol),四(三苯基膦)钯(0.52g,0.45mmol)加入250ml的双口烧瓶,加入甲苯及甲醇的混合溶剂,抽通充氮气三次,升温至90℃,搅拌过夜。待反应液冷却至室温后加水,并用乙酸乙酯萃取,硫酸钠干燥,减压蒸馏除去有机溶剂,硅胶拌样柱层析分离得到目标产物p29共5.4g,产率53%。ms:
679[m
+
]
[0149]
实施例3:化合物p33合成
[0150][0151]
称取z17(8.32g,15mmol),z17a(4.32g,15mmol),碳酸钾(6.21g,45mmol),四(三苯基膦)钯(0.52g,0.45mmol)加入250ml的双口烧瓶,加入甲苯及甲醇的混合溶剂,抽通充氮气三次,升温至90℃,搅拌过夜。待反应液冷却至室温后加水,并用乙酸乙酯萃取,硫酸钠干燥,减压蒸馏除去有机溶剂,硅胶拌样柱层析分离得到目标产物p33共4.96g,产率46%。ms:719[m
+
]
[0152]
实施例4:化合物p41合成
[0153][0154]
称取z17b(5.39g,10mmol),z17a(2.88g,10mmol),碳酸钾(6.21g,30mmol),四(三苯基膦)钯(0.52g,0.3mmol)加入250ml的双口烧瓶,加入甲苯及甲醇的混合溶剂,抽通充氮气三次,升温至90℃,搅拌过夜。待反应液冷却至室温后加水,并用乙酸乙酯萃取,硫酸钠干燥,减压蒸馏除去有机溶剂,硅胶拌样柱层析分离得到目标产物p41共3.58g,产率51%。ms:703[m
+
]
[0155]
实施例5:化合物p55合成
[0156][0157]
称取z15(6.28g,20mmol),z11(10.3g,20mmol),碳酸钾(8.28g,60mmol),四(三苯基膦)钯(0.7g,0.6mmol)加入250ml的双口烧瓶,加入甲苯及甲醇的混合溶剂150ml,抽通充氮气三次,升温至90℃,搅拌过夜。待反应液冷却至室温后加水,并用乙酸乙酯萃取,硫酸钠干燥,减压蒸馏除去有机溶剂,硅胶拌样柱层析分离得到目标产物p55共8.6g,产率61%。ms:705[m
+
]
[0158]
实施例6:化合物p59合成
[0159][0160]
称取z25a(7.72g,15mmol),z25(3.72g,15mmol),碳酸钾(6.21g,45mmol),四(三苯基膦)钯(0.52g,0.45mmol)加入250ml的双口烧瓶,加入甲苯及甲醇的混合溶剂,抽通充氮气三次,升温至90℃,搅拌过夜。待反应液冷却至室温后加水,并用乙酸乙酯萃取,硫酸钠干燥,减压蒸馏除去有机溶剂,硅胶拌样柱层析分离得到目标产物p59共7g,产率73%。ms:639[m
+
]
[0161]
实施例7:化合物p77合成
[0162][0163]
称取z16(5.96g,20mmol),z17(11.1g,20mmol),碳酸钾(8.28g,60mmol),四(三苯基膦)钯(0.7g,0.6mmol)加入250ml的双口烧瓶,加入甲苯及甲醇的混合溶剂150ml,抽通充氮气三次,升温至90℃,搅拌过夜。待反应液冷却至室温后加水,并用乙酸乙酯萃取,硫酸钠干燥,减压蒸馏除去有机溶剂,硅胶拌样柱层析分离得到目标产物p77共7g,产率48%。ms:729[m
+
]
[0164]
实施例8:化合物p100合成
[0165][0166]
将z18(7.98g,30mmol)溶解在无水四氢呋喃中,降温至-78℃,缓慢加入丁基锂(1.6m,18.8ml)。约0.5小时后向反应瓶中滴加金刚烷酮(4.5g,30mmol)的无水四氢呋喃溶液,在此温度下继续反应半小时,后升至室温,并继续反应8h。减压下除去溶剂,加入盐酸和乙酸,回流约2小时。降至室温,并加入去离子水,后用乙酸乙酯萃取。浓缩后过硅胶柱分离,除去溶剂得到z19共7.39g,产率77%。
[0167]
将z19(6.4g,20mmol)溶解在二氯甲烷中,冰浴下滴加液溴,搅拌2h后停止反应,加入亚硫酸钠水溶液,分液,并用乙酸乙酯萃取,浓缩过硅胶柱得到白色固体z20共6.92g,产率87%。
[0168]
将化合物z20(5.97g,15mmol)、二苯胺(2.54g,15mmol)溶解在无水甲苯中,加入叔丁醇钠(1.73g,18mmol)及三二亚苄基丙酮二钯(0.41g,0.45mmol),置换氮气三次后,加入三叔丁基膦(0.45mmol),逐渐升温至80℃,搅拌反应12小时,移开热源。待体系冷却后,加入去离子水,分离有机层,并用乙酸乙酯萃取三次,减压下浓缩,过硅胶柱得到6g产物z21,产率82%;
[0169]
称取z21(4.87g,10mmol),z3(3.04g,10mmol),碳酸钾(4.14g,30mmol),四(三苯基膦)钯(0.35g,0.3mmol)加入250ml的双口烧瓶,加入甲苯及甲醇的混合溶剂,抽通充氮气三次,升温至90℃,搅拌过夜。待反应液冷却至室温后加水,并用乙酸乙酯萃取,硫酸钠干燥,减压蒸馏除去有机溶剂,硅胶拌样柱层析分离得到目标产物p100共4.76g,产率67%。ms:711[m
+
]
[0170]
实施例9:化合物p135合成
[0171][0172]
称取z3(7.33g,12mmol),z23a(3.65g,12mmol),碳酸钾(5g,36mmol),四(三苯基膦)钯(0.42g,0.36mmol)加入250ml的双口烧瓶,加入甲苯及甲醇的混合溶剂,抽通充氮气三次,升温至90℃,搅拌过夜。待反应液冷却至室温后加水,并用乙酸乙酯萃取,硫酸钠干燥,减压蒸馏除去有机溶剂,硅胶拌样柱层析分离得到目标产物p135共4.65g,产率49%。ms:791[m
+
]
[0173]
实施例10:化合物p144合成
[0174][0175]
将化合物z22(5.5g,20mmol)、z23(9.44g,20mmol)溶解在无水甲苯中,加入叔丁醇钠(2.3g,24mmol)及三二亚苄基丙酮二钯(0.55g,0.6mmol),置换氮气三次后,加入三叔丁基膦(0.6mmol),逐渐升温至80℃,搅拌反应12小时,移开热源。待体系冷却后,加入去离子水,分离有机层,并用乙酸乙酯萃取三次,减压下浓缩,过硅胶柱得到6.93g产物z24,产率52%;
[0176]
称取z24(6.67g,10mmol),z25(2.48g,10mmol),碳酸钾(4.14g,30mmol),四(三苯基膦)钯(0.35g,0.3mmol)加入250ml的双口烧瓶,加入甲苯及甲醇的混合溶剂,抽通充氮气三次,升温至90℃,搅拌过夜。待反应液冷却至室温后加水,并用乙酸乙酯萃取,硫酸钠干燥,减压蒸馏除去有机溶剂,硅胶拌样柱层析分离得到目标产物p144共5.14g,产率65%。ms:791[m
+
]
[0177]
实施例11:化合物p152合成
[0178][0179]
将化合物z26(9.48g,20mmol)、z26a(4.38g,20mmol)溶解在无水甲苯中,加入叔丁醇钠(2.3g,24mmol)及三二亚苄基丙酮二钯(0.55g,0.6mmol),置换氮气三次后,加入三叔丁基膦(0.6mmol),逐渐升温至80℃,搅拌反应12小时,移开热源。待体系冷却后,加入去离子水,分离有机层,并用乙酸乙酯萃取三次,减压下浓缩,过硅胶柱得到5.52g产物z27,产率45%;
[0180]
称取z27(4.9g,8mmol),z22(2.43g,8mmol),碳酸钾(3.31g,24mmol),四(三苯基膦)钯(0.28g,0.24mmol)加入250ml的双口烧瓶,加入甲苯及甲醇的混合溶剂,抽通充氮气三次,升温至90℃,搅拌过夜。待反应液冷却至室温后加水,并用乙酸乙酯萃取,硫酸钠干燥,减压蒸馏除去有机溶剂,硅胶拌样柱层析分离得到目标产物p152共4.44g,产率70%。ms:793[m
+
]
[0181]
实施例12:化合物p176合成
[0182][0183]
称取z28(4.36g,20mmol),z15(6.28g,20mmol),碳酸钾(8.28g,60mmol),四(三苯基膦)钯(0.7g,0.6mmol)加入250ml的双口烧瓶,加入甲苯及甲醇的混合溶剂,抽通充氮气三次,升温至90℃,搅拌过夜。待反应液冷却至室温后加水,并用乙酸乙酯萃取,硫酸钠干燥,减压蒸馏除去有机溶剂,硅胶拌样柱层析分离得到目标产物z29共5.78g,产率64%。
[0184]
将化合物z29(5.42g,12mmol)溶解在无水甲苯中,加入三乙胺,降温至0℃后,滴加三氟甲磺酸酐,反应1小时后升至室温,搅拌过夜。反应完后加入去离子水,分离有机层,并用乙酸乙酯萃取三次,减压下浓缩,过硅胶柱得到5.75g产物z30,产率82%;
[0185]
将化合物z30(4.67g,8mmol)、z31(2.28g,8mmol)溶解在无水甲苯中,加入叔丁醇钠(0.92g,9.6mmol)及三二亚苄基丙酮二钯(0.22g,0.24mmol),置换氮气三次后,加入三叔
丁基膦(0.24mmol),逐渐升温至80℃,搅拌反应12小时,移开热源。待体系冷却后,加入去离子水,分离有机层,并用乙酸乙酯萃取三次,减压下浓缩,过硅胶柱得到3.85g产物p176,产率67%;ms:719[m
+
]
[0186]
实施例13:化合物p200合成
[0187][0188]
将化合物z35(6.22g,15mmol)、z31(4.27g,15mmol)溶解在无水甲苯中,加入叔丁醇钠(1.73g,18mmol)及三二亚苄基丙酮二钯(0.41g,0.45mmol),置换氮气三次后,加入三叔丁基膦(0.45mmol),逐渐升温至80℃,搅拌反应12小时,移开热源。待体系冷却后,加入去离子水,分离有机层,并用乙酸乙酯萃取三次,减压下浓缩,过硅胶柱得到6.25g产物z36,产率69%;
[0189]
称取z36(6.04g,10mmol),z25(2.48g,10mmol),碳酸钾(4.14g,30mmol),四(三苯基膦)钯(0.35g,0.3mmol)加入250ml的双口烧瓶,加入甲苯及甲醇的混合溶剂,抽通充氮气三次,升温至90℃,搅拌过夜。待反应液冷却至室温后加水,并用乙酸乙酯萃取,硫酸钠干燥,减压蒸馏除去有机溶剂,硅胶拌样柱层析分离得到目标产物p213共3.86g,产率53%。ms:728[m
+
]。
[0190]
实施例14:化合物p202合成
[0191][0192]
将化合物z6(3.67g,15mmol)、z37(5.25g,15mmol)溶解在无水甲苯中,加入叔丁醇钠(1.73g,18mmol)及三二亚苄基丙酮二钯(0.41g,0.45mmol),置换氮气三次后,加入三叔丁基膦(0.45mmol),逐渐升温至80℃,搅拌反应12小时,移开热源。待体系冷却后,加入去离子水,分离有机层,并用乙酸乙酯萃取三次,减压下浓缩,过硅胶柱得到4.55g产物z38,产率59%;
[0193]
称取z38(4.12g,8mmol),z3(2.43g,8mmol),碳酸钾(3.31g,24mmol),四(三苯基膦)钯(0.28g,0.24mmol)加入250ml的双口烧瓶,加入甲苯及甲醇的混合溶剂,抽通充氮气三次,升温至90℃,搅拌过夜。待反应液冷却至室温后加水,并用乙酸乙酯萃取,硫酸钠干燥,减压蒸馏除去有机溶剂,硅胶拌样柱层析分离得到目标产物p202共4.06g,产率73%。ms:695[m
+
]。
[0194]
实施例15:化合物p203合成
[0195][0196]
称取z39(4.44g,15mmol),z25(3.72g,15mmol),碳酸钾(6.21g,45mmol),四(三苯基膦)钯(0.52g,0.45mmol)加入250ml的双口烧瓶,加入甲苯及甲醇的混合溶剂,抽通充氮气三次,升温至90℃,搅拌过夜。待反应液冷却至室温后加水,并用乙酸乙酯萃取,硫酸钠干燥,减压蒸馏除去有机溶剂,硅胶拌样柱层析分离得到z40共4.53g,产率72%。
[0197]
将化合物z40(4.2g,10mmol)、z31(2.85g,10mmol)溶解在无水甲苯中,加入叔丁醇钠(1.15g,12mmol)及三二亚苄基丙酮二钯(0.27g,0.3mmol),置换氮气三次后,加入三叔丁基膦(0.3mmol),逐渐升温至80℃,搅拌反应12小时,移开热源。待体系冷却后,加入去离子水,分离有机层,并用乙酸乙酯萃取三次,减压下浓缩,过硅胶柱得到3.88g产物p203,产率58%;ms:669[m
+
]。
[0198]
2、oled器件的制备及表征
[0199]
下面通过具体实施例来详细说明采用上述的oled器件的制备过程。
[0200]
器件中所涉及的化合物结构如下:
[0201][0202]
器件实施例1制备步骤如下:
[0203]
清洗ito导电玻璃阳极层,后用去离子水、丙酮、异丙醇超声清洗15分钟,然后在等离子体清洗器中处理5分钟以提高电极功函。在ito阳极层上,通过真空蒸镀方式蒸镀空穴注入层材料hatcn,厚度为5nm,蒸镀速率在空穴注入层上,通过真空蒸镀方式蒸镀空穴传输材料ht,厚度为90nm。在空穴传输层之上电子阻挡层p17,厚度为20nm。在电子阻挡层上蒸镀发光层,rh作为主体材料,rd作为掺杂材料,rd和rh的质量比为2:98,厚度为40nm。在发光层之上,通过真空蒸镀方式蒸镀电子传输材料et和liq,比例为5:5,厚度为30nm。在电子传输层之上,真空蒸镀电子注入层liq,厚度为2nm。在电子注入层之上,真空蒸镀阴极al层,厚度80nm。
[0204]
器件实施例2至实施例15以及器件比较例1至3的制备方法与器件实施例1基本相同,区别在于:
[0205]
器件实施例2:有机电致发光器件的电子阻挡层变为p29。
[0206]
器件实施例3:有机电致发光器件的电子阻挡层变为p33。
[0207]
器件实施例4:有机电致发光器件的电子阻挡层变为p41。
[0208]
器件实施例5:有机电致发光器件的电子阻挡层变为p55。
[0209]
器件实施例6:有机电致发光器件的电子阻挡层变为p59。
[0210]
器件实施例7:有机电致发光器件的电子阻挡层变为p77。
[0211]
器件实施例8:有机电致发光器件的电子阻挡层变为p100。
[0212]
器件实施例9:有机电致发光器件的电子阻挡层变为p135。
[0213]
器件实施例10:有机电致发光器件的电子阻挡层变为p144。
[0214]
器件实施例11:有机电致发光器件的电子阻挡层变为p152。
[0215]
器件实施例12:有机电致发光器件的电子阻挡层变为p176。
[0216]
器件实施例13:有机电致发光器件的电子阻挡层变为p200。
[0217]
器件实施例14:有机电致发光器件的电子阻挡层变为p202。
[0218]
器件实施例15:有机电致发光器件的电子阻挡层变为p203。
[0219]
器件比较例1:有机电致发光器件的电子阻挡层变为c1。
[0220]
器件比较例2:有机电致发光器件的电子阻挡层变为c2。
[0221]
器件比较例3:有机电致发光器件的电子阻挡层变为c3。
[0222]
表1.器件表征结果
[0223][0224]
表1中发光效率是电流密度为10ma/cm2时所得相对值,lt95是电流密度为10ma/cm2时所得相对值。可以看出,相比器件比较例1至3,器件实施例1至实施例15采用本发明的芳胺化合物作为电子阻挡材料,可以有效的提高有机电致发光器件的发光效率和寿命。苯基相邻基团之间因为位阻作用分子结构会发生扭曲,其在蒸镀后对于载流子的传输比较有利,此外基团的扭转降低了分子内基团间的共轭程度,提高了分子的三线态能级,减少了发光层激子的非辐射跃迁,因此苯基相邻的芳香基团可有效提高器件的发光效率和寿命。且芴与芳胺连接时器件效果有较明显的优势。至于ar3,若其为杂原子稠环,一般来说,该连接位置产生的位阻越大,器件效果提升的越明显,并且通常比ar3为萘或菲的效果更好。
[0225]
以上所述实施例的各技术特征可以进行任意的组合,为使描述简洁,未对上述实施例中的各个技术特征所有可能的组合都进行描述,然而,只要这些技术特征的组合不存
在矛盾,都应当认为是本说明书记载的范围。
[0226]
以上所述实施例仅表达了本发明的几种实施方式,其描述较为具体和详细,但并不能因此而理解为对发明专利范围的限制。应当指出的是,对于本领域的普通技术人员来说,在不脱离本发明构思的前提下,还可以做出若干变形和改进,这些都属于本发明的保护范围。因此,本发明专利的保护范围应以所附权利要求为准。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1