一种透明质酸酶活性检测方法与流程
1.本发明涉及酶活性检测的技术领域,尤其涉及一种透明质酸酶活性检测方法。
背景技术:
2.透明质酸酶(hyaluronidase,haase),也称玻璃酸酶,是一种能够特异性水解透明质酸的酶类的总称。
3.透明质酸酶于1928年被发现,1940年研究确定命名,1948年即被fda批准在美国上市,作为扩散剂与其他药物合用。2004年,fda批准了两种透明质酸酶制剂
‑‑
istapharmaceuticals公司的羊型透明质酸酶(vitrase)和amphastarpharmaceuticals公司的牛型透明质酸酶(amphadase)。2005年底,fda又批准了2种新型透明质酸酶制剂的上市申请,即primapharm公司研制的纯化牛睾丸透明质酸酶(hydase)和halozyme制药有限公司与百特(baxter)公司共同研制的重组人透明质酸酶(hylenex)。
4.美国halozyme公司的重组人透明质酸酶hylenex是采用重组dna技术在cho细胞中高效表达,高度纯化后获得的产品,具有纯度高,免疫原性低等优点,因此快速取代动物提取的透明质酸酶而广泛应用。临床上透明质酸酶与其他注射药物合用,增加后者的吸收和分散,可用于皮下输液,促进手术及创伤后局部水肿或血肿消散以及皮下尿道造影术之中(改善造影剂硫酸钡的再吸收)。透明质酸酶还常与麻药在眼科手术时合用,加快麻醉药的起效速度。此外,全球生物制药巨头如罗氏、强生等公司将重组人透明质酸酶hylenex和其旗下的数个全球销量超过50亿美金的抗体产品联用于肿瘤治疗,将昂贵的抗体给药方式由传统的静脉输液替换为皮下注射,极大的简化了肿瘤病人的治疗方案,大幅降低病人和医疗系统的费用支出。
5.国内上市的透明质酸酶(玻璃酸酶)注射液为上海生化的牛睾丸酶,其检测方法参照中国药典执行,装量为每支1500单位(iu)。
6.透明质酸酶作为一种药品,其最关键的指标即透明质酸酶的酶活。文献中报道,透明质酸盐可以在酸性条件下与血清蛋白络合,形成混悬液,而当透明质酸盐经过透明质酸酶的降解,随着透明质酸盐分子量的降低,它与酸性条件下的血清蛋白的络合能力降低,混悬液浊度下降。根据这一原理,在1957年,针对透明质酸酶酶活测定建立了一项国际标准:牛睾丸透明质酸酶冻干粉与乳糖混合制成片剂,通过浊度法测定酶活。这种方法规定0.1mg的透明质酸酶国际标准制剂的酶活为1iu(international unit)。美国药典(usp)(2002)采用马血清作为与ha反应的沉淀剂。2020版《中国药典》第四部1207《玻璃酸酶测定法》中采用新鲜牛血清或冻干牛血清,先将血清贮备液蒸干然后干燥至恒重后,使得血清固形物含量为1.67%~2%。
7.与采用牛血清或者马血清经过干燥至恒重后重新稀释至一定浓度相比,采用试剂型的牛血清白蛋白直接配制成一定浓度的反应液,试剂更加简单易得,使用方便。
8.相应的,药典中并没有明确作为底物的透明质酸盐的分子量范围,而我们在实践中发现,过高或者过低分子量的透明质酸盐作为底物溶液,无法形成良好的“酶活单位
‑
浊
度”标准曲线。当透明质酸盐分子量过高时,在酸性条件下,高分子透明质酸与牛血清白蛋白络合成团,无法形成稳定的悬浊液,当透明质酸盐分子量过低时,在酸性条件下,低分子透明质酸与牛血清白蛋白形成的浊度过低,干扰酶活测定。
9.专利申请cn202020855194.4《一种细菌透明质酸酶活性检测试剂盒》提供了一种利用dns法测定细菌产透明质酸酶酶活的试剂盒,但是dns法相对于浊度法,根据已有文献oettl m(2000)《biochemische charakterisierung bovinerhyaluronidase und untersuchungen zum einfluβvon hyaluronidase undauf das wachstum von tumoren》报道,dns法所规定的1u与浊度法1000iu相当,因此,dns法灵敏度远低于浊度法的灵敏度。
技术实现要素:
10.为了解决上述问题,本发明提供了一种透明质酸酶活性检测方法,其是采用透明质酸盐作为底物溶液,将透明质酸酶酶解前后的溶液与酸性牛血清白蛋白反应,比较酶解前后浊度的变化,从而精确测定透明质酸酶酶活。
11.本发明具体技术方案如下:
12.1.一种透明质酸酶活性检测方法,其使用分子量为200kda
‑
800kda透明质酸盐作为底物来检测透明质酸酶活性。
13.2.根据项1所述的检测方法,所述方法包括下述步骤:
14.底物溶液配制:使用第一缓冲液配制分子量为200kda
‑
800kda透明质酸盐溶液;
15.酸性牛血清白蛋白溶液的配制:使用第二缓冲液配制牛血清白蛋白溶液,并调节ph范围为3.0~4.0;
16.标准品溶液的配制:将第一缓冲液加入透明质酸酶标准品中得到标准品溶液;
17.供试品溶液的配制:将第一缓冲液加入透明质酸酶供试品中得到供试品溶液;
18.测定:分别使用透明质酸酶标准品溶液和透明质酸酶供试品溶液对底物溶液进行酶解,并将酶解前后的溶液与酸性牛血清白蛋白进行反应,测定在550nm
‑
640nm的吸光度得到供试品的酶活。
19.3.根据项2所述的检测方法,其中,在标准品溶液的配制和供试品溶液的配制步骤中,所述第一缓冲液中加入水解明胶。
20.4.根据项2
‑
3中任一项所述的检测方法,其中,酸性牛血清白蛋白溶液的ph为3.1。
21.5.根据项1
‑
4中任一项所述的检测方法,其中,酶活测定时的吸光度为640nm。
22.6.根据项2
‑
5中任一项所述的检测方法,其中,所述第一缓冲液为磷酸二氢钠
‑
磷酸氢二钠缓冲液或磷酸二氢钾
‑
磷酸氢二钾缓冲液。
23.7.根据项2
‑
6中任一项所述的检测方法,其中,所述透明质酸盐为透明质酸钠或透明质酸钾。
24.8.根据项2
‑
7中任一项所述的检测方法,其中,所述酸性牛血清白蛋白的浓度为0.2
‑
0.4wt%,优选的,所述底物溶液的浓度为0.4
‑
0.6mg/ml。
25.9.根据项2
‑
8中任一项所述的检测方法,其中,所述透明质酸酶标准品溶液为每1ml中含有8
‑
12酶活力单位的溶液。
26.10.根据项2
‑
9中任一项所述的检测方法,其中,所述检测方法检测供试品酶活的
范围为每1ml中含有8
‑
12酶活力单位的溶液。
27.发明的效果
28.本发明所述的检测方法与药典方法相比,采用特定分子量的透明质酸盐作为底物溶液,利用酶解前后的溶液与酸性牛血清白蛋白发生反应,比较酶解前后的浊度变化,从而精确地测定透明质酸酶酶活。
附图说明
29.图1是实施例1中的标准曲线图。
30.图2是实施例2中的标准曲线图。
31.图3是实施例3中的标准曲线图。
32.图4是实施例4中的标准曲线图。
33.图5是实施例5中的标准曲线图。
34.图6是实施例6中的标准曲线图。
35.图7是实施例7中的标准曲线图。
36.图8是对比例1中的标准曲线图。
37.图9是对比例2中的标准曲线图。
38.图10是对比例3中的标准曲线图。
具体实施方式
39.下面结合附图所描述的实施方式对本发明做以详细说明,其中所有附图中相同的数字表示相同的特征。虽然附图中显示了本发明的具体实施例,然而应当理解,可以以各种形式实现本发明而不应被这里阐述的实施例所限制。相反,提供这些实施例是为了能够更透彻地理解本发明,并且能够将本发明的范围完整的传达给本领域的技术人员。
40.需要说明的是,在说明书及权利要求当中使用了某些词汇来指称特定组件。本领域技术人员应可以理解,技术人员可能会用不同名词来称呼同一个组件。本说明书及权利要求并不以名词的差异作为区分组件的方式,而是以组件在功能上的差异作为区分的准则。如在通篇说明书及权利要求当中所提及的“包含”或“包括”为开放式用语,故应解释成“包含但不限定于”。说明书后续描述为实施本发明的较佳实施方式,然而所述描述乃以说明书的一般原则为目的,并非用以限定本发明的范围。本发明的保护范围当视所附权利要求所界定者为准。
41.本发明提供了一种透明质酸酶活检测方法,其使用分子量为200kda
‑
800kda透明质酸盐作为底物来检测透明质酸酶活性。
42.在一个实施方案中,所述检测方法包括下述步骤:
43.底物溶液配制:使用第一缓冲液配制分子量为200kda
‑
800kda透明质酸盐溶液;
44.酸性牛血清白蛋白溶液的配制:使用第二缓冲液配制牛血清白蛋白溶液,并调节ph范围为3.0~4.0;
45.标准品溶液的配制:将第一缓冲液加入透明质酸酶标准品中得到标准品溶液;
46.供试品溶液的配制:将第一缓冲液加入透明质酸酶供试品中得到供试品溶液;
47.测定:分别使用标准品溶液和供试品溶液对底物溶液进行酶解,并将酶解前后的
溶液与酸性牛血清白蛋白进行反应,测定在550nm
‑
640nm的吸光度得到供试品的酶活。所述牛血清白蛋白是牛血清中的一种球蛋白,包含607个氨基酸残基,分子量为66.446kda,等电点为4.7。牛血清白蛋白在生化实验中有广泛的应用。
48.例如,所述透明质酸盐的分子量为200kda、300kda、400kda、500kda、600kda、700kda、800kda等。
49.本发明使用透明质酸盐为底物溶液,采用透明质酸酶酶解底物溶液,并将酶解前后的溶液与酸性牛血清白蛋白发生反应,比较酶解前后浊度的变化,从而精确地测定透明质酸酶的酶活。
50.本发明使用上述特定分子量的透明质酸盐作为底物溶液,防止出现透明质酸盐的分子量过高或者过低导致的测定失败。
51.在一个实施方案中,在标准品溶液的配制和供试品溶液的配制步骤中,所述第一缓冲液中加入水解明胶。
52.所述水解明胶以纯净的明胶50g,加水1000ml,加热至121℃90min,冷冻干燥。
53.在一个实施方案中,所述底物溶液的浓度为0.4
‑
0.6mg/ml。
54.在一个实施方案中,酸性牛血清白蛋白溶液的ph为3.1。
55.在一个实施方案中,酶活测定时的吸光度为640nm。
56.在一个实施方案中,所述第一缓冲液为磷酸二氢钠
‑
磷酸氢二钠缓冲液或磷酸二氢钾
‑
磷酸氢二钾缓冲液。
57.在一个实施方案中,所述透明质酸盐为透明质酸钠或透明质酸钾。
58.使用第一缓冲液配制底物溶液时,当透明质酸盐为透明质酸钠时,使用磷酸二氢钠
‑
磷酸氢二钠缓冲液进行配制,而当透明质酸盐为透明质酸钾时,使用磷酸二氢钾
‑
磷酸氢二钾缓冲液进行配制。
59.在一个实施方案中,所述酸性牛血清白蛋白的浓度为0.2
‑
0.4wt%。
60.例如,所述酸性牛血清白蛋白的浓度可以为0.2wt%、0.3wt%、0.4wt%等。
61.本发明通过使用特定分子量的透明质酸盐作为底物溶液,并使用特定浓度的酸性牛血清白蛋白溶液与酶解前后的溶液进行反应,比较酶解前后的浊度变化,从而精确地测定透明质酸酶的酶活。
62.在一个实施方案中,所述透明质酸酶标准品溶液为每1ml中含有8
‑
12酶活力单位的溶液。
63.优选的,所述透明质酸酶标准品为已标定浊度法酶活的透明质酸酶,优选为上海生化提供的标准透明质酸酶。
64.在一个实施例中,配制一系列的底物溶液,并分别使用透明质酸酶标准品溶液对底物溶液进行水解,酶解结束后,将酶解前后的溶液分别与酸性牛血清白蛋白发生反应,在640nm测定吸光度,从而得到标准曲线。
65.在一个实施方案中,所述检测方法检测供试品酶活的范围为每1ml中含有8
‑
12酶活力单位的溶液。
66.所述的透明质酸酶供试品可以为任何种类的透明质酸酶或者可以降解透明质酸的酶,例如,所述透明质酸酶供试品可以为提取的或异源表达获得的人透明质酸酶、水蛭透明质酸酶、蛇毒透明质酸酶、细菌透明质酸酶等。
67.本发明使用特定分子量的透明质酸盐以及使用特定浓度的酸性牛血清白蛋白,能够防止透明质酸盐的分子量过高从而与牛血清白蛋白产生沉淀的问题,经过精确测定透明质酸酶的酶活,并且与药典中使用的新鲜血清或冻干血清相比,牛血清白蛋白更加方便购买,溶液配制简便。
68.实施例
69.本发明对试验中所用到的材料以及试验方法进行一般性和/或具体的描述,在下面的实施例中,如果无其他特别的说明,%表示wt%,即重量百分数。所用试剂或仪器未注明生产厂商者,均为可以通过市购获得的常规试剂产品。
70.本方法标准酶采购自上海生化的透明质酸酶(玻璃酸酶)注射针剂,装量为每支1500单位(iu)。
71.实施例1
72.(1)底物溶液的配制:
73.a.取磷酸二氢钠(nah2po4·
h2o)2.5g,无水磷酸氢二钠(na2hpo4)1.0g与氯化钠(nacl)8.2g(均精确至0.01g),加水使溶解成1000ml,得到第一缓冲液;
74.b.取预先经五氧化二磷减压干燥48h的分子量为530kda透明质酸钠,加水制成每1ml中含1.0mg的溶液,在0℃以下保存,可稳定3~4周得到透明质酸钠贮备液;
75.c.取透明质酸钠贮备液50ml,用第一缓冲液50ml稀释,配制成浓度每1ml中含0.5mg的溶液,为临用时配制,得到底物溶液。
76.(2)酸性牛血清白蛋白的配制:取醋酸钠11.73g,加水200ml溶解,加冰醋酸20.5ml,加水使成1000ml,得到第二缓冲液;称取2.0g牛血清白蛋白,加入100ml水溶解,加第二缓冲液400ml混匀,制成0.4%的牛血清蛋白溶液,用4mol/l盐酸液调节溶液的ph值至3.1,在冰箱中放置18~24h得到酸性牛血清白蛋白溶液,备用。此液在0~4℃保存,可稳定3~4周。
77.(3)标准品溶液的配制:称取水解明胶330mg(精确至1mg),加第一缓冲液与水各250ml,摇匀,使溶解,在0~4℃保存得到水解明胶溶液。如溶液不发生浑浊,可继续使用。取透明质酸酸酶标准品1支,按标示的单位,加冷的水解明胶稀释液制成每1ml中含10酶活力单位的溶液,临用时配制。
78.(4)供试品溶液的配制:加冷的水解明胶稀释液稀释制成每1ml中约含10酶活力单位的溶液,临用时配制。
79.(5)测定:
80.a.标准曲线的制备:取大小相同的试管12支,按顺序用刻度吸管分别加入标准品溶液0.00、0.10、0.20、0.30、0.40、0.50ml,每份2支,再依次相应加入水解明胶稀释液0.50、0.40、0.30、0.20、0.10、0.00ml,每次间隔30秒钟顺序加入透明质酸钠溶液0.50ml,摇匀,立即置37℃
±
0.5℃水浴中,每管准确保温30分钟,每次间隔30秒钟顺序取出,立即顺序加入酸性牛血清白蛋白溶液4ml,摇匀,在室温放置30分钟,摇匀,照紫外
‑
可见分光光度法,在640nm的波长处测定吸光度。另取试管1支,用刻度吸管加入磷酸盐缓冲液0.50ml及水解明胶稀释液0.50ml,摇匀,按上述方法自“置37℃
±
0.5℃水浴中”起同法操作,作空白。以吸光度为纵坐标,标准品溶液的单位数为横坐标绘标准曲线,计算回归方程式,所述标准曲线如图1所示,其为y=
‑
0.1271x+0.7666,r2=0.9999。
81.b.取大小相同的试管6支,按顺序用移液器分别加供试品溶液稀释液0.20、0.30ml与0.40ml,每份2支,再依次相应加入水解明胶稀释液0.30、0.20ml与0.10ml,使各管的总体积为0.50ml,每次间隔30秒钟顺序加入透明质酸钠溶液0.50ml,摇匀,立即置37℃
±
0.5℃水浴中,每管准确保温30分钟,每次间隔30秒钟顺序取出,立即顺序加入酸性牛血清白蛋白溶液4ml,摇匀,在室温放置30分钟,摇匀,在640nm的波长处测定吸光度。另取试管1支,用刻度吸管加入磷酸盐缓冲液0.50ml及水解明胶稀释液0.50ml,摇匀,按上述方法自“置37℃
±
0.5℃水浴中”起同法操作,作空白。
82.c.由供试品溶液测得的吸光度,先用回归方程式计算各供试品管的单位数(或从标准曲线中查得),再按下式计算:
[0083][0084]
算出6份供试品的平均数,即为透明质酸酶的效价单位,其中,供试品上海生化玻璃酸酶(1500iu/支)的酶活为1514iu。
[0085]
实施例2
[0086]
实施例2和实施例1的区别在于,透明质酸钠的分子量为770kda,标准品溶液为每1ml含有12酶活单位的溶液,得到标准曲线为图2,测试得到供试品上海生化玻璃酸酶(1500iu/支)的酶活为1524iu。
[0087]
实施例3
[0088]
实施例3和实施例1的区别在于,使用的是0.2%的牛血清白蛋白,透明质酸钾的分子量为220kda,相应的缓冲液为磷酸二氢钾、磷酸氢二钾溶液,标准品溶液为每1ml含有8酶活单位的溶液,得到标准曲线为图3,测试得到供试品上海生化玻璃酸酶(1500iu/支)的酶活为1483iu。
[0089]
实施例4
[0090]
实施例4和实施例1的区别在于,使用的是透明质酸钾,透明质酸钾的分子量为490kda,透明质酸钾的底物溶液浓度为0.5mg/ml,相应的缓冲液为磷酸二氢钾、磷酸氢二钾溶液,得到标准曲线为图4,测试得到供试品上海生化玻璃酸酶(1500iu/支)的酶活为1547iu。
[0091]
实施例5
[0092]
实施例5和实施例1的区别在于,使用的是0.6%的牛血清白蛋白,所得到的标准曲线如图5所示,测试得到供试品上海生化玻璃酸酶(1500iu/支)的酶活为1533iu。
[0093]
实施例6
[0094]
实施例6和实施例1的区别在于,使用的是0.2%的牛血清白蛋白,所得到的标准曲线为如图6所示,测试得到供试品上海生化玻璃酸酶(1500iu/支)的酶活为1497iu。
[0095]
实施例7
[0096]
实施例7和实施例1的区别在于,使用的是分子量为220kda的透明质酸钠,所得到的标准曲线为如图7所示,测试得到供试品上海生化玻璃酸酶(1500iu/支)的酶活为1519iu。
[0097]
实施例8重复性的测定
[0098]
按照实施例1中的供试品处理方式,取与实施例1同一批号样品,平行制备6份,标
准品溶液以及检测条件同实施例1相同,测定结果如表2所示。
[0099]
对比例1
[0100]
对比例1和实施例1的区别在于,透明质酸钠的分子量为940kda,得到标准曲线为图8。
[0101]
由图可见,由于采用的透明质酸钠的分子量高,与酸性牛血清白蛋白形成絮状沉淀,降低初始悬浊液的浊度。而当底物透明质酸钠加入透明质酸酶后,分子量有所降低,才可以与酸性牛血清白蛋白形成稳定的悬浊液。因此,以分子量为940kda透明质酸钠为底物溶液制作标准曲线进行透明质酸酶酶活检测不可行。
[0102]
对比例2
[0103]
对比例2和实施例1的区别在于,透明质酸钠的分子量为150kda,得到标准曲线为图9。
[0104]
由图可见,由于采用低分子量透明质酸钠,当透明质酸酶加至4iu时,a640已经接近为0,无法做出酶活
‑
a640标准曲线。
[0105]
对比例3
[0106]
对比例3和实施例1的区别在于,标准品溶液为每1ml含有15酶活单位的溶液,得到标准曲线为图10。
[0107]
由图可见,由于加入的透明质酸酶酶活过量,当透明质酸酶加至6iu时,a640已经接近为0,无法做出酶活
‑
a640标准曲线。
[0108]
表1实施例1
‑
7和对比例1
‑
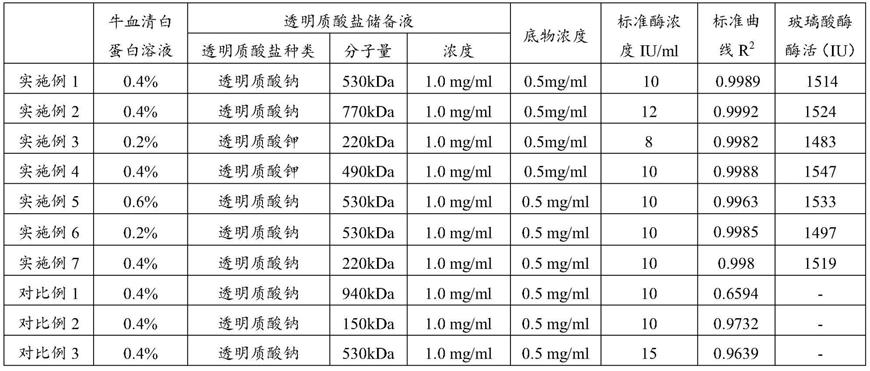
3所用到的工艺条件及测试的酶活表
[0109][0110]
表2实施例8玻璃酸酶酶活的测定结果
[0111][0112][0113]
从表2可以看出,采用本发明所述的方法进行测定,稳定性较好。
[0114]
实验例1
[0115]
以实施例1方法测定芽孢杆菌(bacillus sp.)a50 cgmcc no.5744产透明质酸酶酶制剂(标准10000iu/ml),测定结果为10254iu/ml。
[0116]
实验例2
[0117]
以实施例1方法测定sigma货号h3757牛睾丸酶(标示300
‑
1000u/mg),测定结果为869iu/mg。
[0118]
综上所述,采用特定分子量的透明质酸盐作为底物溶液,并使用酸性牛血清白蛋白与酶解前后的溶液进行反应,根据酶解前后溶液的浊度变化能够准确测出透明质酸酶的酶活。
[0119]
以上所述,仅是本发明的较佳实施例而已,并非是对本发明作其它形式的限制,任何熟悉本专业的技术人员可能利用上述揭示的技术内容加以变更或改型为等同变化的等效实施例。但是凡是未脱离本发明技术方案内容,依据本发明的技术实质对以上实施例所作的任何简单修改、等同变化与改型,仍属于本发明技术方案的保护范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1