一种氢取代石墨单炔材料及其制备方法和应用
1.本发明涉及碳材料领域,具体涉及一种氢取代石墨单炔材料及其制备方法和应用。
背景技术:
2.自从c
60
的发现者获得了诺贝尔奖后,碳材料在近几十年引起了许多科研工作者的关注,大家更致力于发现新的碳材料,例如碳纳米管、石墨烯等。石墨炔作为一种由sp和sp2杂化形成新型二维碳材料,早在1987年baughman首次从理论上预测了其能够稳定存在,其结构可视为由苯环和炔键交替连接形成的具有二维平面网络结构的全碳分子。理论计算表明,石墨炔材料存在dirac锥结构,具有超高载流子迁移率和量子霍尔效应,在能源领域具有广阔的应用前景。
3.氢取代石墨单炔是在石墨炔的基础之上提出来的一种新型的富碳材料,是由sp杂化的炔基将苯环间位连接,形成二维平面网状结构。结构中除了碳元素的存在之外,还含有一定比例的氢元素。该结构所含的网孔较大,有利于离子或分子的迁移,在锂离子电池充放电、电催化反应中具有较大的应用潜力。
4.虽然石墨炔在理论计算和化学合成上处于研究热潮,但目前有关于氢取代石墨单炔材料的合成和研究却非常少,而且申请人发现目前合成氢取代石墨单炔材料的反应方法中或多或少存在一些不足之处,比如前体分子大气稳定性差、反应时间漫长、反应温度较高等问题,真正意义上的氢取代石墨单炔材料的合成问题并没有得到实质性的解决。
技术实现要素:
5.本发明的目的就是为了克服上述现有技术存在的缺陷而提供一种降低制备的成本以及难度的氢取代石墨单炔材料及其制备方法和应用。
6.本发明的目的可以通过以下技术方案来实现:
7.本发明是针对目前氢取代石墨单炔材料所选用的前体分子大气稳定性差、反应时间漫长、反应温度较高等问题而提出一种全新的氢取代石墨单炔材料的制备方法,来降低氢取代石墨单炔材料制备的成本以及难度,具体方案如下:
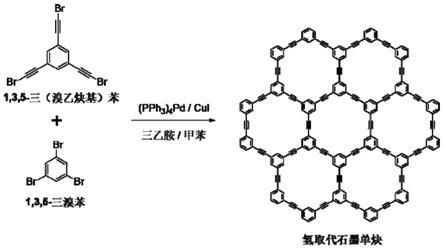
8.一种氢取代石墨单炔材料的制备方法,该方法为:在惰性气氛保护下,将1,3,5
‑
三(溴乙炔基)苯和1,3,5
‑
三溴苯进行脱氧处理,再在溶剂环境中,催化剂和有机胺的氛围下,进行交叉偶联反应,得到氢取代石墨单炔。
9.进一步地,所述的催化剂包括四(三苯基膦)钯和/或碘化亚铜。
10.进一步地,所述的1,3,5
‑
三(溴乙炔基)苯和1,3,5
‑
三溴苯的摩尔比为(1
‑
3):1。
11.进一步地,所述的溶剂包括甲苯,所述的有机胺包括三乙胺。
12.进一步地,所述的溶剂与有机胺的体积比为(0.5
‑
2):1。
13.进一步地,所述的1,3,5
‑
三(溴乙炔基)苯的初始摩尔浓度为(1.3
‑
1.6)
×
10
‑2mol/l。
14.进一步地,所述的惰性气氛为氮气,所述交叉偶联反应的温度为75
‑
85℃,时间为8
‑
15h。
15.进一步地,该方法包括以下步骤:
16.(1)将1,3,5
‑
三(溴乙炔基)苯、1,3,5
‑
三溴苯和催化剂在反应器中混合,并进行无水、无氧处理;
17.(2)接着,向反应体系中加入三乙胺和溶剂,置于惰性气氛环境中,进行交叉偶联反应;
18.(3)反应停止后,将产物清洗、干燥后,得到黄棕色的氢取代石墨单炔。
19.一种如上所述方法制备的氢取代石墨单炔材料。
20.一种如上所述的氢取代石墨单炔材料的应用,该材料可应用于海水淡化、电催化材料或能源材料领域。
21.与现有技术相比,本发明具有以下优点:
22.(1)本发明前体分子具有更高的稳定性和反应选择性,能够在大气环境中稳定存在,能够减少偶联过程中副产物的产生,利于高效制备氢取代石墨单炔材料;
23.(2)本发明相较于以往的制备条件,反应时间缩短,且原料廉价易得。
附图说明
24.图1为实施例1中的氢取代石墨单炔的扫描电镜图(sem);
25.图2为实施例1中的氢取代石墨单炔的拉曼光谱;
26.图3为实施例1中的氢取代石墨单炔的红外光谱;
27.图4为实施例1中的氢取代石墨单炔的x射线衍射图谱(xrd);
28.图5为实施例1中的氢取代石墨单炔的x射线光电子能谱(xps)全谱图;
29.图6为实施例1中的氢取代石墨单炔的x射线光电子能谱(xps)高分辨碳谱图;
30.图7为实施例1中的氢取代石墨单炔的接触角测试;
31.图8为实施例1中的氢取代石墨单炔的热重曲线;
32.图9为实施例1中的氢取代石墨单炔的紫外可见漫反射吸收光谱;
33.图10为本发明交叉偶联合成氢取代石墨单炔的制备过程示意图。
具体实施方式
34.下面结合附图和具体实施例对本发明进行详细说明。本实施例在以本发明技术方案为前提下进行实施,给出了详细的实施方式和具体的操作过程,但本发明的保护范围不限于下述的实施例。
35.一种氢取代石墨单炔材料的制备方法,该方法包括以下步骤:
36.(1)将1,3,5
‑
三(溴乙炔基)苯、1,3,5
‑
三溴苯和催化剂在反应器中混合,并进行无水、无氧处理;其中,催化剂包括四(三苯基膦)钯和/或碘化亚铜。1,3,5
‑
三(溴乙炔基)苯和1,3,5
‑
三溴苯的摩尔比为(1
‑
3):1;
37.(2)接着,向反应体系中加入三乙胺和溶剂,置于惰性气氛环境中,进行交叉偶联反应;溶剂包括甲苯,所述的有机胺包括三乙胺。溶剂与有机胺的体积比为(0.5
‑
2):1。其中,1,3,5
‑
三(溴乙炔基)苯的初始摩尔浓度为(1.3
‑
1.6)
×
10
‑2mol/l。惰性气氛为氮气,所
述交叉偶联反应的温度为75
‑
85℃,时间为8
‑
15h;
38.(3)反应停止后,将产物清洗、干燥后,得到黄棕色的氢取代石墨单炔。
39.实施例1
40.在25ml的三颈瓶中容器中,加入1,3,5
‑
三(溴乙炔基)苯(40mg,0.1mmol)、1,3,5
‑
三溴苯(32mg,0.1mmol)、四(三苯基膦)钯和碘化亚铜,并进行无水、无氧处理;
41.接着向反应体系中加入6ml的三乙胺和6ml的甲苯,置于80℃,n2的环境中,反应10h。
42.反应停止后,用离心机离心出固体产物,并将产物依次用二氯甲烷、乙醇、丙酮、氨水、丙酮溶液多次清洗,再将产物进行干燥,得到黄棕色的粉末,即为hsgy。
43.样品的sem图(图1)显示出材料的表面形貌呈球状颗粒无规则的团聚,比较符合粉末材料的形貌特点。
44.样品的拉曼光谱(图2)显示出有三个吸收峰,分别是1352cm
‑1、1593cm
‑1、2215cm
‑1、1352cm
‑1的峰是d峰对应的是缺陷和边缘;1593cm
‑1的峰为g峰,是sp2杂化碳原子的特征峰,表明了样品中拥有丰富的芳香环结构;2215cm
‑1处的特征峰归因于共轭二炔的伸缩振动。
45.红外光谱(图3)中与前体分子的红外光谱相比,也同样显示出2188cm
‑1的炔基特征峰的出现以及c
‑
br的特征峰减少,与拉曼结果相符。
46.x射线衍射谱(xrd)(图4)表明样品为无定形碳材料,由布拉格方程得该材料的层间距为
47.x射线光电子能谱(xps)(图5)表明所制备的氢取代石墨单炔材料含有最主要的元素是碳元素,且为sp2和sp杂化。元素o的存在可归因于空气的吸附、炔基氧化产生的少量含氧官能团和缺陷等。元素pd、cu的存在可归因于催化剂在样品表面的残留等。
48.在对c1s进行分峰拟合的过程(图6),其中对应的sp2和sp杂化碳的面积之比约为2:1,与理论值γ
‑
hsgy(n=2)结构中的面积比一致。
49.样品的接触角测试结果(图7)显示该材料具有良好的疏水性,接触角为118
°
。
50.样品的热重曲线(图8)显示出该材料在氮气气氛中于120℃左右开始失重,直到700℃时,失重百分比约为37.10%。其中在120℃开始有轻微的热失重现象的发生,产生该现象的原因是由于在样品粉末材料的表面吸附的水分子,以及在后处理过程中会有一小部分的有机小分子残留在粉末中由于温度升高造成挥发而出现质量减少的现象。当温度继续升高至320℃左右时失重速率相比较之前开始加快,在该温度阶段发生的失重与石墨烯类材料相类似,其主要原因是由于在该温度下结构中碳骨架的煅烧。
51.样品带隙通过紫外漫反射吸收光谱测试(图9),结果显示样品的带隙为1.86ev。
52.以上所述,仅是本发明的较佳实施例而已,并非是对本发明作其它形式的限制,任何熟悉本专业的技术人员可能利用上述揭示的技术内容加以变更或改型为等同变化的等效实施例。但是凡是未脱离本发明技术方案内容,依据本发明的技术实质对以上实施例所作的任何简单修改、等同变化与改型,仍属于本发明技术方案的保护范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1