一种Os-Pd双金属有机分子笼及其制备方法与应用
一种os-pd双金属有机分子笼及其制备方法与应用
技术领域
1.本发明属于有机分子笼材料技术领域。更具体地,涉及一种os-pd双金属有机分子笼及其制备方法与应用。
背景技术:
2.放射治疗(以下简称放疗)是利用高能电磁辐射根除恶性肿瘤的一种治疗方法,近年来被广泛应用于临床肿瘤治疗的第一线。放疗具有无创、无深度限制、全身毒性低的优点,使其成为临床治疗的主要手段之一。然而,由于肿瘤细胞的放射抗性,放疗在临床上的疗效往往受到限制。为了克服这一局限性,科学家提出了放射增敏剂的概念,放射增敏剂可以与放疗结合,通过提高肿瘤细胞对放疗的敏感性来增强对肿瘤细胞的杀伤效果。
3.在过去的几年里,不同成分的放射增敏剂,由于其具有优异的x射线能量吸收能力和进一步将辐射能量沉积到肿瘤细胞的能力而引起了极大的关注。含重金属材料的放射增敏剂由于能够增强光电效应和康普顿效应,减少辐射剂量和对正常组织的损伤而得到迅速发展。
4.金属-有机分子笼(mocs)是由金属离子与有机配体在配位作用驱动下组装而成的具有特定尺寸和空腔的分立笼状三维寡聚体,研究发现其可以作为放射增敏剂用于化疗中。其中,mocs可以根据空腔的大小,通过特定的主客体相互作用来封装药物小分子,达到药物传递、定向转运、缓释等作用,但大多数mocs的激发波长与发射波长都相对较短,当激发波长较短时,在生物体上穿透能力弱,限制材料在生物体里被激发的能力;当发射波长较短时,由于生物体自身发蓝绿光,材料发射光会与自身荧光形成干扰,严重阻碍生物学应用范围。如中国专利申请公开了一种超分子笼配合物,该超分子笼配合物具有一定的荧光性能,但其发射波长在418nm附近,属于短波长的蓝光区,短波长对组织的渗透作用差,而且对组织细胞的伤害也高,在生物成像和药物传递方面的应用受到限制。
技术实现要素:
5.本发明要解决的技术问题是克服现有荧光mocs的激发波长与发射波长在短波长范围,造成其在生物成像和药物传递方面的应用受到限制的缺陷和不足,提供一种在近红外光发射、具有优异细胞溶酶体靶向和肿瘤细胞靶向作用的os-pd双金属有机分子笼。
6.本发明的目的是提供一种os-pd双金属有机分子笼的制备方法。
7.本发明的另一目的是提供一种os-pd双金属有机分子笼在制备抗肿瘤药物中的应用。
8.本发明的另一目的是提供一种抗肿瘤药物。
9.本发明的上述目通过以下技术方案实现:
10.一种os-pd双金属有机分子笼,结构式如式(ⅰ)所示:
[0011][0012]
本发明进一步保护os-pd双金属有机分子笼的制备方法,包括如下步骤:
[0013]
s1.将(nh4)2oscl6和有机配体l溶于有机溶剂中,加热至150~250℃反应完全,冷却、分离后加入nabf4溶液反应完全,后处理得osl3;
[0014]
s2.将步骤s1所得osl3溶于有机溶剂中得溶液a,钯盐溶于有机溶剂中得溶液b,将溶液a与溶液b混合均匀后加热至50~100℃反应完全,后处理,即得;
[0015]
其中,有机配体l的结构式如式(ⅱ)所示:
[0016][0017]
优选地,在步骤s1中,所述(nh4)2oscl6和有机配体l的摩尔比为1:(2~4)。
[0018]
优选地,在步骤s1中,所述nabf4与(nh4)2oscl6的摩尔比为1:(2~4)。
[0019]
优选地,在步骤s1中,所述加热的方法为微波加热,功率为75~150w。
[0020]
更优选地,所述微波加热的时间为10~20min。
[0021]
优选地,在步骤s1中,所述分离的方法为先用水稀释,再离心。
[0022]
更优选地,所述水为超纯水。
[0023]
优选地,在步骤s1中,所述后处理的步骤为离心收集沉淀、洗涤、丙酮萃取、干燥、柱层析分离得到粗产物,将粗产物用乙腈-水混合溶液溶解,加入nabf4的饱和溶液析出沉淀,再次离心收集、沉淀、洗涤、丙酮萃取、干燥。
[0024]
更优选地,所述乙腈-水混合溶液中乙腈与水的体积比为1:(0.5~2)。
[0025]
更优选地,所述干燥的温度为40~100℃,时间为12~24h。
[0026]
优选地,在步骤s2中,所述钯盐包括pd(ch3cn)4(bf4)2、pd(no3)2。
[0027]
更优选地,在步骤s2中,所述钯盐为pd(ch3cn)4(bf4)2。
[0028]
优选地,在步骤s2中,所述osl3与钯盐的摩尔比为1:(0.5~2)。
[0029]
优选地,在步骤s2中,所述反应的时间为2~8h。
[0030]
优选地,在步骤s2中,所述后处理的步骤为:先加入乙酸乙酯析出沉淀,再离心收集沉淀、洗涤、干燥。
[0031]
优选地,在步骤s1、s2中,所述有机溶剂为乙二醇、dmso、乙醇、dmf、乙腈中的一种或多种。
[0032]
本发明进一步保护os-pd双金属有机分子笼在制备抗肿瘤药物中的应用。
[0033]
优选地,所述os-pd双金属有机分子笼作为载体,负载小分子药物。
[0034]
更优选地,所述小分子药物包括香豆素、沙利度胺或苯丙酸氮芥。
[0035]
优选地,所述os-pd双金属有机分子笼有近红外发射和x射线增敏的性质。
[0036]
本发明进一步保护一种抗肿瘤药物,包括所述os-pd双金属有机分子笼。
[0037]
优选地,所述os-pd双金属有机分子笼的结构为具有空腔的八面体结构。
[0038]
本发明制备得到的os-pd双金属有机分子笼具有明确的空腔,小分子药物与os-pd双金属有机分子笼可以通过范德华力、π-π堆积、氢键等非共价作用力将小分子药物包载在os-pd双金属有机分子笼的空腔内形成主客体结构。包载小分子药物的os-pd双金属有机分子笼以胶束的形式通过高通透性和滞留效应靶向到达肿瘤细胞的溶酶体,在溶酶体的酸性环境下,胶束经过x光照射产生单线态氧,破坏溶酶体膜结构,释放小分子药物,从而实现协同放疗和化疗的作用,加速癌细胞死亡。
[0039]
锇(ii)金属配合物具有近红外发射的优点,引入锇(ii)金属配合物使制备得到的os-pd双金属有机分子笼同时具有近红外发射和x射线敏化的性质,其在x射线辐射下能产生单线态氧,使其具有辐射增敏作用,达到增强杀死肿瘤细胞的作用。
[0040]
与现有技术相比,本发明具有以下有益效果:
[0041]
本发明制备得到的os-pd双金属有机分子笼具有近红外发射和x射线敏化的性质,其在x射线辐射下能产生单线态氧,使其具有辐射增敏作用,达到增强杀死肿瘤细胞效果的作用。本发明分子笼的空腔可以包载抗癌药物形成主客体结构,主客体结构以胶束的形式实现细胞溶酶体靶向和肿瘤靶向的作用,显著增强肿瘤靶向性;并且,药物被包载后生物毒性减小,降低了对正常组织细胞的损害,从而减轻药物的毒副作用。
附图说明
[0042]
图1为实施例1所得osl3的1h nmr图谱。
[0043]
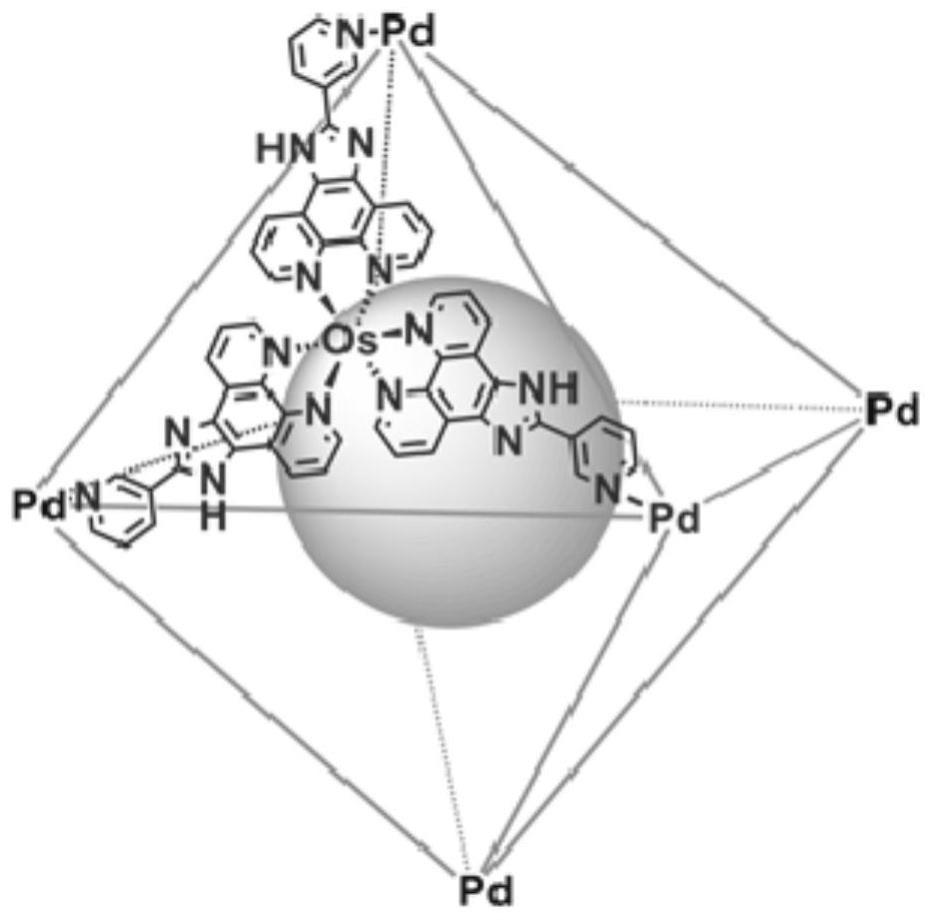
图2为实施例1所得os-pd双金属有机分子笼的结构图。
[0044]
图3为实施例1所得os-pd双金属有机分子笼的1h nmr图谱。
[0045]
图4为实施例1所得os-pd双金属有机分子笼的1h-1
h cosy图谱。
[0046]
图5为实施例1所得os-pd双金属有机分子笼的高分辨质谱图。
[0047]
图6为实施例2中os-pd双金属有机分子笼与香豆素的核磁滴定图。
[0048]
图7为实施例2中os-pd双金属有机分子笼与香豆素主客体的hill方程滴定曲线。
[0049]
图8为实施例2中os-pd双金属有机分子笼与香豆素主客体的job曲线。
[0050]
图9为实施例3中os-pd双金属有机分子笼与香豆素主客体复合物的纳米粒子合成示意图。
[0051]
图10为实施例3所得纳米粒子的透射电镜图。
[0052]
图11为实施例3所得纳米粒子的水合粒径图。
[0053]
图12为实施例3所得纳米粒子的x光辐射细胞毒性图。
[0054]
图13为实施例3所得纳米粒子协同治疗后的肿瘤体积变化图。
[0055]
图14为实施例3所得纳米粒子协同治疗后的肿瘤重量变化图。
具体实施方式
[0056]
以下结合说明书附图和具体实施例来进一步说明本发明,但实施例并不对本发明做任何形式的限定。除非特别说明,本发明采用的试剂、方法和设备为本技术领域常规试剂、方法和设备。
[0057]
除非特别说明,以下实施例所用试剂和材料均为市购。
[0058]
实施例1 os-pd双金属有机分子笼的制备
[0059]
反应路线如下:
[0060][0061]
1.有机配体l的合成:
[0062]
将1,10-邻二氨杂菲-5,6-二酮(210g/mol,10mmol,2.1g)和醋酸铵(77g/mol,200mmol,15.4g)加入到100ml的单口圆底烧瓶中,然后加入40ml冰醋酸,在120℃的油浴中加热10min溶解至澄清溶液,再加入1.59ml吡啶-3-甲醛,在120℃下反应3h得反应液,将反应液转移到200ml的烧杯中,加入100ml蒸馏水,冷却至室温,在磁力搅拌下加入浓氨水中和至ph=7左右,出现大量黄色的沉淀,抽滤,蒸馏水洗涤三次后,置于100℃烘箱中烘干得到。
[0063]
2.化合物osl3的合成:
[0064]
向配有磁力搅拌子的50ml圆底烧瓶里加入(nh4)2oscl6(87.8mg,0.2mmol)和有机配体l(178.4mg,0.6mmol),然后加入20ml乙二醇超声溶解,装上空气冷凝管,于200℃下微波(100w)加热回流15min后得黑色粘稠液体,冷却至室温并用等体积超纯水稀释,离心除去不溶物,向上清液中加入5ml nabf4的饱和溶液,立即有大量棕黑色沉淀析出,继续搅拌2h后将沉淀离心收集,水洗后用丙酮萃取,得黑绿色溶液,旋蒸除去丙酮,50℃下真空干燥过夜,得粗产物。
[0065]
将上述粗产物用乙腈-水(2:1,v/v)混合溶剂恰好溶解,加入20ml层析用硅胶(300目,下同),使产物充分被吸附后旋蒸除去溶剂,将得到的硅胶样品小心加在乙腈中装好的硅胶柱顶端,用乙腈:水:饱和硝酸钾溶液=16:3:1将黑绿色带完全冲下并收集,旋蒸除去
乙腈后水相有大量黑色固体,将此固体收集,水洗(10ml
×
3)后用乙腈-水(1:1,v/v)混合溶剂恰好溶解,向其中加入5ml nabf4的饱和溶液,得到大量棕黑色沉淀,离心收集并用水洗涤(10ml
×
5),用丙酮萃取得黑绿色溶液,旋蒸除去溶剂,于50℃下真空干燥过夜得黑色固体产物osl3。
[0066]
谱图如图1所示:δ4.37(s,3h),9.52(s,3h),8.85(d,j=7.6hz,6h),8.74(d,j=4.4hz,3h),8.63(d,j=7.6hz,3h),7.94(d,j=5.2hz,6h),7.63-7.59(m,9h).
[0067]
3.os-pd双金属有机分子笼的合成:
[0068]
向配有磁力搅拌子的50ml圆底烧瓶中先后加入6ml osl3(251.1mg,0.2mmol)的dmso溶液和2ml pd(ch3cn)4(bf4)2(66.7mg,0.15mmol)的dmso溶液,于80℃下搅拌5h,然后向体系中加入30ml乙酸乙酯,得到大量黑色沉淀,经离心、洗涤和干燥后得224.0mg黑色粉末状固体。
[0069]
os-pd双金属有机分子笼的结构如图2所示:本发明的os-pd双金属有机分子笼呈八面体结构,具有明确的空腔。
[0070]
核磁谱图如图3所示:δ10.03(s,24h),9.18(s,24h),8.70(d,j=7.2hz,24h),8.59(d,j=7.6hz,24h),8.47(d,j=7.2hz,24h),7.86(s,24h),7.74(m,48h),7.39(m,24h),7.31(m,24h);
[0071]1h-1
h cosy谱图如图4所示,为了对本发明的双金属有机分子笼的质子峰进行准确的归属,通过分析图中相近碳原子上质子的相互耦合情况,对os-pd双金属有机分子笼上的七组峰进行了准确的归属(标峰a-f),归属图与1h nmr中一一对应。
[0072]
高分辨质谱图如图5所示:m/z[c
432h265n120b22f88
pd6os8]
7+
{[pd6(osl3)8]
28+
+hbf4+21bf
4-}1600.9384;[c
432h265n120b21f84
pd6os8]
8+
{pd6(osl3)8]
28+
+hbf4+20bf
4-}1389.9454;[c
432h265n120b20f80
pd6os8]
9+
{[pd6(osl3)8]
28+
+hbf4+19bf
4-}1225.8397;[c
432h265n120b19f76
pd6os8]
10+
{[pd6(osl3)8]
28+
+hbf4+18bf
4-}1094.6550;[c
432h264n120b17f68
pd6os8]
11+
{[pd6(osl3)8]
28+
+17bf
4-}979.2316;[c
432h264n120b16f64
pd6os8]
12+
{[pd6(osl3)8]
28+
+16bf
4-}890.3796。
[0073]
实施例2 os-pd双金属有机分子笼与香豆素主客体的制备
[0074]
将20eq香豆素的粉末(客体)加入0.5mm os-pd双金属有机分子笼(主体)的重水溶液中,在室温下超声10min,离心过滤除去不溶解的客体分子后,通过1h nmr氢谱表征,谱图如图6所示:在os-pd双金属有机分子笼体系中加入客体香豆素后,os-pd双金属有机分子笼与香豆素主客体中的香豆素与单独香豆素的核磁谱图相比化学位移明显向高场移动。说明双金属有机分子笼对客体香豆素具有明显的主客体作用。
[0075]
图6中的coumarin为香豆素,moc-43为os-pd双金属有机分子笼,coumarin moc-43为os-pd双金属有机分子笼与香豆素主客体。
[0076]
1、hill方程滴定
[0077]
为了确定os-pd双金属有机分子笼与香豆素之间的结合常数,在os-pd双金属有机分子笼浓度不变(0.5mmol/l)的条件下,将其和不同浓度的香豆素溶液中进行1h nmr滴定。分别制备一定浓度的双金属有机分子笼、香豆素溶液,然后将香豆素溶液依次加入到os-pd双金属分子笼溶液中,主客体复合物在反应平衡10分钟后再做核磁测试。
[0078]
利用hill方程对所得数据进行进一步处理,利用非线性曲线拟合方法估计出主客
体的缔合常数ka(计算公式为:),以对log[g]作图可得一条直线。其中θ为饱和度,是任意客体浓度下主体g质子化学位移的变化与滴定终点时该质子化学位移的变化之比;[g]为任意时刻体系中客体的浓度,单位mol l-1
;ka为主客体平均结合常数,单位l mol-1
;n为hill系数,是衡量体系中客体分子对主体结合的协同作用的参数。如图7所示,可知主客体的平均结合常数为432l mol-1
。
[0079]
2.job曲线
[0080]
配制os-pd双金属有机分子笼溶液(2m m)的氘代溶液和香豆素溶液(2mm)作为储备液(dmso/d2o=1:3,v/v)。精密量取2mm香豆素储备液0、240、360、420、450、480、510、540、552、570、600ul于2.0ml离心管中,再依次加入2mm双金属有机分子笼溶液储备液600、360、240、180、150、120、90、60、48、30、0ul于上述香豆素溶液中。固定主体和客体的总浓度为2mm不变,溶液在10分钟内达到平衡后记录1h nmr,如图8所示,用得到的数据中客体的摩尔分数作为横坐标,客体的摩尔分数和相对于自由客体的化学位移变化值的乘积作为纵坐标绘制job曲线。从图中可以看出随着客体香豆素的摩尔分数的逐渐增加至0.8时(os-pd双金属有机分子笼的摩尔分数为0.2),纵坐标的变化在出现最大值,也就是说主-客体的结合比是1:4,即一个os-pd双金属有机分子笼能包合4个香豆素分子。
[0081]
实施例3 os-pd双金属有机分子笼与香豆素主客体纳米粒子(cmnps)的制备
[0082]
将香豆素与双金属有机分子笼按照1:20的摩尔比在重水环境中超声10min,然后将混合溶液冻干,再将冻干粉末溶于1ml dmso中,再与1ml含20mg dspe-peg2000的氯仿溶液混合,得到澄清溶液b。澄清溶液b迅速注入20ml去离子水(di水)中。采用微针探头超声对水中有机组分进行5分钟的强力分散。然后立即将澄清溶液b减压旋转蒸发除去氯仿,用透析袋纯化24h。最后,用100kda的超滤膜过滤,浓缩至5mg/ml,4℃冰箱保存备用。合成过程如图9所示。
[0083]
纳米粒子的表征:
[0084]
用透射电镜(tem)观察实施例2制备得到的纳米粒子(cmnps)形貌,操作步骤如下:取2ul纳米粒子(cmnps)的水溶液(0.2mg/ml)滴在纯碳膜铜网上,在室温下晾干后,再用3%的醋酸铀染色2min,在球差电镜下观察。如图10所示可知纳米粒子(cmnps)的粒径在38~40nm范围内。
[0085]
用zeta电位及粒度测定仪检测纳米粒子(cmnps)的粒径,粒径值取三次测量的平均值。如图11所示,其粒径为42nm。
[0086]
实施例4 辐射增敏的细胞毒性测试
[0087]
os-pd双金属有机分子笼纳米粒子(mnps)的制备
[0088]
将双金属有机分子笼按在重水环境中超声10min,然后将溶液冻干,再将冻干粉末溶于1ml dmso中,再与1ml含20mg dspe-peg2000的氯仿溶液混合,得到澄清溶液c。澄清溶液c迅速注入20ml去离子水(di水)中。采用微针探头超声对水中有机组分进行5分钟的强力分散。然后立即将澄清溶液c减压旋转蒸发除去氯仿,用透析袋纯化24h。最后,用100kda的超滤膜过滤,浓缩至5mg/ml,4℃冰箱保存备用。
[0089]
采用细胞计数试剂(cck-8)法测定纳米粒子(mnps和cmnps)在x射线照射或未照射下的细胞毒性。4t1细胞以每孔10000个细胞的密度接种于96孔板,孵育12h,获得贴壁细胞
(pbs组);用含纳米粒子0.5mg/ml的新鲜培养基替代细胞培养液,培养12h,分别得到mnps组和cmnps组。
[0090]
然后将三组分别用3gy或6gy x射线照射,孵育24h后,每孔加入10μl cck-8溶液,在37℃下孵育2h。按照制造商的说明书进行cck-8检测。如图12所示,当辐射剂量从3gy增加到6gy时,pbs组的4t1细胞活力未见明显下降。相比之下,mnps和cmnps组在x射线照射下对4t1细胞均表现出剂量依赖性的抗增殖活性,表明moc-43具有良好的放射增敏作用。cmnps的4t1细胞活力比mnps的还低,说明主客体结构能进一步增加os-pd双金属有机分子笼对4t1细胞的毒性作用。
[0091]
实施例5 小鼠抗肿瘤治疗
[0092]
将4t1荷瘤小鼠随机分为6组:第1组静脉注射生理缓冲盐水(pbs);第2组注射0.5mg/ml mnps的pbs溶液;第3组注射0.5mg/ml cmnps的pbs溶液;第4组注射pbs溶液,x线照射(3gy);第5组注射0.5mg/ml mnps的pbs溶液,x线照射(3gy);第6组注射0.5mg/ml cmnps的pbs溶液,x线照射(3gy),第4、5、6组照射的时间一致,每3天进行一次,共5次注射。每4天记录4t1荷瘤小鼠的体重和肿瘤体积。
[0093]
如图13~14所示,与第1、2、3组相比,第5、6组表现出明显的肿瘤生长抑制现象。在x射线辐射下,第6组对肿瘤生长的抑制效果最好,这与放疗配合香豆素诱导的化疗有关。第6组肿瘤的平均体积约为113.63
±
59.78mm3,约为第1组(2404.43
±
168.52mm3)的22倍。x射线辐射下,第6组的平均肿瘤重量约为0.13
±
0.06g,第1组的平均肿瘤重量约为2.09
±
0.31g。进一步说明在x射线辐射下,注射了cmnps纳米粒子溶液的治疗效果非常优异,证明了主客体负载的双金属有机金属笼的辐射增敏作用。
[0094]
上述实施例为本发明较佳的实施方式,但本发明的实施方式并不受上述实施例的限制,其他的任何未背离本发明的精神实质与原理下所作的改变、修饰、替代、组合、简化,均应为等效的置换方式,都包含在本发明的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1