一种低共熔溶剂提取,动态轴向色谱制备羟基山椒素方法
1.本发明为一种低共熔溶剂提取,动态轴向色谱制备羟基山椒素方法,属于天然产物提取领域。
背景技术:
2.藤椒(竹叶花椒,zanthoxylum armatum dc)是中国传统药食两用资源,气味清香、柔和、无刺激和苦涩味。研究表明,山椒素及其由烷基不饱和度差异或碳链氧化引起结构变化的酰胺类同系物被视为藤椒麻味物质基础,也是重要品质保障,以羟基-α-山椒素、羟基-β-山椒素,羟基-γ-山椒素,羟基-ε-山椒素为主,可能通过激活瞬时受体电位(transient receptor potential,trp)v1和trpa1或阻断离子通道引发辛麻感,同时具有麻醉镇痛、消炎、保护肠道等功能。然而,该类化合物结构不稳定,在空气中极易发生异构化、水解和氧化,导致高纯度山椒素类的大规模制备存在技术瓶颈。目前国内外尚未建立花椒/藤椒麻味评价及适用于工业生产的麻味物质提取的标准方法,导致花椒和藤椒原料及其制品的质量良莠不齐,严重影响消费者的利益和市场有效监管。
3.中国专利cn102771747b,cn102690208a,cn105237430a公布的山椒素类化合物的制备工艺包括,利用有机溶剂或超临界co2等对花椒/藤椒样品进行提取,进而采用硅胶、凝胶色谱纯化,收集不同洗脱条件下的馏分,进而利用制备型薄层色谱、制备/半制备型hplc等仪器得到较高纯度单体,制备过程繁琐复杂,制备量小,效率低,因此,研究一种能够从藤椒中快速、宏量提取制备出多种高纯度单体的制备工艺具有重大的科学意义和工程应用价值。
技术实现要素:
4.本发明的目的在于针对现有技术的不足,提供一种低共熔溶剂提取,动态轴向色谱制备羟基山椒素方法,该方法是一种基于绿色新型低共熔溶剂提取,工业级快速制备高纯度羟基山椒素类化合物的方法,为藤椒麻味成分分析和质量评价提供对照品。
5.本发明的目的通过下述技术方案来实现:
6.一种工业级快速制备高纯度山椒素类化合物的方法,包括以下步骤:
7.s1,以超临界co2萃取藤椒油为原料,加入低共熔溶剂(des),超声辅助提取,萃取完成后离心,收集下层des层,得到羟基山椒素类成分des提取液;所得提取液经有机溶剂反萃取法,回收羟基山椒素类成分,得到羟基山椒素类成分富集产物。
8.作为优选,所述低共熔溶剂由如下方法制得,氢键供体与氢键受体按一定摩尔比比例混合,封口后置于80℃加热共溶至澄清,形成des溶剂,常温下静置备用。
9.作为优选,所述氢键供体为氯化胆碱,氢键受体为甲酸、乙酸、乳酸中的一种,摩尔比为1:2。
10.作为优选,所述离心转速为4000r/mi,离心时间为10min。
11.作为优选,所述超声辅助的处理条件为料液比为1:5~1:10(w/v),萃取功率为150
~200w,提取时间为0.5h。
12.作为优选,所述反萃取采用的有机溶剂为乙酸乙酯,料液比为1:5~1:10。
13.s2,动态轴向制备色谱分离纯化:山椒素类富集物用1-3倍质量体积的流动相完全溶解,采用动态轴向压缩制备液相分离,流动相为甲醇和水,检测波长为254nm,根据不同保留时间收集目标成分,洗脱液经减压旋蒸浓缩,冷冻干燥后得到各单体化合物。
14.作为优选,所述动态轴向制备液相色谱中动态轴压缩柱填料选自nucifera c18、hedera ods-2、acchrom x5、acchrom c18pe中的一种或几种,发明人通过筛选可知,nucifera c18、hedera ods-2可实现羟基山椒素的有效分离。
15.十八烷基反向硅胶,硅胶的粒径为5~10μm,更优选为5μm;所述动态轴向压缩柱的规格优选50mm
×
250mm。
16.作为优选,所述流动相比例为甲醇:水=65:35~85:15(v/v)。
17.作为优选,所述洗脱的流速为10-40ml/min。
18.作为优选,所述进样液浓度为50~150mg/ml。
19.低共熔溶剂由氢键供体(如酰胺、羧酸和多元醇等化合物)和氢键受体(如季铵盐)通过氢键组合而成,具有显著低于各个组分纯物质的熔点,且绿色环保,无毒,原料成本低,溶剂可回收。本专利设计合成萃取效率更高的dess,结合动态轴向制备色谱,实现藤椒中系列高纯度山椒素类化合物的大规模工业级制备。
20.与现有技术相比,本发明的积极效果体现在:
21.(一)本发明以氯化胆碱和酸类混合制成des溶剂,相较于已知萃取溶剂,显著提高了羟基山椒素类化合物的萃取率。
22.(二)本发明首次采用低共熔溶剂萃取/纯化-动态轴向压缩柱分离为核心的整套技术从藤椒油中同时分离羟基-α-山椒素、羟基-β-山椒素,羟基-γ-山椒素,羟基-ε-山椒素的方法,建立了一种从藤椒中提取、纯化、分离4种单体化合物的工艺路线,该工艺过程简单,不需要大量的纯化步骤,溶剂方便回收,纯度高,适合大批量工业化生产,具有很强的使用价值。
附图说明
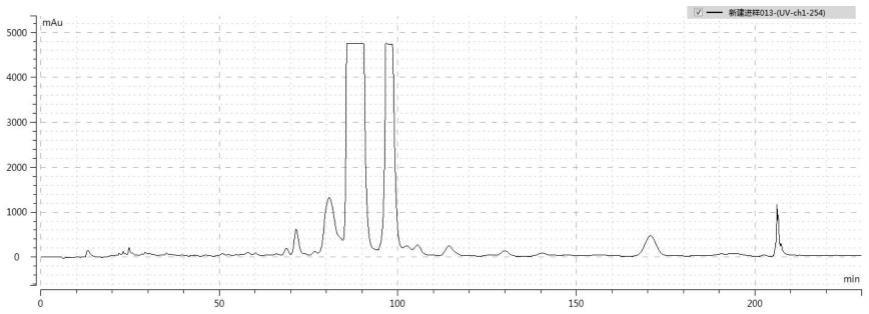
23.图1为实施例1利用dac进行分离的hplc图谱,其中a,b,c,d依次代表了羟基-α-山椒素、羟基-β-山椒素,羟基-γ-山椒素,羟基-ε-山椒素。
24.图2为实施例1所制得的羟基-α-山椒素hplc图谱,纯度为97.63%。
25.图3为实施例1所制得的羟基-β-山椒素hplc图谱,纯度为99.96%。
26.图4为实施例1所制得的羟基-γ-山椒素hplc图谱,纯度为98.57%。
27.图5为实施例1所制得的羟基-ε-山椒素hplc图谱,纯度为100%。
具体实施方式
28.提供下述实施例是为了更好地进一步理解本发明,并不局限于所述最佳实施方式,不对本发明的内容和保护范围构成限制,任何人在本发明的启示下或是将本发明与其他现有技术的特征进行组合而得出的任何与本发明相同或相近似的产品,均落在本发明的保护范围之内。
29.本技术中所记载的料液比,如无特殊情况说明,均表示物料的质量g与液体体积ml的比例关系。
30.实施例1:
31.(1)低共熔溶剂(des)制备:将氯化胆碱与乙酸按摩尔比为1:2比例混合,封口后置于80℃加热共溶至澄清,形成des溶剂,常温下静置备用。
32.(2)基于低共熔溶剂的山椒素类化合物提取:取50g藤椒油(优选经超临界co2萃取得到的,比如幺麻子藤椒油)为原料,按物料比1:10(w/v)加入des,超声辅助提取30min,4000rpm离心10min收集des层,得到羟基山椒素类des提取液;所得提取液按料液比1:8加入乙酸乙酯回收山椒素类,过滤收集滤液,旋蒸浓缩得到羟基山椒素类成分富集产物。
33.(3)动态轴向压缩分离:色谱柱采用nucifera c18u(5μm,50
×
250mm)用流动相平衡至色谱基线平稳,羟基山椒素类成分富集产物用流动相配置成80mg/ml,过滤得进样液,通过工业型制备色谱分离,以体积分数为65%的甲醇为流动相,流速为40ml/min,检测波长为254nm,根据不同保留时间收集目标成分,收集液经35℃减压浓缩,真空下冷冻干燥得到各单体化合物。
34.(4)单体化合物经hplc检测,羟基-α-山椒素的纯度为97.63%、羟基-β-山椒素的纯度为99.96%,羟基-γ-山椒素的纯度为98.57%,羟基-ε-山椒素的纯度为100.00%。
35.实施例2:
36.(1)低共熔溶剂(des)制备:将氯化胆碱与甲酸按摩尔比为1:2比例混合,封口后置于80℃加热共溶至澄清,形成des溶剂,常温下静置备用。
37.(2)基于低共熔溶剂的山椒素类化合物提取:取100g超临界co2萃取藤椒油为原料,按物料比1:10加入des,超声辅助提取30min,4000rpm离心10min收集des层,得到山椒素类des提取液;所得提取液按料液比1:8加入乙酸乙酯回收山椒素类,过滤收集滤液,旋蒸浓缩得到羟基山椒素类成分富集产物。
38.(3)动态轴向压缩分离:色谱柱采用nucifera c18u(5μm,50
×
250mm),用流动相平衡至色谱基线平稳,羟基山椒素类成分富集产物用流动相配置成100mg/ml,过滤即得进样液,进样液通过工业型制备色谱分离,采用梯度洗脱,0min-60min,甲醇/水=65:35(v/v),60min-80min,甲醇/水=85:15,流速为40ml/min,检测波长为254nm,根据不同保留时间收集目标成分,收集液经35℃~45℃减压浓缩,真空下冷冻干燥得到各单体化合物。
39.(4)单体化合物经hplc检测,羟基-α-山椒素纯度为97.57%、羟基-β-山椒素纯度为96.38%,γ-山椒素纯度为98.30%,羟基-ε-山椒素纯度为97.70%。
40.实施例3
41.(1)低共熔溶剂(des)制备:将氯化胆碱与乙酸按摩尔比为1:2比例混合,封口后置于80℃加热共溶至澄清,形成des溶剂,常温下静置备用。
42.(2)基于低共熔溶剂的山椒素类化合物提取:取100g超临界co2萃取藤椒油为原料,按物料比1:10加入des,超声辅助提取30min,4000rpm离心10min收集des层,得到山椒素类des提取液;所得提取液按料液比1:8加入乙酸乙酯回收山椒素类,过滤收集滤液,旋蒸浓缩得到羟基山椒素类成分富集产物。
43.(3)动态轴向压缩分离:色谱柱采用hedera ods-2(5μm,50
×
250mm),用流动相平衡至色谱基线平稳,羟基山椒素类成分富集产物用流动相配置成100mg/ml,过滤即得进样
液,进样液通过工业型制备色谱分离,以体积分数为65%的甲醇为流动相,流速为45ml/min,检测波长为254nm,根据不同保留时间收集目标成分,收集液经35℃~45℃减压浓缩,真空下冷冻干燥得到各单体化合物。
44.(4)单体化合物经hplc检测,羟基-α-山椒素纯度为97.24%、羟基-β-山椒素纯度为98.23%,羟基-γ-山椒素纯度为96.54%,羟基-ε-山椒素纯度为99.39%。
45.对比例1
46.相较于实施例1,未使用des溶剂,而是使用甲醇作为萃取溶剂。
47.对比例2
48.相较于实施例1,使用尿素、乙酰胺(酰胺基)作为氢键供体。
49.对比例3
50.相较于实施例1,色谱柱采用acchrom c18pe(7um,50*250mm)。所得单体化合物经hplc检测,羟基-α-山椒素纯度为90.64%、羟基-β-山椒素纯度为64.68%,羟基γ-山椒素纯度为62.45%,羟基-ε-山椒素纯度为85.82%。相比于实施例1、2、3,杂质含量较多,纯度下降。
51.测试例1
52.将上述制备得到的物质进行光谱检测,采用高效液相色谱(hplc)进行检测,色谱条件为:流动相a:水,流动相b:甲醇;0~50min,a:b=50:50~25:75;流速:1ml/min,柱温:30℃;紫外检测波长:254nm,进样量:10ul。计算各提取方法的萃取率,萃取率等于山椒素类化合物在萃取溶剂中的含量与两相中总含量的百分比。
53.其中实施例1、2、3萃取率分别为24%,23%,23%;使用甲醇代替des溶剂的对比例1,相较于实施例而言,属于传统的萃取花椒/藤椒中酰胺类物质的方法,萃取率为20%,说明des溶剂对目标化合物的萃取有着至关重要的作用。通过观察对比例2的萃取率,其中,以尿素为氢键供体,其萃取率仅为15%,因此酸类氢键供体提取效率更高,可能源于酰胺类化合物与酸类氢键供体发生结合,导致酰胺类化合物到溶液的传质过程,从而促进酰胺类物质的充分萃取。
54.综上所述,本发明以氯化胆碱与酸类混合制得的des溶剂,结合超声辅助萃取进行萃取,协同作用下显著提高了萃取效果。进而结合动态轴向压缩柱分离从藤椒油中同时分离羟基-α-山椒素、羟基-β-山椒素,羟基-γ-山椒素,羟基-ε-山椒素的方法,建立了一种从藤椒中提取、纯化、分离4种单体化合物的工艺路线,该工艺过程简单,不需要大量的纯化步骤,溶剂方便回收,纯度高,适合大批量工业化生产,具有很强的使用价值。
55.以上所述仅为本发明的较佳实施例而已,并不用以限制本发明,凡在本发明的精神和原则之内所作的任何修改、等同替换和改进等,均应包含在本发明的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1