一种含有二氰基异佛尔酮基的咔唑衍生物荧光探针及其制备方法和用途
1.本发明涉及一种含有二氰基异佛尔酮基的咔唑衍生物荧光探针及其制备方法和用途,具 体用于检测clo-离子,属于离子检测和荧光分子探针领域。
背景技术:
2.活性氧(ros)作为氧代谢的副产物,已经被证明是重要的细胞内信号分子,密切参与许多 基本的生物过程和各种疾病的发病机制。clo-作为ros之一,在先天免疫系统中具有极强的 杀菌作用。在生理条件下,clo-可与多种生物分子(如氨基酸、蛋白质、膜脂、dna)快速 反应,因此适当浓度的clo-是有益的,而异常clo-对人体是有害的,可引起氧化损伤,诱发 多种人类疾病,如肺损伤、类风湿性关节炎、神经元变性、心血管疾病以及癌症等。同时, clo-具有漂白和杀菌的双重功能,广泛应用于家庭漂白、饮用水消毒等日常生活中。鉴于 hclo的上述生理和病理特性,迫切需要一种特定的超快速检测工具来可视化检测活细胞中 clo-的浓度变化。因此,开发一种可以快速、特异性及可视化识别clo-离子的荧光探针用于 实时监测生物细胞中或水中的clo-离子具有非常重要的意义。
技术实现要素:
3.本发明旨在提供一种含有二氰基异佛尔酮基的咔唑衍生物荧光探针及其制备方法和用 途,所要解决的技术问题是通过分子设计合成能够检测识别clo-的荧光探针。
4.本发明含有二氰基异佛尔酮基的咔唑衍生物荧光探针是一种比率荧光探针,在其它离子 存在的情况下仍对clo-离子有较高的选择性和灵敏性,并且本发明荧光探针与clo-离子混合 产生明显的颜色变化现象可以实现裸眼识别和比色分析。
5.本发明含有二氰基异佛尔酮基的咔唑衍生物荧光探针的结构式如下所示:
[0006][0007]
本发明含有二氰基异佛尔酮-噻吩醛基的咔唑衍生物具有良好的分子内电荷转移效应,分 子中二氰基异佛尔酮基团上含有的c=c键常被用作hclo的反应位点,在常温的条件下, hclo可以将其氧化为醛或酮,从而使整个分子体系的分子内电荷转移效应发生改
变,导致原 探针化合物的紫外及荧光现象发生变化,实现该探针分子对clo-离子的快速检测。
[0008]
本发明含有二氰基异佛尔酮基的咔唑衍生物荧光探针的制备方法,包括如下步骤:
[0009]
步骤1:中间体i-dcm的合成
[0010]
称取3-甲酰基-6-碘-n-丁基咔唑(0.7430g,1.91mmol)和dcm(0.4051g,2.17mmol)溶 于25ml乙醇中,滴加0.6ml哌啶于圆底烧瓶内,该反应在回流状态下搅拌6小时;反应 结束后,产物从热乙醇中析出,趁热过滤,将滤饼用乙醇洗涤三次得到0.7112g红色固体。
[0011]
步骤2:sfq的合成
[0012]
分别取150mg i-dcm(0.27mg)、62.4mg 5-醛基-2-噻吩硼酸(0.40mg)和31mg pd(pph3)
4 (0.27mmol)倒入三颈瓶,充入n2保证无氧环境,用注射器注入20ml甲苯和乙醇(3:1,v/v) 的混合溶液和3ml饱和k2co3溶液,该反应在80℃下反应24小时;反应完毕后冷却至室 温,将产物倒入大量蒸馏水中,用二氯甲烷萃取并合并有机相(平均萃取三次),有机相用无 水mgso4干燥过夜,过滤后将滤液减压旋干得到粗产物;使用石油醚、二氯甲烷和乙酸乙酯 (8:1:1,v/v/v)为洗脱剂,经硅胶柱层析分离技术纯化,最终得到54mg红色固体。
[0013]
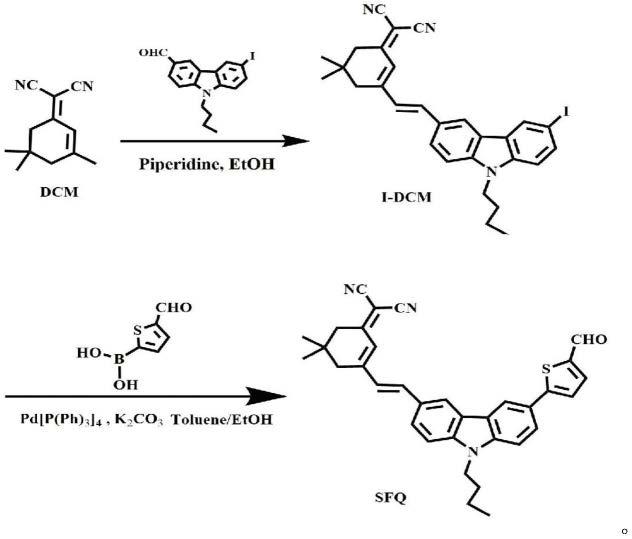
本发明合成路线如下所示:
[0014][0015]
本发明含有二氰基异佛尔酮基的咔唑衍生物荧光探针的用途,是在定性或定量检测clo-时作为检测试剂使用。
[0016]
进一步地,在有机溶剂介质中进行紫外-可见吸收光谱测定,通过溶液颜色的变化实现对 clo-的定性或定量检测。
[0017]
进一步地,在有机溶剂介质中进行荧光光谱测定,通过双通道荧光强度的变化实现对clo-的定性或定量检测。
[0018]
所述有机溶剂介质为dmf。
[0019]
本发明荧光探针可用于clo-离子的识别、检测,对多种其他离子有较强的抗干扰能力, 并且本发明荧光探针与clo-离子混合产生明显的颜色变化现象可以实现裸眼识别和比色分 析。
[0020]
本发明的有益效果体现在:
[0021]
本发明荧光探针化合物具有多功能性,可以通过紫外-可见分光光度法和荧光光谱法分别 实现对clo-离子的识别。本发明的荧光探针能够特异性识别clo-离子,在探针的dmf中溶 液中加入clo-离子,在紫外光谱中,可见在468nm处的吸收带明显红移了25nm,且伴随着 吸收强度的减小;在普通室内光下探针溶液显示为橙色,加入clo-离子后,溶液颜色变为粉 红色,而在365nm紫外灯下,能看到溶液颜色由橙红色变为青色。在荧光光谱中,clo-离 子的加入使探针溶液473nm处的荧光增加,发光位置逐渐红移至486nm,与此同时,613nm 处的荧光减弱且发射峰消失,呈现出比率荧光现象,探针sfq显示两个不同的发射通道,这 使其能够在超短时间内以比率方式检测clo-离子。探针可以通过紫外-可见分光光度法和荧光 光谱法实现对clo-离子的识别及定量检测,在其它离子存在的情况下仍有很好的抗干扰性、 高选择性和灵敏性。
[0022]
本发明荧光探针可用于真实水样中对clo-离子进行快速的识别和定量检测,而且对clo-离子的识别具有较高的选择性和较好的抗干扰能力,并且明显的颜色变化现象可以实现裸眼 识别和比色分析。真实水样测试,说明该探针在实际水样中应用具有良好前景;在生物应用 方面对探针的实用性探究表明,该探针溶液可对细胞中外源性的clo-离子的进行检测。上述 实验结果说明我们的探针在环境监测及生物体中有良好的应用潜质。
附图说明
[0023]
图1a为本发明荧光探针(sfq)在dmf中加入不同离子的紫外吸收光谱(插图为加入 clo-前后的颜色变化)。
[0024]
图1b为本发明荧光探针(sfq)在dmf中加入不同离子的荧光光谱(插图为加入clo-前后的在365nm紫外灯照射下颜色变化)。
[0025]
图2a为本发明荧光探针(sfq)(10μm)在dmf中添加不同浓度clo-(0-32.5μm)的 紫外吸收滴定光谱。
[0026]
图2b为在纯dmf中本发明荧光探针(sfq)(10μm)添加不同浓度clo-(0-40μm)在 370nm激发下的荧光滴定光谱。
[0027]
图2c为在纯dmf中本发明荧光探针(sfq)(10μm)添加不同浓度clo-(0-40μm)在 470nm激发下的荧光滴定光谱。
[0028]
图3a为本发明荧光探针(sfq)(10μm)紫外吸收强度与不同浓度clo-(12.5-25μm) 的线性关系。
[0029]
图3b为本发明荧光探针(sfq)荧光强度比f
489
/f
613
与clo-浓度(13-27.5μm)的函数 关系。
[0030]
图4a为本发明荧光探针(sfq)(10μm)在clo-存在下加入其他被分析物时的紫外吸收 响应。sfq加入其他被分析物(2equiv.)后的紫外吸收;sfq在clo-和其他 被分析物(2equiv.)同时存在时的紫外吸收情况。
[0031]
图4b为本发明荧光探针sfq(10μm)在clo-存在下加入其他被分析物时的荧光强度
比 (f
489
/f
613
)。代表sfq加入其他被分析物(2equiv.)后的荧光强度比(f
489
/f
613
);代表sfq在clo-和其他被分析物(2equiv.)同时存在时的荧光强度比(f
489
/f
613
)。
[0032]
图5为本发明荧光探针sfq中添加不同浓度的clo-后在489nm处的荧光强度随时间的 变化(λ
ex
=370nm)。
[0033]
图6为本发明荧光探针sfq中添加clo-后产物的质谱图。
[0034]
图7为本发明荧光探针sfq(10μm)与clo-(3.0equiv.)在dmso-d6中的核磁滴定氢 谱图。
[0035]
图8为在hepg2细胞中捕获的荧光强度对比图。
[0036]
具体实施方式
[0037]
本发明可以通过以下的实施例进一步说明,但不仅仅局限于实施例。
[0038]
实施例1:荧光探针sfq的合成
[0039]
称取3-甲酰基-6-碘-n-丁基咔唑(0.7430g,1.91mmol)和dcm(0.4051g,2.17mmol)溶 于25ml乙醇中,滴加0.6ml哌啶于圆底烧瓶内,该反应在回流状态下搅拌6小时。反应 结束,产物从热乙醇中析出,趁热过滤,将滤饼用乙醇洗涤三次得到0.7112g红色固体 (i-dcm)。产率为68%。
[0040]1h nmr(600mhz,dmso-d6)δ8.68(s,1h),8.57(s,1h),7.82(d,j=8.6hz,1h),7.75(d, j=8.6hz,1h),7.67(d,j=8.6hz,1h),7.53(d,j=8.6hz,1h),7.47(d,j=8.4hz,2h),6.85(s, 1h),4.40(t,2h),2.64(s,2h),2.61(s,2h),2.51(s,2h),1.74(m,2h),1.29(m,2h),1.06(s,6h), 0.88(t,3h).[m-h]
+
:545.1249.
[0041]
分别取150mg i-dcm(0.27mg)、62.4mg 5-醛基-2-噻吩硼酸(0.40mg)和31mg pd(pph3)
4 (0.27mmol)倒入三颈瓶中,充入n2保证无氧环境,用注射器注入20ml甲苯和乙醇(3:1, v/v)的混合溶液和3ml饱和k2co3溶液,在80℃下反应24小时。反应完毕后冷却至室 温,将产物倒入大量蒸馏水中,用二氯甲烷萃取并合并有机相(平均萃取三次),有机相用无 水mgso4干燥过夜,过滤后将滤液减压旋干得到粗产物。然后采用石油醚、二氯甲烷和乙酸 乙酯(8:1:1,v/v/v)为洗脱剂,经硅胶柱层析技术纯化,最终得到红色固体(sfq)54mg, 产率为37.5%。
[0042]1h nmr(400mhz,dmso-d6)δ9.87(s,1h),8.71(s,1h),8.65(s,1h),8.04(d,j=3.9hz, 1h),7.90(d,j=8.5hz,1h),7.80(d,j=9.7hz,1h),7.78
–
7.62(m,3h),7.50
–
7.39(m,2h), 6.84(s,1h),4.42(t,2h),2.59(d,j=6.8hz,4h),1.79
–
1.68(m,2h),1.30
–
1.24(m,2h),1.02(s, 6h),0.83(t,3h).
13
c nmr(101mhz,cdcl3)δ182.69(s),169.37(s),155.74(s),154.59(s), 142.04(s),141.61(d,j=3.2hz),138.19(s),137.93(s),127.68(s),127.01(s),126.10(s),125.08 (d,j=3.6hz),123.52-123.10(m,3c),122.72(s),120.74(s),118.65(s),113.90(s),113.19(s), 109.90(d,j=2.9hz),43.41(s),43.08(s),39.37(s),32.14(s),31.21(s),29.78(s),28.16(s),20.60 (s),13.92(s).ir(kbr,cm-1
)2210(-cn),1384(-ch3),674(c-s).[m-h]
+
:529.2154.
[0043]
实施例2:荧光探针sfq的选择性光谱研究
[0044]
选择性作为探针检测离子的参数之一,具有重大的意义。从图1a中可以看出,在n,n‑ꢀ
二甲基甲酰胺(dmf)溶液中,探针sfq(10μm)在468nm处显示出一个强吸收峰,这可 能归因于sfq内的n-π
*
跃迁。在探针sfq中分别加入2倍当量的各种分析物(cl-,hso
3-, so
32-,hco
3-,scn-,ch3coo-,onoo-,no
2-,h2o2,cu
2+
,fe
3+
,na
+
,mg
2+
,co
2+
,cys, gsh和lysine)后,其紫外吸收基本上无变化,仅存在clo-时,sfq在468nm处的吸收带 明显红移了25nm,且伴随着吸收强度的减小(图1a)。探针sfq溶液在普通室内光下显示 为橙色,加入clo-后,溶液颜色变为粉红色(图1a中的插图),这一现象与紫外吸收变化相 吻合。在荧光光谱中,clo-的加入使sfq溶液呈现出比率荧光现象,473nm处的荧光增加 了近10倍左右,发光位置红移至486nm,与此同时,613nm处的荧光减弱且发射峰消失(图 1b)。在365nm紫外灯下,溶液颜色由橙红色变为青色(图1b中的插图),而其他分析物的 加入并无明显改变。以上结果表明,探针sfq仅对clo-具有高度的选择性。
[0045]
实施例3:荧光探针(sfq)的滴定光谱研究
[0046]
探针sfq对clo-的紫外及荧光滴定光谱实验进一步被探究。如图2a所示,随着clo-的 浓度不断增大,sfq在469nm位置的吸收峰逐渐红移并且在慢慢减弱,与此同时,在364nm 处的峰也逐渐移动到370nm。探针sfq(10μm)与clo-的浓度在12.5-25μm范围内存在良 好的线性关系(r2=0.9919),a
469
=-0.0064[clo-]+0.2558(图3a)。根据dl=3σ/k,计算 得出探针sfq在紫外-可见吸收光谱中对clo-的检测限为1.13μm。图2b和图2c分别是探针 sfq(10μm)添加不同浓度clo-(0-40μm)在470nm和370nm激发下的荧光滴定光谱。 如图2b所示,在470nm激发时,探针在613nm处的发射逐渐降低,而在370nm激发时, 探针在473nm处的发射逐渐增强且发射峰位置逐渐移到489nm处。为此,我们做了荧光强 度比f
489
/f
613
与clo-浓度的函数关系,在13-27.5μm范围内,荧光强度比f
489
/f
613
与clo-浓 度呈现良好的线性关系(r2=0.9930),f
489
/f
613
=1.5126[clo-]﹣12.1015(图3b)。根据dl=3σ/k, 计算得出探针sfq在荧光光谱中对clo-的比率检测限为0.14μm。
[0047]
实施例4:荧光探针(sfq)的竞争性研究
[0048]
为了探究探针sfq对clo-检测的抗干扰性,我们进行了紫外-可见吸收光谱和荧光光谱 的竞争性实验。在紫外吸收光谱中显示,仅在clo-存在的体系下探针sfq的紫外吸收才会降 低(图4a),其他被分析物的存在几乎不会影响到clo-的检测。同样地,仅在clo-存在的体 系下探针sfq的荧光强度比(f
489
/f
613
)明显增大十几倍,其他分析物的存在几乎无法对clo-的检测造成干扰(图4b),探针sfq对clo-具有高度的选择性和抗干扰性。因此,该探针有 望成为一种可被开发应用的传感器用于在复杂的环境中完成对clo-的检测。
[0049]
实施例5:荧光探针(sfq)的时间响应
[0050]
众所周知,快速时间响应在实际应用中对于荧光探针检测各种阴阳离子和氨基酸等分析 物的意义至关重要。如图5所示,在向探针sfq(10μm,dmf)中分别加入12.5μm、25μm、 50μm,均在5秒内快速响应,在20秒内基本达到平衡,满足作为瞬态代谢产物中实时检测 clo-的要求。我们查阅了近几年国内外检测clo-的相关文献并进行了比较,可以看出该探针 对clo-的响应明显快于其他文献所报道的探针。
[0051]
实施例6:荧光探针sfq对clo-的响应机制研究
[0052]
为了研究探针sfq对clo-的响应机制,我们将探针sfq对clo-反应后的产物做了质谱 以及核磁滴定。如图6所示,一个峰m/z=481.2607可归因于[sfq-o+h]
+
,这可能是-c=c(cn) 被氧化为-c=o。为了继续验证该猜测,我们进行核磁滴定测试,从实验结果可以看
出:ha, hb,hc,和hd均向高场移动,化学位移分别由δ7.46ppm,7.43ppm,6.84ppm,8.65ppm 移至6.50ppm,6.42ppm,5.69ppm和8.52ppm(图7),这可能是由于两个强吸电子基(-cn) 被氧化成中等吸电子基(-c=o),所致。由此可以证明探针sfq的吸电子cn基团受到clo-的攻击从而被氧化成酮基。
[0053]
实施例7:荧光探针sfq对水样中clo-的检测
[0054]
为了考察sfq在实际生活中的潜在应用,我们选取了安徽大学附近湖水和实验室自来水 为例进行真实水样内测试clo-。用dmf配制探针sfq(10μm)溶液,分别用湖水和自来水 配成10-2
m的clo-溶液。分别加入5μm,10μm,15μm,20μm的三种clo-溶液,测定其 荧光强度。实验结果由表1可知,测得的clo-浓度与所加浓度误差很小,且测试回收率在 98.5%-103%范围内,以上说明探针sfq在真实水样中检测clo-具有很高的准确性,可应用 于真实水样中clo-的检测。
[0055]
表1本发明荧光探针sfq对多种真实水样中clo-的检测。
[0056][0057]
实施例8:在细胞中荧光探针化合物sfq对clo-的荧光显影测试
[0058]
借助共聚焦显微镜,可观察到经sfq(10μm)染色30分钟的hepg2细胞,在红色通 道及青色通道均捕获到荧光,当继续向细胞中加clo-(50μm)培养0.5小时后,可以观察到 红色通道里的荧光明显减弱,而青色通道中展现出了较强的荧光发射。细胞中捕获的荧光强 度如图8所示,该细胞共聚焦成像与实验现象一致。由此可见,探针sfq具有较强的细胞膜 穿透能力并且能够通过双通道的荧光变化检测出细胞内外源性clo-的分布情况。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1