一种氧气纳米探针及其制备方法与应用与流程
本发明涉及光学成像应用
技术领域:
,更具体的说是涉及一种氧气纳米探针及其制备方法与应用。
背景技术:
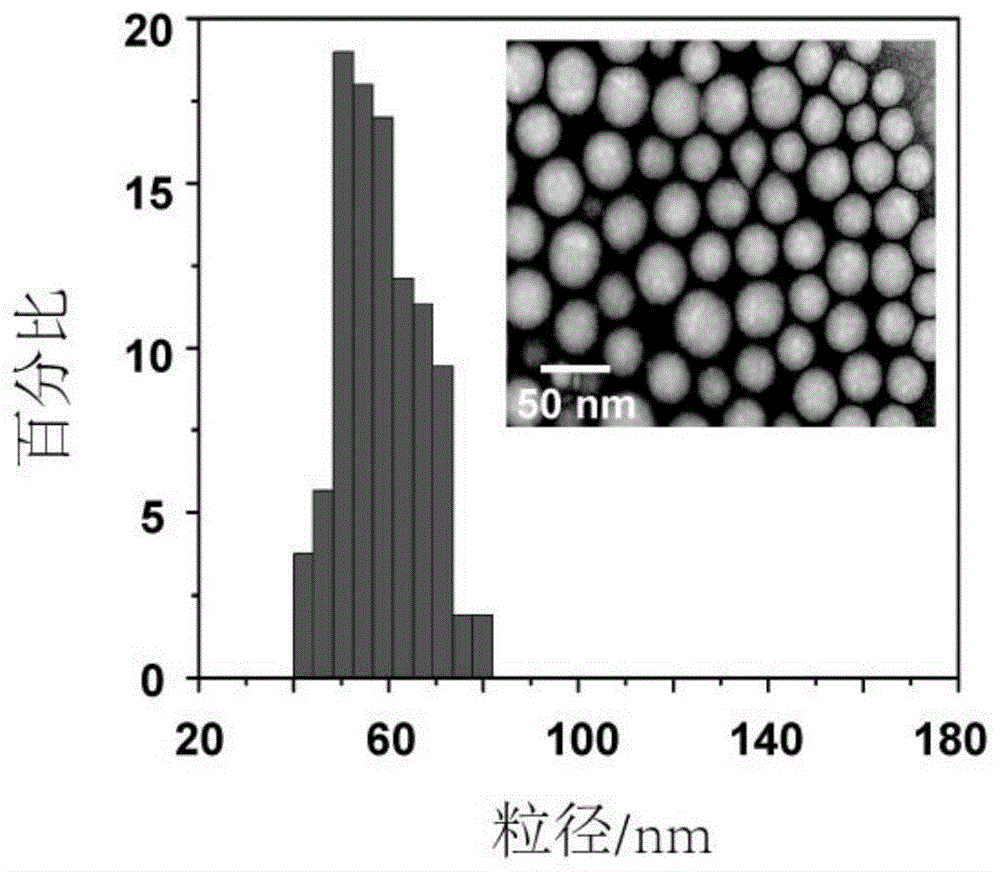
:氧气在生物中起着至关重要的作用,细胞内氧浓度受到微循环系统的严格调控。体内氧稳态的紊乱通常会导致诸如心血管疾病和中风之类的严重疾病。因此,研究者们一直致力于开发各种各样的技术,用来检测细胞内和组织中的氧气水平。目前常用的方法包括正电子发射断层扫描(pet)成像,血氧水平依赖性磁共振成像(bold-mri),光学方法和常规的氧电极方法。然而,氧电极方法是侵入性的,单点测量并且消耗氧气的。基于bold-mri的测量仅仅只能提供血液中的氧合血红蛋白(oxyhb)和脱氧血红蛋白(deoxyhb)的变化信息,并不能直接提供组织中氧气的真实含量。此外,pet成像需要用到放射性的元素,其会对机体正常的部位造成放射性损伤。光学成像技术具有高灵敏度和高时空分辨率的特点,目前利用光学成像技术测量氧气含量主要集中在发光强度成像的方法上。然而,基于发光强度的成像方法易受荧光团浓度,组织穿透深度,激光功率密度,探测器增益等的影响。因此,基于强度的成像方法只能定性的检测氧气含量,其并不能定量直观的检测氧气的真实水平。因此,提供一种检测结果准确、易于操作的氧气含量测量方法是本领域技术人员亟需解决的问题。技术实现要素:有鉴于此,本发明提供了一种氧气纳米探针及其制备方法与应用。为了实现上述目的,本发明采用如下技术方案:一种氧气纳米探针,包含如下质量百分含量的组分:0.4%的发光体和99.6%的连接材料;所述发光体为有机染料、金属配合物或量子点中任意一种。优选的,所述有机染料为多环芳烃、吖啶黄或四碘荧光素。优选的,所述金属配合物为钯配合物、铂配合物、钌配合物、铱配合物或铑配合物。优选的,所述量子点为cdte量子点、zns:cu量子点或石墨烯量子点。优选的,所述连接材料为卵磷脂、聚乙二醇、白蛋白或抗体。一种氧气纳米探针的制备方法,包括如下步骤:(1)将所述发光体配制成质量浓度为2mm的发光体储备溶液;(2)将连接材料溶于有机溶剂中配制成质量浓度5mg/ml的连接材料溶液;所述有机溶剂为氯仿、四氢呋喃、乙醇、甲醇、二氯甲烷或甲苯。(3)将发光体储备溶液加入到连接材料溶液中,二者体积比为1:100,并通过超声波震荡混合,得混合液;(4)移取混合液加入纯水中,混合液与纯水的体积比为1:1,在室温下搅拌5分钟后,去除有机溶剂,之后通过孔径为0.13μm的水相过滤器过滤得氧气纳米探针,置于4℃条件下保存备用。氧气纳米探针在发光寿命成像检测中的应用。作为发光的另一个表征参数,和传统的发光强度成像相比,发光寿命成像具有如下两个主要优点。其一,生物背景发光寿命与发光指示剂的寿命往往是不同的,这样就可以很方便的利用寿命衰减信号将生物背景区分开来。其二,发光寿命成像不依赖于由于照射不均匀造成的强度变化,其也不依赖于指示剂的浓度、组织的穿透深度和检测器的增益,其只和氧气的浓度有关。优选的,可用于肝脏氧气的定量检测。优选的,检测系统包括激发光源,滤光片,波形发生器,检测器和计算机,检测步骤如下:(1)将不同浓度的氧气通过气体流量计通入到氧气纳米探针水溶液中,用激发光源激发,并用检测器收集氧气纳米探针的发光强度衰减信号,之后利用计算机计算出发光寿命值,从而得到不同氧气浓度的氧气纳米探针的发光寿命工作曲线;(2)利用步骤(1)方法得到待检测样品的发光寿命值;(3)将步骤(2)得到的发光寿命值代入发光寿命工作曲线中,从而得到待测样品中的氧气含量。优选的,所用的激发光源为激光、氙灯或led灯;所述的检测器为电子倍增ccd、ingaas相机或像增强型ccd。经由上述的技术方案可知,与现有技术相比,本发明取得的有益效果为:(1)与稳态的荧光强度不同,荧光寿命是一种内在的分子属性,其是绝对的,仅仅与荧光团所处的微环境有关。发光寿命不受影响强度信号的因素的影响,即使激光强度、组织的厚度或检测器增益发生改变,所记录的荧光寿命却不会发生变化。(2)氧气纳米探针的发光寿命不随其浓度的差异而发生变化,其仅和氧气浓度有关。(3)利用氧气纳米探针的发光寿命可以定量的检测样品中的氧气浓度。附图说明为了更清楚地说明本发明实施例或现有技术中的技术方案,下面将对实施例或现有技术描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图仅仅是本发明的实施例,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据提供的附图获得其他的附图。图1附图是本发明实施例2制备的氧气纳米探针的电镜图;图2附图为本发明实施例2中所制备的氧气纳米探针发光寿命成像随氧气浓度的变化图;图3附图为本发明实施例2中制备的氧气纳米探针的不同氧气浓度的发光寿命工作曲线;图4附图为本发明实施例3中利用发光寿命成像检测肝脏急性乏氧,其中a为肝脏缺血再灌注模型的示意图;b为在缺血-再灌注期间小鼠肝脏的发光寿命成像图;c为在缺血-再灌注期间小鼠肝脏的发光寿命直方图;d为在缺血-再灌注期间小鼠肝脏的氧气浓度直方图;图5附图是本发明实施例4中利用发光寿命成像检测皮下肿瘤乏氧,其中a为接种皮下肿瘤小鼠的肿瘤区域和肝脏区域寿命成像图;b为接种皮下肿瘤小鼠的肿瘤区域和肝脏区域的发光强度直方图;c为接种皮下肿瘤小鼠的肿瘤区域和肝脏区域的发光寿命直方图;d为接种皮下肿瘤小鼠的肿瘤区域和肝脏区域的氧气浓度直方图;图6附图是本发明实施例5中利用发光寿命成像检测肝脏原位肿瘤乏氧;其中a为接种原位肝脏肿瘤小鼠的超声成像图;b为接种原位肝脏肿瘤小鼠的发光寿命成像图;c为接种原位肝脏肿瘤小鼠的发光强度直方图;d为接种原位肝脏肿瘤小鼠的发光寿命直方图;e为接种原位肝脏肿瘤小鼠的氧气浓度直方图。具体实施方式下面将结合本发明实施例中的附图,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。实施例1量子点氧气纳米探针的制备(1)将zns:cu量子点分散在1ml氯仿中制备2mm的量子点储备溶液;(2)将10mg卵磷脂溶于2ml的氯仿中用以制备卵磷脂溶液;(3)将20μl量子点储备溶液加入到2ml上述卵磷脂溶液中并通过超声波震荡混合,得混合液;(4)移取混合液并快速加入2ml搅拌的纯水中,在室温下搅拌5分钟后,通过旋转蒸发仪旋蒸出有机溶剂,并通过孔径为0.13μm的水相过滤器过滤。将获得的氧气纳米探针溶液储存在4℃冰箱中以备下次使用。所获得的氧气纳米探针经透射电镜表征为85±4nm。实施例2基于氧气纳米探针dspeg-pdtptbp的体外溶液样本中寿命成像检测(1)氧气纳米探针的制备①将1.84mg四苯基四苯并钯卟啉(pdtptbp)溶解在1ml四氢呋喃中制备2mm的金属配合物储备溶液;②将10mg磷脂peg(dspe-peg)溶于2ml的四氢呋喃中用以制备dspe-peg-2000溶液;③将20μl金属配合物储备溶液加入到2ml上述dspe-peg-2000溶液中并通过超声波震荡混合,得混合液;④移取混合液并快速加入2ml搅拌的纯水中,在室温下搅拌5分钟后,通过旋转蒸发仪旋蒸出有机溶剂,并通过孔径为0.13μm的水相过滤器过滤。将制得的氧气纳米探针溶液储存在4℃冰箱中备用。图1是该氧气纳米探针的电镜图。(2)不同氧气浓度的发光寿命工作曲线的建立取所制备的氧气纳米探针溶液放入到容器中,利用气体质量流量计,向容器中的溶液中通入不同比例的氧气/氩气混合气体,通入10分钟后,放在发光寿命成像系统中对氧气纳米探针进行寿命成像,结果如图2所示。由图2结果可知,随着容器中氧气含量不断减少,氧气纳米探针的发光寿命急剧增加。说明发光寿命成像方法可以在体外高灵敏的检测乏氧情形。将由图2测的寿命平均值和通入的氧气浓度建立不同氧气浓度的发光寿命工作曲线,结果如图3所示。实施例3基于氧气纳米探针dspeg-pdtptbp的小鼠肝脏急性乏氧检测(1)探针的制备:同实施例2。(2)检测将dspeg-pdtptbp探针溶液(0.6ml,20μm)通过尾部静脉内注射到小鼠(6周龄)体内。注射探针12小时后,用异氟烷麻醉小鼠,将其肢体以仰卧位固定。用1%碘消毒小鼠的腹部,并用组织剪刀逐层切开以暴露腹腔。用非侵入性血管夹钳夹住肝脏中叶、左肝叶和胆管的血管,导致肝脏缺血70%左右,同时保持肝脏右侧和尾侧叶的血液供应。阻断后,阻塞区肝脏颜色由鲜红色变为深红色,表明缺血肝脏模型成功建立。移除血管夹后构建肝再灌注模型。在缺血再灌注前后,使用发光寿命成像系统对小鼠肝脏进行成像,结果如图4所示。由图4结果可知,在缺血之前,通过发光寿命成像系统测量的小鼠肝脏的平均磷光寿命为约84μs,计算所得出的肝脏平均氧压力为14.9mmhg。在将血管夹紧2分钟后,小鼠肝脏的平均磷光寿命急剧上升至171μs,与之相对应的肝脏平均氧压力下降到4.0mmhg。当移除血管夹允许血流再灌注时,小鼠肝脏的平均磷光寿命逐渐恢复,约2分钟恢复至106μs。再灌注10分钟后,肝脏的平均磷光寿命恢复到其原始值(缺血前),并在20分钟后肝脏平均氧压力保持稳定水平(14.9mmhg)。实施例4基于氧气纳米探针dspeg-pdtptbp的小鼠皮下肿瘤乏氧检测(1)探针的制备:同实施例2。(2)检测小鼠肿瘤构建方法经复旦大学药学院机构动物护理与使用委员会指导批准。为了构建皮下植入小鼠的肝细胞癌hepg2肿瘤模型,将对数生长期hepg2细胞(1×107/0.2ml)皮下注射到小鼠的右侧下肢(4周龄)。约20天后,肿瘤生长至约5-10mm的直径,并可用于随后的成像实验。通过尾静脉将dspeg-pdtptbp探针的水溶液(0.6ml,20μm)注射到荷瘤小鼠中。在注射后的12小时后用异氟烷气体麻醉小鼠,然后置于发光寿命测量系统下进行成像,如图5所示。由图5结果可知,来自肝脏器官的磷光强度信号强于肿瘤区域。然而,计算肿瘤和肝脏区域中磷光强度的延迟表明肝脏中的平均磷光寿命(101μs)小于肿瘤部位(192μs),与之相对应的肝脏平均氧压力为12.2mmhg和肿瘤区域平均氧压力为2.9mmhg。实施例5基于氧气纳米探针dspeg-pdtptbp的小鼠原位肝脏肿瘤乏氧检测(1)探针的制备:同实施例2。(2)检测根据以下主要操作步骤建立原位肝脏肿瘤小鼠模型。取一个生长良好的皮下肿瘤,用剪刀将其切成约2mm×2mm×1mm的肿瘤组织块。使用气体麻醉系统对小鼠(6周龄)进行气体麻醉,麻醉剂为异氟烷。在动物麻醉后,取出仰卧位,并用组织剪刀逐层切割皮肤。开口长度约1cm,肝脏暴露。然后使用套管针轻轻戳在肝叶中间约3毫米深的隧道。在此过程中,使用无菌棉签轻轻按压血液以阻止血液。将制备好的肿瘤组织块小心地放入隧道中,然后选择生物粘合剂(ob胶)在闭合腹部之前粘合伤口。约3周后,肿瘤生长至约5-10mm的直径,并可用于随后的成像实验。通过尾静脉将dspeg-pdtptbp探针的水溶液(0.6ml,20μm)注射到荷瘤小鼠中。注射后,对小鼠以及上述皮下肿瘤小鼠进行成像,结果如图6所示。由图6结果可知,使用发光强度方法无法定位肿瘤缺氧区域。然而,拟合小鼠肝脏磷光强度的延迟,正常肝脏区域和肿瘤区域之间的磷光寿命明显不同。活体小鼠中整个肝脏区域的氧气压力直方图清楚地显示出正常肝脏部位的平均氧压力为12.4mmhg和肿瘤性肝脏部位的平均氧压力为5.5mmhg。实施例6基于氧气纳米探针dspeg-pdtptbp的小鼠正常肝脏氧气检测(1)探针的制备:同实施例2(2)检测方法:通过尾静脉将dspeg-pdtptbp探针的水溶液(0.6ml,20μm)注射到正常小鼠中。在注射后的12小时后用异氟烷气体麻醉小鼠,然后置于发光寿命测量系统下进行成像,将所测得的发光寿命值代入实施例2中得到的氧气纳米探针的不同氧气浓度的发光寿命工作曲线,可测得小鼠正常肝脏的氧气浓度。检测结果如表1所示。表1小鼠正常肝脏氧气检测结果肝脏平均寿命肝脏平均氧气压力小鼠184μs15.0mmhg小鼠295μs12.5mmhg小鼠3104μs10.9mmhg小鼠498μs12.0mmhg小鼠5101μs11.4mmhg小鼠6104μs10.9mmhg小鼠796μs12.4mmhg小鼠894μs12.7mmhg小鼠9110μs10.0mmhg由表1结果可知,通过我们设计的发光寿命变化的氧气纳米探针测得的小鼠正常肝脏的平均氧气压力为10.0-15.0mmhg。本说明书中各个实施例采用递进的方式描述,每个实施例重点说明的都是与其他实施例的不同之处,各个实施例之间相同相似部分互相参见即可。本文中所定义的一般原理可以在不脱离本发明的精神或范围的情况下,在其它实施例中实现。因此,本发明将不会被限制于本文所示的实施例,而是要符合与本文所公开的原理和新颖特点相一致的最宽的范围。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1